肾交感消融通过抑制氧化应激和过度自噬减轻大鼠心肌缺血再灌注损伤
胡晶晶 周伟 胡笑容
(1.钟祥市人民医院心内科,湖北 钟祥 431900;2.武汉大学中南医院,湖北 武汉 430071)
心肌梗死后再灌注治疗是治疗心梗最有效的方法,而再灌注损伤很大程度地限制了再灌注治疗的疗效。心梗后自主神经失衡,表现为交感神经过度激活,迷走神经活性相对减弱是加重心肌损伤和恶性心律失常的重要原因,而再灌注治疗不能降低交感神经活性。研究[1]证实,迷走神经刺激可以通过增加迷走活性,相对抑制交感神经活性减轻心肌缺血再灌注(ischemiaandreperfusion,IR)损伤。因此抑制交感活性可能是治疗心肌缺血再灌注损伤的可靠手段。肾交感消融(renalsympathetic denervation,RSD)是降低心脏交感活性的有效方法[2],与左侧星状神经节消融为目前临床研究最多的心交感神经消融方法,二者均可治疗高血压和特定类型的室性心律失常,如儿茶酚胺敏感型室速。RSD与心肌损伤研究鲜有报道,前期的研究[3]证实,RSD可以显著抑制心梗模型中心交感活性和心肌氧化应激水平。本研究主要探讨RSD对大鼠IR损伤的影响及可能机制。
1 材料与方法
1.1实验分组与动物模型建立 18只18~20周龄雄性SD大鼠,体质量180~200 g,购于湖北省疾控中心。根据随机数字表分为3组:假手术组,(SO组):大鼠开腹暴露双侧肾脏,45 min后开胸、前降支下穿线不结扎;缺血再灌注组(IR组):大鼠麻醉后开腹暴露双侧肾脏,45 min后开胸,结扎LAD 30 min,再灌注4 h;RSD+IR组:大鼠麻醉后开腹,暴露双侧肾脏,行RSD,RSD成功后等待30 min开胸,结扎LAD 30 min,再灌注4 h。
1.2RSD 暴露双侧肾脏后,剪断肾门和肾动脉所有可见神经纤维,为保证RSD效率,用棉签蘸取10%乙醇苯酚溶液湿敷肾门和肾动脉15 min。
1.3建立动物模型 大鼠采用2%苯巴比妥钠腹腔麻醉(45 mg/kg),将大鼠仰卧位固定于恒温板上,剔除颈部、胸部和内侧腹部毛发,在环状软骨下2节气管插管(70 bpm,吸呼比1∶1.5,潮气量1 mL)。沿腹部切口分离双侧肾脏,后沿左侧胸部切口暴露心脏,剪开心包膜,在左心耳下2 mm处将LAD与中空带凹槽的乳胶管结扎,结扎后远处心肌变白表明结扎成功,缺血30 min后,剪断结扎线,再灌注4 h。
1.4ELisa 检测血清肌钙蛋白I(cardiac troponin I,cTnI)和肌酸激酶同工酶(creatine kinase-MB,CK-MB)评价心肌损伤情况,检测心肌组织间NE(interstitial norepinephrine,iNE)浓度,评价交感神经活性。经大鼠颈静脉采血,离心(3 000 r×15 min)后取上清检测。采用Elabscience公司试剂盒,严格按照说明书操作。检测范围:CK-Mb:31.25~2000 pg/mL;cTnI:31.25~2000 pg/mL;iNE:0.31~20 ng/mL。
1.5生物化学检测法 检测缺血区心肌(梗死心肌周围5 mm内)超氧化物歧化酶(SOD)、丙二醛(MDA)和总抗氧化能力(T-Aoc),评价心肌组织氧化应激水平和抗氧化能力。选用南京建成生物工程研究所试剂盒,严格按照说明书操作。
1.6Western blot法 检测缺血区心肌Beclin-1、LC3- Ⅱ评价心肌细胞自噬水平。匀浆后测定总蛋白浓度,每孔上样量为40 μg,跑胶、转膜后,与一抗(Beclin-1:1∶500稀释,Abcam;LC3:1∶500稀释,北京博奥森生物技术有限公司)4℃孵育过夜,与相应的二抗孵育后,ECL法显色。

2 结 果
2.1心肌损伤 与SO组比较,IR组血清CK-Mb和cTnI表达均显著增加。与IR组比较,RSD可以显著降低血清CK-Mb和cTnI的表达。见表1。

表1 血清CK-Mb、cTnI及心肌组织iNE的表达
2.2心肌组织NE浓度 与SO组比较,IR组心肌组织中NE浓度显著增加;与IR组比较,RSD组中NE浓度显著降低。见表1。
2.3心肌氧化应激水平 与SO组比较,IR组缺血区心肌组织氧化应激水平(MDA)显著增加,抗氧化能力(SOD,T-Aoc)显著减弱;与IR组比较,RSD可以减轻缺血区心肌组织氧化应激水平,增加抗氧化能力。见表2。

表2 心肌MDA表达以及SOD和T-Aoc活性
2.4心肌自噬水平 与SO组比较,IR组中Beclin-1表达水平(0.75±0.11 VS 0.18±0.024,P<0.05)和LC3-Ⅱ(0.32±0.048 VS 0.087±0.0068,P<0.05)显著增加;与IR组比较,RSD可以显著抑制Beclin-1的表达(0.47±0.051,P<0.05)和LC3- Ⅱ(0.21±0.032,P<0.05)的表达。见图1,表3。
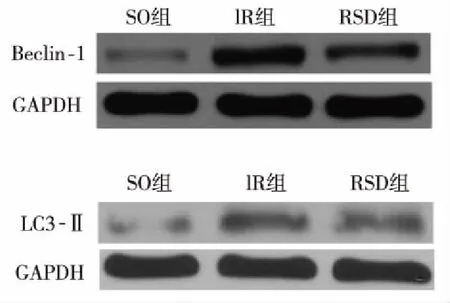
图1 Beclin-1和LC3-Ⅱ相对表达量

表3 心肌组织Beclin-1和LC3-Ⅱ相对表达
3 讨 论
RSD为心交感消融的有效方法,前期大量研究[4-5]表明,RSD可以通过抑制心交感过度激活降低患者血压以及缺血后房性、室性心律失常以及心衰的发生。RSD可以通过下丘脑室旁核,延髓头端腹外侧,双侧星状神经节支配心脏交感活性。我们前期研究证实,RSD可以显著抑制心梗后左侧星状神经节活性,即心交感活性,抑制室性心律失常的发生。本研究发现,RSD可以显著抑制心肌组织NE水平,进一步印证了RSD为心交感消融的有效方法,可以显著抑制IR中心交感过度激活。
交感过度激活是加重心肌IR损伤的重要因素,前期B.Buchholz等[6]研究证实,通过长时间低强度迷走神经刺激可以激活交感神经,进而加重心肌IR损伤,而这种作用可以完全被倍他乐克阻断。组织中过高浓度的NE也是加剧IR损伤的重要因素,血清中NE浓度的过高也提示了不良预后[7-8]。本研究发现RSD可以显著抑制心肌IR损伤,降低组织NE浓度,因此我们推测,RSD可以通过抑制交感活性和NE浓度减轻心肌IR损伤
心肌缺血时,氧供中断、ATP耗竭,为保证机体所需,交感激活,增加心肌收缩力和心率,进一步加剧耗氧,导致心肌抗氧化能力耗竭,再灌注时富氧血流再通,引起局部心肌氧化/抗氧化失衡,氧化应激水平激增。过高的氧化应激水平可以持续开放线粒体膜通透性转换孔,诱导线粒体肿胀破裂,呼吸链中活性氧大量释放,进一步加重氧化应激。有研究表明,离断交感神经可以减轻肝脏IR中氧化应激水平[9]。NE可以通过NADPH途径诱导外周血单核细胞产生活性氧[10]。RSD减轻脑中氧化应激水平[11],肾盂积水模型中,肾脏的氧化应激水平[12]。结合本研究结果我们推测,RSD可以通过抑制交感过度激活和组织中NE表达减轻大鼠心肌氧化应激水平,增加抗氧化能力。
自噬是心肌IR损伤的重要机制,目前普遍认为在缺血期自噬可以清除受损蛋白和细胞器,促进细胞存活,为保护机制,而再灌注时,由于自噬过度激活,可以促进细胞凋亡,为损伤机制。自噬可分为巨自噬、微自噬和分子伴侣介导的自噬,其中巨自噬为自噬的主要形式,损伤的细胞器或者大分子蛋白被双层质膜包裹形成自噬小体,与溶酶体结合降解。目前认为VPS34-VPS15-Beclin-1复合物是激活自噬小体形成的关键酶复合物,其参与了磷脂酰肌醇(PI)磷酸化形成PI3P,而PI3P为形成自噬小体的必需物质。LC3-Ⅱ泛素化复合物是自噬小体形成的另一个重要介质,LC3-Ⅱ分布在自噬小体上,与溶酶体结合后降解,因此LC3-Ⅱ反应了自噬的水平。本研究发现RSD可以显著抑制心肌组织Beclin-1的表达,降低LC3-Ⅱ的表达即抑制细胞巨自噬的水平。氧化应激可以通过多种途径调节自噬水平,研究表明,过量活性氧可以通过抑制PI3K-Akt-mTOR通路、激活AMPK通路、抑制Atg活性等引起细胞内Beclin-1和LC3-Ⅱ的聚集,激活自噬[13]。因此我们推测RSD可以通过抑制氧化应激减轻心肌自噬水平。
综上所述,RSD为心脏交感神经消融的有效方法; RSD可以通过抑制交感神经活性减轻大鼠心肌氧化应激和自噬水平,进而减轻大鼠心肌IR损伤; RSD减轻大鼠心肌自噬可能与抑制氧化应激有关。

