谷赖胰岛素治疗胰岛素抗体阳性糖尿病患者的效果分析
姜立娟 宗 琦 赵 冉 车选强
济南市第五人民医院内分泌科,山东济南 250022
胰岛素在临床中应用是糖尿病治疗历史上的重大突破,目前仍是临床上广泛应用的降糖药物。胰岛素的研发经历了两个飞跃,一是从动物胰岛素到基因重组人胰岛素,从而解决了动物胰岛素带来的过敏以及免疫性胰岛素抵抗等不良反应;二是胰岛素类似物的出现,使其药代动力学更接近人体生理性胰岛素的分泌,大大减少了临床上低血糖事件的发生。目前,临床中应用的速效胰岛素类似物主要有赖脯胰岛素、门冬胰岛素及谷赖胰岛素,且这三种胰岛素类似物都能应用于胰岛素泵[1]。本文对我院诊治的4例抗人胰岛素抗体(insulin autoantibody,IAA)阳性的住院糖尿病患者在胰岛素泵中应用谷赖胰岛素治疗的情况进行分析与总结,现报道如下。
1 临床资料
1.1 一般资料
4例抗人IAA阳性糖尿病患者患者的一般资料如表1所示,其中男女各2例,年龄分别为54、65、78和81岁,2型糖尿病3例,1例为成人隐匿性自身免疫性糖尿病(latent autoimmune diabetes in adults,LADA)。4例患者糖尿病的病程分别为8、3、30及20年,且体重指数(BMI)均未超重。入院时查糖化血红蛋白(HbA1c)均>8.5%,IAA滴度较正常值均明显升高。
1.2 治疗与结果
病例1:入院前在家中应用降糖方案为门冬胰岛素30注射液(商品名:诺和锐30)早20U、晚18U(餐前皮下注射),阿卡波糖50mg(3次/d)和二甲双胍0.5g(2次/d)。入院时追问病史,患者血糖波动大,且自测有出现低血糖(<3.9mmol/L),故入院后停用二甲双胍,改用谷赖胰岛素装入胰岛素泵中治疗,胰岛素起始基础剂量为12U,三餐前追加剂量各4U,继续应用阿卡波糖。结果发现患者入院后第3天血糖开始升高;第4天谷赖胰岛素基础剂量加量至16U,三餐前追加剂量加量至6U,结果发现第5、6天空腹及三餐后血糖不但没有下降,反而急剧上升。第7天改为门冬胰岛素装入胰岛素泵中治疗后,患者空腹及三餐后血糖迅速下降,血糖稳定达标后将门冬胰岛素基础剂量调整为14U,三餐前追加剂量各4U,较谷赖胰岛素总量明显减少,结果见图1。
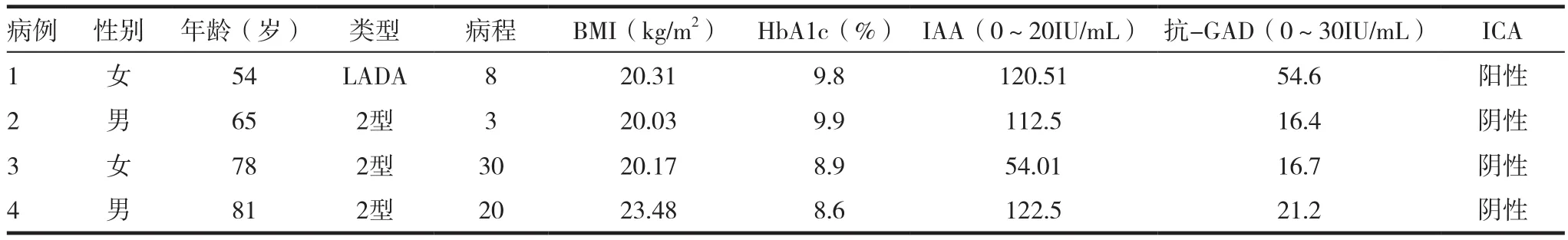
表1 4例抗人IAA阳性糖尿病患者的一般资料
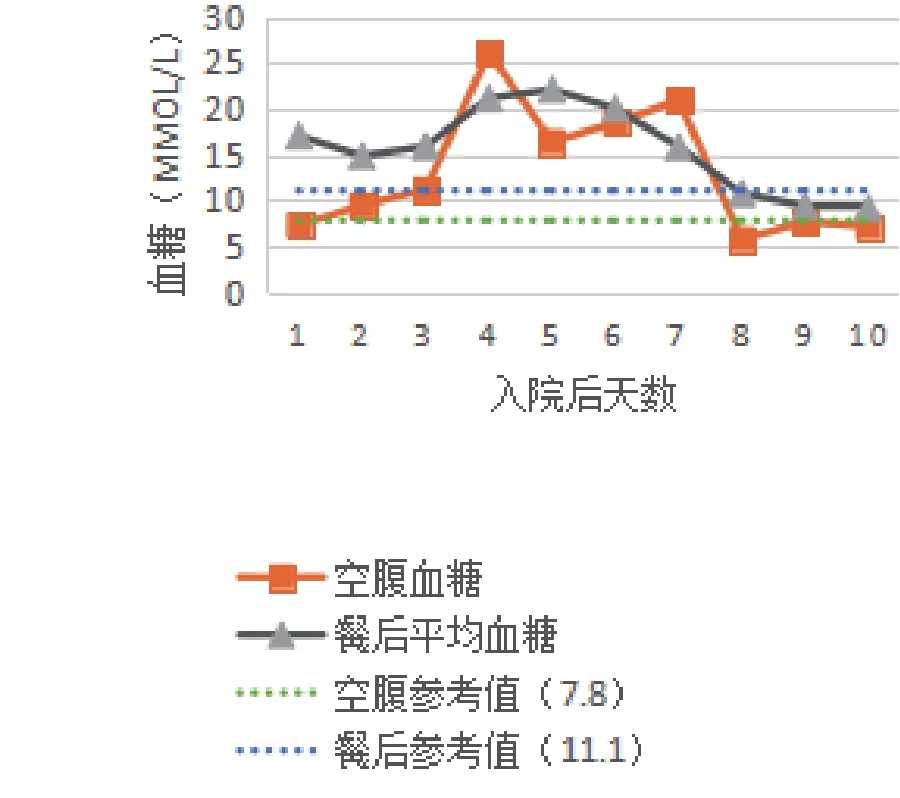
图1 病例1血糖变化情况
病例2:入院前在家中应用降糖方案为精蛋白生物合成人胰岛素注射液预混50R(商品名:诺和灵50R)早20U、晚10U(餐前30min皮下注射),阿卡波糖50mg(3次/d)。入院时追问病史,患者血糖波动大,入院后检测HbA1C明显升高,改用谷赖胰岛素装入胰岛素泵中治疗,胰岛素起始基础剂量为16U,三餐前追加剂量各5U,继续应用阿卡波糖。结果发现患者入院后第3天血糖开始升高,第4、5天血糖急剧上升;第6天谷赖胰岛素基础剂量加量至18U,三餐前追加剂量加量至7U,结果发现患者第6、7天空腹及三餐后血糖仍持续处于高水平状态。第8天改为门冬胰岛素装入胰岛素泵中治疗后,患者空腹及三餐后血糖迅速下降,血糖稳定达标后将门冬胰岛素基础剂量调整为16U,三餐前追加剂量分别为5、6、6U,较谷赖胰岛素总量明显减少,结果见图2。
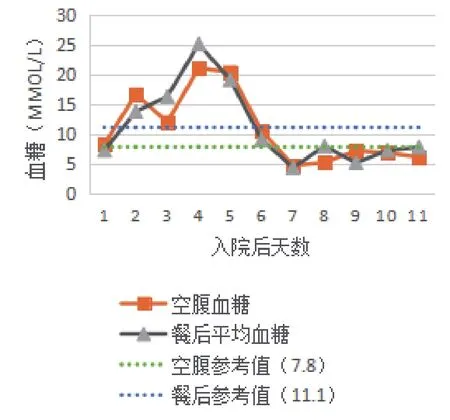
图2 病例2血糖变化情况
病例3:入院前在家中应用降糖方案精蛋白锌重组人胰岛素混合注射液(商品名:优泌林70/30)早18U、晚16U(前30min皮下注射),阿卡波糖50mg(3次/d)。入院时,患者诉在家空腹血糖为8mmol/L,未监测餐后血糖,入院后应用谷赖胰岛素装入胰岛素泵中治疗,胰岛素起始基础剂量为16U,三餐前追加剂量各4U,继续应用阿卡波糖。结果发现患者入院后第2天血糖开始明显升高,第3天谷赖胰岛素加量后血糖仍持续在高水平状态,家属要求第4天停用谷赖胰岛素,改用门冬胰岛素装入胰岛素泵中治疗后,患者空腹及三餐后血糖迅速下降,血糖稳定达标后门冬胰岛素基础剂量调整为16U,三餐前追加剂量各4U,较谷赖胰岛素总量明显减少,见图3。
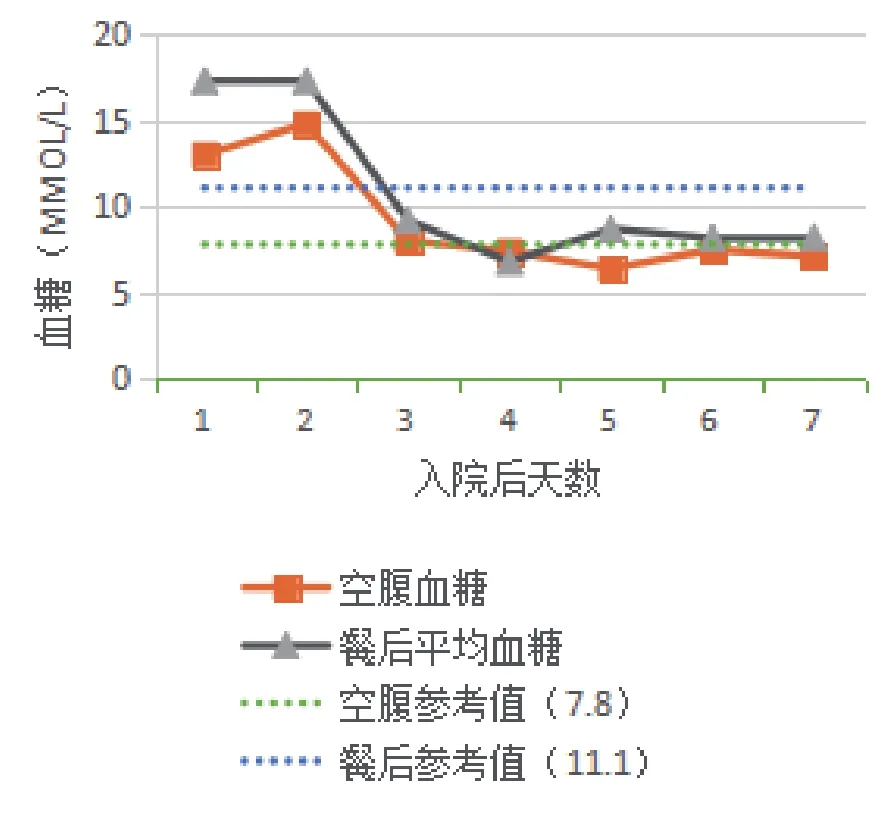
图3 病例3血糖变化情况
病例4:入院前在家中应用降糖方案为门冬胰岛素30注射液(商品名:诺和锐30)早20U、晚16U(餐前皮下注射),阿卡波糖100mg(3次/d)和二甲双胍0.5g(2次/d)。入院时询问病史,患者在家中空腹血糖控制在7~9mmol/L,未监测餐后血糖,未发现低血糖,入院后给予患者谷赖胰岛素装入胰岛素泵中治疗,胰岛素起始基础剂量为16U,三餐前追加剂量各4U,继续口服降糖药物。结果发现患者入院后第3、4天血糖开始升高,第5天谷赖胰岛素基础剂量加量至20U,三餐前追加剂量加量各6U,第6天空腹及三餐后血糖仍持续升高。第7天改为门冬胰岛素装入胰岛素泵中治疗后,患者空腹及三餐后血糖迅速下降,血糖稳定达标后门冬胰岛素基础量调整为18U,三餐前追加剂量分别为4、4、3U,较谷赖胰岛素总量明显减少,结果见图4。
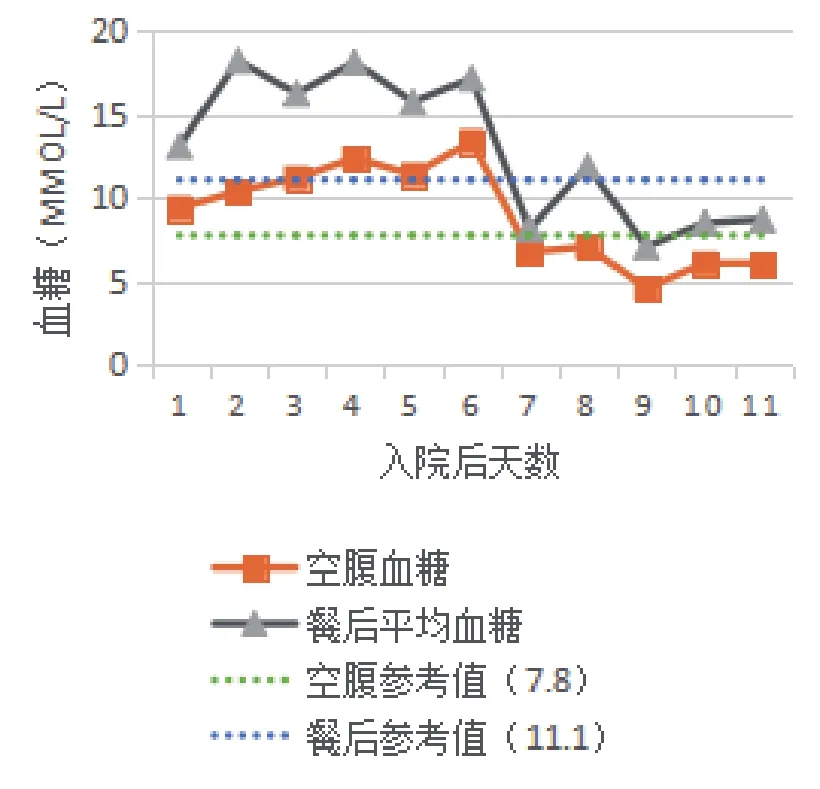
图4 病例4血糖变化情况
2 讨论
糖尿病患者最主要的三个特征是慢性高血糖、低血糖和血糖的波动[2],不论是空腹血糖还是餐后高血糖,慢性高血糖都是糖尿病并发症的重要危险因素[3]。然而,数据显示餐后高血糖更是糖尿病远期并发症的独立危险因素[4]。降低餐后血糖可降低微血管和大血管并发症的发生[5]。低血糖是糖尿病治疗过程中常见问题,若未及时给予纠正,可导致患者发生严重的心律失常、急性心肌梗死、不可逆的脑损伤,甚至危及患者的生命安全[6]。因此,低血糖的出现也是临床中控制血糖难以达标的原因之一。此外,血糖的波动也与心血管疾病的发生风险密切相关。
目前,临床主要应用的降低餐后血糖的胰岛素有胰岛素类似物和常规人胰岛素。研究表明,速效胰岛素类似物和重组人胰岛素比较,不仅可以较好地改善1型糖尿病患者的HbA1C,减少严重低血糖的发生率[7],而且还能在2型糖尿病患者基础-餐时强化治疗方案中对HbA1C及餐后血糖的改善更显著[8]。自1996年第一个速效胰岛素类似物——赖脯胰岛素在美国上市以来,随后几年时间内门冬胰岛素和谷赖胰岛素先后上市。谷赖胰岛素由于本身的独特分子结构,目前在临床上已得到广泛应用。
谷赖胰岛素是用赖氨酸代替B链第3位天门冬氨酸,谷氨酸代替B链第29位赖氨酸,形成其独特的分子结构,且B29位的谷氨酸可以与A链N端相连,增加单体稳定性。谷赖胰岛素溶液中采用聚山梨醇酯20作为稳定剂,而不是锌离子,其在溶液中主要以单体和二聚体形式存在,溶液中的状态以解离平衡为主[9],且这种无锌结构能使胰岛素迅速解离为单体,更快吸收[10],更好地模拟人正常生理状态下胰岛素的分泌[11]。谷赖胰岛素和赖脯胰岛素、门冬胰岛素在控制HbA1c、出现低血糖(尤其是夜间低血糖及严重低血糖)方面没有明显差异[12]。有研究提示,谷赖胰岛素和赖脯胰岛素应用胰岛素泵治疗的稳定性较门冬胰岛素略差,堵管的频率更多[13]。但也有研究表明,这三种胰岛素用于胰岛素泵治疗,对HbA1c的改善、严重的低血糖以及堵管的频率无显著性差异[14]。但谷赖胰岛素由于其特殊无锌分子结构,吸收更快,对餐后血糖较门冬胰岛素有更快的降糖效应[15],且能缓解其他胰岛素由于锌所致的过敏反应。
目前,国内外文献尚无应用谷赖胰岛素治疗IAA阳性糖尿病患者的相关报道,本文通过分析报道谷赖胰岛素安装入胰岛素泵治疗4例IAA阳性的糖尿病患者,结果发现谷赖胰岛素无效或疗效极差。因为目前收集到的病例数少,希望学者在今后的研究中对这部分病例进行关注,进一步证实该结果的可靠性,从而深入探讨出现这种结果的原因。

