高龄急性冠脉综合征患者经皮冠状动脉介入治疗后接受6 个月的双联抗血小板的临床疗效分析
赵久平,邓慧君,孟令东
(青海红十字医院心血管内科,西宁 810000)
与稳定性缺血性心脏病患者相比,患有急性冠状动脉综合征(acute coronary syndrome,ACS)的患者复发性缺血事件的风险更高[1]。因此,美国心血管学会/美国心脏协会(ACC/AHA)标准指南建议除非有出血风险过高等禁忌症,在ACS 患者中使用阿司匹林和P2Y12抑制剂的双联抗血小板治疗(dual antiplatelet therapy,DAPT)12 个月或更长时间[2]。然而,在临床实践中占ACS 的大部分患者,特别是75 岁及以上的老年人,在为指南提供证据的随机试验中,由于代表性不足往往被排除在外。这类患者通常更容易受到抗血栓药物负荷剂量的不良影响。最值得注意的并发症之一是出血,其与住院时间延长和死亡率增加有关[3]。但是,除接受溶栓治疗的患者外,所有年龄段在指南中的建议均相同。虽然,越来越多的研究集中于老年患者的抗血小板治疗,如Elderly-ACS 研究和POPular AGE 研究[4-5]。然而,对于接受PCI 治疗的75 岁及以上的高龄ACS 患者,关于DAPT 的有效性和安全性的数据有限。因此,本研究试图在75 岁及以上的ACS 患者中评估6 个月DAPT 的临床疗效,旨在确定DAPT 是否适合该类人群。
1 资料与方法
1.1 一般资料在2014 年1 月~2017 年12 月期间,选择在本院接受药物洗脱支架治疗且符合所有入选标准的75 岁及以上ACS 患者作为研究对象。根据欧洲心脏病学学会、欧洲心胸外科协会的最新建议,患者必须在冠状血管中至少有一个病灶,参考直径为2.25~4.25 mm,并且通过视觉评估,狭窄超过50%,适用于经皮冠状动脉介入治疗支架[6]。纳入标准:(1)符合ACS 诊断标准;(2)目标病变必须可接受PCI 治疗。排除标准:(1)已知患者对以下任何药物过敏或禁忌症:肝素、阿司匹林、氯吡格雷、依维莫司、唑他罗非司和造影剂;(2)活动性病理性出血患者;(3)前3 个月内胃肠道或泌尿生殖道出血,或2 个月内大手术;(4)有出血史,已知凝血障碍(包括肝素诱导的血小板减少),或拒绝输血。
1.2 方法所有患者均根据标准技术采用第二代药物洗脱支架进行经皮冠状动脉介入治疗。手术过程中采用普通肝素或低分子肝素抗凝。所有患者在经皮冠状动脉介入治疗前至少12 小时口服300mg 阿司匹林和300mg 或600mg 氯吡格雷。手术后,根据首次接触药物24 小时内接受的抗血小板治疗的类型和剂量,将患者分为2 组:仅服用阿司匹林(阿司匹林组),同时服用阿司匹林和P2Y12 受体抑制剂(DAPT 组)。阿司匹林组每日一次口服100mg 阿司匹林,DAPT 组在阿司匹林组的基础上维持使用替格瑞洛(每日两次口服90mg)或氯吡格雷(每日一次口服75mg)。手术后,所有患者遵循标准的ACC/AHA3 指南接受最佳药物治疗[2]。在经皮冠状动脉介入治疗后1、3 和6 个月进行临床随访(电话和门诊复诊随访),记录患者的数据,包括结果事件和不良事件,评估阿司匹林或P2Y12 抑制剂的使用信息。
1.3 结局指标研究的主要终点是两个治疗组的6 个月无事件生存率(心脏死亡、心肌梗死、血运重建和大出血)。次要终点包括全因死亡、心脏死亡、非致命性心肌梗死、冠状动脉血运重建、明确或可能的支架血栓形成以及主要出血事件。主要心血管不良事件的具体定义如下[7]:心肌梗死定义为心肌酶(心肌肌钙蛋白或肌酸激酶的心肌带分数)高于参考上限,伴有缺血症状或心电图表现,表明缺血与指数经皮冠状动脉介入治疗无关。血运重建定义为任何一种临床指示经皮或外科冠状动脉血运重建。根据学术研究联合会(ARC)的定义,支架血栓形成定义为明确或可能的支架内血栓形成。根据出血学术研究联合会(BARC)的标准对出血事件进行分类。
1.4 数据分析连续变量表示为平均值±标准差。分类变量用百分比表示。根据是否呈正态分布,连续变量采用学生t 检验或Wilcoxon 检验进行比较。分类变量采用卡方检验或Fischer 精确检验进行比较。获得在分析中考虑的每个组或亚组的无事件存活的Kaplan-Meier曲线,并通过对数秩检验进行比较。P 值<0.05 认为具有统计学意义。所有统计分析均使用SPSS19.0 进行。
2 结果
2.1 患者的基线特征在研究期间,共招募了540 名患者。其中,135 名患者分配接受阿司匹林治疗,405名患者分配接受DAPT 治疗。两组患者在所有基线人口学和临床特征方面保持平衡。两组的血管造影和手术数据也相似。总的来说,超过25%的患者患有糖尿病,超过30%的患者为急性STEMI,近50%的患者患有多支血管疾病,约60%的患者接受了左主干或左前降支病变的治疗。根据随机方案,三分之一的患者植入依维莫司洗脱支架、佐他罗莫司洗脱支架和biolimus洗脱支架。阿司匹林组的中位持续时间为184 天(IQR 177~236)或6.1 个月(IQR 5.9~7.9),DAPT 组为191 天(178~260)或6.3 个月(5.6~8.1)。
2.2 临床结局在整个研究人群中,DAPT 组的6 个月内有效性结局发生率远高于阿司匹林组(MACE:3.0% vs. 0.7%;全因死亡:2.7%vs. 0.7%,均P=0.010)(表1),主要原因是心脏死亡发生率较高。与阿司匹林组相比,DAPT 组的主要不良心脑血管事件(MACE)和全因死亡的累积危险性也更高(图1A、B)。在多变量校正分析中,服用DAPT 与6 个月内MACE(HR=1.67,95%CI=1.14-2.45,P=0.011)(表2)。

表1 两组6个月时的临床主要和次要结果,n(%)
DAPT 组在出院后6 个月内的大出血和所有出血事件的发生率明显高于阿司匹林组(大出血:6.2% vs.2.2%,P<0.001;所有出血:10.6% vs. 5.2%,P<0.001)(表3)。在Kaplan-Meier 曲线中可以发现DAPT 组出血的更高累积风险(图1C、D)。在多变量分析中,DAPT 与出院后6 个月大出血相关(HR=2.34,95%CI=1.75-3.13,P<0.001)(表3)。
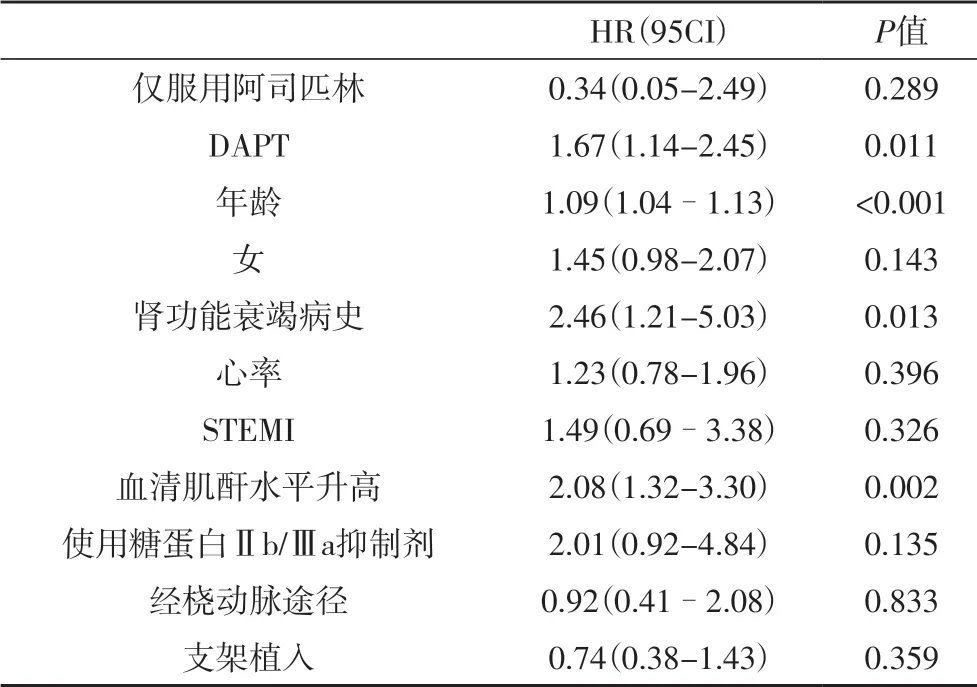
表2 出院后6个月内MACE的独立预测因子

图1 出院后6个月有效性和安全性结果的累积kaplan-meier曲线评估。(A)MACE,(B)全因死亡,(C)大出血,(D)全部出血
3 讨论
衰老导致一系列的生理变化和共病,使老年患者更容易出现副作用,降低了可预测的有效性[8]。在当前的临床实践中,所有ACS 患者,不论年龄大小,都建议在PCI 治疗后接受抗血小板药物的标准治疗。然而,75 岁及以上的患者往往被低估甚至排除在随机试验之外。以前的研究已经确定老年患者具有独立的出血风险,所有抗血小板药物都会不同地增加与年龄相关的主要出血风险[3]。因此,当老年ACS 患者在接受DAPT时,他们可能处于最高的出血风险。此外,很少有研究评价DAPT 的有效性和安全性。在阿司匹林和P2Y12受体抑制剂的负荷剂量指南中,大多数建议都是基于观察数据和专家的意见,因为没有对照试验可用于指导这一策略。大多数P2Y12 受体抑制剂的研究评估了DAPT 与单用阿司匹林的有效性,但是很少有研究探讨DAPT 对75 岁以上患者的影响。在这项试验中,我们比较了75 岁及以上ACS 患者接受单用阿司匹林与DAPT 的临床疗效,结果显示在出院后6 个月,使用阿司匹林和P2Y12 受体抑制剂的DAPT 治疗可显著增加大出血的风险,但与降低MACE 的风险无关。

表3 出院后6个月内大出血的独立预测因子
关于ACS 中阿司匹林负荷剂量的建议最初来自只有阿司匹林可用于口服抗血小板治疗的时期,并且很少有研究评估负荷剂量与急性期非负荷剂量相比的影响。大多数关于P2Y12 受体抑制剂的研究评估了DAPT(氯吡格雷加阿司匹林)与单用阿司匹林的有效性。只有1 项注册研究比较了75 岁以上患者使用氯吡格雷负荷剂量与标准剂量的效果;但是,该研究未提及使用阿司匹林[9]。本研究中540 名患者的相对较小的样本量可能无法在早期并发症中检测到统计学意义。因此,老年患者是否需要使用DAPT 是基于相对有限的证据。
在本研究中,单用阿司匹林与DAPT 相比,符合非劣效性。然而,考虑到6 个月的DAPT 的主要终点的实际发生率为3.0%,非劣效性界限似乎较宽,但是主要试验的非劣效性界限与本研究相似,甚至比本研究更宽(3.7%)[10]。值得注意的是,本研究发现DAPT 组大出血的发生率高达6.2%,而单用阿司匹林组为2.2%。出血对老年患者尤其危险,因为出血可能导致患者死亡[11]。此外,出血还可能导致缺血性事件的发生,因为当大出血发生时,抗血栓治疗可能会停止[12]。因此,本研究不能得出结论:DAPT 在接受当前药物洗脱支架经皮冠状动脉介入治疗的75 岁及以上ACS 患者中是安全的。
总之,本研究表明,在接受PCI 治疗的75 岁及以上的ACS 患者中,DAPT 治疗与大出血风险增加相关,但与MACE 风险降低无关。

