总蛋白、白蛋白在新型冠状病毒肺炎患者肝功能损伤诊断中的应用价值
徐亚林 张梦晗 杨群 马梦兰 李澄 张亚丽
新型冠状病毒肺炎(简称新冠肺炎)是由一种新型β属冠状病毒感染导致的传染病,目前已在全球多个国家蔓延,对人民生命健康造成了严重威胁[1]。2020年1月12日,世界卫生组织(World Health Organization,WHO)将导致新冠肺炎的新型冠状病毒命名为2019新型冠状病毒(2019 novel coronavirus,2019-nCoV),2月11日,WHO宣布将2019-nCoV引起的疾病命名为“COVID-19”。2月12日,国际病毒分类委员会(International Committee on Taxonomy of Viruses,ICTV)宣布2019-nCoV的正式分类名为严重急性呼吸综合征冠状病毒2(severe acute respiratory syndrome coronavirus 2,SARS-CoV-2)。2019-nCoV的迅速传播引起了全世界的关注,WHO已将其列为国际关注的突发公共卫生事件。
新冠肺炎作为一种新出现的疾病,因其传染性较强而被广泛关注,且针对该疾病目前还没有特效治疗药物[2]。虽已有部分学者研究并报道了其临床特征,但总体来说,人们对新冠肺炎的认识仍严重不足,只能基于实践和科学研究不断更新诊断及治疗方法。我国已将新冠肺炎纳入《中华人民共和国传染病防治法》规定的乙类传染病,并采取甲类传染病的预防、控制措施。目前国家卫生健康委员会(卫健委)发布的新冠肺炎诊疗方案已更新至第七版,规范诊治是提高治愈率、降低病死率的关键[3]。赤壁市蒲纺医院是湖北省赤壁市新冠肺炎定点救治医院,本研究分析我院新冠肺炎确诊患者的常规血生化检查结果,旨在探讨血浆总蛋白(total protein,TP)和白蛋白(albumin,ALB)在新冠肺炎患者肝功能损伤诊断中的应用价值,现将结果报告如下。
1 资料与方法
1.1 研究对象
1.1.1 标本来源 本院自2019年12月21日起收治新冠肺炎确诊患者25例(包括重症患者1例),其中男性14例(占56.0%),女性11例(占44.0%),年龄22~57岁,平均(42.5±11.3)岁。
1.1.2 诊断标准[4-5]新冠肺炎确诊病例或疑似病例为具备以下病原学证据之一者:① 呼吸道标本或血液标本经反转录-聚合酶链反应(reverse transcription polymerase chain reaction,RT-PCR)2019-nCoV核酸检测呈阳性;② 呼吸道标本或血液标本病毒基因测序与已知的2019-nCoV高度同源。
1.1.3 呼吸道症状 25例(100.0%)患者均有发热、咳嗽,18例(72.0%)患者呼吸频率明显加快。
1.1.4 消化道症状 7例(28.0%)患者出现腹泻,24例(96%)患者出现食欲减退。
1.1.5 流行病学 25例(100.0%)患者均有武汉地区旅游居住史或有新冠肺炎确诊患者接触史,其中23例(92.0%)去过武汉,2例(8.0%)接触过武汉返乡人员。患者潜伏期2~14 d。
1.2 仪器与试剂 一次性真空采血管(批号:20190422,产品注册证号:赣械注准20152410066)由江西格兰斯医疗器械有限公司提供;Randox质量控制(质控)血清(中值质控血清型号HN1530,批号1284un;高值质控血清型号HE1532,批号981un)由英国朗道实验室有限公司生产。Beckman Coulter AU 680型全自动生化分析仪购自美国贝克曼公司;所需配套试剂均由北京利德曼生化有限公司提供(生产许可证号:京食药监械生产许20000439号)。
1.3 检测方法 仪器日常维护保养状态正常,每日使用中、高值质控血清进行室内质控,结果稳定在控。采集所有患者空腹静脉血3 mL,经3 500 r/min(离心半径16.1 cm)离心10 min分离血清,使用原始管上机,严格按照试剂说明书进行检测。
1.4 观察指标 检测所有患者入院时(治疗前)以及治疗5 d(治疗后)的TP、ALB、丙氨酸转氨酶(alanine aminotransferase,ALT)、天冬氨酸转氨酶(aspartate aminotransferase,AST)、直接胆红素(direct bilirubin,DBil)、肌酐(creatinine,Cr)、二氧化碳结合力(carbon dioxide combining power,CO2CP)、尿酸(uric acid,UA)、总胆红素(total bilirubin,TBil)、血尿素氮(blood urea nitrogen,BUN)水平,比较上述指标治疗前后的变化。
1.5 伦理学 本研究符合医学伦理学标准,对患者的治疗和检测均参照国家卫健委实时发布的新冠肺炎诊疗方案,获得患者知情同意。
1.6 统计学方法 使用SPSS 17.0统计软件对数据进行分析,符合正态分布的计量资料以均数±标准差()表示,采用t检验;计数资料以例表示。P<0.05为差异有统计学意义。
2 结果
25例新冠肺炎患者治疗5 d后TP、ALB水平均较治疗前明显降低(均P<0.01),UA水平较治疗前明显降低(P<0.05);治疗5 d后患者ALT较治疗前有所升高,但差异无统计学意义(P>0.05);其余各指标治疗前后变化不大,比较差异均无统计学意义(均P>0.05)。见表1。
表1 25例新冠肺炎患者治疗前后常规血生化指标比较()
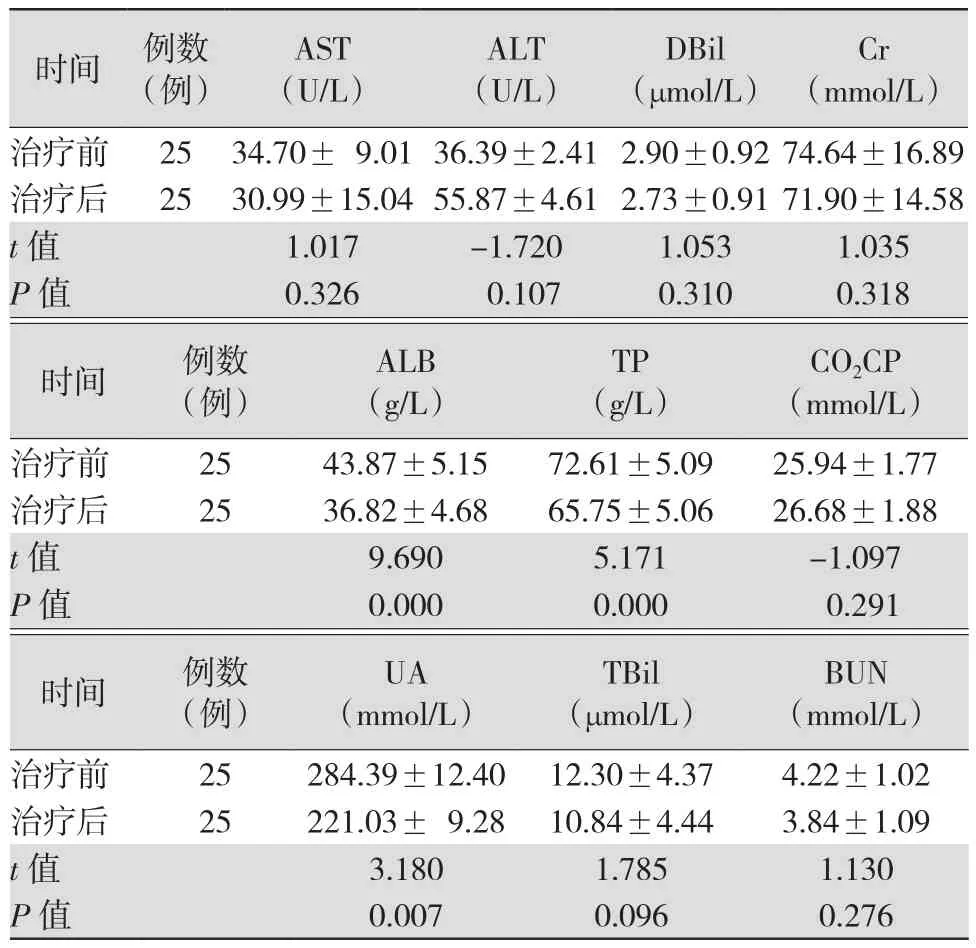
表1 25例新冠肺炎患者治疗前后常规血生化指标比较()
注:AST为天冬氨酸转氨酶,ALT为丙氨酸转氨酶,DBil为直接胆红素,Cr为肌酐,ALB为白蛋白,TP为总蛋白,CO2CP为二氧化碳结合力,UA为尿酸,TBil为总胆红素,BUN为血尿素氮
Cr(mmol/L)治疗前 25 34.70± 9.01 36.39±2.41 2.90±0.92 74.64±16.89治疗后 25 30.99±15.04 55.87±4.61 2.73±0.91 71.90±14.58 t值 1.017 -1.720 1.053 1.035 P值 0.326 0.107 0.310 0.318时间 例数(例)AST(U/L)ALT(U/L)DBil(μmol/L)CO2CP(mmol/L)治疗前 25 43.87±5.15 72.61±5.09 25.94±1.77治疗后 25 36.82±4.68 65.75±5.06 26.68±1.88 t值 9.690 5.171 -1.097 P值 0.000 0.000 0.291时间 例数(例)ALB(g/L)TP(g/L)BUN(mmol/L)治疗前 25 284.39±12.40 12.30±4.37 4.22±1.02治疗后 25 221.03± 9.28 10.84±4.44 3.84±1.09 t值 3.180 1.785 1.130 P值 0.007 0.096 0.276时间 例数(例)UA(mmol/L)TBil(μmol/L)
3 讨论
目前所知冠状病毒仅感染脊椎动物,与多种疾病密切相关。有研究显示,血管紧张素转换酶2(angiotensin converting enzyme 2,ACE2)是冠状病毒感染的关键受体,只要表达ACE2受体的细胞均为冠状病毒的侵袭对象,ACE2在肺部、肝脏等器官中发挥重要作用[6]。多项研究表明,除常见的呼吸道症状(如咳嗽)和发热外,重型新冠肺炎患者常存在循环系统、消化系统、泌尿系统、神经系统等多器官病变,低氧血症引发的“细胞因子风暴”和多器官功能障碍综合征可导致包括肝肾损伤在内的其他症状[7-8]。本研究表明,新冠肺炎患者肝脏功能损伤在病程进展中十分明显。
4.1 肝脏合成除γ球蛋白以外的几乎所有血浆蛋白质,如ALB、纤维蛋白原、凝血因子和转运蛋白质等。在肝功能受损时蛋白质代谢发生异常,主要表现为血浆蛋白质含量降低,其降低程度取决于肝脏损伤类型、严重程度和持续时间[9],本组患者治疗后TP、ALB水平均明显低于治疗前,表明2019-nCoV感染后随着疾病进展患者肝功能出现不同程度的损伤,表现为肝脏合成蛋白质的能力下降,直接表现为血清蛋白水平进行性降低。
4.2 ALT是反映肝脏损伤的敏感指标,临床上主要用于肝脏疾病的诊断。发生急性肝损伤(如急性病毒性肝炎、药物或酒精中毒性肝炎)时,血清ALT水平可在临床症状(如黄疸)出现前就急剧升高。ALT和AST是临床应用最广泛的肝酶,当致病因子侵入肝脏时引起细胞变性,导致细胞膜通透性发生改变,即造成ALT升高。但当肝细胞线粒体被进一步破坏时才会引起AST升高,临床上ALT较为敏感,1%的肝细胞坏死即可使血清中ALT增加1倍,其升高程度与肝细胞受损程度有关。本组新冠肺炎患者治疗前后ALT和AST水平比较差异均无统计学意义,随病程进展,ALT呈升高趋势。由于本研究中新冠肺炎患者绝大多数为轻症(仅1例为重症),患者肝功能受损程度普遍较轻,因而肝脏酶学变化不显著,仅表现为ALT轻微升高,而AST变化不明显。
综上所述,新冠肺炎患者治疗前后常规血生化检验结果的变化可在一定程度上反映2019-nCoV对患者肝脏的损害程度,提示在新冠肺炎的临床治疗过程中要重视对肝功能的监测,加强对肝脏的保护,防止多器官并发症的发生,保证救治质量,有效提升救治水平和救治能力。
利益冲突 所有作者均声明不存在利益冲突

