牛血清白蛋白与二苯酮-4相互作用的荧光法研究进展
陈开意 何文妮 邵波


摘要:二苯甲酮类紫外吸收剂是一类应用较为广泛的防晒剂,其优点包括适用范围广,综合性能较好, 价格低廉等,在化妆品中被广泛地使用。但在人体和动植物体内,紫外防晒剂存在干扰内分泌系统,影响生殖发育系统等潜在危害。本实验的研究对象为典型的二苯甲酮类紫外吸收剂—二苯酮-4。利用荧光光谱法来探究BP-4作用于BSA时发生作用的荧光猝灭过程及结合点数、通过热力学参数来探究相互作用的作用力类型、用同步荧光法来探究相互作用的作用位点。结果表明,BP-4作用于BSA时的猝灭作用主要是静态猝灭过程,且与BSA有较强的结合能力,同时可以获得在不同温度下,猝灭过程的猝灭常数,计算了300k、305k、310k三个温度条件下的热力学参数ΔG、ΔH和ΔS,即获悉两者的作用过程是自发进行的,BP-4与BSA之间相互结合的作用力类型是范德华力和氢键作用。结论BP-4能与牛血清白蛋白发生结合作用。
关键词:牛血清白蛋白;二苯酮-4;荧光光谱
中图分类号:X57 文献标识码:A 文章编号:2095-672X(2020)10-0-03
DOI:10.16647/j.cnki.cn15-1369/X.2020.10.068
Abstract:Diphenylketone ultraviolet absorbent is a kind of widely used sunscreen, its advantages include wide range of application, better comprehensive performance, low price, etc., it is widely used in cosmetics.However, in biological bodies,ultraviolet sunscreen has some toxicological problems such as disrupting the endocrine system.The research object of this experiment is a typical ultraviolet absorbent of diphenylketone, diphenylketone -4.Fluorescence spectroscopy was used to explore the fluorescence quenching process and binding points of bp-4 when it ACTS on BSA, the types of interaction forces were explored by thermodynamic parameters,and the interaction sites were explored by synchronous fluorescence method.Results show that the BP - 4 ACTS on the quenching effect of BSA was mainly a static quenching process,and have strong ability of combining with BSA at different temperature can be obtained at the same time, the quenching constants of quenching process, calculates the 300 k, 305 k, 310k, three thermodynamic parameters of temperature, Δ H and Δ Δ G S, is aware of the role of the process is a spontaneous, BP - 4 type is the power of the combination between BSA and van der Waals force and hydrogen bond action. Conclusion bp-4 can bind to bovine serum albumin.
Key words:Organic UV filters;Benzophenone-4;Bovine serum albumin
1 概述
1.1 研究的背景與意义
近年来,防晒化妆品的使用日益增长,这使得防晒剂中的主要成分有机紫外吸收剂逐渐成了一种新型环境污染物,其环境污染问题在各国普遍存在[1]。有健康研究表明,部分有机紫外防晒剂对内分泌系统有干扰作用,并且会危害人体和生物体的生殖系统和遗传系统,不利于胚胎的发育以及出生后的发育,非但如此还会对人类身体健康造成潜在危害和对周边生态环境造成污染[2]。因此,有机紫外防晒剂被大家认定为一种新的内分泌干扰物质[3-4]。有机紫外线防晒剂是指能够吸收长波紫外线和中波紫外线的一类有机化合物,这些紫外线会晒黑甚至晒伤我们的皮肤[5]。紫外线吸收剂的分子都包含可以吸收波长小于400nm的紫外线的发色团,发色团为了实现紫外线屏蔽功能通过吸收紫外线并将其转换为热能,化学能或者其他非紫外线能。紫外线吸收剂的品种较多,在各种类型的有机紫外线防晒剂中,二苯甲酮类防晒剂拥有良好的性能,价格便宜和应用范围广,在紫外线吸收剂中占据着重要的地位[6]。由于有机紫外线防晒剂被广泛使用,因此,在使用过程中必须通过各种方式进入环境。另外,大多数紫外线防晒剂都是可以溶解在非极性溶剂,残留在环境中周期长,不易被降解。有机紫外线防晒剂有两种方式进入环境,分为直接方式和间接方式。其中直接方式包括通过废水排放防晒剂,将有机紫外防晒剂带入水生生态系统中,而间接方式包括通过每天洗涤,游泳,沐浴等途径带入水中。它们可以渗出皮肤或通过食物链进入人类身体。Janjua[7]等经过大量研究发现有机紫外防晒剂二苯酮-3和4-甲基苄亚甲基樟脑可以通过皮肤进入人体内,并计算出了人体血浆中含有的最大浓度分别为238 ng·mL-1和18 ng·mL-1。通过对二苯酮-4作用于BSA时的作用机理的研究,可以了解在生物体内血清蛋白与二苯酮-4之间的结合作用,而且对于现在的环境状况来说,有机紫外吸收剂与血清蛋白之间的相互作用的结果可以为环境污染的治理提供参考。总的来说,这个实验研究已经成为一个很有研究价值和意义的研究。
1.2 有机紫外防晒剂的毒性效应
有研究表明,有机紫外防晒剂有较高毒性,而且有机紫外防晒剂通常都还有不饱和链和苯环导致其残留在环境中难以降解,容易对环境造成持续影响。目前,有机紫外吸收剂存在于多种环境介质中,例如:大气生态系统,土壤生态系统,水生生态系统等等。Vila[8]等人经过检测得出BP-4 容易对藻类造成风险,而 BP-3 和 EHMC 则更容易对鱼类造成危害。另外,人体内也被不断检测出存在有机紫外防晒剂,证实了有机紫外防晒剂通过食物链的富集最终进入人体和动植物体内。已有报道指出,有机紫外防晒剂对人体和动物体的内分泌系统,生殖发育系统,遗传系统和神经系统等都有不同程度的不良影响。
1.3 二苯酮-4的性质
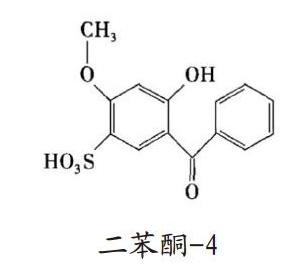
二苯酮-4(Benzophenone-4,)是一种奶白色至黄色的粉末,无气味。分子式是C14H12O6S,相对分子质量是308.04,溶解度为0.65。下图是其结构式,是一种常见的有机紫外防晒剂,属于水溶性化学防晒剂。
1.4 牛血清白蛋白的性质
牛血清白蛋白(bovine serum albumin),是一种乳白色的片状粉末。它的相对分子质量为104,血清蛋白是血液的主要成分,其分子量是68000,血清蛋白包含581个氨基酸组成,其中带有的17个二硫键是由35个半胱氨酸组成,而游离巯基组成第34个肽链,血清白蛋白能够和多种阴、阳离子以及小分子结构的物质结合在一起[9]。血液中的白蛋白主要有以下几种作用,维持渗透压、缓冲pH、承担载体和营养作用。在动物细胞无血清培养中,添加白蛋白可起到载体作用和生理和机械保护作用。
1.5 有机紫外吸收剂对生物大分子的研究
牛血清白蛋白是一种常用的载体蛋白,它在人体内的血液循环系统中起到贮存和运输物质的重要作用。将牛血清蛋白作为研究对象,探究其与内源或外源性物质相互联结而发生作用后的影響机理已成为生命科学、环境科学和临床医学研究的重要方向,血清白蛋白是血浆中含量最丰富的载体蛋白,它具备广泛的结合能力,同时具有很强的内源性荧光。外源性化合物与蛋白质份子相互感化会导致蛋白质的内源性荧光强度下降,这就说明其发生荧光猝灭[10]。目前荧光光谱法已成为研究某些物质作用于血清蛋白时的分子机理和作用程度的有效方法。敖俊杰[11]等人研究了三种常见的有机紫外防晒剂与牛血清白蛋白的相互作用的作机理通过荧光分光光度法。
本实验通过研究二苯酮-4与牛血清白蛋白相互作用来间接验证其对人体的影响。本文利用荧光分光光度法来探求二苯酮-4与BSA相互作用的机理,了解两者相互作用的猝灭机理;根据测定的数据来绘制荧光光谱图,分析结果可知二苯酮-4与牛血清蛋白相互作用的荧光猝灭规律以及相对应的猝灭常数,二苯酮-4与牛血清蛋白互相作用的作用力类型可以通过计算分析热力学参数来确定。这有利于让我们了解其在人体的分布情况和运输过程,对于我们认识紫外防晒剂的毒性有着非常重大的意义,同时这也有助于推动关于有机紫外防晒剂的生态毒性的研究进展。
2 实验部分
2.1 实验设备与材料
2.1.1 实验设备
荧光分光光度计:Rf-5301pc荧光分光光度计(日本日立)。
电子分析天平:al-204型(上海精密科学仪器有限公司)。
冰箱:bcd-216zdjJ型的冰箱(青岛海尔有限公司)。
电热恒温水槽:Dk-8D型数控超级恒温槽(上海森信实验仪器有限公司)。
纯水机:paoifio-t-2-20型。
pH计:phsj-4F型实验室pH计(上海仪电科学有限公司)。
常见玻璃仪器:玻璃棒,100mL,250mL容量瓶,1mL,5mL移液管
100mL烧杯。
2.1.2 实验材料
牛血清蛋白:购于上海如吉生物科技有限公司。
二苯酮-4:购于上海榕柏生物技术有限公司(100g,纯度>99%)。
2.2 试验方法
2.2.1 溶液配置方法
1×10-5mol/L BSA标准储备液体:用电子天平称取0.068g的牛血清白蛋白,用超纯水溶解在烧杯中,移入100m的容量瓶中,用超纯水稀释至刻度,摇匀,放置于4℃冰箱中进行保存。
1×10-4mol/L 二苯酮-4标准溶液:用电子天平准确称取0.0031g的二苯酮-4,溶于少量超纯水中,移入100mL容量瓶中,用超纯水稀释至刻度并摇匀,放置于4℃冰箱中进行保存。
0.2mol/L Tris-HCl缓冲溶液:准确称取24.228g的Tris药品倒入1L的大烧杯中,溶于超纯水中,将超纯水加至约700mL,用浓HCl调节pH至7.40±0.05,然后移入容量瓶中,用1 000mL超纯水定容稀释,摇匀,放置于室温下进行保存。
2.2.2 荧光猝灭实验
在10 mL比色管中分别加入2mL Tris-HCl 缓冲液、5mL的BSA溶液以及适量的二苯酮-4溶液,用超纯水定容并摇匀,使药物的最终浓度分别为0、0.9×10-6mol/L、1.8×10-6mol/L、2.7×10-6mol/L、3.6×10-6mol/L、4.5×10-6mol/L、6.3×10-6mol/L、7.2×10-6mol/L、8.1×10-6mol/L。将上述溶液置于恒温水槽中,水温分别调节为300、305、310K,在恒温条件下作用30min至平衡后测定其荧光光谱。将荧光分光光度计中发射波长参数设置为375nm,固定激发波长设置为285nm,狭缝宽度设置为10nm,然后测定在250~500nm这一范围区间内的发射光谱,将荧光强度最大时对应的发射波长记录下来[12]。
3 结果与讨论
3.1 二苯酮-4与BSA的相互作用的荧光光谱
3.1.1 二苯酮-4与BSA相互作用的猝灭机理
由于蛋白质大分子具有酪氨酸(Tyr)、色氨酸(Trp)等小分子结构,所以可以产生较强的内源性荧光。当蛋白质分子与外源性化合物互相作用时可能会降低蛋白质的内源性荧光强度。如下图所示,二苯酮-4(BP-4)于BSA相互作用产生的荧光光谱图。其中从B到J的药物浓度分别为0、0.9×10 -6、1.8×10-6 、2.7×10-6、3.6×10 -6 、5.4×10 -6 、7.2×10-6 、8.1×10-6、9.0×10 -6 mol/L,BSA的浓度始终为1×10-5 mol/L。由图1可见,向BSA 中加入 BP-4后,BSA在340nm 附近出现荧光峰值并且激发峰与发射峰的位置与形状几乎相同,这说明二苯酮-4作用于牛血清白蛋白时有荧光猝灭作用,引起此处内源性荧光有规律的猝灭,随着二苯酮-4浓度的不断升高,BSA的荧光强度有规律得降低。
在普遍情况下,我们将荧光猝灭的过程包括动态猝灭和静态猝灭两种类型[13]。在动态猝灭过程中的作用机理是对quencher对激发态作用,通过能量转移或电荷移动使其丧失激发能,蛋白质自身的活性和结构并不受影响。而静态猝灭从实质上来说是因为是荧光体和quencher通过结合形成了基态复合物,这在微观层面上影响蛋白质的二级构造,从宏观层面上影响其生理活性。另一种判断方法是通过双分子猝灭常数Kq来进行判断,温度会影响猝灭作用以及吸收光谱的变化。温度对荧光猝灭作用的影响以及荧光光谱的变化进行分辨。随着温度的不断上升,由于有效碰撞的离子数不断增加引起电子迁移的过程加剧属于动态猝灭;反之如果猝灭常数随温度的不断升高而下降,则属于静态猝灭。这是由于复合物的稳定性随着温度的变化而变化。为了更加深入地证实此猝灭过程的种类,我们把它当作动态猝灭来处理,借助斯特恩-沃尔默方程进行计算[14]:
其中,F0和F分别是不存在二苯酮-4时的荧光强度和存在不同浓度二苯酮-4后的荧光强度;Kq是静态过程中猝灭反应速率常数;τ0是不存在猝灭剂时荧光分子平均寿命,通常生物大分子的荧光寿命为10-8s;[Q]为二苯酮-4的浓度;Ksv为动态猝灭常数。根据上式所得的结果,以[Q]为横坐标,F0/F为纵坐标作Stern-Volmer图。以 F0/F 对[Q]进行建模,可以得到线性回归方程,我们就可以计算出猝灭速率常数,结果如下表1所示。
根据表1数据可知,猝灭常数随着温度的升高而减少,且Kq的数量级大大超过了生物大分子在水溶液中的最大扩散碰撞猝灭常数1个数量级,这表明二苯酮-4与牛血清白蛋白相互作用产生了不具有荧光性的配合物,该过程属于静态猝灭。
3.1.2 二苯酮-4在BSA上的结合位点及结合模式分析
结果表明,二苯酮-4对BSA的猝灭机理属于静态猝灭,因此二苯酮-4的浓度与荧光强度的关系就符合Lineweaver-Burk双导数方程[15],见下公式(2):
式中:F0为没有加入猝灭剂时的荧光强度,F为加入猝灭劑后的荧光强度;n是结合位点数;Ka是结合常数;[Q]是猝灭剂二苯酮-4的浓度。
通过lg([ F0-F]/F)对lg[Q]进行拟合,得到线性回归方程,由此可以分别计算出在不同温度下二苯酮-4与BSA相互作用的结合常数,结合位点数。见表2。
由表2数据可见,二苯酮-4与BSA二者结合紧密。证明了二者之间剧烈的联结作用,且二苯酮-4与BSA之间的联结位点数基本为1,则表明二苯酮-4与BSA之间形成一个结合位点。
3.1.3 二苯酮-4与BSA相互作用的热力学参数与结合力
一般来说,有机小分子与蛋白质等生物大分子相互作用时的作用力主要包括Van der Walls力,疏水作用力,氢键结合力等[16-17]。当温度变化范围不大时,可近似把焓变熵变当作常数,根据范霍夫方程来计算反应的焓变和熵变:
式中K为不同温度条件下的联结常数,R为标准气体常数,△H为反应焓变,△S为反应熵变,再可由公式ΔG=ΔH-TΔS来计算反应的自由能变。之后以结合常数的对数为纵坐标,温度的倒数为横坐标进行线性拟合,根据方程的截距和斜率分别计算得△H、△S及△G值。
从热力学基本关系式来看,在温度和压力一定的情况下,体系中的ΔG决定了小分子物质与蛋白质的相互作用能否自发进行,当ΔG<0时,该反应可以自发进行。Ross等人[18]研究并总结出的判断生物大分子自身相互作用力性质以及生物大分子与小分子物质之间相互作用力的规律通过比较反应发生前后热力学焓变ΔH和熵变ΔS的相对大小,如果是典型的疏水作用力则ΔH>0,ΔS>0;如果是氢键和范德华力则ΔH<0,ΔS<0;如果是静电引力ΔH<0,ΔS>0。
所得数据表明,BP-4的 ΔG<0,表明它可与BSA自发反应;根据ΔH和ΔS判断,BP-4主要通过氢键和范德华力与BSA结合。
4 结论
根据分析上述实验数据,可以得出以下结论:(1)二苯酮-4与BSA相互作用使得其自身的荧光发生明显猝灭现象,且这种猝灭作用随二苯酮-4的浓度升高而增强,可得出该过程属于静态猝灭。(2)二苯酮-4(BP-4)与BSA之间的结合位点数为1左右,表明两者之间存在一种类型的结合位点。(3)经过计算二苯酮-4与BSA互相作用的热力学参数,可以知道两者的作用过程是自发进行的,并且BP-4与BSA之间的相互作用力属于氢键和范德华力[19]。
目前我国的有机紫外防晒剂的污染问题日益严峻,人们也越来越重视对其毒理性质的研究。本实验提醒二苯酮-4能在人体中通过血清白蛋白进行转运和储蓄。目前有有机紫外吸收剂对水生动物鱼类的内分泌干扰的相关研究[20-21]。但是对于人体组织细胞的影响研究还很少,需要进一步深入探索,目前的研究进展尚不能解释有机紫外防晒剂和内分泌系统之间的干扰效应,所以,在未来的研究内容中,我们应该更加进一步去研究有机紫外防晒剂产生的不同内分泌干扰效应的机理。这样才能让我们更加完整科学得认识有机紫外防晒剂对不同生物包括人体健康的各种危害。这不仅让我们进一步了解在平时日常生活中如何正确运用防晒剂这类个人护理用品,与此同时,也可以为相关部门提供数据,方便科学决策。
参考文献
[1]黄方千,李强林,杨东洁,等.有机紫外线吸收剂研究进展[J].印染,2011,37(20):47-52.
[2]敖俊杰,高礼,施玉衡,等.有机紫外防晒剂与牛血清白蛋白相互作用的荧光光谱特征[J].环境与健康杂志,2014,31(4):305-308.
[3]Krause M,Klit A,Blomberg Jensen M,et al.Sun- screns:Are they beneficial for health?An overview of endocrine disrupting properties of UV-filters [J]. International Journal of Andrology,2012,35(3): 424-436.
[4]李立平,魏东斌,李敏,等.有机紫外防晒剂内分泌干扰效应研究进展[J].环境化学,2012,31(2):150-156.
[5]李英,王成云,刘丽,等.气相色谱-质谱法测定化妆品中的防晒剂[J].分析实验室,2003,22(3):77-80.
[6]郭振宇,丁著明.二苯酮类紫外线吸收剂的研究进展[J].塑料助剂,2018(02):1-5.
[7] Janjua N R,Kongshoj B,Andersson A M,et al. Sunscreens in human plasma and urine after repeated whole-body topical application[J]. JEADV,2008,22: 456-461.
[8] Vila M, Lamas J P, Garcia-Jares C, et al. Ultrasound-assisted emulsification microextraction followed by gas chromatography–mass spectrometry and gas chromatography–tandem mass spectrometry for the analysis of UV filters in water[J]. Microchemical Journal, 2016, 124: 530-539.
[9]杨灿,李莉,杨轶博,等.磺胺类兽药的环境行为及生态毒理学研究进展[J].绿色科技,2015(5):209-211.
[10]赵妍,曹娥,韩凤梅,等.荧光猝灭法对肉桂酸与人血清白蛋白间的相互作用的研究[J].光谱学与光谱分析,2008,28(4):904-907.
[11]敖俊杰,高礼,施玉衡,等.有机紫外防晒剂与牛血清白蛋白相互作用的荧光光谱特征[J].环境与健康杂志,2014,31(4):305-308.
[12]孫建平,郑平,胡宝兰.多种抗生素对畜禽废水厌氧消化的联合抑制[J].环境科学,2009,30(9):2619-2624.
[13]王婧.多酚类化合物与牛血清蛋白相互作用的研究[D].杭州:浙江工业大学,2013.
[14]许金钩,王尊本.荧光分析法[M].北京:科学出版社,2006:65-70.
[15]冯喜增,白春礼,林璋.吖啶橙与牛血清白蛋白的相互结合作用[J].分析化学,1998,26(2):154-157.
[16]BraunAM,MauretteMT.Photochemicaltechnology[M].NewYork: Oliveros EW,1991:41.
[17] Liu BS,Xue CL,Wang J. Study of the conjugation reaction between bovine serum albumin and gentamicin with ponceau S as fluores- cence probe[J]. Monatsh Chem,2012,143:203-209.
[18] Ross PD,Subramanian S. Thermodynamics of protein association reactions: forces contributing to stability[J]. Biochemistry,1981,20:3096.
[19]郭灿城,李和平,张晓兵,等.meso-5,10,15,20-四[4-( N-吡咯烷基)苯基]卟啉的合成及对牛血清白蛋白的作用[J].高等学校化学学报,2003,24(2):282-287.
[20] Christen V,Zuchi S,Fent K.Efects of the UV-fil- ter 2-ethyl-hexyl-4-trimethoxycinnamate(EHMC)on expresion of genes involved in hormonal pathways in fathead minnows (Pimephales promelas)and link to vitelogenin induction and histology [J].Aquatic Toxicology,2011,102(3-4):167-176.
[21] Kunz P Y,Gries T,Fent K.The ultraviolet filter 3- benzylidene camphor adversely afects reproduction in fathead minnow (Pimephales promelas)[J].Toxi-cological Sciences,2006,93(2):311-321.
收稿日期:2020-08-01

