超声造影调整乳腺BI-RADS 3、4类肿块的临床价值
朱桂新 武 爽 董立阳 林艳慧
2013版乳腺影像报告和数据系统(breast imaging reporting and data system,BI-RADS),对超声BI-RADS部分进行了大量修改,但其对血流信息概括简单,且未涉及超声造影内容。BI-RADS 4类肿块恶性概率跨度大,若均行穿刺活检,会造成过度治疗和医疗资源浪费。超声造影能够清晰显示肿瘤组织微血管灌注情况,提示肿瘤新生血管分布形态、走行变化,弥补血流信息的不足。本研究应用超声造影评分调整BI-RADS分类,旨在分析其在乳腺BI-RADS 3、4类肿块良恶性鉴别诊断中的价值。
资料与方法
一、临床资料
收集2019年3月至2020年4月在我院经穿刺活检或手术病理证实的乳腺肿块患者71例,均为女性,年龄20~77岁,平均(47.6±11.8)岁。单发67例,多发4例,共76个病灶,常规超声BI-RADS分类3、4类;其中良性43个,包括乳腺纤维腺瘤14个,乳腺增生症13个,乳腺增生伴纤维腺瘤形成7个,炎症3个,乳腺导管扩张症2个,乳腺增生伴炎症、导管内乳头状瘤、浆细胞性乳腺炎、硬化性腺病各1个;恶性33个,包括浸润性导管癌23个,浸润性癌4个,导管内癌和导管原位癌各2个,实性乳头状癌伴浸润和浸润性小管癌各1个。纳入标准:①所有患者均行常规超声及超声造影检查,且常规超声BI-RADS 3、4类;②单侧肿块个数2个的患者;③首诊且拟行粗针穿刺或手术治疗的患者。排除标准:①妊娠或哺乳期妇女;②检查前有手术、放化疗病史患者;③自身情况不能接受超声造影检查者。本研究经我院医学伦理委员会批准,所有患者均签署知情同意书。
二、仪器与方法
1.常规超声及超声造影检查:使用Aplio i800彩色多普勒超声诊断仪,线阵探头,频率18 MHz;超声造影剂为SonoVue(意大利Bracco公司);超声造影机械指数为0.10。患者取仰卧位,双臂外展,暴露双侧乳腺、腋窝。选择常规超声检查模式,以乳头为中心,沿顺时针方向轮辐状序贯扫查,明确肿块位置,观察记录肿块大小、位置、形态、边缘、肿块内部回声及其后方回声特征,明确钙化大小、位置及血流分布情况等;选取肿块显示满意的常规超声切面后切换至超声造影模式,采用实时双幅显像,观察图像包括的肿块及周围正常腺体组织,经肘正中静脉快速团注4.8 ml造影剂,随后立即用0.9%生理盐水5.0 ml进行冲洗,探头保持不动,同时启动超声仪器内置计时器并存储动态图像,连续实时观察肿块的动态灌注过程3 min。
2.常规超声图像分析及诊断恶性标准:根据2013版BIRADS分类标准[1],对乳腺肿块特征进行描述并分类,4B类提示恶性。
3.超声造影评分标准[2]:1分,造影全程病灶无造影剂进入;2分,病灶与周边乳腺组织呈等增强,造影模式下未见明显肿块轮廓;3分,病灶呈均匀或不均匀增强,边界规整、清晰,增强范围与二维相同;4分,病灶呈均匀或不均匀增强,边界不规则,增强范围大于二维;5分,病灶不均匀增强,伴/不伴局部无增强区,周边可见“蟹足样”增强。根据超声造影评分标准对常规超声BI-RADS分类进行调整[3]:1~2分,分类下调一类;3分,保持原分类不变;4~5分,分类上调一类。
所有图像分析均由两名具有常规超声及超声造影诊断经验的医师采用盲法独立完成阅片,若存在分歧时,共同商议决定或邀请第三名具有诊断经验的超声医师参与决定。本研究对BI-RADS 4类乳腺肿块行组织学活检。
三、统计学处理
应用SPSS 20.0统计软件,计数资料以频数或率表示,组间比较行χ2检验。以病理结果为金标准,绘制受试者工作特征(ROC)曲线,计算调整前、后BI-RADS分类预测乳腺恶性肿块的曲线下面积,行Z检验。P<0.05为差异有统计学意义。
结 果
一、调整前、后BI-RADS分类结果
调整前BI-RADS分类提示良性肿块41个,恶性肿块35个,其中3、4A、4B、4C类的乳腺肿块恶性概率分别为0(0/13)、28.6%(8/28)、63.2%(12/19)、81.3%(13/16);调整后BI-RADS分类提示良性肿块39个,恶性肿块37个,其中2类7个、3类12个(3类保持不变4个)、4A类20个(3类上调2个)、4B类15个、4C类11个、5类11个。BI-RADS 4类肿块8个降为3类,11个升为5类,活检率由100%(63/63)降至69.8%(44/63),误诊率仅为1.6%(1/63),调整前后活检阳性率分别为52.4%(33/63)、52.3%(23/44)。见表1和图1,2。
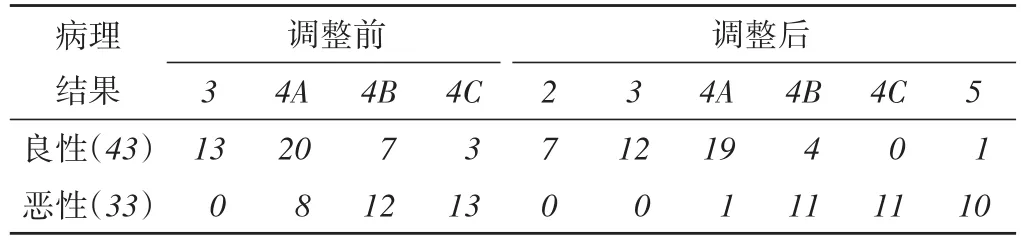
表1 76个乳腺肿块调整前、后BI-RADS分类结果 个
二、调整前、后BI-RADS分类诊断效能比较
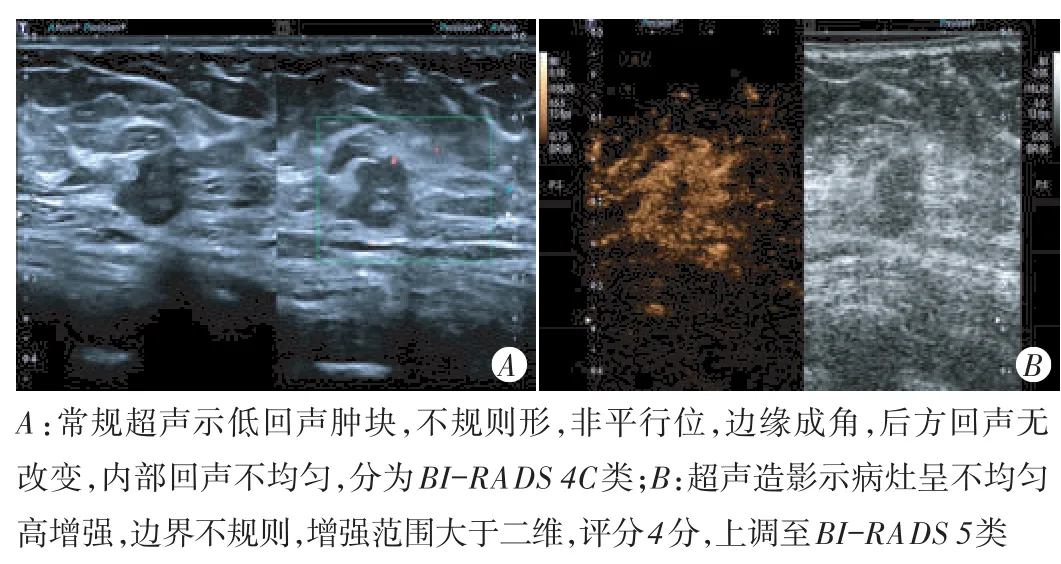
图1 浸润性导管癌(Ⅱ级)常规超声和超声造影图
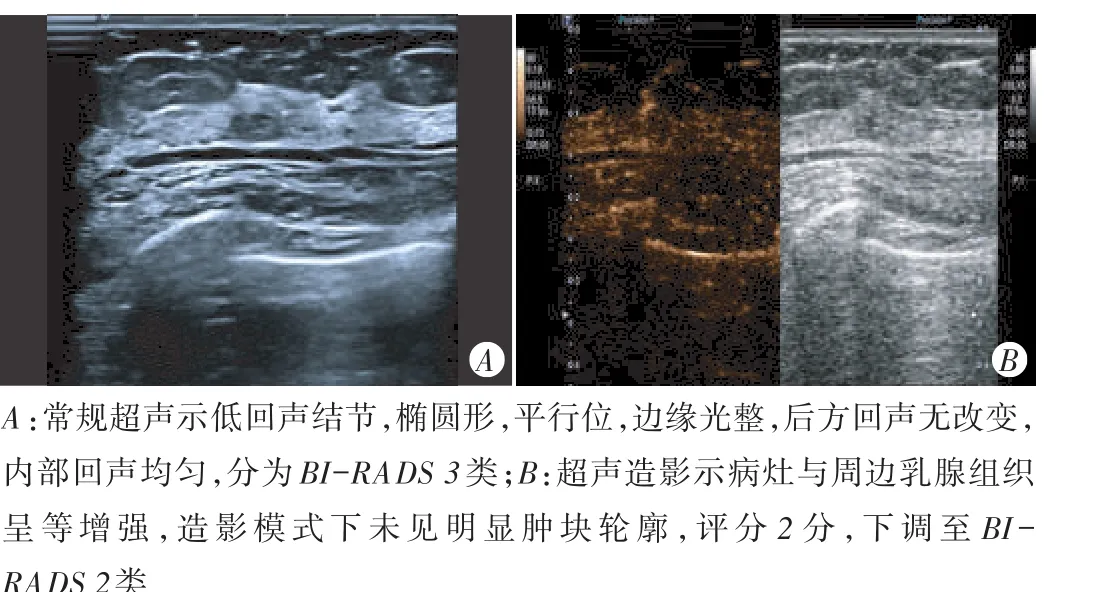
图2 乳腺增生症常规超声和超声造影图
调整前、后BI-RADS分类诊断的敏感性、特异性、准确率分别为75.8%、76.7%、76.3%和97.0%、88.4%、92.1%。见表2,3。以病理结果作为金标准,调整前、后BI-RADS分类预测乳腺恶性病灶的ROC曲线下面积分别为0.763、0.927,差异有统计学意义(Z=3.965,P<0.05)。见图3。

表2 调整前BI-RADS分类诊断效能 个

表3 调整后BI-RADS分类诊断效能 个
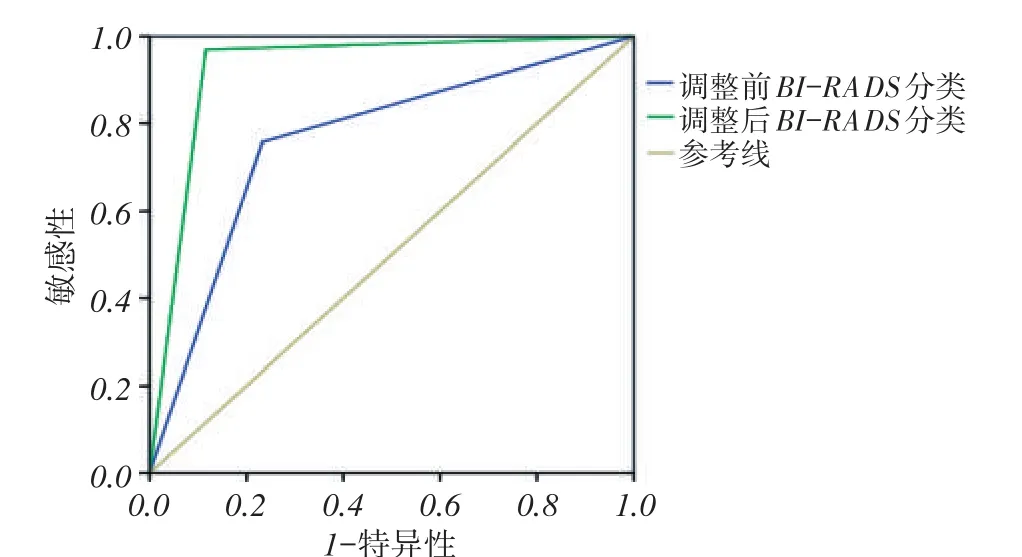
图3 调整前、后BI-RADS分类预测乳腺恶性病灶的ROC曲线图
讨 论
乳腺癌患者早期大多无明显临床症状,主要依靠影像学检查。乳腺超声BI-RADS分类因其报告标准化,乳腺声像图解读和临床处理原则统一,已广泛应用于临床。其分类主要根据乳腺肿块形状、纵横比、边缘、内部回声、后方回声特点、有无钙化及钙化的性质等相关征象[1]。然而,乳腺肿块表现多样,尤其是BI-RADS 3类和4A类肿块,部分良恶性征象存在重叠,且4类肿块恶性概率跨度大,达2%~95%[1,3],增加了许多不必要的穿刺活检等有创性检查,以及过度治疗等。
肿瘤新生血管是其快速生长的物质和形态学基础,与肿瘤侵袭及预后密切相关。然而BI-RADS分类对血流信息概括简单,多普勒显像技术不易显示低速微小血管,而超声造影作为纯血池显像技术,能够显著提高对微血管显示的敏感性。本研究通过超声造影评分调整常规超声BI-RADS分类鉴别乳腺肿块良恶性,结果显示,调整后BI-RADS分类较调整前BI-RADS分类诊断效能高,可明显提高乳腺肿块良恶性诊断准确率,ROC曲线下面积分别为0.763、0.927,差异有统计学意义(Z=3.965,P<0.05)。调整前BI-RADS 4A、4B类肿块诊断恶性概率(28.6%、63.2%)较BI-RADS分类指南概率(2%<4A 10%、10%<4B 50%)高,与样本量较小,分类相对保守,诊断信心不足有关。BI-RADS 4类肿块调整后由63个降至44个,使8个BI-RADS 4类良性肿块降为3类,可以短期随访代替穿刺活检,11个BI-RADS 4类恶性肿块升为5类,使肿块诊断更加明确;活检率由100%降至69.8%,误诊率仅为1.6%,与既往研究[4-5]基本一致。
本研究常规超声BI-RADS 3类的肿块共13个,均为良性肿块,下调至2类7个,保持3类4个,上调至4A类2个。上调的2个肿块病理类型均为乳腺增生症,超声造影表现为高增强,边界不清,范围扩大,不均匀增强,评分均4分,上调一类。究其原因,乳腺增生症所处阶段不同,病理组织形态不同,超声表现亦不同[6-7],本研究2个乳腺增生症超声造影表现可能与导管上皮增生活跃,细胞排列紊乱,局部血管增生明显有关。乳腺增生症超声造影常表现为边界不清,形态不规则,但其增强模式常表现为慢进低增强、同进等增强,且造影后肿块的范围不变或缩小或完全与周围腺体融为一体,极少出现滋养血管或充盈缺损等表现有助于鉴别[8]。常规超声BI-RADS分类为4类的肿块共63个,包括恶性肿块33个,上调至5类10个;良性肿块30个,下调至3类8个,上调至5类1个。由常规超声和超声造影同时提示恶性而上调至5类的肿块病理结果为浆细胞性乳腺炎,常规超声表现为形态不规则,水平位,边缘成角,后方呈混合回声,超声造影呈高增强,范围增大。误诊的原因可能与导管周围炎症及小叶结构破坏,形成以浆细胞浸润为主的血管数量和通透性增加的肉芽肿[8],以及医师阅片无患者临床信息作为参考有关。
综上所述,在二维超声基础上,应用超声造影检查进行BIRADS分类,对乳腺肿块进行综合分析,可以提高乳腺BIRADS 3、4类肿块良恶性的诊断,减少BI-RADS 4类肿块不必要的穿刺活检,对BI-RADS分类提供新的诊断依据。但本研究样本量较少,且超声医师对图像分析存在一定的主观性,尚待以后进一步研究的证实。

