室间隔缺损胎儿产前超声及遗传学检查结果分析
涂 鹏 谷孝艳 张晓航 刘东云 林 芸 张雪梅 董虹美 何怡华 冉素真
室间隔缺损(ventricular septal defect,VSD)是胎儿期最常见的先天性心脏病之一,近年来随着产前超声和胎儿血清学筛查技术迅速发展,以及我国二胎政策放开、高危孕妇数量增加,胎儿期VSD检出率、相关遗传学检查异常率均较以往有所提高,增加了孕妇的心理负担和产前医师咨询难度。目前国内外对VSD胎儿的研究[1-4]大多集中在其病理分型及手术预后,对其相关遗传学病因报道较少。本研究通过回顾性分析我院77例VSD胎儿的超声异常表型及进一步的染色体微阵列分析(CMA)、全外显子测序(WES)等遗传学检查结果,旨在为VSD胎儿产前咨询和预后评估提供依据。
资料与方法
一、研究对象
选取2016年11月至2018年12月我院行系统超声检查和超声心动图检查检出的77例VSD胎儿,均有完整的遗传学检测资料且随访至妊娠终止,孕妇年龄21~42岁,平均(30.3±3.5)岁;孕20~33周,平均孕(24.9±3.2)周。纳入标准:产前超声心动图检查存在VSD,且经新生儿期超声心动图证实或胎儿引产后解剖证实。本研究经我院医学伦理委员会批准,所有孕妇均签署知情同意书。
二、仪器与方法
1.超声检查:产前超声检查使用GE E 10、E 8及三星WS 80A彩色多普勒超声诊断仪,探头频率2.0~5.0 MHz。新生儿超声心动图检查使用Philips iE 33彩色多普勒超声诊断仪,探头频率2.6 MHz。参照我国《胎儿心脏病产前超声诊断咨询及围产期管理指南》[5]和国际妇产超声协会(ISUOG)2013版胎儿心脏超声筛查实践指南[1],经腹横切面、四腔心切面、心室流出道切面、三血管-气管切面对胎儿心脏进行序列检查,记录心脏大血管异常类型、VSD位置及大小。VSD超声诊断标准[4]:经彩色多普勒和频谱多普勒同时证明VSD存在。
2.胎儿遗传学检测:当产前超声发现胎儿结构异常时,根据孕妇自愿原则依据胎龄选择在我院产前诊断中心进行羊水或脐带血穿刺,行染色体核型分析、快速荧光原位杂交和单核苷酸多态性比较基因组杂交(SNP-array)及WES检查。终止妊娠者签署胎儿大体解剖及遗传学检测同意书,收集胎儿组织。在父母知情同意下采集父母双方外周血各5 ml(乙二胺四乙酸抗凝)。标本立即置于-80℃冰箱冷冻,按照DP318基因组提取试剂盒[天根生化科技(北京)有限公司]推荐步骤提取收集胎儿组织的基因组DNA(gDNA)。基因测序内容:①采用低深度全基因组测序(CNV-seq)检测拷贝数异常(CNVs)和非整倍体:测序平台为Illumina Hiseq2500,检测100 kb以上的CNVs。对检出的CNVs,通过检测DGV(http://dgv.tcag.ca/dgv/app/home)、Decipher(https://decipher.sanger.ac.uk/)、OMIM(http://www.ncbi.nlm.nih.gov/omim)及PUBMED(https://www.ncbi.nlm.nih.gov/pubmed/)等数据库综合分析,并依据美国医学遗传学会(ACMG)对拷贝数异常结果解读指南[2]对其进行致病性判定,将CNVs分为已知致病、疑似致病、临床意义不明、疑似良性及良性5类。同时对携带已知致病、疑似致病CNVs胎儿的父母外周血样进行检测,明确来源。②WES检测单基因变异:将全基因组外显子区域DNA捕捉,病富集后进行外显子目标区域捕获测序(Illumina Hiseq2500,测序类型:PE100 bp),对原始测序数据进行低质量过滤,利用标准生物信息分析流程检测单核苷酸变异和小的插入缺失,对变异位点进行检出、过滤及注释。变异位点过滤标准包括人群数据库中频率(ExAC或千人基因组)<5%、最小覆盖深度为10X,以及变异功能变化(非同义突变、剪切位点变化、无义突变、移码突变)等。
3.基因突变验证:对发现遗传变异的家系进行产前超声咨询及围产儿预后咨询,根据胎儿父母自愿原则,进行Sanger测序验证。
4.随访:孤立性VSD胎儿随访至生后1年,观察VSD预后及治疗情况,同时由我院儿童保健科进行大运动及智力发育专业评估。
结 果
一、VSD胎儿合并心脏及心外超声结构异常表型情况
77例VSD胎儿中,孤立性VSD胎儿最多,为41例(53.2%),其次为VSD同时合并心脏及心外畸形16例(20.8%)、VSD仅合并心脏畸形14例(18.2%)、VSD仅合并心外畸形6例(7.8%)。
1.合并心外畸形22例(28.6%),其中单发畸形13例(59.1%),合并2种及以上畸形9例(40.9%),具体种类及检出率见表1。
2.合并心脏畸形30例(39.0%),均为圆锥动脉干畸形;其中肺动脉狭窄/闭锁伴VSD最多,为15例(50.0%),其次为法洛四联症6例(20.0%)、右室双出口6例(20.0%)、大动脉转位3例(10.0%)。另外伴发主动脉弓位置异常8例(26.7%)、永存左上腔静脉5例(16.7%)、无名静脉走行异常2例(6.7%)、静脉导管缺如2例(6.7%)、房室间隔缺损2例(6.7%)、左心发育不良综合征1例(3.3%)、肺动脉瓣缺如1例(图3,3.3%)、右锁骨下动脉迷走1例(3.3%)、冠状动脉瘘1例(3.3%)。
二、VSD胎儿遗传学检查结果
77例胎儿中共检出遗传学异常16例,检出率20.8%。染色体非整倍体异常、基因点突变情况及胎儿超声表型情况见表2~4。在核型正常VSD胎儿中检出12例异常,其中致病性CNVs 8例(6例微缺失和2例微重复),4例单基因病,分子诊断率分别提高了15.1%、7.5%。TUBA1A基因点突变胎儿(case14)产前超声和Sanger测序结果见图1,2;22q11.2微缺失胎儿(case5)相关超声图像见图3,CNVs结果见图4。

表1 22例胎儿心外畸形类型及其检出率
1.41例孤立性VSD胎儿中,2例(4.9%,case11、12)检出遗传学异常,均为CNVs,case11检出2q13微重复,case12检出Xp22.31微重复;均未进行双亲验证。

表2 4例染色体非整倍体异常胎儿心脏及心外超声表型
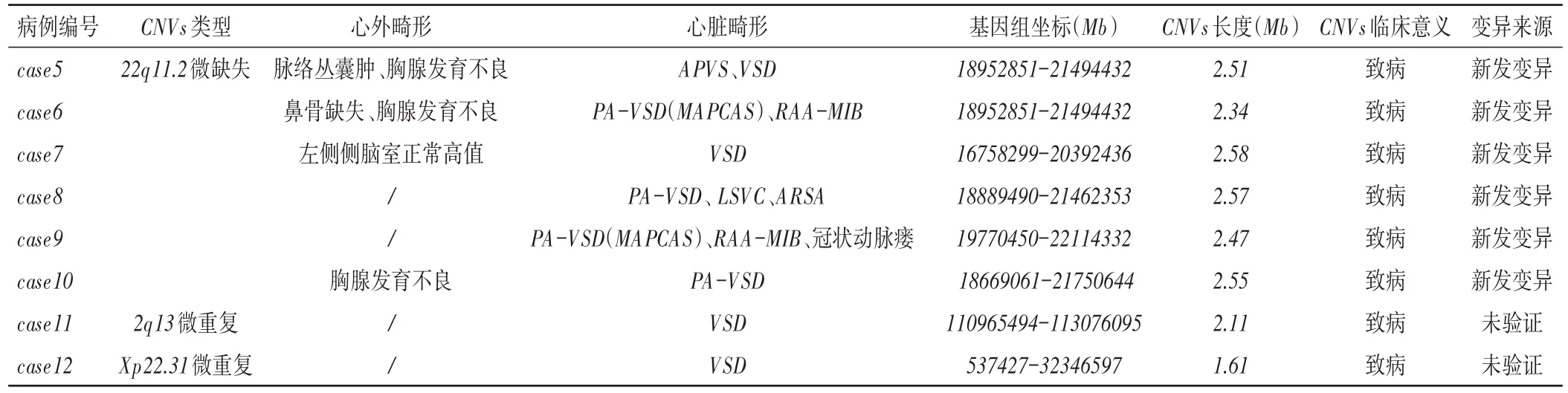
表3 8例致病性CNVs胎儿心脏及心外超声表型

表4 4例基因点突变胎儿心脏及心外超声表型
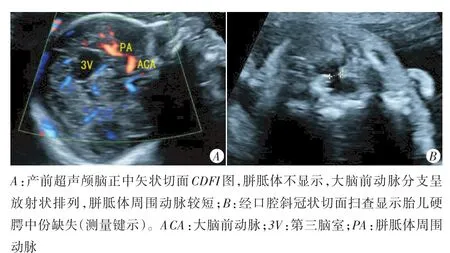
图1 TUBA1A基因点突变胎儿(case14)产前超声显示胎儿胼胝体缺如、单纯腭裂
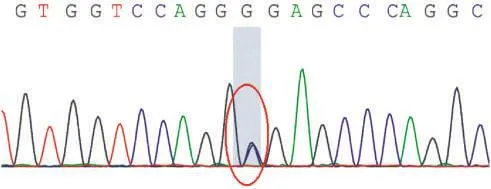
图2 TUBA1A基因点突变胎儿(case14)Sanger测序结果

图3 22q11.2微缺失胎儿(case5)超声心动图显示胎儿肺动脉瓣缺如、胸腺发育不良

图4 22q11.2微缺失胎儿(case5)及其父母CNVs检测结果
2.14例VSD仅合并心脏畸形胎儿中,5例(35.7%)检出遗传学异常。染色体异常2例,case1检出8P-三体综合征,双亲验证后为新发变异;case4检出4q重复综合征,重复区域为q26-q35,但该胎儿双亲拒绝进行验证。CNVs 2例(case8、9),均检出22q11.2微缺失,双亲验证后为新发变异。case13为单基因病,检出其携带DNNAAF1基因的1个复合杂合突变c.767C>T(p.P256L),测序验证该突变分别来自胎儿健康父母。
3.2 例VSD仅合并心外畸形胎儿中,2例(33.3%,case3、7)检出遗传学异常,染色体异常1例,case3检出为18-三体;CNVs 1例,case7检出22q11.2微缺失,双亲验证后为新发变异。
4.16 例VSD同时合并心脏及心外畸形胎儿中,7例(43.8%)检出遗传学异常。染色体异常1例(case2),为9号染色体环状变形,双亲验证后为新发变异。CNVs 3例(case5、6、10),均检出22q11.2微缺失,双亲验证后均为新发变异。单基因病3例:case14检出携带TUBA1A基因的已知致病突变c.1169G>C(p.R390P),为新发突变;case15检出携带FGFR3基因的已知致病突变c.G1144A(p.G382R),为新发突变。case16检出携带MLL2基因的已知致病突变c.11729_c.11734delAGCAAC(p.Q3910_L3912delinsL),为新发突变。
讨 论
VSD是由于胚胎期心室间隔发育不完全,导致左、右心室间形成异常血流交通,是常见的胎儿期及新生儿期心脏病,根据缺损部位通常将其分为膜周部、流出道、流入道及肌部4类。虽然胎儿期VSD检出率有所提高,但主要以孤立性VSD常见,30%病例会合并其他心脏异常。目前外科手术治疗已经能对大部分出生后VSD进行有效干预,封堵成功率达95%[4]。新的遗传检测手段CNV-seq、WES的应用使胎儿VSD在分子水平的诊断成为可能,为临床及患儿家属提供了更多产前咨询信息。
一、VSD胎儿心脏及心外超声结构异常解读
既往研究[6]显示,孤立性VSD病例的缺损处<3 mm、位于膜周部或肌部时,自然闭合率达60%,性别、是否使用辅助生殖技术等均不影响预后。但若VSD伴发心脏其他结构异常或遗传学异常,自然闭合可能性小[4],尤其是由遗传缺陷引起的先天性心脏病多伴有其他并发症,即使手术成功修补VSD缺口,仍会因其他并发症导致预后不佳。故决定VSD胎儿的预后除其缺损大小、部位外,更应关注胎儿是否合并心脏、心外畸形。本研究中非孤立性VSD胎儿中同时合并心脏及心外畸形比例最高,达44.4%;而在遗传学异常VSD胎儿中,同时合并心脏及心外畸形胎儿遗传学比例也最高,达43.8%。提示当检查发现胎儿存在VSD时,应仔细扫查胎儿心脏及心外是否同时存在多发畸形,这对胎儿的手术预后及后续遗传学检查有着重要的指导意义。
另外,本研究中30例合并心脏畸形的VSD胎儿均为圆锥动脉干畸形,这可能与胚胎期瓣下圆锥与心室间隔对接过程中发生吸收、旋转移位、向下融合封闭室间孔过程异常有关[7],发生率较高的分别为肺动脉狭窄/闭锁伴VSD、法洛四联症、右室双出口。
二、VSD胎儿遗传学检查结果分析及产前咨询指导
文献[8-9]报道,CMA/CNV-seq及WES可在超声检查和染色体核型分析均正常的胎儿中将阳性检出率提高8%~42%,对改善妊娠结局的临床管理有所帮助,能更好地为患儿家庭的生育决策提供信息。本研究核型正常的VSD胎儿中,运用CMA/CNV-seq和WES技术额外检出12例异常,其中致病性CNVs 8例、单基因病4例,分子诊断率分别提高了15.1%、7.5%,其中VSD同时合并心脏及心外畸形胎儿、VSD仅合并心脏畸形胎儿的遗传学异常率较高,分别达到43.8%、35.7%,以CNVs和单基因病的比例更高(分别为21.4%、37.6%),提示VSD胎儿若合并心脏或心外异常时,其预后除关注超声表型外,有必要进一步行遗传学检查。
本研究致病性CNVs中,6例(75%)为22q11.2微缺失综合征;但有2例单纯VSD胎儿检出了CNVs异常,既往文献[10]均未报道与VSD相关:case11检出2q13片段微重复,该片段与生长发育迟缓及神经系统发育异常相关;case12检出Xp22.31片段微重复,该片段与遗传性儿童癫痫相关[11]。但此2例胎儿双亲均拒绝进行来源验证,为其再次妊娠的遗传咨询造成了困难。
4例单基因病例中,case13为DNAAF1[12]的复合杂合突变,属于常染色体隐性遗传,可以导致异质度高的先天性心脏病管和神经管缺陷异常,遗传咨询后告知患者自然受孕得到正常胎儿的概率约1/4,建议可通过植入前诊断选择健康胚胎受孕。case14为TUBA1A基因突变导致的无脑回3型[13],为常染色体显性遗传,以脑畸形、小头畸形、发育迟缓为主要临床特征,case14主要是胼胝体缺失表型符合,而单纯腭裂、PA-VSD等超声表现拓展了该病的产前表型谱;case15为成纤维细胞生长因子受体3(FGFR3)基因[14]突变,主要为引起骨发育不良相关表型,与本研究病例心外异常表型部分相符;case16为MLL2基因突变,为常染色体显性遗传,可以引起主动脉弓缩窄和骨骼系统异常[15],与本研究病例心外畸形表型部分相符。通过Sanger验证,以上3例父母均未携带此位点,为新发突变,遗传咨询后建议可再次自然受孕,对此3例孕妇再次妊娠时的遗传学指导有重要意义。
本研究局限性:为单中心研究,我中心为产前超声诊断中心,部分病例为周边地区异常转诊病例,所以VSD合并心脏及心外畸形胎儿比例明显高于孤立性VSD胎儿,且部分VSD病例孕妇因为自身原因选择了放弃遗传学检查,可能会对本研究结果产生潜在的选择性偏倚,无法全面显示VSD胎儿超声表型及遗传变异真实情况,后续的工作中将继续增加病例数来完善相关疾病数据库。
综上所述,产前超声检查发现胎儿VSD时,应仔细扫查心脏及心外是否合并异常,帮助临床医师进行全面的手术预后评估。同时还应根据超声表型异常类型进行进一步遗传学检查,对VSD胎儿的产前评估、预后咨询及孕妇再次妊娠能提供更多信息和遗传咨询指导。

