散养猪口蹄疫、猪瘟分类分段免疫抗体检测试验
姜玉芳,宣小龙,田晓霞
(1.宁夏回族自治区隆德县城关畜牧兽医工作站,宁夏 隆德 756300;2.宁夏回族自治区隆德县动物疾病预防控制中心,宁夏 隆德 756300;3.宁夏回族自治区隆德县张程畜牧兽医工作站,宁夏 隆德 756300)
近年来,国家规定散养户猪强制免疫重大动物疫病的种类主要有猪瘟、口蹄疫、高致病性猪蓝耳病三种[1],高致病性猪蓝耳病已于2017年退出强制免疫接种计划。猪瘟、猪口蹄疫(O型口蹄疫,A型口蹄疫)仍然实施国家强制免疫项目。猪瘟(classical swine fever,CSF)是由黄病毒科猪瘟病毒属的猪瘟病毒引起的一种急性、发热、接触性传染病,具有高度传染性和致死性,本病在自然条件下只感染猪,不同年龄、性别、品种的猪和野猪都易感,一年四季均可发生。口蹄疫(foot-and-mouth disease,FMD)是由口蹄疫病毒所引起的偶蹄动物的一种急性、热性、高度接触性传染病,主要侵害偶蹄兽,偶见于人和其他动物。其临诊特征为口腔黏膜、蹄部和乳房皮肤发生水疱。两种疫病是威胁我国养猪业的主要疫病,接种疫苗是目前控制疫病的主要措施。规模养殖场的猪实行程序化免疫接种,免疫抗体水平一直维持在80%以上,散养户的猪以春秋两季集中免疫加平时加强免疫相结合的方式免疫接种,免疫抗体水平不太理想,易出现抗体水平不达标甚至为0。为提高免疫抗体水平,本试验采取分类分段免疫方法[2],分类即在同步免疫接种时,对猪口蹄疫O型疫苗、A型疫苗、猪瘟疫苗分别注射在猪的肩颈、臀部等不同部位,避免在同一部位免疫接种;分段就是免疫接种一种或两种疫苗后间隔一定时间再进行另外一种或两种疫苗的免疫接种。
1 材料与方法
1.1 试验动物
散养猪,对猪的品种、年龄、体重、饲养环境、生物安全管理水平进行统计并划分,日龄在 80 d以下初次免疫的猪做母源抗体检测,并做好记录。分类免疫试验选择相同品种、年龄、体重、饲养环境的散养猪400头;分段免疫试验选择母源抗体相同的80 d以下未免疫的散养猪90头。
1.2 疫苗
猪瘟耐热保护剂活疫苗(细胞源),国药集团扬州威客生物工程有限公司生产,批号0418001,用量为1头份/头。O型口蹄疫疫苗,杨凌金海生物技术有限公司,批号JH170102,用量为2 ml/头。A型口蹄疫疫苗,中农威特生物科技股份有限公司,批号C170802J,用量为1 ml/头。
1.3 试剂
猪瘟病毒抗体ELISA试剂盒(哈尔滨元亨生物药业有限公司,规格96头份);改进型口蹄疫病毒O型液相阻断ELISA抗体检测试剂盒(中国农业科学院兰州兽医研究所,规格50~100份血清样品);改进型口蹄疫病毒A型液相阻断ELISA抗体检测试剂盒(中国农业科学院兰州兽医研究所,规格50~100份血清样品)。
1.4 试验方案及影响因素设计
按照散养户猪重大动物疫病强制免疫要求,制定分类分段6个试验因素12个试验。
分类试验即对猪瘟、口蹄疫实行分类接种(猪瘟、O型口蹄疫、A型口蹄疫3个试验因素),间隔一定时间(5~7 d)进行疫苗的免疫接种,分3个试验(见表1)。A组试验数量120头,同一接种部位同时免疫猪瘟、O型口蹄疫、A型口蹄疫三种疫苗;B组试验数量130头,第一次免疫口蹄疫疫苗(分别接种不同部位),间隔5~7 d后第二次免疫猪瘟疫苗;C组试验数量150头,第一次免疫猪瘟疫苗,间隔5~7 d后第二次免疫口蹄疫疫苗(分别接种不同部位)。连续7 d测体温,观察有无精神萎靡、皮肤发红、呕吐、呼吸急促、食欲减退、死亡等免疫副反应,记录数量。
分段试验是根据抗体产生曲线时间变化,在分类免疫基础上,再经过一定时间采取加强免疫(10~20 d、20~30 d、30~40 d3个试验因素),以此来提高所有免疫项目的抗体水平,分9个试验(见表2)。第一组试验在分段免疫后间隔10~20 d加强免疫猪瘟及O、A型口蹄疫疫苗,第二组试验在分段免疫后间隔20~30 d加强免疫猪瘟及O、A型口蹄疫疫苗,第三组试验在分段免疫后间隔30~40 d加强免疫猪瘟及O、A型口蹄疫疫苗;第四组试验在分段免疫后间隔10~20 d加强免疫猪O、A型口蹄疫疫苗,第五组试验在分段免疫后间隔20~30 d加强免疫猪O、A型口蹄疫疫苗,第六组试验在分段免疫后间隔30~40 d加强免疫猪O、A型口蹄疫疫苗;第七组试验在分段免疫后间隔10~20 d加强免疫猪瘟疫苗,第八组试验在分段免疫后间隔20~30 d加强免疫猪瘟疫苗,第九组试验在分段免疫后间隔30~40 d加强免疫猪瘟疫苗。每组10头,分别于分段免疫接种前,分段免疫后进行采血,实验室检测抗体水平。

表1 散养猪分类免疫试验方案

表2 分段因素试验检测
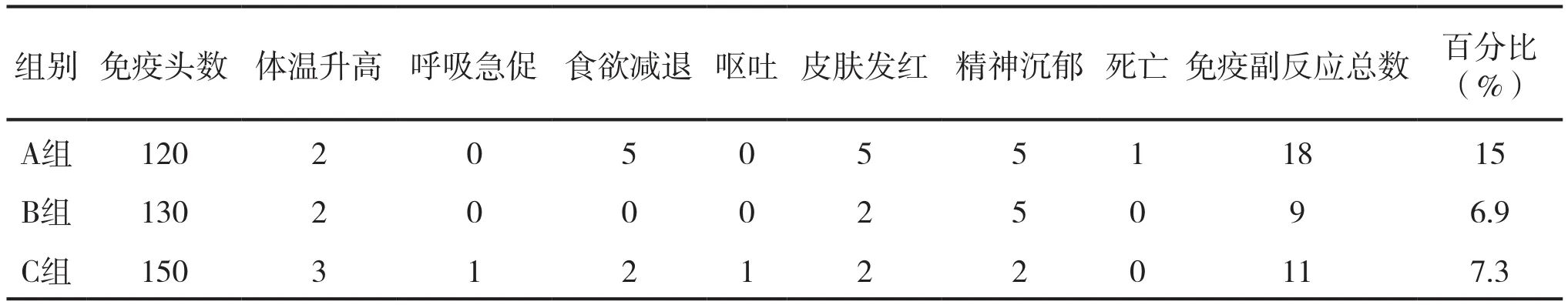
表3 不同试验组免疫副反应观察结果
1.5 免疫
所有免疫按照春秋两季重大动物疫病集中免疫执行,免疫剂量:按照疫苗规定计量注射,对照组进行生理盐水注射。免疫方式按照《口蹄疫免疫接种技术规范》NYT 1955-2010中对疫苗的使用要求和日常防疫员实际行为开展免疫,免疫方式均为皮下注射。
1.6 采血
按照抗体监测采血要求和前面试验设计要求进行监测采血,并做好记录
1.7 检测方法
采用《中华人民共和国农业行业标准 猪瘟诊断技术》GB/T 16551-2008、《中华人民共和国国家标准 口蹄疫诊断技术》GB/T 18935-2003进行检测和结果判定。
2 结果
2.1 不同试验组免疫副反应观察结果
对表3数据进行整理后,采用SPASS19.0统计软件进行卡方分析得出,A、B、C三组相比较,A组出现免疫副反应总数达18例,免疫副反应15%;B组免疫副反应总数9例,免疫副反应6.9%;C组免疫副反应11例,免疫副反应7.3%。A、B、C三组相比,B组与C组差异不显著,B组、C组与A组差异显著,说明分类免疫副反应低的为B组和C组,所以,在重大动物疫病免疫接种过程中,可采用B组或C组方案进行免疫接种。
2.2 不同组免疫抗体合格率试验验证结果
对表4数据整理后,采用SPASS19.0统计软件进行T检验,分析得出CSF分段之前与分段之后九组数据差异不显著,也就是说,CSF进行免疫接种,只要保证首免科学、规范、到位,再间隔10~20 d、20~30 d、30~40 d,注射部位在肩颈部或臀部,实验室免疫抗体水平均保持在80%以上,抗体水平合格率均达到农业农村部规定标准以上。
FMD分段之前与分段之后前六组数据差异极显著。第一组A-FMD免疫抗体合格率76.2%(分段前)80.1%(分段后);O-FMD免疫抗体合格率74.5%(分段前)79.6%(分段后)。第二组A-FMD免疫抗体合格率76.3%(分段前)85.6%(分段后);O-FMD免疫抗体合格率76.0%(分段前)84.9%(分段后)。第三组A-FMD免疫抗体合格率75.9%(分段前)80.2%(分段后);O-FMD免疫抗体合格率76.8%(分段前)81.2%(分段后)。第四组A-FMD免疫抗体合格率73.6%(分段前)83.3%(分段后);O-FMD免疫抗体合格率77.0%(分段前)82.3%(分段后)。第五组A-FMD免疫抗体合格率74.8%(分段前)88.7%(分段后);O-FMD免疫抗体合格率77.2%(分段前)88.1%(分段后)。第六组A-FMD免疫抗体合格率78.3%(分段前)83.1%(分段后);O-FMD免疫抗体合格率76.9%(分段前)82.5%(分段后)。卡方检验得出FMD分段之后第七、八、九组免疫抗体合格率与前六组结果差异极显著,从表4可以看出,9组数据免疫抗体合格率均达到70%以上,符合国家规定标准,尤其是第七组、第八组、第九组A-FMD免疫抗体合格率、O-FMD免疫抗体合格率与前六组相比较,前六组均高于73%,第二组(免疫间隔20d~30 d)、第四组(免疫间隔10~20 d)FMD免疫抗体合格率与其他第一组、第三组、第五组、第六组结果差异显著。
通过实验室检测免疫间隔10~20 d、20~30 d、30~40 d免疫不同疫苗时动物血清的抗体水平得出CFS免疫抗体合格率与分段因素无关,FMD免疫抗体合格率在分段20~30 d间隔时最佳,即采用第二组方案最佳。
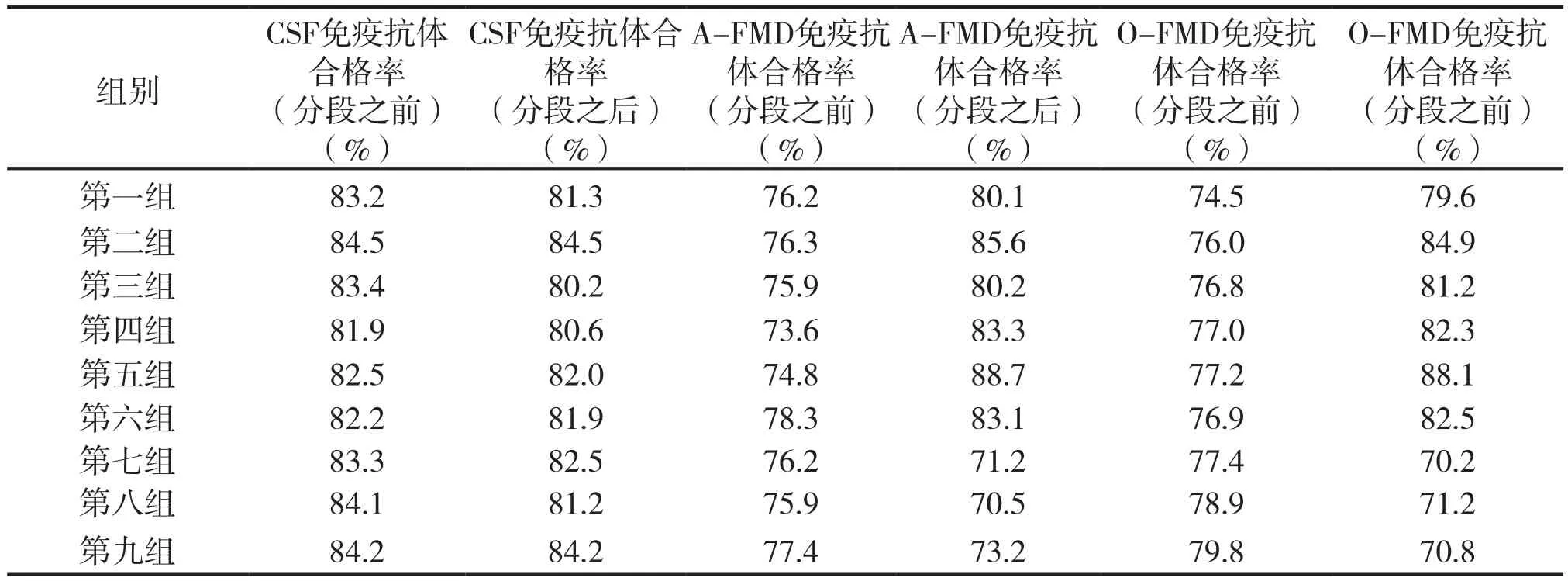
表4 不同试验组不同间隔时间免疫抗体合格率(为均数)
3 试验结论及展望
3.1 试验结论
通过分类分段试验及研究结果显示,散养户猪分类免疫的确可以降低免疫副反应造成的损失,尤其对猪口蹄疫(O、A)与猪瘟疫苗间隔5~7 d进行免疫注射,副反应最小,均低于7.3%;从表4数据分析得出,分段免疫过程中,猪瘟分段免疫差异不显著,所以猪瘟在首次免疫中做好免疫注射就能达到预期目标。但是口蹄疫必须进行加强免疫,免疫间隔时间最佳方案为间隔20~30 d时再次免疫口蹄疫疫苗,方能达到最佳效果。
3.2 展望
影响免疫抗体水平因素杂多,既有主观因素,又有客观因素。主观因素比如每个防疫技术人员操作技能、免疫注射消毒、疫苗保存运输,是否按照剂量要求操作和按照疫苗使用说明书操作等等。客观因素包括畜禽个体差异,饲养环境、应激、科学饲喂,疫苗生产厂家等等。但从多年的重大动物疫病免疫接种副反应统计汇总及此次试验结果可以看出,同时进行猪瘟、口蹄疫免疫接种,副反应很大,不食、发烧、死亡、流产等比较严重,进行分类免疫可以大大降低免疫副反应造成的经济损失,尤其在分类免疫过程中不能同时接种两种以上疫苗,间隔5~7 d,免疫副反应最小,所以在首次免疫过程中分类免疫特别必要。但为了有效提高免疫抗体水平,必须进行加强免疫,加强免疫的时间间隔点20~30 d,也就是分段免疫的时间点为20~30 d,分段免疫是根据免疫抗体应答过程中产生抗体水平的曲线和抗体峰值进行有必要的再次加强免疫,由于时间点把握不准确都会影响抗体水平和免疫质量,通过此次试验,再次验证了分段加强免疫的最佳时间段为20~30 d。此试验的验证对于今后广大兽医工作者开展免疫服务中能够提供准确的技术指导和参考,对于全面有效提高猪瘟、口蹄疫免疫接种质量起到一定的参考依据,并有一定的推广和应用价值。

