例析电池串联装置中电池类型的判断
◇ 广西 马德信
电化学原理是高考必考知识点,主要考查原电池和电解池的工作原理和电极反应式,有时也将原电池和电解池结合在一起,综合考查电池正负极、阴阳极的判断,电子或离子的移动方向,电极反应式的书写和化学计算等知识,是高考试卷中的重要题型.解答试题的关键是判断电池种类.
1 根据电化学装置判断
例1如图1是一个化学过程的示意图.已知甲池的总反应式为2CH3OH+3 O2+4 KOH=2 K2CO3+6 H2O,请回答:

图1
(1)甲池是________池,通入O2的电极作为________极,电极反应式为________.
(2)乙池是________池,A电极名称为________极,电极反应式为________.乙池中的总反应离子方程式为________,溶液的p H________(填“增大”“减小”或“不变”).
(3)当乙池中B极(Ag)的质量增加5.40 g时,甲池中理论上消耗O2_______mL(标准状况下).
分析(1)甲装置自发地发生反应:2CH3OH+3 O2+4 KOH=2 K2CO3+6 H2O,为原电池,通入氧气的一极为原电池的正极,电极方程式为O2+2 H2O+4e-=4 OH-.
(2)乙池为电解池,A与原电池正极相连,为电解池的阳极,发生氧化反应,电极方程式为4 OH--4e-=O2↑+2 H2O,电解硝酸银溶液,阳极生成氧气,阴极生成银,电解总反应式为4 Ag+O2↑+4 H+,则溶液p H减小.
(3)乙池中B极电极方程式为Ag++e-=Ag,则转移电子0.05 mol,由电极方程式O2+2 H2O+4e-=4 OH-可知消耗O20.012 5 mol,则标准状况下V(O2)=280 mL.
2 根据电池中的电极材料和电解质溶液判断
例2某课外小组同学按图2装置进行实验,回答下列问题:
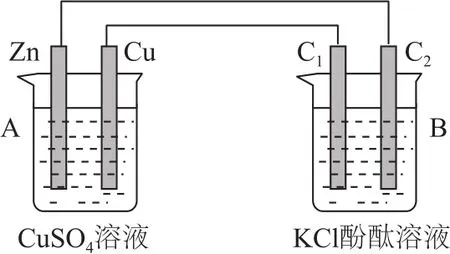
图2
(1)根据电极材料和电解质溶液,判断A池为________,B池为________.
(2)Zn电极为________极,Cu电极反应式为________,C1为________极,电极反应式为________,C2附近发生的现象为________.
(3)开始时Zn电极和Cu电极质量相等,当C2极析出标准状态下224 mL气体,Cu电极和Zn电极质量差为________g.
分析(1)A电池中的两个电极不同,且锌能和硫酸铜发生置换反应,构成原电池;B电池中两个电极都是碳棒,相当于外加电源,是电解池.
(2)锌比铜活泼,锌是负极,铜是正极,发生还原反应,电极反应式是Cu2++2e-=Cu.C1与电源的正极相连,是电解池的阳极,电极反应式为2Cl--2e-=Cl2↑;电极C2和电源的负极相连作阴极,电极反应式为2 H2O+2e-=H2↑+2 OH-,破坏溶液中水的电离平衡,使C2电极周围溶液显碱性,实验现象为碳棒上产生气泡且附近溶液变红.
(3)标准状况下224 mL气体是氢气,物质的量是0.01 mol,则转移0.02 mol电子,消耗锌的物质的量是0.01 mol,质量是0.65 g,正极析出铜的质量是0.64 g.设开始时Zn电极和Cu电极质量都为mg,实验后Cu电极和Zn电极质量差为

总之,多池串联装置中电池类型的判断,可根据装置直接判断,也可以根据构成电池的条件判断,还可以根据实验过程中的电极反应现象判断.

