普通型新型冠状病毒肺炎并HIV感染病例报告并文献分析
王 继,宾松涛,李 明,谭 力
(昆明市儿童医院呼吸内科,昆明 650000)
2019年12月以来,湖北省武汉市发生了严重急性呼吸综合征冠状病毒2(severe acute respiratory syndrome coronvirus 2,SARS-CoV-2)引发的人类新型冠状病毒肺炎(COVID-19)〔1-2〕。湖北省为本次疫情的重灾区,全国各省响应国家“一省包一市”的号召。笔者作为援鄂医疗队成员参与湖北省赤壁市的援助工作,在援助过程中发现1 例普通型COVID-19 合并人类免疫缺陷病毒(HIV)感染病例,本文分析此病例的临床特征及治疗方案,并与未感染HIV 的普通型病例进行对比,现报告如下。
1 病例资料
1.1一般资料男性,38 岁,因“呼吸不畅伴低热盗汗3 d”于2020 年2 月9 日住院,患者2020 年1月23 日乘火车(火车上无疑似或确诊病例)从深圳(未接触疑似或确诊病例)返回赤壁,未经武汉,途中一直带有口罩防护。下火车后私家车接回家,途中无疑似或确诊病例接触史,回家后一直未外出,家庭成员中无疑似或者确诊病例,于2 月5日感觉呼吸不畅,咽部不适,伴低热盗汗,自行测量体温37.5 ℃,既往体健。入院查体:体温(T):37.3 ℃,脉搏(P):86 次∕min,呼吸(R):22 次∕min,血压(BP):109∕81 mmHg(1 mmHg = 0.133 3 kPa),血氧饱和度(SpO2):96%,神志清楚,皮肤巩膜无黄染,咽部充血,三凹征(-),口唇无发绀,双肺呼吸音粗,无啰音,心率86 次∕min,律齐,未闻及病理性杂音。腹部软,无压痛及反跳痛,移动性浊音阴性,双下肢无水肿。
1.2实验室检查结果患者入院后检查血常规结果见表1。2020 年2 月10 日COVID-19 核酸检测结果 为 阳性,2020 年2 月19 日HIV 快 速 试 验 及 化 学发光检查检测阳性。病例实验室检查表现为白细胞计数治疗过程中逐渐升高,淋巴细胞计数逐渐减少,中性粒细胞计数逐渐升高,C 反应蛋白(C-reactive protein,CRP)升高,考虑治疗过程中可能存在细菌或真菌感染所致,调整用药后,复查CRP 逐渐下降;COVID-19 核酸检测为阳性,其余病原学检查均阴性,确诊为COVID-19。

表1 血常规及CRP结果
1.3影像学检查患者胸部CT 影像可见多发小片状磨玻璃样改变,其余多个层面,可见类似改变;2020 年2 月20 日复查胸部CT:截取相同层面,可见肺部病变较前片明显进展加重,多个层面可见病变加重;2020 年2 月24 日再次复查胸部CT:截取相同层面,可见病变较前片已明显吸收好转,多个层面可见病变明显吸收。见图1和表2。
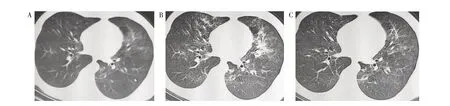
图1 患者胸部CT影像

表2 胸部CT诊断结果
1.4临床诊断及治疗患者确诊COVID-19并HIV感染。患者入院后治疗10 d,仍时有发热,热峰38.7 ℃,轻度咳嗽,仍感觉时有呼吸不畅,无喘息气促及呼吸困难,生命体征尚平稳,查体:神志清楚,呼吸平稳,三凹征(-),口唇、肢端无发绀,双肺呼吸音粗,无啰音,经过前期治疗后,患者呼吸道症状及体征无加重,但仍发热。2020 年2 月19 日HIV快速试验及化学发光检查均阳性,考虑肺部可能合并细菌或真菌感染,由于医院条件所限,无法做相关病原学检查,故经验性调整治疗,2020 年2 月19 日至26 日予复方磺胺甲噁唑片0.96 g,口服,每日3 次,氟康唑氯化钠注射液0.2 g,静脉滴注,每日1 次,洛匹那韦∕利托那韦0.5 g,口服,每日2 次。于2020 年2 月24 日复查胸部CT:肺部病变明显吸收好转;患者体温正常3 d,肺部CT示炎症明显吸收好转,出院前2 次COVID-19 核酸检测阴性,达到出院标准,于2020 年2 月27 日出院,出院后一直口服洛匹那韦∕利托那韦,1 月后复查胸部CT,肺部炎症基本吸收。见表3。
2 讨论
同院收住的未合并HIV 的普通型COVID-19 患者,均常规使用盐酸阿比多尔和利巴韦林治疗,其中盐酸阿比多尔0.2 g,口服,每日2 次;利巴韦林注射液500 mg∕次,静脉滴注,每日2 次。最终所有患者均病情好转出院。
本例患者存在HIV 感染,前期予阿比多尔及利巴韦林抗病毒等治疗后,肺部病变无好转,换用洛匹那韦∕利托那韦抗病毒,并予复方磺胺甲噁唑片,氟康唑氯化钠注射液抗感染治疗后,患者肺部CT示病变明显好转,患者呼吸道症状、体征无加重,故病情有无好转主要依据肺部CT,提示治疗有效。

表3 入院后治疗用药
洛匹那韦∕利托那韦为复方制剂。洛匹那韦为HIV 蛋白酶抑制剂,可阻断HIV 病毒Gag-Pol 聚蛋白的分裂,导致产生未成熟、无感染力的病毒颗粒,利托那韦的作用位点是病毒的天冬氨酰蛋白酶,通过抑制HIV 蛋白酶,使该酶无法处理Gag-Pol多聚蛋白的前体。两者均可导致病毒装配失败而成为未成熟的非感染性病毒。此外,利托那韦通过抑制CYP3A 介导的洛匹那韦代谢,从而增加洛匹那韦的血浆浓度。两者联用可协同增效,抑制病毒反转录〔3〕。
COVID-19 和HIV 病毒同属RNA 病毒,治疗方面可能存在共性。在病毒的复制组装过程中,SARS-CoV-2 可能与HIV 有相似的蛋白功能,洛匹那韦∕利托那韦等HIV蛋白酶抑制剂在抗COVID-19感染时可能通过抑制SARS-CoV-2 蛋白从而发挥治疗作用〔4〕。
HIV 感染人体后通过直接和间接的多种方式杀伤人体免疫细胞,损害免疫调节功能,破坏机体的免疫稳态,因此感染者易出现各种机会性感染和肿瘤〔5-6〕。HIV 可感染人体多种免疫细胞,如CD4+T淋巴细胞、巨噬细胞、树突状细胞等,也可感染脑组织中的小胶质细胞、星形胶质细胞和神经前体细胞,并可在这些细胞中长期低水平复制。CD4+T 淋巴细胞被认为居于免疫系统的核心,其数目的减少、功能的下降是艾滋病的重要特征〔7-8〕。
机会性感染多发生于免疫功能高度抑制的艾滋病患者。研究发现,CD4+T 淋巴细胞计数<200个∕μL 的患者合并侵袭性真菌病的发生率明显高于CD4+T 淋巴细胞计数≥200 个∕μL 的患者,且机会性感染主要发生于CD4+T淋巴细胞计数<100个∕μL的患者〔9-10〕,该患者CD4+T 淋巴细胞计数、CD8+T 淋巴细胞计数均正常,HIV感染处于潜伏期,尚未到达艾滋病期,机会性感染证据不足,但使用抗艾滋病药物及预防机会性感染治疗后,患者病情明显好转。
COVID-19以发热、干咳、乏力为主要表现,少数患者伴鼻塞、流涕、咽痛、肌痛和腹泻等症状〔1〕,该患者以呼吸不畅及发热为主要表现,呼吸道症状及体征不重,病情变化主要依据肺部CT的变化。COVID-19并HIV 感染尚未见报道,我们推测HIV 患者免疫抑制,故予常规利巴韦林及阿比多尔抗感染,效果欠佳。
综上所述,本病例治疗经过提示,当COVID-19患者入院时,需要评估其有无基础性疾病,有无其他传染性疾病,有无混合感染等,全面掌握患者的病史才能为患者提供更好的诊治。尽早使用抗艾滋病药物,以免病情加重。由于医院条件所限,洛匹那韦处于缺药状态,故治疗时无法常规使用该药;若条件允许,建议首先使用洛匹那韦抗病毒治疗,可尽量避免合并HIV 感染的COVID-19 患者病情加重。该患者出院后一直口服洛匹那韦,1 月后复查胸部CT,肺部炎症基本吸收,复查COVID-19核酸阴性,达到痊愈。

