致癌转录因子FOS样抗原1在非小细胞肺癌中的表达及临床意义*
李超明, 张春宁, 李明尧, 林华明
南方医科大学附属茂名市人民医院肿瘤一科,茂名 525000
肺癌(lung carcinoma,LC)是全球癌症相关死亡的主要原因[1],其中非小细胞肺癌(non-small cell lung carcinoma,NSCLC)占全部肺癌的80%[2]。随着早期诊断和治疗方法的进步,早期NSCLC生存率显著提高,但晚期NSCLC预后仍不尽人意,5年生存率低于15%[3]。因此,迫切需要寻找和鉴定新的分子标志物和治疗靶点,以改善NSCLC患者的临床结局[4-5]。致癌转录因子FOS样抗原1(FOS-like antigen 1,FOSL1)是FOS家族的成员,是原癌基因KRAS和c-Jun的下游效应分子,具有促进肿瘤细胞增殖和分化的功能[6]。在体外研究中,发现胃癌、卵巢癌、乳腺癌、胰腺癌细胞系均可检测到FOSL1 mRNA异常表达[7],胃癌细胞中FOSL1高表达可通过调节PI3K/Akt和p53信号通路而促进胃癌进展[8]。体外研究已经证实鳞状细胞癌细胞系中FOSL1基因高表达可促进癌细胞增殖和侵袭[9]。在肺癌细胞系中,发现FOSL1表达上调,并通过调节p53表达而抑制细胞凋亡[10]。尽管如此,FOSL1在NSCLC组织中的表达模式和临床价值尚未见报道。本研究旨在探讨NSCLC中FOSL1的表达,及其与NSCLC患者临床病理特征间的关系及预后价值。
1 材料与方法
1.1 患者病理组织标本收集
收集2013年1月至2015年1月于南方医科大学附属茂名市人民医院接受肺癌手术治疗的110例NSCLC患者肺癌组织标本,经甲醛溶液固定、石蜡包埋处理后,所有组织标本在纳入研究前经2位病理医师根据NSCLC病理分期(TNM分期第8版)标准进行重新确认[11]。纳入标准:①首次诊断NSCLC且按NCCN指南原则进行治疗;②患者除NSCLC外,不存在其他部位的恶性肿瘤;③患者有完整的病历和随访资料。排除标准:随访资料不全或者失访者。本研究通过医院伦理委员会批准同意实施。共30例患者接受了术前新辅助化疗,术后患者均按NCCN指南进行后续化疗。
1.2 患者临床资料的收集和随访
从患者病例资料中获得临床病理数据,包括患者性别、年龄、吸烟状况、肿瘤大小、组织学类型、肿瘤状态、淋巴结转移、远处转移和TNM分期。总生存时间定义为从手术到最后一个随访日或患者死亡之间的时间间隔。无瘤生存时间定义为从手术到首次随访发现复发或随访截止日之间的时间间隔。每半年随访1次,电话或者门诊随访,随访内容包括肿瘤复发和生存情况等,随访截止时间为2020年2月。
1.3 免疫组化染色
将甲醛溶液固定、石蜡包埋的病理组织制备成4 μm切片,组织切片脱蜡并在梯度乙醇中再水合,通过在pH 6.0的乙二胺四乙酸缓冲液中煮沸切片3 min行抗原修复,用3%过氧化氢作用30 min淬灭内源性过氧化物酶活性,使用兔单克隆抗FOSL1抗体(货号ab184441,Abcam,英国)在4℃下孵育过夜,然后与辣根过氧化物酶缀合的抗兔二抗(Sigma-Aldrich,美国)在37℃温育30 min,最后使用辣根过氧化物酶和3,3’-二氨基联苯胺色原溶液处理切片并以苏木精复染。
1.4 免疫组化评分
通过组织切片阳性细胞的密度和染色强度来确定免疫组织化学评分(IHS),即通过病理切片中FOSL1染色的阳性细胞百分比评分与染色强度评分乘积作为最终半定量评分。染色强度评分如下:0分(阴性),1分(弱阳性),2分(中度阳性)和3分(强阳性);FOSL1阳性细胞的百分比评分如下:1分为0%~,2分为11%~,3分为51%~,4分为81%~。免疫组化总得分理论上从0~12分不等。IHS<4分的标本定义为FOSL1低表达,IHS≥4分的标本定义为FOSL1高表达,FOSL1低表达组共42例,FOSL1高表达组共68例。
1.5 统计学分析
使用SPSS 19.0统计软件(SPSS Inc,Chicago,IL)行统计学分析。χ2检验用于检测FOSL1表达与临床病理变量的相关性。使用Kaplan-Meier方法绘制生存曲线,并使用对数秩检验进行比较。Cox比例风险模型用于影响预后的多变量分析。以P<0.05为差异具有统计学意义。
2 结果
2.1 NSCLC组织中FOSL1表达情况
NSCLC组织样品中FOSL1蛋白阳性染色主要定位于NSCLC细胞细胞质中。在110个样本中61.8%(68/110)FOSL1高表达,38.2%(42/110)FOSL1低表达。NSCLC组织中FOSL1典型免疫组化染色见图1。
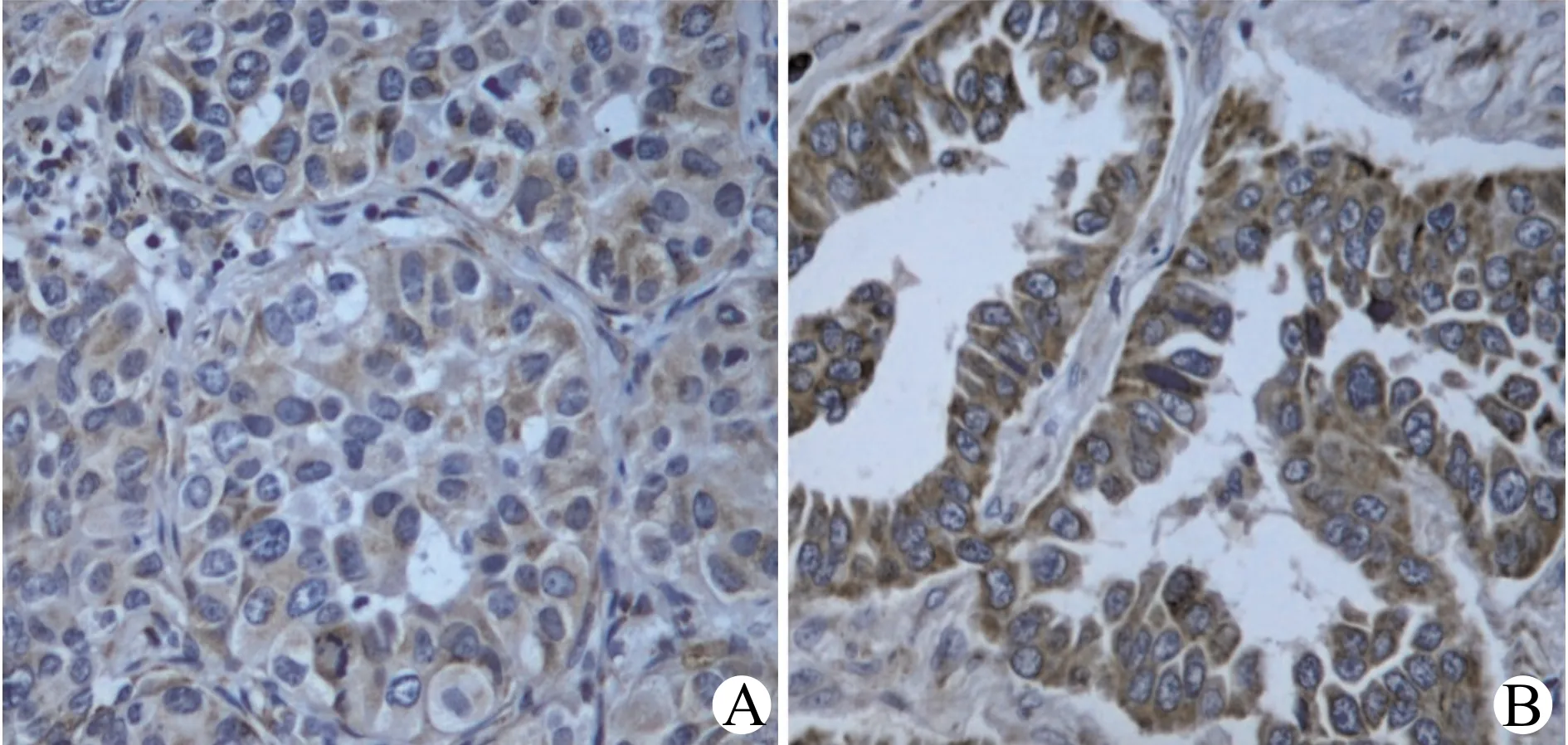
A:FOSL1低表达;B:FOSL1高表达图1 NSCLC组织中FOSL1表达(免疫组化染色,×400)Fig.1 FOSL1 expression in non-small cell lung cancer tissues(Immunofluorescence staining,×400)
2.2 NSCLC组织中FOSL1表达与患者临床病理特征的关系
通过χ2检验分析FOSL1表达与NSCLC临床病理特征间的关系,发现癌组织中的FOSL1表达水平与TNM分期(P=0.022)和淋巴结转移(P<0.01)显著相关,与性别、年龄、肿瘤大小、吸烟状态、组织学类型、远处转移、新辅助化疗及术后化疗无相关性,见表1。

表1 NSCLC患者癌组织中FOSL1表达与 临床病理因素的关系[n(%)]Table 1 Association between clinicopathological factors and FOSL1 expression in NSCLC patients[n(%)]
2.3 NSCLC患者癌组织中FOSL1表达与预后的关系
通过绘制FOSL1高表达和低表达组生存曲线评估FOSL1对NSCLC患者的预后价值。FOSL1高表达组患者无瘤生存率和总生存率均显著低于FOSL1低表达患者(均P<0.01)。FOSL1高表达组患者5年无瘤生存率和总生存率分别为19.3%和29.6%,而FOSL1低表达组患者5年无瘤生存率和总生存率分别为33.5%和43.5%,见图2。
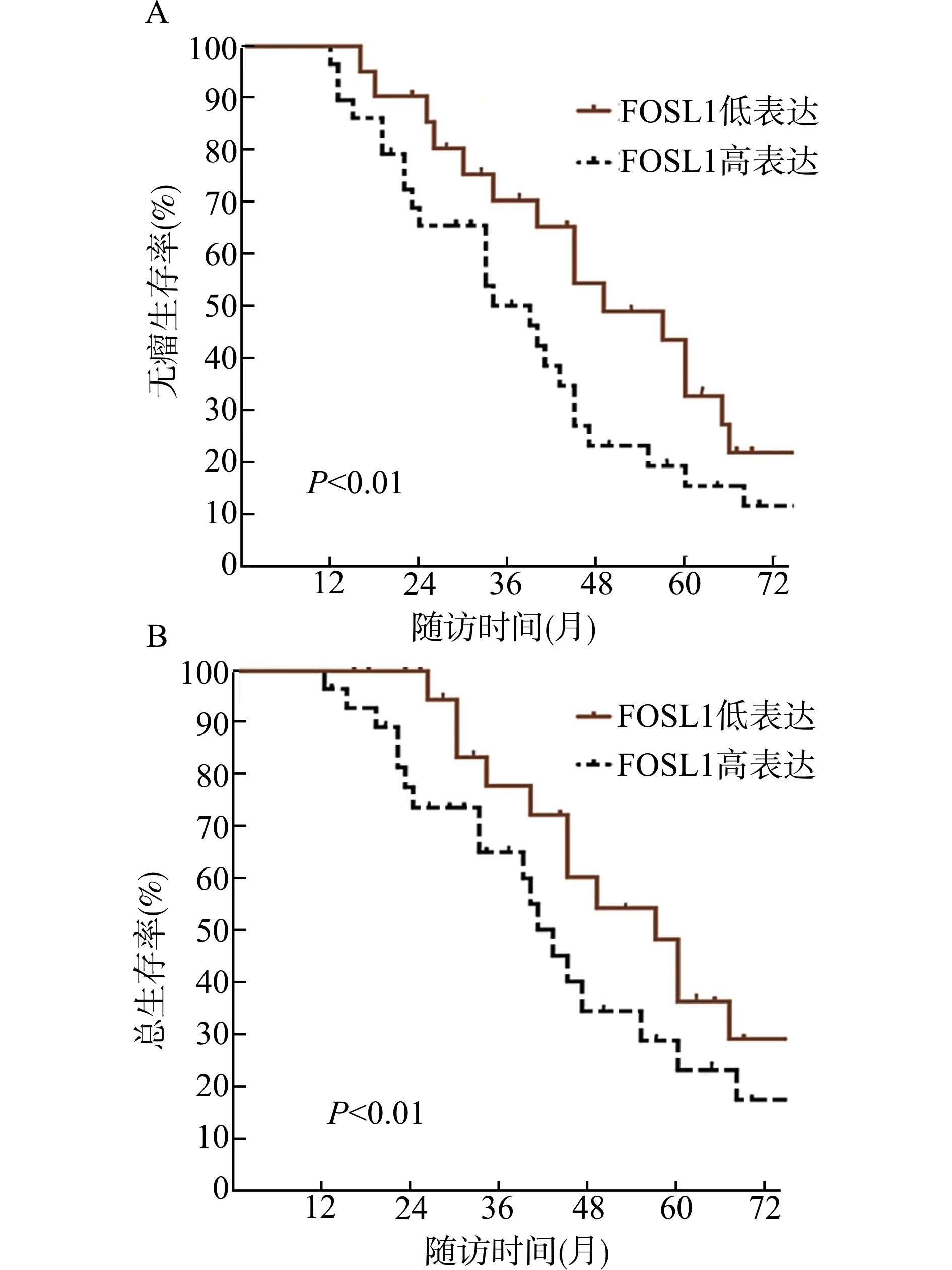
图2 Kaplan-Meier法比较FOSL1高、低表达组患者无瘤生存率(A)和总生存率(B)Fig.2Comparison of tumor-free survival(A)and overall survival(B)between high and low FOSL1 expression NSCLC groups by Kaplan-Meier method
2.4 影响NSCLC患者无瘤生存率的单因素和多因素分析
单因素分析示FOSL1表达、TNM分期及淋巴结转移是影响NSCLC患者无瘤生存率的影响因素;多因素Cox回归分析显示,FOSL1表达、TNM分期及淋巴结转移是影响NSCLC患者无瘤生存率的独立危险因子,见表2。
2.5 影响NSCLC患者总生存率的单因素和多因素分析
单因素分析示FOSL1表达、TNM分期、淋巴结转移及远处转移为影响NSCLC患者总生存率的因素;多因素Cox回归分析显示,FOSL1表达、TNM分期、淋巴结转移及远处转移为影响NSCLC患者总生存率的独立危险因素,见表3。
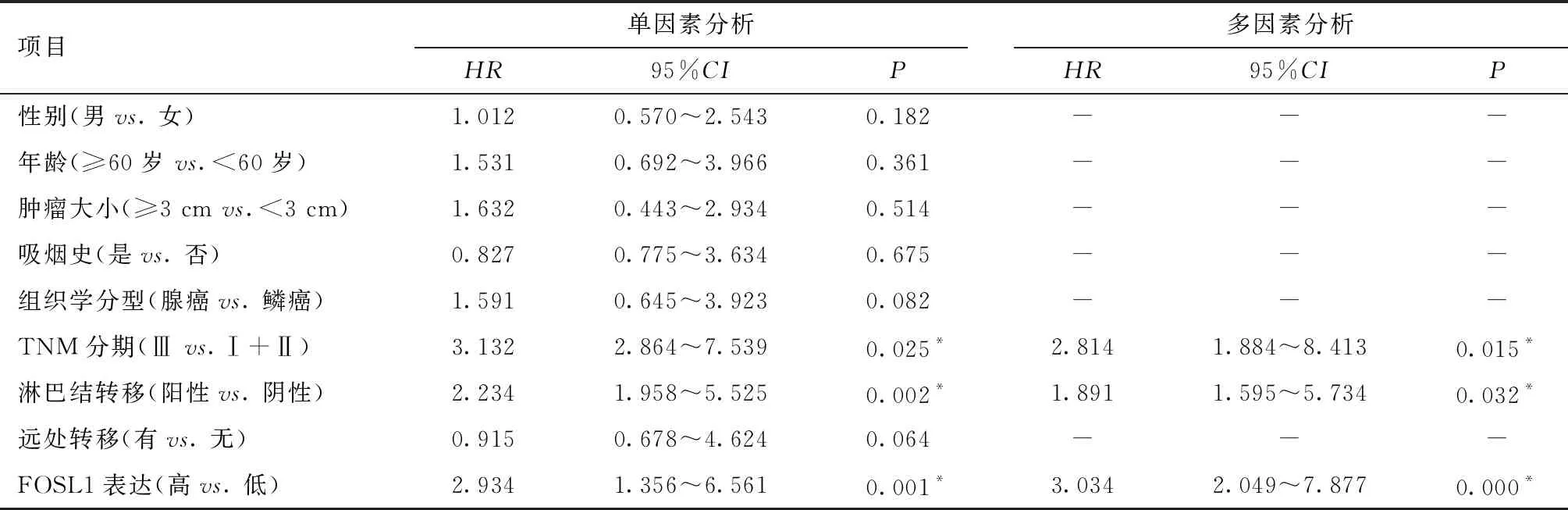
表2 影响NSCLC患者无瘤生存率的单因素和多因素Cox风险比例模型分析Table 2 Cox proportional hazards model analysis of prognostic factors affecting tumor-free survival rate of NSCLC patients
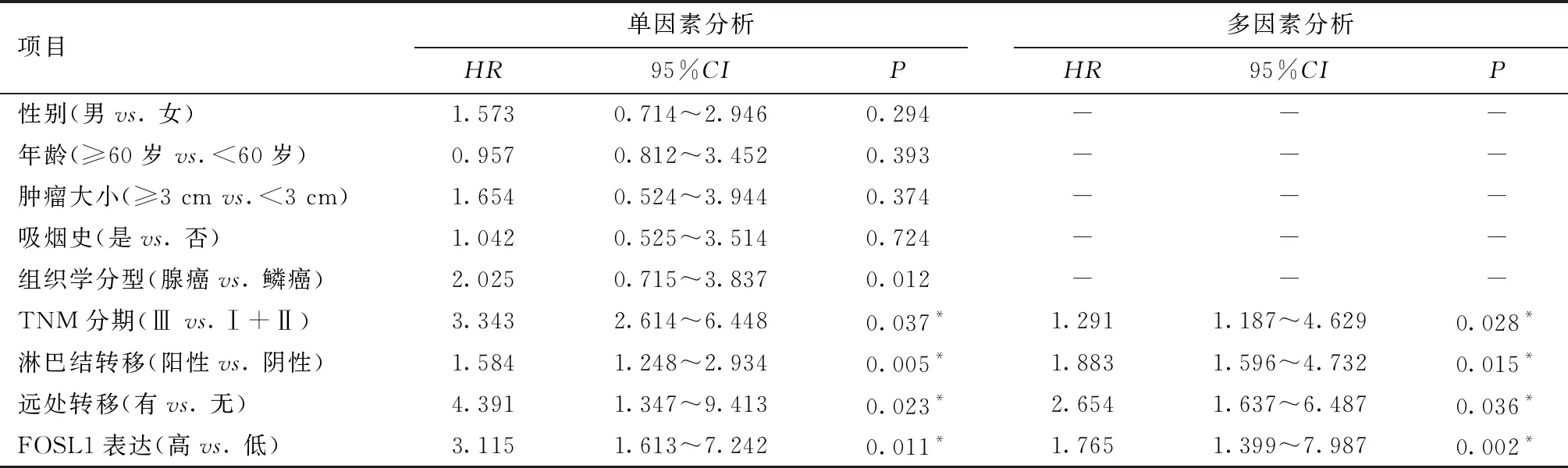
表3 影响NSCLC患者总生存率的单因素和多因素Cox风险比例模型分析Table 3 Cox proportional hazards model analysis of prognostic factors affecting overall survival rate of NSCLC patients
3 讨论
肺癌发病率和死亡率在我国均居恶性癌症第1位[12],且其死亡率高于西方发达国家,死亡人数也不断上升,成为我国居民健康的重要杀手[13]。寻找预测预后并作为治疗靶标的特异性分子标志物对改善NSCLC患者预后尤为重要[14]。
FOSL1是FOS蛋白家族的重要成员之一,FOS蛋白家族还包括FOS、FOSB和FOSL2等蛋白,均由位于11q13.1的基因编码,是KRAS和c-Jun 2个原癌基因的重要下游效应蛋白之一[15]。KRAS是人类上皮肿瘤尤其是肺癌、胰腺癌、结肠癌的原癌基因[16],目前尚无直接抑制KRAS基因的药物,探索新方法用于抑制KRAS的下游分子以消除KRAS的致癌作用已成为研究的热点[17]。目前已经鉴定FOS等8个基因在不同组织来源的突变KRAS肿瘤中过表达[7]。探讨FOSL1在NSCLC中的表达和临床意义可能为NSCLC治疗带来新希望。
本研究发现在110例NSCLC病理标本中61.8%(68/110)高表达FOSL1,38.2%(42/118)低表达FOSL1。最近研究报道[18]在115例胃腺癌患者中,通过免疫组化方法检测FOSL1表达模式,发现FOSL1高表达69例,低表达46例,与本研究结果类似,显示FOSL1在不同癌症中存在表达差异。本研究发现NSCLC组织中的FOSL1表达水平与TNM分期(P=0.012)和淋巴结转移(P<0.01)显著相关,与性别、年龄、肿瘤大小、吸烟状态、组织学类型、远处转移及新辅助化疗和术后化疗无关。研究报道FOSL1高表达与TNM分期和淋巴结转移密切相关,提示FOSL1高表达与患者疾病严重程度和肿瘤侵袭性密切相关[19],上述结果提示FOSL1高表达的NSCLC患者,其肿瘤显示出更高的恶性程度。
本研究通过Kaplan-Meier生存分析发现FOSL1高表达的NSCLC患者预后显著差于FOSL1低表达患者,Cox比例风险模型分析提示FOSL1表达为影响患者无瘤生存率和总生存率的独立预后标志物。据文献报道[18],在胃腺癌患者中,FOSL1高表达可作为影响术后总生存率的独立危险因素[18]。有研究通过检索NCBI Gene Expression Omnibus数据库,检测577例结肠癌病理标本中FOSL1表达情况,发现FOSL1高表达是结直肠癌患者无瘤生存率独立预测因素,虽未探讨FOSL1表达对结直肠癌患者总生存率的影响,但研究证实FOSL1高表达是促进结直肠癌转移的一个重要促进分子[20]。
FOSL1高表达和NSCLC患者不良预后相关的机制尚不清楚,其可能机制如下:①在KRAS癌基因驱动的肺癌中,研究发现与正常肺上皮相比,NSCLC组织中FOSL1表达显著增加[7],FOSL1是KRAS下游效应分子,突变KRAS和MAPK激活通常促进细胞异常有丝分裂和细胞增殖[21],其高表达可能通过促进癌细胞增殖而参与NSCLC增殖和进展,并影响预后;②体外研究显示在前列腺癌细胞中FOSL1高表达可促进肿瘤细胞上皮-间质转化,并促进癌细胞增殖、侵袭和转移[22],而在黑色素瘤细胞系中也存在类似发现,即FOSL1高表达有利于上皮-间质转化过程并促进癌细胞脱落[23];③ FOSL1可能受到非编码RNA或miRNA调控而发生表达异常,研究显示,在食管癌中长链非编码RNA AGAP2-AS1可上调miRNA-195-5p并抑制FOSL1基因表达进而抑制食管癌细胞的增殖和侵袭能力[24]。在NSCLC中,FOSL1通过何种机制而影响其预后尚不清楚,值得进一步研究。
本研究存在如下不足:本研究为单中心的回顾性研究,纳入病例数目较少,尚需要多中心大样本研究来证实本研究结论,同时,FOSL1影响NSCLC患者预后的分子机制尚需要进一步研究。
总之,本研究发现NSCLC组织中FOSL1高表达与患者TNM分期和淋巴结转移密切相关;FOSL1高表达是NSCLC患者预后不良的独立危险因素,可作为预测NSCLC预后的新的分子标志物。未来需要进一步探索FOSL1促进NSCLC进展的具体机制。

