基于实验专题的模型认知——以常见气体的制备微专题为例
重庆 王 明 陈厚波

一、气体制备实验的基本思维模型

1.发生装置
发生装置的选择应从反应原理入手,根据反应物的状态和反应条件综合选择。高中化学中有如图所示几类发生装置值得我们重点注意。
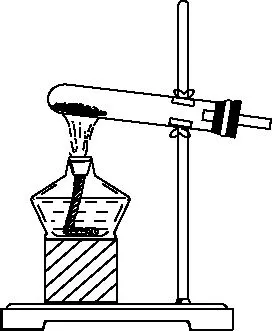
图1
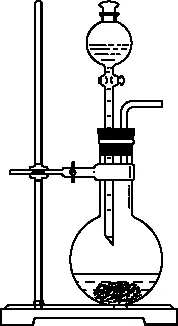

2.净化除杂
反应原理中涉及的易挥发的物质,如反应物、副产物或水蒸气等,是最主要的杂质气体。为避免对后续的收集或性质检验造成影响,应想办法将其一一除去。

图4

图5

图6
(1)洗气瓶:如上图4所示,注意气体“长进短出”时进行的步骤为洗气。
(2)干燥管:球形干燥管(如上图5所示),气体应“大进小出”;“U”形干燥管(如上图6所示),气体可从任意一边进入。
(3)要注意气体在进入加热的玻璃仪器前,都应该先干燥以避免仪器受热不均而炸裂。
3.收集装置
根据制备气体的物理性质(密度、溶解性等),选择合适的收集装置是气体制备实验的重要环节。通过对历年高考试题和考试大纲的分析发现,有如下两种方式值得我们重点注意。
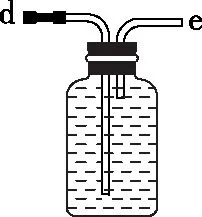
图7

图8
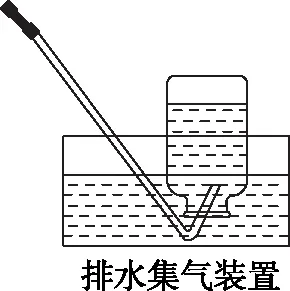
(1)排水法:装置如上图7所示,集气瓶中应事先装满水,气体应该从e口进入。
(2)排空气法:装置如上图8所示,密度比空气小的气体应该从e口进入,密度比空气大的气体应该从d口进入。
4.尾气处理
化学核心素养中“科学精神和社会责任”,要求化学教师和有化学素养的学生能够改变大众对化学的固有认识——有毒、有害、污染严重。气体制备或性质检验实验完成后,为了避免对环境的污染,通常需要进行尾气处理。
(1)溶液吸收:酸性气体用碱性溶液吸收,如CO2、Cl2和SO2可以用NaOH溶液吸收;碱性气体可以用酸溶液吸收,如NH3可用稀硫酸吸收;易溶于水的气体可用蒸馏水吸收,如NH3、HCl。还应注意的是,某些气体如NH3,在用溶液吸收尾气时,要注意防倒吸。
极易溶于水的气体才考虑防止倒吸,如NH3(1∶700)、HCl(1∶500)、SO2(1∶40);其余如CO2、Cl2等,即使用NaOH溶液吸收,也不考虑防倒吸。
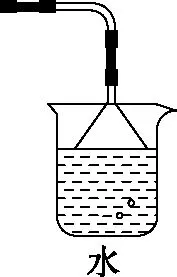
(2)固态试剂吸收:如SO2、CO2、Cl2等酸性气体,可以用装有碱石灰的干燥管吸收。

(4)吸收尾气同时防止空气中的某种成分进入:常见的是装置最后连接装有碱石灰的干燥管,除了吸收尾气外还具有隔离空气中的水和CO2的功能;类似的装置还可以是,最后连接装有浓硫酸的洗气瓶,除了吸收碱性的尾气外也可以隔离空气中的H2O(g)。
二、高中常见气体的制备模型
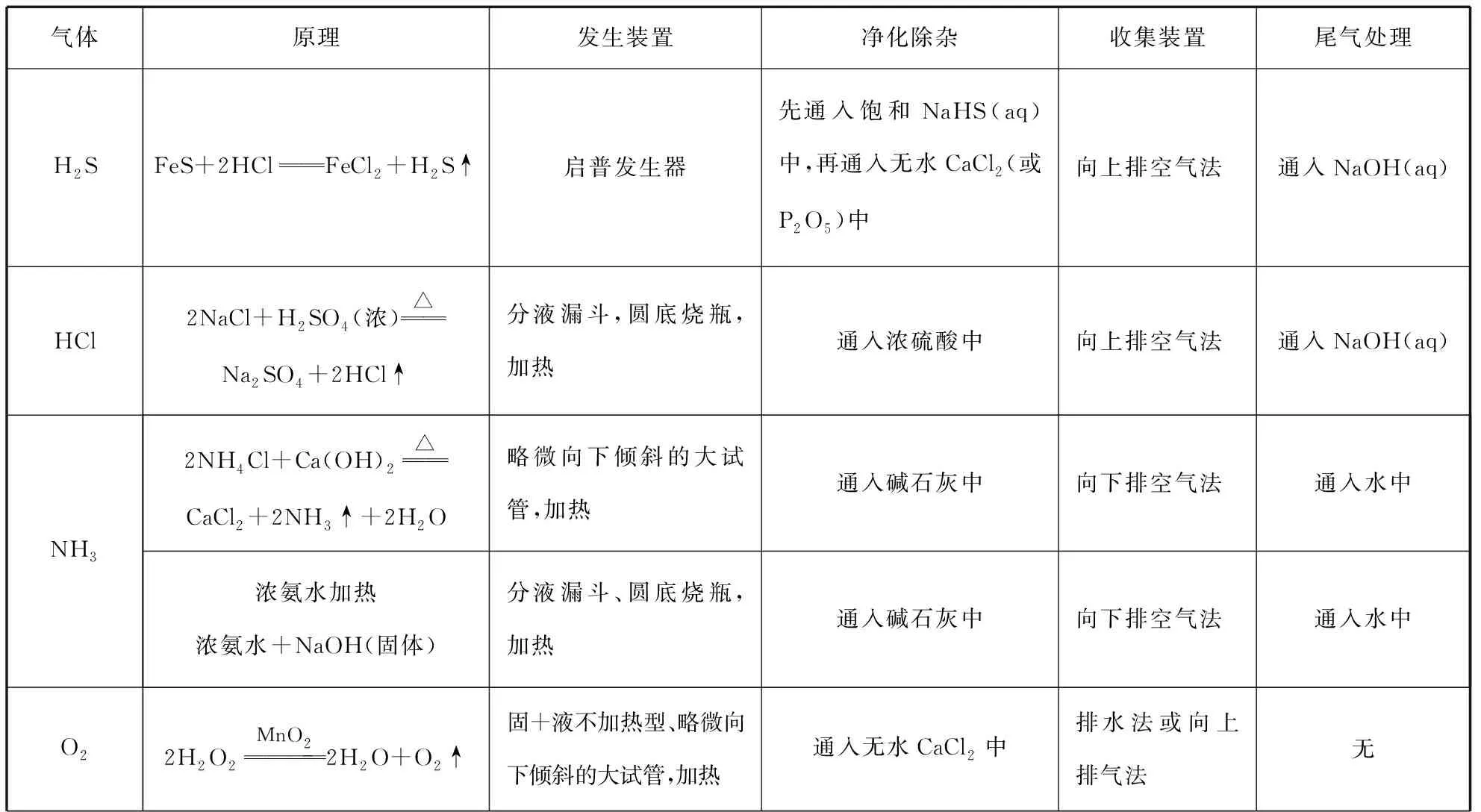
气体原理发生装置净化除杂收集装置尾气处理H2SFeS+2HClFeCl2+H2S↑启普发生器先通入饱和NaHS(aq)中,再通入无水CaCl2(或P2O5)中向上排空气法通入NaOH(aq)HCl2NaCl+H2SO4(浓)△Na2SO4+2HCl↑分液漏斗,圆底烧瓶,加热通入浓硫酸中向上排空气法通入NaOH(aq)NH32NH4Cl+Ca(OH)2△CaCl2+2NH3↑+2H2O略微向下倾斜的大试管,加热通入碱石灰中向下排空气法通入水中浓氨水加热浓氨水+NaOH(固体)分液漏斗、圆底烧瓶,加热通入碱石灰中向下排空气法通入水中O22H2O2MnO22H2O+O2↑固+液不加热型、略微向下倾斜的大试管,加热通入无水CaCl2中排水法或向上排气法无

续表
三、模型认知基础上的证据推理
气体制备及其性质检验作为化学实验的重要组成部分,在高考中频繁出现,有时甚至成为实验考试的主角。熟练掌握上述的几种制备方法后,运用思维模型,辅以严密的证据推理即可解决高考中出现的相关问题。
【例1】(2019·全国卷Ⅰ·9)实验室制备溴苯的反应装置如下图所示,关于实验操作或叙述错误的是
( )
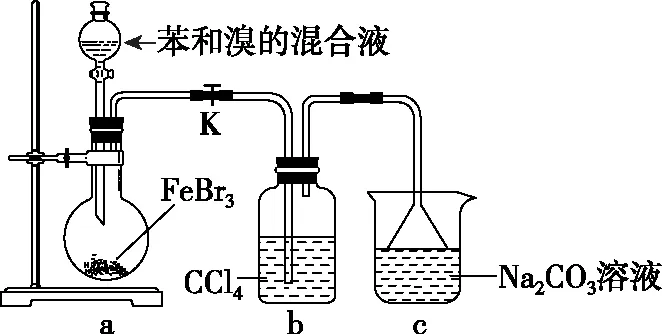
A.向圆底烧瓶中滴加苯和溴的混合液前需先打开K
B.实验中装置b中的液体逐渐变为浅红色
C.装置c中的碳酸钠溶液的作用是吸收溴化氢
D.反应后的混合液经稀碱溶液洗涤、结晶,得到溴苯
【答案】D
【解析】此题类似于气体制备,并检验、吸收某些物质。运用上述的思维模型可得:


无收集HBr装置。
据此分析,A、B、C均正确,D中应是利用苯和溴苯的沸点差距进行蒸馏。故答案为D。
【例2】(2017·全国卷Ⅰ·10)实验室用H2还原WO3制备金属W的装置如图所示(Zn粒中往往含有硫等杂质,焦性没食子酸溶液用于吸收少量氧气)。下列说法正确的是
( )

A.①、②、③中依次盛装KMnO4溶液、浓H2SO4、焦性没食子酸溶液
B.管式炉加热前,用试管在④处收集气体并点燃,通过声音判断气体纯度
C.结束反应时,先关闭活塞K,再停止加热
D.装置Q(启普发生器)也可用于二氧化锰与浓盐酸反应制备氯气
【答案】D


后面没有收集和尾气处理装置。④处收集并点燃气体判段纯度(除去空气)。根据前述分析得出:A错误;B正确;反应结束时,为避免④后空气中的氧气进入氧化金属W,应“先停止加热,待冷却后再关闭活塞,停止产生H2”,故C错误;启普发生器并不能加热,故D错误。
【例3】(2016·全国卷Ⅰ·26节选)选氮的氧化物(NOx)是大气污染物之一,工业上在一定温度和催化剂条件下用NH3将NOx还原生成N2。某同学在实验室中对NH3与NO2反应进行了探究。回答下列问题:
(1)氨气的制备

A

B

C
D

E

F
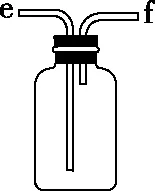
①氨气的发生装置可以选择上图中的________,反应的化学方程式为_________________
②欲收集一瓶干燥的氨气,选择上图中的装置,其连接顺序为:发生装置→________________(按气流方向,用小写字母表示)。

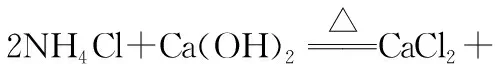



四、实验方案的分析与评价
从思维层级来看,上述试题仅涉及了解、模仿、应用等低层级思维,高考作为一种选拔性考试,肯定会涉及分析、综合、评价等高层级思维。对制备或性质检验实验的评价与分析的本质——对模型“发生→净化除杂→收集→尾气处理”中的某个或某几个部分提出评价和改进意见。

(1)草酸晶体受热分解后得到的气体主要成分有________,甲同学利用下图的装置验证分解产物中的CO2,乙同学仔细分析后认为此装置最大的问题是________。
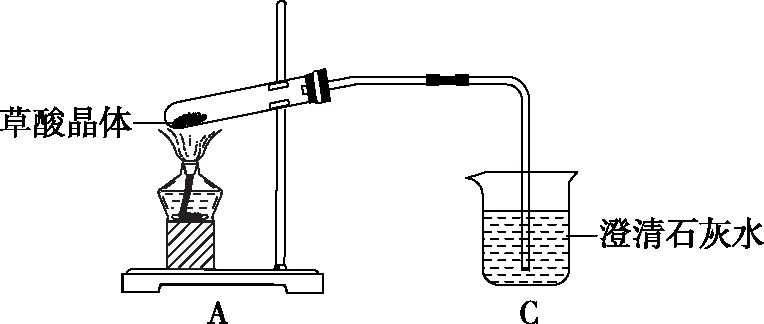
(2)乙同学改进后的装置如下图所示,则装置B的作用是_________________
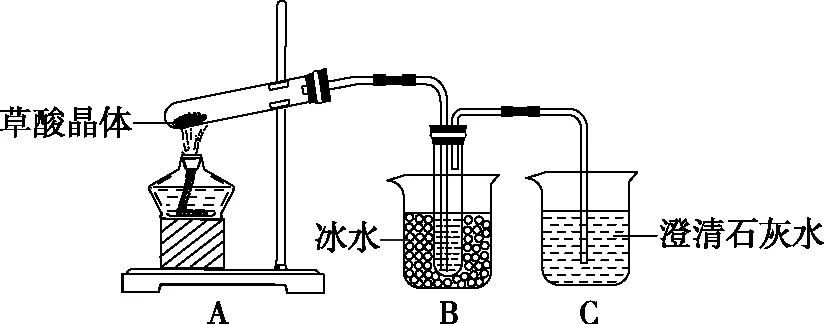
(3)丙同学仔细观察乙同学设计的装置图后,认为方案中A装置的大试管口应略向下倾斜。这种认识是否正确,并简要说明理由_________________
(4)甲、乙、丙三位同学讨论后,决定对A装置再次改进,下列哪种改进方案最合理________。(填序号)

a
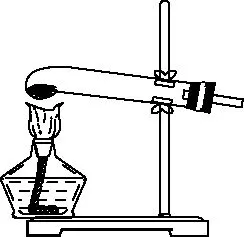
b

c
(5)丁同学为了验证分解产物中的CO,选用乙同学实验中的装置A、B和如图所示的部分装置(可以重复选用)进行实验。

D

E

F

G
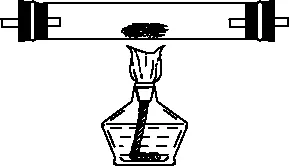
H
I
①丁同学的实验装置中,依次连接的合理顺序为A、B、________。装置H反应管中盛有的物质是________。
②能证明草酸晶体分解产物中有CO的现象是_________________
【答案】(1)CO、CO2和H2C2O4·2H2O(g) 净化装置部分没有排除H2C2O4·2H2O(g)对CO2鉴别的干扰
(2)使H2C2O4·2H2O(g)冷凝,排除对CO2鉴别的干扰
(3)错误,草酸晶体的熔点为101℃,此物质受热分解变为液态,试管口向下倾斜是错误的
(4)b
(5)①F、D、G、H、D、I CuO粉末 ②H中的黑色粉末变红,H后连接的D中澄清石灰水变混浊
【解析】(1)根据分解反应的化学方程式和题目已知能得出受热分解的主要气体有:CO、CO2和H2C2O4·2H2O(g);根据题目信息能使澄清石灰水变混浊的也可能是H2C2O4·2H2O(g),所以实验装置最大的问题是净化装置部分没有排除H2C2O4·2H2O(g)对CO2鉴别的干扰。
(2)装置B中用冰水冷凝的作用是将H2C2O4·2H2O(g)冷凝,排除对CO2鉴别的干扰。
(3)按固体加热实验操作规范,试管口确实应该略向下倾斜,但根据信息草酸晶体的熔点为101℃,此物质在分解升华前应先变为液态,若发生装置的试管口仍然向下倾斜会使液体下滴,故乙同学的看法是错误的。
(4)固体加热时试管口向上不符合操作规范,但试管口向下又会使液体下滴,所以综合来看b是最好的解决方案。
(5)检验CO时应利用其还原性,但有还原性气体很多,故需要同时检验反应后的产物CO2;同时,CO2和H2C2O4·2H2O(g)的存在对CO检验的现象有影响,故在检验之前应考虑利用净化装置将其除去;完成实验后,应考虑有毒气体CO的尾气处理,还要注意的是气体物质在进入加热装置前最好先干燥,以免引发试管破裂的危险。①合理顺序为A→B→F→D→G→H→D→I;H中应加入黑色的CuO粉末。②H中的黑色粉末变红,其后连接的D中澄清石灰水变混浊。
化学核心素养中“证据推理与模型认知”揭示了学生在考试中解决化学问题的一般方法——头脑中提取解题模型→题目中获取各种证据→证据推理和数据演绎→正确答案。实际教学实践中教师和学生总是希望一个模型能解决所有的化学问题,而这是绝不可能达到的!为了解决这个矛盾,学生会争取多“刷题”,希望能建立起足够多的解题模型,以便解决各种考试中的化学问题。教师应该做些什么呢?笔者认为,教师应该通过自己的分析总结让一个模型尽可能多的解决化学问题,从而真正的解放和提升学生。

