高三复习中有关条件控制类试题归纳与详解
江苏 季宗宝
化学与我们的生产生活联系非常紧密,通过分析2016~2019年全国卷各卷区的高考试题,在化学实验题、工艺流程题里面一定会出现条件控制类的试题,而且这类试题的出题形式也越来越向着多样化、创新化形式发展,是高考化学中重点考查的题型之一。通过条件控制等来解决实际问题,也是化学在生产、生活中应用的一种重要体现。题目一般不是很难,只要明确问题形式,掌握基础知识,就能够得到相应的分数,对于提高学生成绩,培养学生学习化学的兴趣,有重要的意义。下面笔者就对条件控制问题的常见考查角度、相应的措施和目的进行归纳,并通过历年真题的形式了解在高考试题中的应用,从而了解命题的规律和解题的方法,最终提高考生解决化学问题能力,提升考生的化学核心素养。
一、常见考查角度
类型1:工业操作中条件控制的措施
【例1】(2019·全国卷Ⅲ·26改编)高纯硫酸锰作为合成镍钴锰三元正极材料的原料,工业上可由天然二氧化锰粉与硫化锰矿(还含Fe、Al、Mg、Zn、Ni、Si等元素)制备,工艺如图所示。回答下列问题:

相关金属离子[c0(Mn+)=0.1 mol/L]形成氢氧化物沉淀的pH范围如下:

金属离子Mn2+Fe2+Fe3+Al3+Mg2+Zn2+Ni2+开始沉淀的pH8.16.31.53.48.96.26.9沉淀完全的pH10.18.32.84.710.98.28.9
(1)为了提高“溶浸”的反应速率,可以采取的措施有______________________________(答出一点即可)。
(2)“调pH”除铁和铝,溶液的pH范围应调节为________~6之间。
(3)在“氧化”过程中,氧化剂除了可以选择MnO2,还可以使用________。
【答案】(1)将矿石粉碎、适当增加硫酸的浓度、加热、加快搅拌等
(2)4.7
(3)H2O2
【解析】(1)提高“溶浸”反应速率的答案有很多,但也要注意答题语言的规范性,如“粉碎”不可写作“压扁”,“搅拌”最好写成“加快搅拌”,另外“催化剂”尽量少写或不写,因为催化剂只是针对少部分反应才有效。
(2)“调pH”除铁和铝,溶液的pH一定要大于等于Fe3+和Al3+完全沉淀时的pH,故应该为4.7。
(3)对于氧化剂的选择要注意不能引入新的杂质,最好反应后便于除去,氧化Fe2+,最常用试剂是H2O2,此外这个反应的离子方程式也是常考考点之一。
【拓展练习】题干信息同【例1】
(1)在“溶浸”时,需加入的试剂是________;
(2)除了使用MnO2进行“氧化”,还可以采用什么试剂________;
(3)在“沉锰”过程中,反应温度不能太高,实验中,可采取的措施是______________。
【答案】(1)稀硫酸
(2)H2O2
(3)放入冰水浴中
【注意】1.确定pH的调节范围时要根据离子完全沉淀或开始沉淀的数值来选择,要避免取值范围有所重叠。若要除去Mn2+溶液中含有的杂质Fe2+,应该先加双氧水把Fe2+氧化成Fe3+,再调节pH至2.8~8.1。

类型2:与控制条件有关的目的或原因分析
【例2】题干信息同【例1】
(1)“氧化”中添加适量的MnO2的作用是____________________________。
(2)“除杂1”的目的是除去Zn2+和Ni2+,“滤渣3”的主要成分是________。
(3)“除杂2”的目的是生成MgF2沉淀除去Mg2+。若溶液酸度过高,Mg2+沉淀不完全,原因是______________________。
【答案】(1)将Fe2+氧化成Fe3+
(2)ZnS和NiS


【例3】(2019·全国卷Ⅰ·27改编)硫酸铁铵[NH4Fe(SO4)2·xH2O] 是一种重要铁盐。为充分利用资源,变废为宝,在实验室中探究采用废铁屑来制备硫酸铁铵,具体流程如下:

回答下列问题:
(1)步骤①的目的是去除废铁屑表面的油污,方法是________________________________________。
(2)步骤②需要加热的目的是______________,
温度保持80~95℃,采用的合适加热方式是______________。
(3)步骤③中选用足量的H2O2,理由是__________________。分批加入H2O2,同时为了______________,溶液要保持pH小于0.5。
【答案】(1)碱煮水洗
(2)加快反应 热水浴
(3)将Fe2+全部氧化为Fe3+且不引入杂质 防止Fe3+水解
【解析】(1)热碱溶液可以洗去油污。(2)加热的目的一般都是加快反应速率,如果保持温度恒定一般采用水浴法,但要写清是“冷水浴”还是“热水浴”,当温度超过100℃时可选择油浴法。(3)由图可知在步骤②中加入稀硫酸则产生Fe2+,而步骤③中产生了Fe3+,则是将Fe2+全部氧化为Fe3+,最后溶液要保持pH小于0.5,则是防止Fe3+水解。
【拓展练习】以软锰矿(主要成分为MnO2、SiO2等)为原料制备高纯MnO2的流程如下:

(1)酸浸时,为提高酸浸速率,通常加入FeSO4溶液,FeSO4的作用可能是______________;
(2)酸性条件下,用合适的氧化剂可以将MnSO4转化为高纯MnO2。
①用NaClO3作氧化剂时会同时产生NaCl,该反应的离子方程式为______________________。反应中NaClO3的用量不宜过多的原因是______________。
【答案】(1)作催化剂
过量的NaClO3在酸性条件下与氯离子反应生成有毒的氯气
【解析】(1)由题干信息可知,操作的目的是“提高酸浸速率”,而且FeSO4溶液又不参与反应,所以应该想到作催化剂,而且Fe3+也是化学反应中常用的一种催化剂。

二、知识要点总结

控制条件措施和目的控制pH1.调节溶液的pH,就是控制溶液的酸碱性,从而抑制某些离子的水解,在某些物质的制备时可通过加酸抑制某些阳离子如Fe3+、Cu2+、Al3+、Zn2+等的水解2.加酸、加碱,使可溶性金属离子进入溶液,不溶物通过过滤除去,如除去铁矿石中的SiO2可加入稀盐酸或稀硫酸,或除去镁铝合金中的铝加入氢氧化钠溶液等3.某些金属离子控制溶液酸碱性使某些金属离子形成氢氧化物沉淀。如除溶液中的Zn2+、Fe3+,加碱形成Zn(OH)2、Fe(OH)3沉淀除去

续表
三、即时训练
【练习】工业上利用废镍催化剂(主要成分为Ni,还含有一定量的Zn、Fe、SiO2、CaO等)制备草酸镍晶体的流程如下:

(1)请写出一种能提高“酸浸”速率的措施:______________________;滤渣Ⅰ的成分是CaSO4和________(填化学式)。
(2)除铁时,控制不同的条件可以得到不同的滤渣Ⅱ。已知滤渣Ⅱ的成分与温度、pH的关系如图所示:
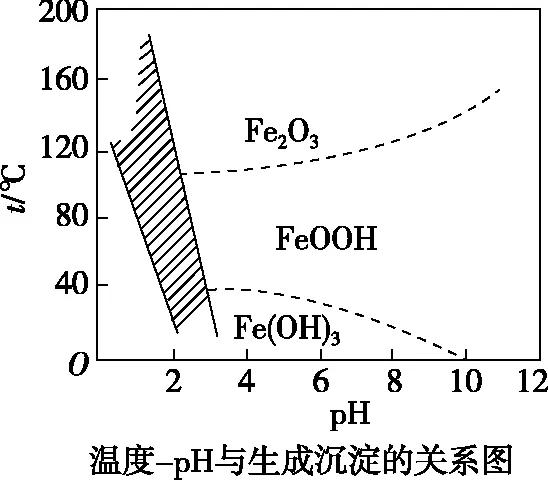
①若控制温度40℃、pH=8,则滤渣Ⅱ的主要成分为________(填化学式)。
②若控制温度80℃、pH=2,可得到黄铁矾钠[Na2Fe6(SO4)4(OH)12] 沉淀(图中阴影部分),写出生成黄铁矾钠的离子方程式:________________________。
(3)已知除铁后所得100 mL溶液中c(Ca2+)=0.01 mol·L-1,加入100 mL NH4F溶液,使Ca2+恰好沉淀完全即溶液中c(Ca2+)=1×10-5mol·L-1,则所加c(NH4F)=________mol·L-1。[已知Ksp(CaF2)=5.29×10-9]
(4)加入有机萃取剂的作用是______________。
【答案】(1)把废镍催化剂粉碎、适当加热,适当增大酸的浓度或搅拌等 SiO2
(3)6.6×10-2
(4)除去溶液中的Zn2+
【点评】本题考查工业上利用废镍催化剂制备草酸镍晶体的工艺流程,侧重考查物质分离的实验设计和方法应用,主要是利用溶液不同条件下离子沉淀的情况不同,控制溶液pH除去杂质离子,同时考查除杂原则不能引入新的杂质,解题时先要弄清制备流程中各步反应原理和目的以及读图能力,从而知道分离提纯的环节中各成分组成,再结合氧化还原反应和沉淀溶度积等知识解决各问题。


