促进核心素养发展的单元复习教学视角分析——以鲁科版新教材“原子结构与元素周期律”单元教学为例
浙江 王爱富
“原子结构与元素周期律”教学单元的学习,主要培养学生宏观辨识与微观探析、证据推理与模型认知以及科学探究与创新意识等化学学科核心素养。该教学单元包括原子结构、元素周期律和元素周期表以及元素周期表的应用三个部分知识,为了使知识更加符合学生的学习规律和认知规律,提升学生化学学科的核心素养,笔者建议本教学单元可以从以下几个方面组织复习教学。
1.明确学习路径,形成结构化教学内容
根据知识的内在逻辑关系以及学生的认知规律,本教学单元的学习路径一般为建立原子结构模型→原子结构与元素性质之间的关系→元素周期律的表现→元素周期表→元素周期表的应用。根据学习路径形成结构化的教学内容,如图1所示。因此促进具体性知识向核心观念的构建转化、结论性知识的获得向能力和素养的转化,需要组织结构化的教学内容。内容的结构化则是实现这种转化的关键,也是课堂教学的首要任务。
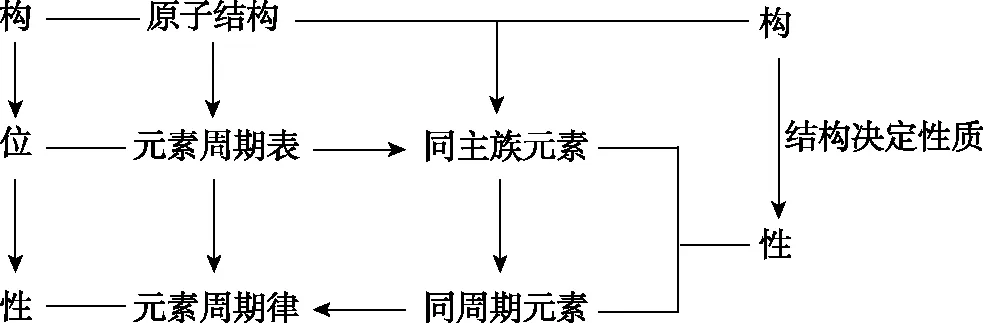
图1 原子结构与元素周期知识的逻辑关系
2.注重认知角度和思路的培养,建立认知模型,促进知识向能力素养的转化
教学要注重从微观结构角度探析原子结构与元素性质之间的关系,从物质的组成、结构、分类角度宏观辨识物质的相似性和递变性,以此建立认识模型,促进知识向能力素养的转化。为此,复习教学要突出以下两个认识模型的构建:
(1)以实例为证据进一步强化“位、构、性”关系的思维模型
元素的原子结构、元素在周期表中的位置及元素的性质(位、构、性)三者之间的关系的思维模型为:

图2 “位、构、性”三者之间的关系的思维模型
【案例1】砷(As)及其化合物被广泛应用于除草剂、杀虫剂以及含砷药物中,已知砷位于周期表中第四周期ⅤA族。回答以下问题:
(1)As原子的最外层电子数是________个;As最低价态对应的氢化物M的化学式是________。
(2)NH3与M相比,稳定性更强的是________。(填化学式)还原性更强的是________。(填化学式)
(3)As元素的最高价氧化物的水化物P的化学式是________;已知As2O3是一种两性偏酸性的氧化物,As2O3是H3AsO3的酸酐。写出As2O3与足量氢氧化钠溶液反应的离子方程式:________________________。

通过实例,理解学业要求“能用原子结构知识解释元素性质及其递变规律,并能结合实验及事实进行说明;能利用元素在周期表中的位置和原子结构特征,分析、预测、比较元素及其化合物的性质”,并能用“位、构、性”关系的思维模型进行思考问题、解决问题,逐步养成“结构决定性质”的核心观念。
(2)建立“物质的一般性质——氧化性和还原性——相似性和递变性”的元素及化合物性质的三维模型
经过无机元素及化合物知识的学习,建立从物质类别的一般属性、元素价态变化的氧化性和还原性等角度认识元素及化合物型性质的认知模型。通过碱金属和卤族元素性质的相似性和递变性的实验探究、第三周期元素性质递变规律的实验探究等,进一步发展元素及化合物化学性质的认知模型,逐渐建立“物质的一般性质——氧化性和还原性——相似性和递变性”的元素及化合物性质的三维模型,如图3所示。
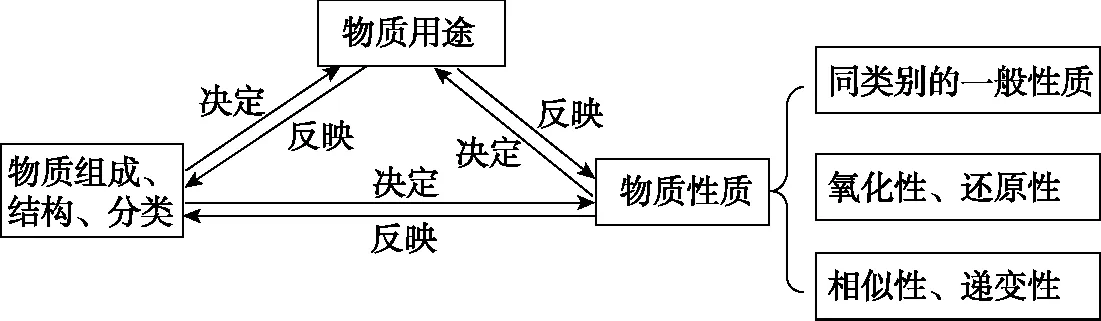
图3 物质结构、性质与用途关系
【案例2】硒(Se)是人体必需的微量元素,在周期表中的位置如表,回答下列有关问题:

(1)根据Se元素在周期表中的位置,请推测Se元素一般表现的化合价有哪些?
(2)写出Se和Br的最高价氧化物对应的水化物的化学式,并比较两者酸性的相对强弱。
(3)工业上在硒的提取过程中用NaOH溶液浸取含硒物料焙烧后生成的二氧化硒,在浸取液中用硫酸酸化后通入SO2,能析出Se。
①请用化学方程式表示该浸取过程的变化;
②根据上述析出Se的变化,比较SO2与SeO2的氧化性强弱。
【解析】根据Se与O、S是同主族元素,则位于元素周期表第ⅥA族,则Br位于第ⅦA族。因同主族元素性质具有相似性,可推测Se元素的化合价应该有-2、+4和+6价;Se与Br位于同周期,据同周期元素性质的递变性,可知Br的非金属性强于Se,即HBrO4的酸性强于H2SeO4。

通过实例分析可知,对元素化合物性质的认识,从“各类物质的一般性质——氧化性和还原性”的二维模型进一步发展到“各类物质的一般性质——氧化性和还原性——相似性和递变性”的三维模型,可以将知识结论转化为学生的思维和认识角度、认识思路和推理路径、推理判据等能力素养的提高,从而彰显核心知识的素养发展价值。
3.充分理解进阶式学习活动任务体系的设计,科学评价学科核心素养,实现“教—学—评”一体化
教材设计了“学习—理解”到“应用—实践”再到“迁移—创新”的学习进阶活动任务体系。已有研究表明,“学习—理解”到“应用—实践”再到“迁移—创新”是从知识到能力再到素养的转化途径,也是学科核心素养发展的学习进阶,更是科学评价学科核心素养水平的能力活动任务体系。所以复习教学应充分理解该进阶式能力活动任务体系,章节的核心素养发展目标与学业要求,为设定教学目标、评价目标提供依据,从而有利于实现“教—学—评”一体化。
本教学单元主要发展学生的宏观辨识与微观探析、证据推理与模型认知以及科学探究与创新意识等核心素养。通过“学习—理解”到“应用—实践”再到“迁移—创新”的学习进阶活动任务的有效设计,实现从知识向能力素养的转化。学习活动进阶设计应注意以下几点:
(1)根据学业要求,充分理解学习活动进阶的设计
学业要求“能画出1~20号元素的原子结构示意图,能用原子结构知识解释元素性质”“元素在周期表中的位置和原子结构特征”“能列举化学科学发展的重要事件,说明对推动社会发展的贡献”等可以从“学习—理解”层面设计学习活动任务;“能利用元素在周期表中的位置与原子结构特征,分析、预测、比较元素及其化合物的性质”等可以从“应用—实践”层面进行学习活动任务的设计;“具有较强的问题意识,能提出化学探究问题,能做出预测和假设”“能从化学的角度分析资源到产品的转化途径,能对资源的开发利用进行评价”等可以从“迁移—创新”层面进行学习活动任务的设计。要促进知识向能力素养的转化,需要进一步加强从“学习—理解”到“应用—实践”再到“迁移—创新”的学习活动任务的完成,除了教材中章节提供的学习活动任务外,复习教学时还要设计好各级学习活动任务。为了更好地理解各级学习进阶活动任务的设计,再看下例:
【案例3】2019年是元素周期表发表150周年,期间科学家为完善周期表做出了不懈努力。中国科学院院士张青莲教授曾主持测定了铟(49In)等9种元素相对原子质量的新值,被采用为国际新标准。
学习—理解:
(1)In的核素有113In和115In,两者之间的关系是________;115In原子核内中子数有________个。
(2)下列有关元素周期表的说法正确的是
( )
A.Li是最活泼的金属,F是最活泼的非金属
B.在周期表中金属与非金属的分界处,可找到作催化剂的材料
C.元素周期表有7个主族,7个副族,1个0族,1个第Ⅷ族,共16纵行
D.同一周期(第一周期除外)的元素,从左到右由金属逐渐过渡到非金属
说明:通过原子结构和元素周期表的学习,理解原子结构的组成以及元素周期表的构成。
应用—实践:
(3)已知铟与铷(37Rb)同周期。
①In元素在周期表中的位置是________;
②In(OH)3和RbOH的碱性强弱:________。
说明:通过原子结构与元素周期表的应用,推测元素在周期表中的位置,以及预测元素的性质变化规律。
迁移—创新:
(4)你认为可以通过哪些方法证明Rb的金属性强于In?
说明:将元素性质通过实验方法进行迁移应用。
(2)设计问题情境,实现“应用—实践”向“迁移—创新”的提升
真实、具有价值的问题情境是学生化学学科核心素养形成和发展的重要平台,为学生化学学科核心素养提供了真实表现机会。所以学习活动任务的设计应以真实问题情境为载体,如上例科学家对元素周期表发展的贡献,实验探究元素及物质的性质变化等事实,通过分析和解决真实问题任务的过程中实现“应用—实践”向“迁移—创新”的提升,真正落实核心素养的培养和发展。


