PPARα 基因多态性对妇科手术患者舒芬太尼镇痛效应的影响
宋劼,郑丹,李莉
(1.江西省妇幼保健院,南昌330006;2.南昌大学第三附属医院妇产科,南昌330008)
术后疼痛直接影响患者的预后和围手术期的生存质量, 虽然腹腔镜微创手术已经广泛地应用于妇科手术治疗中, 但由于切口的存在和二氧化碳造成的气腹,仍可使患者感到疼痛,影响康复[1]。舒芬太尼是是芬太尼类药物的一种, 作为人工合成的强效阿片类镇痛药, 其对受体的亲和力是芬太尼的7-10 倍,因此它起效快。 并且它的镇痛效价强度是芬太尼的5-10 倍, 因此镇痛作用更强,镇痛作用时间更长。 并且舒芬太尼有良好的心血管稳定性,对呼吸的抑制作用更短更弱,具有较宽的安全区域范围[2]。 舒芬太尼在人体内的代谢主要是通过肝脏细胞色素P450(cytochrome P450,CYP)3A4 酶(CYP3A4),它的活性和表达不同造成了舒芬太尼在代谢方面的个体化差异。 本研究旨在通过对PPARars4253728(G>A)的基因型进行分析,探索PPARα 基因多态性对妇科手术患者使用舒芬太尼进行术后镇痛效应的影响, 为使用舒芬太尼作为妇科术后自控静脉镇痛 (patient-controlled intravenous analgesia, PCIA) 患者的临床个体化用药方案提供相应的理论依据。
1 资料与方法
1.1 一般资料 选择2015 年1 月-2016 年6 月在江西省妇幼保健院、 南昌市第一医院妇科因卵巢良性囊肿、 子宫平滑肌瘤在全麻下行妇科腹腔镜手术的患者87 例,ASAⅠ-Ⅱ级,年龄20-65 岁,且所有患者均接受术后自控静脉镇痛。 排除心脏疾病、肺脏功能不全、肝脏功能异常、肾脏功能不全及精神状况异常者,排除长期吸烟、酗酒及慢性疼痛者,排除习惯性镇痛药和精神类药物使用者。 术前向患者讲解术后疼痛对机体的影响,陈述术后镇痛的必要性和重要性, 向受试者解释本研究的目的,获得患者对术后镇痛以及本研究的知情同意和配合。
1.2 方法
1.2.1 DNA 检测方法 所有入选患者进行PPAR rs4253728(G>A)基因多态性检测。 抽取外周静脉血样3ml,加EDTA 抗凝,采用DNA 提取试剂盒提取人全血DNA。 采用聚合酶链反应(PCR)技术,对目的基因进行扩增,进行焦磷酸测序,最后对DNA链进行多态性分析。 按照基因型分为3 组:GG(纯合子组)、GA(杂合子组)和AA(突变型纯合子组)。
1.2.2 麻醉方法 所有患者入手术间后开放静脉通路,常规监测无创血压、心电图、心率、脉搏血氧饱和度、脑电双频指数等生命体征。全身麻醉诱导:顺式苯磺酸阿曲库铵0.15mg/kg,丙泊酚2mg/kg,舒芬太尼0.5μg/kg。气管插管成功后接麻醉机行机械通气,潮气量6ml/kg,呼吸频率15 次/min,吸呼比为1:1.5, 术中调节脑电双频指数40-60、PETCO 235-45mmHg。 术中麻醉维持:间断静脉注射顺式苯磺酸阿曲库铵0.1mg/kg 维持肌松, 丙泊酚4-6mg/(kg·h),瑞芬太尼0.1-0.2ug/(kg·min)。
1.2.3 术后镇痛方案 手术结束前, 所有患者给予静脉注射舒芬太尼0.1g/kg 做为术后镇痛负荷剂量予以桥接,接自控静脉微量泵(PCIA),镇痛药液为舒芬太尼5μg/ml。
1.3 观察指标 观察并记录拔管即刻、术后第1 个24h、术后第2 个24h 患者的舒芬太尼PIC A 的消耗量, 同时记录治疗期间可能出现的副作用 (嗜睡、恶心、呕吐、头晕、皮肤瘙痒、呼吸抑制、下肢麻木、尿潴留及镇痛不全等),镇痛结束后记录患者对镇痛治疗的总体满意度。
1.4 统计学分析 采用SPSS16.0 统计学软件进行分析,计量资料采用均数±标准差表示,并对其进行t 检验; 计数资料进行χ2检验;P≤0.05 为差异有统计学意义。
2 结果
3 组患者的一般情况无统计学差异(P>0.05)。3 种基因型48h 舒芬太尼总用量、PCA 次数有显著差异,其中AA(突变型纯合子组)的少于GA(杂合子组)及GG(纯合子组)(P<0.05),而后两组之间无明显差异(P>0.05)。三组患者在镇静及恶心、呕吐、呼吸抑制等其他不良反应方面无明显差异, 镇痛效果在术后48h 内无明显差异。 见表1。
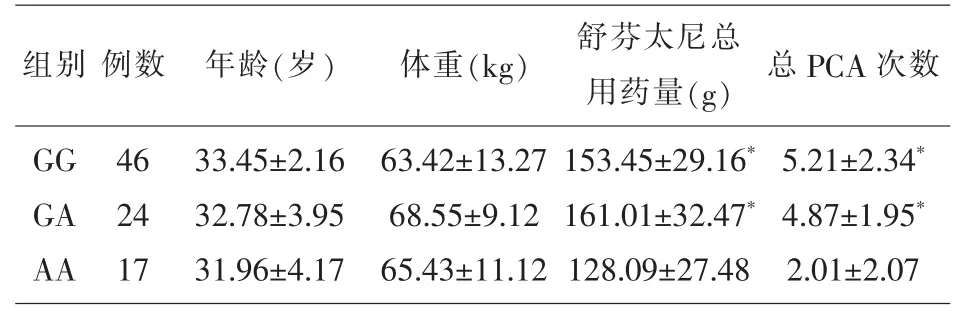
表1 三组间一般资料、舒芬太尼用药量及PCA 按压次数比较
3 讨论
腹腔镜手术是治疗妇科患者中良性卵巢囊肿、子宫平滑肌瘤的主要治疗手段,而手术及麻醉会对患者的免疫应激造成影响, 产生大量炎性因子,加重术后疼痛,影响术后恢复。 因此,做好术后镇痛,有助于减少疼痛引起的并发症的发生,对术后康复有利[3]。 舒芬太尼是芬太尼类药物的一种,是芬太尼N-4 噻吩基衍生物, 主要作用于μ 阿片受体[4]。 它具有极好的脂溶性特点,能迅速进入脊髓和其他组织,直接作用于患者的脊髓、延髓和中脑等痛觉传导区域,镇痛效果显著[5]。 舒芬太尼分布容积小,清除率高,半衰期短,循环稳定,无组胺释放,较少残留呼吸抑制副作用,安全域较高[6]。 它起效快,镇痛长,目前已代替吗啡、芬太尼等广泛用于临床术后镇痛。
药代动力学是研究药物的吸收、分布、代谢、排泄的过程。 随着人类基因组图谱绘制的完成和药物基因学的不断发展, 从基因水平研究麻醉药物代谢动力学已成为一种趋势[7]。 单核苷酸多态性(SPN) 造成人体内与药物代谢相关的酶系表达不同,在临床上表现为药物体内药物代谢动力学、药物效能和不良反应的个体化差异[8],即个体间用药差异。 细胞色素P(CYP)是一大类药物的代谢酶,其中最重要的一类就是CYP450 家族。 而CYP3A4是肝脏中含量最为丰富的CYP450, 占人肝脏CYP450 总量的30%[9], 多种阿片类药物都经其代谢[10],在汉族人群中有11 种多态性[11]。 研究证实,在各种CYP450 蛋白中,仅CYP3A4 对舒芬太尼的体内外代谢发挥主要作用[12]。故而编码CYP3A4 的基因多态性是导致舒芬太尼镇痛效果个体差异的原因[13]。
PPARα (过氧化物酶体增殖物激活受体α)是基因调控机制改变过程的重要转录调控因子[14]。研究报导PPARa rs4253728(G>A)是对CYP3A4 酶活性最具影响力的位点[15]。 这个位点的突变,使CYP 3A4 酶活性降低,代谢减弱,血药浓度升高,从而降低患者术后自控镇痛舒芬太尼的消耗量。 本研究发现,AA 型携带者临床上表现为舒芬太尼代谢减少, 镇痛效应增强, 推测其CYP3A4 的酶活性较GG、GA 型携带者有所降低, 而这个结果与国外学者研究发现的PPARa rs4253728 (G>A)AA 型相较于GG 和GA 型, 其PPARα 蛋白表达水平降低了约1.6 倍[15]相一致。
综上所述,PPARa rs4253728(G>A)基因多态性是引起舒芬太尼药效学个体差异的遗传因素之一。 下一步,通过实验方法检测患者体内CYP3A4酶的活性,将能更证实PPARa rs4253728(G>A)基因多态性与患者体内CYP3A4 酶的活性的关系,从而为本实验的理论提供进一步支持, 更加明确PPARa rs4253728(G>A)基因多态性对患者舒芬太尼的代谢影响的原理, 为舒芬太尼在妇科手术病人术后镇痛中更加精确的个性化用药方案提供理论依据,从而更好地保护患者的健康,降低手术风险。

