麻黄中麻黄碱和伪麻黄碱提取的教学实验改进
梁倩 许忠伟 王芳 王大玮 王猛 刘蔚漪
【摘 要】 目的:对提取盐酸麻黄碱和盐酸伪麻黄碱的甲苯溶剂法进行实验改进。方法:对麻黄的粉碎粒度,提取温度、萃取溶剂、分离方法、展开剂、鉴定方法等进行优化。结果:改进后,麻黄粉碎过30目筛,80~90℃热水提取,抽滤,氯仿萃取,碘和茚三酮检识。结论:改进后的实验过程合理,现象明显,增进学生的实验兴趣,培养实验能力,有效地提高教学质量。
【关键词】 麻黄;盐酸麻黄碱;盐酸伪麻黄碱;实验改进
【中图分类号】 【文献标志码】 A 【文章编号】1007-8517(2020)17-0017-05
Abstract:Objective Improvement on toluene solvent experiments for extraction ephedrine hydrochloride and pseudoephedrine hydrochloride from Ephedra Sinica Stapf. Method The particle size, extraction temperature, extraction solvent, developing agent and identification method of E. sinica were optimized. Result After the improvement, E. sinica was smashed through 30 mesh sieve, hot water extraction at 80-90℃, suction filtration, chloroform extraction, iodine and ninhydrin detection, the experimental results were obvious. Conclusion The phenomena of experiment teaching is obvious, the students interest in experiment were enhanced, and the teaching effect were improved.
Keywords:Ephedra Sinica Stapf;Ephedrine Hydrochloride; Pseudoephedrine Hydrochloride; Improvement on Experimental Teaching
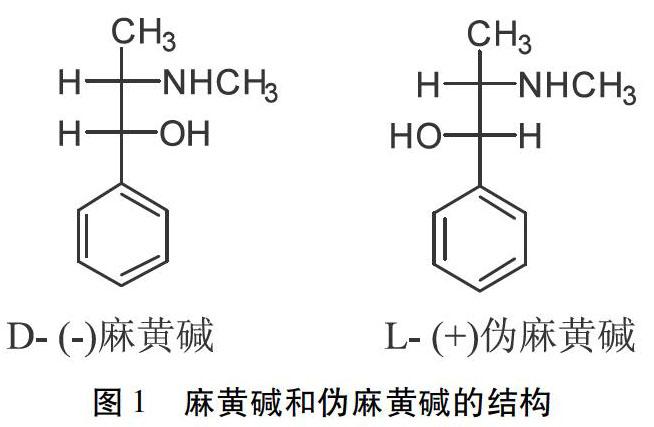
麻黄为麻黄科植物草麻黄(Ephedra sinica stapf)、中麻黄(Ephedra intermedia Schrenk et C.A.Mey.)和木贼麻黄(Ephedra.equisetina Bge.)的干燥草质茎[1]。始载于汉代《神农本草经》,历代本草均有收载。麻黄作为常用中药,味苦涩,因具有发汗解表、止咳平喘及利水的功效而广泛用于临床。麻黄中含有多种生物碱,一般含量为1%~2.5%,主要成分为D-(-)麻黄碱(70%~80%)和L-(+)伪麻黄碱,二者互为立体异构体,结构如图1所示,氮原子连在侧链上,属于有机胺类生物碱[2]。麻黄碱主要作用为平喘,伪麻黄碱主要作用为消炎及选择性收缩呼吸道毛细血管[3]。
麻黄中麻黄碱和伪麻黄碱的提取方法有三种:利用麻黄碱和伪麻黄碱在溶剂中溶解度不同的甲苯溶剂法;利用二者游离状态时具有挥发性的水蒸汽蒸馏法;利用碱性强弱不同的离子交换树脂法[4]。水蒸气蒸馏法提取产率低,且浓缩过程时间长,高温致使部分麻黄碱分解,影响提取生物碱的质量[5-6];离子交换树脂法因投资大,树脂的清洗时间过长和其它工艺问题也不常用[6],因此甲苯溶剂法一般作为学生教学实验。《植物化学》、《生物活性天然产物的分离》、《药用植物资源开发与利用》、《天然产物化学》、《天然药物化学》等课程都可将此实验作为学生综合实验,该实验涵盖加热提取、抽滤、萃取、减压蒸馏、生物碱的分离、结晶、点板、显色等内容,实验过程可有效锻炼学生的综合实验能力。参照《麻黄碱提取與鉴定》[2]的实验过程进行实验时,发现麻黄粉水煮以后过滤困难,没有明确的提取温度,萃取用的甲苯易燃、易爆、有毒致癌,萃取时乳化严重,薄层色谱展开剂的Rf值偏小,鉴定现象不明显等诸多问题,严重影响教学效果。因此,为了制定快速、容易操作及显色明显的实验操作过程,对提取麻黄碱和伪麻黄碱的实验从粉碎粒度、提取温度、提取次数、萃取溶剂、分离方法、鉴定检识方法等方面进行实验优化。
1 材料与方法
1.1 实验材料 草麻黄、盐酸麻黄碱(纯度100%)标准品、盐酸伪麻黄碱标准品(纯度99.8%)、粉碎机、勺子、圆底烧瓶、水浴锅、冷凝管、线手套、滤纸、玻璃棒、pH试纸,分液漏斗、漏斗、铁架台、毛细管、硅胶板、铅笔、尺子、氯仿、草酸、氢氧化钠、氯化钙、浓氨水、无水乙醇、碘、茚三酮、碘化铋钾、溴甲酚绿、浓硫酸、正丁醇、异丙醇、 抽滤瓶、旋转蒸发仪、循环水式真空泵。
1.2 实验步骤
1.2.1 麻黄碱的提取 传统提取方法:①称取25 g麻黄粗粉,放入500 mL圆底烧瓶中;②加入250 mL水;③加热回流提取20 min;④过滤。残渣用150mL水再提取一次,合并两次提取液,用20%的NaOH调pH值为11~12。
改进点:①“称取25 g麻黄粉”改为称取30g麻黄粉;②“加入250 mL水”改为加入300 mL水;③“加热回流提取20 min”改为80~90 ℃热水提取20 min;④“过滤”改为抽滤。
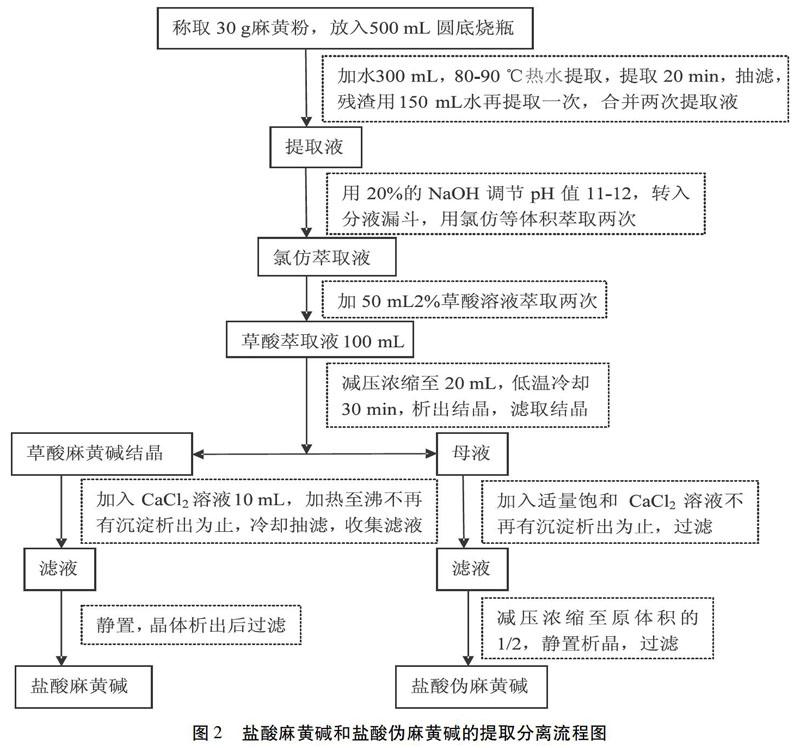
1.2.2 盐酸麻黄碱和盐酸伪麻黄碱的分离 碱化后的溶液转入分液漏斗中:①加50 mL甲苯萃取3次,合并甲苯萃取液,将其转入分液漏斗;再分别加50 mL 2%的草酸溶液萃取两次,合并草酸萃取液,减压浓缩至约20 mL,低温冷却30 min,使结晶析出,滤取结晶即为草酸麻黄碱,草酸伪麻黄碱则留在母液中。把草酸麻黄碱置于烧杯中,加入饱和CaCl2溶液10 mL,加热至沸。②然后冷却后抽滤,收集滤液。③在滤液中加入浓盐酸,调节其pH值为5~6,静置,晶体析出后过滤,即得盐酸麻黄碱。④在搅拌下,给前述母液中加入适量饱和CaCl2溶液至不再有沉淀析出时为止,抽滤。⑤向抽滤后的滤液,滴加浓盐酸调节其pH值为5~6。⑥水浴浓缩至原体积的1/2,静置析晶,过滤后即得盐酸伪麻黄碱。
改进点:①“然后加50 mL甲苯萃取3次,合并甲苯萃取液,将其转入分液漏斗”;改为“然后加等体积的氯仿萃取两次,合并氯仿萃取液,将其转入分液漏斗” ;②“然后冷却后抽滤,收集滤液” 改为 “然后冷却后过滤,收集滤液”; ③“在滤液中加入浓盐酸,调节其pH值为5~6,静置”改为 “静置”; ④“在搅拌下,给前述母液中加入适量饱和CaCl2溶液至不再有沉淀析出时为止,抽滤”,将“抽滤”改为“过滤”; ⑤“向抽滤后的滤液,滴加浓盐酸调节其pH值为5~6”省略该步;⑥“水浴浓缩至原体积的1/2”改为“减压浓缩至原体积的1/2”。
改进后的实验流程图如图2所示。
1.2.3 麻黄碱的鉴定 二缩脲试验:取麻黄碱盐少许,溶于1 mL水中,加入5滴CuSO4试剂,振荡后再加入10滴20%NaOH试剂,即显蓝紫色。加入2 mL乙醚,水层变为蓝色,醚层为紫红色,即表明有麻黄碱存在。改进点:取消二缩脲试验鉴定麻黄碱。
薄层色谱鉴定:利用活化过的硅胶G薄层板,对麻黄碱和伪麻黄碱进行鉴定。展开剂为:1%氨水:异丙醇(1∶9),显色剂为茚三酮试剂。改进点:展开剂为:异丙醇-正丁醇-氨水( 15.7∶2∶2.5) ,显色剂:碘单质在常温下30 s至2 min显色。茚三酮试剂在105~110 ℃,2~7 min显色。
2 实验结果
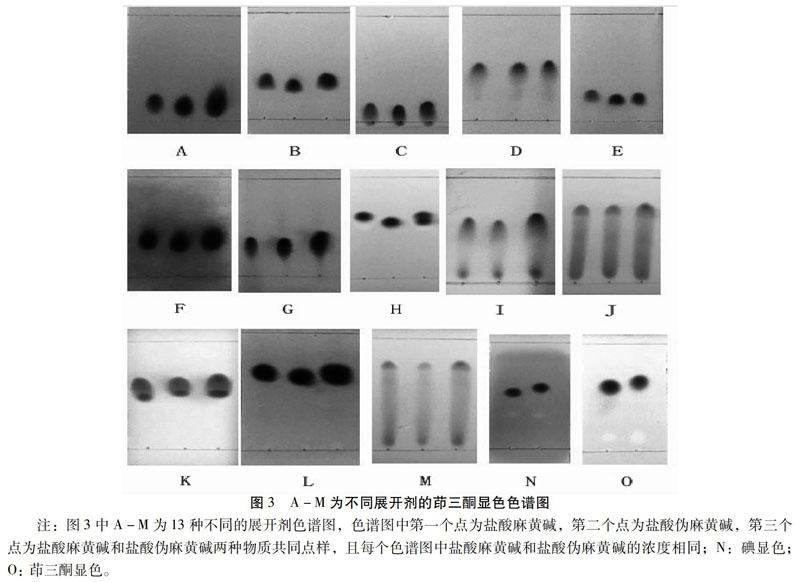
经过多次探索试验,对传统甲苯溶剂法提取、分离麻黄碱和伪麻黄碱过程中的主要步骤进行了如下优化:麻黄粉碎后过30目筛,80~90 ℃热水提取,抽滤,氯仿等体积萃取,分离时不需要用盐酸酸化,異丙醇-正丁醇-氨水( 15.7∶2∶2.5)作展开剂,效果最好(见图3 H),碘单质在常温下30 s至2 min,茚三酮试剂在105~110 ℃,2~7 min盐酸麻黄碱和盐酸伪麻黄碱显色最明显(见图3 N、O)。
3 讨论
3.1 提取方法改进的原因 麻黄中的生物碱通常以盐的形式存在于麻黄草植物细胞壁内的环状纤维上,且麻黄细胞壁质地坚韧,因此将麻黄粉碎,过30目筛,提高提取效率[7]。麻黄中麻黄碱的提取方法主要有煎煮法[8]、水浴温浸法及冷浸法[8],还有冷冻渗漉法[8]、微波法[8]、超声提取法[8]、索氏提取法[9]、振荡提取法[9]等。提取溶剂主要为水(或者加酸酸化),还有有机溶剂乙醇、甲醇和乙醚[9],丙酮[10]等。提取效率:水煎煮回流法>酸性乙醇回流提取法>温浸法> [11]超声提取法[8]>其他提取方法。陈柳蓉等[12]对麻黄提取麻黄碱和伪麻黄碱的提取温度、提取次数、酸度和提取时间进行考察,认为提取温度对提取率影响显著,其次是提取次数,酸度和提取时间等影响较小。水煎煮法提取液温度越高,萃取时越容易乳化[13],高温也会使麻黄碱分解,因此提取温度设置为80~90℃热水提取。麻黄中的鞣质成分较多,水提后过滤困难,采用抽滤的方法进行过滤,可以节省时间,提高效率。
3.2 麻黄碱和伪麻黄碱分离改进的原因 李德玉等[6]对氯仿、乙酸乙酯、甲苯、石油醚、乙醇为萃取溶剂,萃取麻黄碱和伪麻黄碱的效率进行比较,发现氯仿与提取液体积比为1∶1萃取两次,萃取效率最高。抽滤改为过滤的原因是因抽滤比过滤损失要多,损失率为17%。
省略盐酸调节pH值为5~6,是因为滤液本身的pH值就已经为3~4,不需要再用HCl调节。水浴浓缩改为减压蒸馏,是因为水浴浓缩时间较长,规定时间内不能按时完成实验。
3.3 麻黄碱的鉴定
3.3.1 二缩脲试验 麻黄碱和伪麻黄碱与大多数生物碱沉淀试剂不发生反应,麻黄碱与碱性CuSO4生成的铜络盐因反应灵敏度不高,甚至看不到显色。因此不能用二缩脲试验鉴定麻黄中的生物碱。
3.3.2 薄层色谱鉴定
3.3.2.1 展开剂的选择 展开剂为:1%氨水-异丙醇(1∶9)[2](实验书上的展开剂)展开时(见图3 A),Rf值偏小,不能有效区分麻黄碱和伪麻黄碱。《中国药典》对麻黄碱和伪麻黄碱的展开剂用氯仿-甲醇-氨水(20∶5∶0.5)[1],展开结果见图3 B,也是不能区分麻黄碱伪麻黄碱。因此对包括药典在内的13种关于麻黄碱和伪麻黄碱的展开剂进行了筛选,展开剂为:A. 1%氨水-异丙醇(1∶9)(见图3 A)[2] ; B. 氯仿-甲醇-氨水(20∶5∶0.5[1],20∶ 3.5∶ 0.25 [14],100∶8∶1[15],10∶2∶0.1[16])(见图3 B);C. 氯仿-正丁醇-水(10∶4∶0.5)[17](见图3 C);D. 氯仿-醋酸乙酯-甲醇-水(13∶40∶22∶10)[18](见图3 D);E. 氯仿-醋酸乙酯-甲醇-氨水(15∶4∶3∶0.3)[19](见图3 E);F. 乙醇-氯仿-水-氨水(10∶1∶4∶0.5)[20](见图3 F);G. 氯仿-正丁醇-乙醇(1∶1∶1.5)[21,22] ( 0.5 mol /L 氢氧化钠喷雾碱化)(见图3 G);H. 异丙醇-正丁醇-氨水( 15.7∶ 2∶ 2.5) [23-25](见图3 H);I. 正丁醇-乙酸乙酯-水( 4∶ 1∶5) 的上层溶液[26](见图3 I);J. 正丁醇-乙醇-水(24∶ 12∶ 4) [27-29](见图3 J);K. 正丁醇-冰醋酸-水(8∶2∶1)[30](见图3 K);L. 乙酸乙酯-甲醇-氨水(15∶5∶2[31]; 17∶2∶1[32])(见图3 L);M. 正丁醇-甲醇-水(6∶2∶1)[33](见图3 M)。其中展开剂H:异丙醇-正丁醇-氨水(15.7∶ 2∶ 2.5)能有效区分盐酸麻黄碱和盐酸伪麻黄碱(见图3 H),其它的展开剂均不能区分(图3:A-M及O均为茚三酮显色,N为碘显色)。
3.3.2.2 显色剂的选择 薄层色谱展开后,用茚三酮试剂显色,没有指明显色温度,常温下不显色。因此对生物碱显色试剂及常见显色剂:碘、碘化铋钾、茚三酮、硫酸乙醇和溴甲酚绿进行显色实验。碘单质在常温下30 s至2 min,盐酸麻黄碱和盐酸伪麻黄碱显色明显(见图3 N),茚三酮试剂在105~110 ℃,2~7 min盐酸麻黄碱和盐酸伪麻黄碱显色明显(见图3 O),碘化铋钾、硫酸乙醇和溴甲酚绿试剂对盐酸麻黄碱和盐酸伪麻黄碱不显色。
4 讨论
麻黄碱中的氮原子是连接在支链上而不是连接在苯环上,与大多数生物碱试剂不发生反应,所以本实验对常用生物碱试剂进行筛选,找到对麻黄碱和伪麻黄碱显色明显的生物碱试剂。麻黄中麻黄碱的含量较低,一般为1%~2.5%,因此在实验中要求提取、分离麻黄碱的实验条件均需达到最优,否则薄层色谱很难检测到生物碱的存在,本实验对麻黄中麻黄碱和伪麻黄碱提取、分离方法进行改进后提高了麻黄碱的提取效率,今后可以利用植物的亲缘关系或者活性成分化学结构的相似性寻找麻黄碱含量较高的植物资源,代替麻黄资源做该提取实验。本实验优化后的实验过程经过多次操作验证,实验现象明显,科学规范,能有效提高学生实验的积极性,加深学生对本次实验的思考和认识,增强学生的动手能力,有效提高教学质量。
参考文献
[1]中华人民共和国卫生部药典委员会.中华人民共和国药典2015年版一部[S].北京:人民卫生出版社,2015:320.
[2]李炳奇,廉宜君.天然产物化学实验技术[M].北京:化学工业出版社,2012:281-283.
[3]李景莊,刘兴莉.伪麻黄碱在制剂中的合理应用[J].中成药,1992,12:48.
[4]苗雨瑞,杨巧荷,于姝燕,等.麻黄碱與伪麻黄碱的研究进展[J].内蒙古医学院学报,2011,33(4):490-494.
[5]李俐,陈坚.麻黄碱和伪麻黄碱的提取工艺及分析[J].中国医药工业杂志,2003,34(4):202-205.
[6]李德玉,李雅臣,杨秀贤,等.麻黄碱提取方法的实验研究[J].天津药学,1994,6(2):29-31.
[7]高林霞,王秀霞,万端极.提取麻黄碱的新工艺[J].应用化工,2008,37(10):1254-1256.
[8]刘昌美,陶建生,冯怡,等.中药麻黄浸提方法的比较研究[J].上海中医药杂志,2000(4):47-49.
[9]张丽静,解成喜,符继红.麻黄草中麻黄碱浸提方法的比较研究[J].新疆大学学报(自然科学版),2004,4(1):386-388.
[10]林凯.麻黄药材的指纹图谱研究及其生物碱含量测定研究[D].重庆:重庆医科大学,2006.
[11]沈红,狄留庆,黄耀洲.不同提取方法对麻黄中麻黄碱提取得率的比较研究[J].南京中医药大学学报,2004,20(3):170-172.
[12]陈柳蓉,邵青.麻黄提取工艺的优化选择[J].中成药,1996,18(8):10-11.
[13]周玲,吴德康,唐于平,等.麻黄中化学成分研究进展[J].南京中医药大学学报,2008,24(1):71-72.
[14]吕长淮.复方盐酸伪麻黄碱缓释胶囊的薄层色谱鉴别方法[J].安徽医药,2007,11(11):1004-1005.
[15]张秀华,姜泓,初正云.麻黄提取工艺比较[J].时珍国医国药,2000,11(11):963.
[16]张素华,贾春华,庞宗然,等.薄层扫描法测定桂麻合方中麻黄碱[J].中草药,2007,38(5):708-709.
[17]刘慧琼,郭书好,王定勇,等.薄层扫描法测定金水六君煎胶囊中盐酸麻黄碱的含量[J].光谱实验室,2005,22(4):687-689.
[18]韩桂茹,赵志军,徐韧柳.薄层扫描法测定麻黄及其制剂中盐酸麻黄碱的含量[J].中成药,2003,25(3):2003-2005.
[19]温爱平,杨树平,李红英,等.双波长薄层扫描法测定异麻匹林片中咖啡因和盐酸伪麻黄碱含量[J].中国医院药学杂志,2000,20(5):262-264.
[20]李春玲,徐本明.薄层扫描法测定祛痰口服液中盐酸麻黄碱的含量[J].山东医药工业,1996,15(4):3-4.
[21]陆燕萍,刘佳丽,巩晓宇,等.麻黄药理作用及含量测定的研究进展[J].中国医药导报,2013,10(24):38-40.
[22]吴新荣,苏如雄.薄层扫描法测定盐酸麻黄碱合剂中盐酸麻黄碱含量[J].中国医院药学杂志,1998,18(1):22-23.
[23]曾诠,刘成基,郑丽真,等.麻黄及其炮制品中L-麻黄碱和D-伪麻黄碱的分离测定[J].中国药科大学学报,1990,21(4):236-238.
[24]汪瑗,张进治,马新勇.麻黄生物碱中一对光学异构体在薄层色谱原位的表面增强拉曼光谱研究[J].光谱学与光谱分析,2004,24(11):1373-1375.
[25]乔蓉霞.薄层扫描法测定复方遗尿颗粒中盐酸麻黄碱的含量[J].陕西中医,2001,22(8):495-496.
[26]毛丹,许勇,陆继伟,等.复方桔梗麻黄碱糖浆质量标准研究[J].中成药,2012,34(8):1518-1522.
[27]李萍,高向军,周娟.薄层色谱法测定止咳平喘胶囊中麻黄碱的含量[J].华西药学杂志,1999,14(2):129-130.
[28]崔丽华,靳春荣.薄层扫描法测定咳喘宁颗粒中盐酸麻黄碱的含量[J].中国药品标准,2001,2(4):37-39.
[29]张敏敏,麻淑兰.双波长薄层扫描法测定制剂中盐酸麻黄碱的含量[J].药学通报,1985,20(12):719-720.
[30]胡英,刘庆荣.感冒软胶囊中盐酸麻黄碱的薄层色谱鉴别方法探讨[J].中国药事,2006,20(9):573.
[31]张君,王颖.风寒感冒颗粒麻黄薄层色谱鉴别方法研究[J].中国民族民间医药,2011,20(24):50-51.
[32]洪立湘,周春莲,沈丽娟.双波长薄层扫描法测定复方川贝精片中盐酸麻黄碱的含量[J].吉林大学学报(医学版)2002,28(4):435.
[33]潘晶晶,王冬梅.薄层扫描法侧定止咳清热合剂中盐酸麻黄碱的含量[J].天津中医学院学报,2004,23(2):84-85.
(收稿日期:2020-04-15 编辑:刘斌)

