参术补钙颗粒的质量标准研究
赵建平,李艳玲,张春霞,王亚利,常凤姣,李利红
(河南牧业经济学院,郑州 450000)
缺钙是动物一种常见疾病,多发生在动物的生长阶段和老年阶段。严重影响了宠物和食品动物的经济效益。缺钙易导致宠物畸形和影响毛色的光泽度,也会影响食品动物的肉的品质。所以补钙已经成为畜牧业重点关注的问题。
动物的补钙产品虽然很多,但把中药和补钙相结合在一起的却基本没有。参术补钙颗粒是中西药复方制剂,由甘草、党参、白术等五味中药再加入维生素D3、碳酸钙,以淀粉、蔗糖等辅料制备而成的,为淡黄色至棕黄色的颗粒,气味微甜。在该产品中,中药调理脾胃促进食欲消化,西药补钙补充维生素D。其功效为益气健脾、补充钙质。本实验通过对参术补钙颗粒中甘草、白术、党参三味药进行薄层鉴别来作为定性鉴别标准,通过对钙和维生素D3用高效液相进行含量测定来进行定量控制,力求制定出能够很好控制参术补钙颗粒质量的标准。
1 材 料
1.1 药材 甘草、党参、白术、山药和茯苓均购自北京同仁堂有限公司,经鉴定甘草是豆科植物甘草(Glycyrrhiza uralensis Fisch)的干燥根和根茎;党参是桔梗科植物党参(Codonopsis pilosula (Franch.) Nannf.)的干燥根;白术是菊科植物党参(Atractylodes macrocephala)的干燥根茎;山药是薯蓣科植物薯蓣(Dioscorea opposita Thunb.) 的干燥根茎;茯苓是多孔菌科真菌茯苓(Poria cocos(Schw.)Wolf)的干燥菌核。
1.2 标准品 维生素D3(含量:不低于99%,批号:A06J9L65206,上海源叶生物);碳酸钙工作基准试剂(含量:99.95%~100.05%);甘草对照药材(批号:161213-04,成都普思生物科技公司);党参对照药材(批号:P23N9F75819,上海源叶生物);白术对照药材(批号:Z08A9B67489,上海源叶生物);山药对照药材(批号:Y19A9H59254,上海源叶生物);茯苓对照药材(批号:P12J9F65406,上海源叶生物)
1.3 样品 参术补钙颗粒及阴性样品均由河南牧业经济学院制药工程学院自制。
1.4 仪器 原子吸收分光光度计(型号WFX-120B,北京瑞利分析仪器有限公司),Waters高效液相色谱仪(型号Alliance),电子天平(型号BSA224S,北京赛多利斯科学仪器有限公司).
1.5 试剂 正己烷(分析纯),甲醇(分析纯),盐酸(分析纯),氧化镧(分析纯)。
2 方法与结果
2.1 薄层定性鉴别
2.1.1 甘草的薄层鉴别
2.1.1.1 供试品的制备 称取样品5.00 g,加三氯甲烷40 mL,加热回流1 h后过滤,药渣挥尽三氯甲烷(没刺激性气味即可),残渣加甲醇50 mL,加热回流1 h后滤过,滤液蒸干用水30 mL溶解,用水饱和过的正丁醇振摇提取两次,每次25 mL,正丁醇液蒸干,加甲醇0.5 mL溶解,作为供试品。
2.1.1.2 阴性对照的制备 取缺甘草的阴性样品,同上述供试品的方法制备。
2.1.1.3 对照药材的制备 同供试品的制备。
2.1.1.4 薄层鉴别 取上述样品溶液各5 μL,分别点于同一硅胶G板上,以三氯甲烷:乙酸乙酯:甲醇:水(15∶40∶22∶10)10 ℃以下放置的下层溶液作为展开剂,展开,取出,晾干,喷10%硫酸乙醇,加热5至10 min,置紫外365 nm下检视(图1)。

1、缺甘草阴性对照溶液;2-4二批、三批和四批供试品溶液;5、甘草对照药材溶液1、Licorice deficiency negative control solution;2-4、Two,three and four batches of test solution;5、Glycyrrhiza reference solution图1 甘草薄层鉴别色谱图(紫外365 nm)Fig 1 TLC identification chromatogram of Glycyrrhiza uralensis Fisch
薄层鉴别结果显示:在和甘草对照药材相对应的位置,样品2、3、4均出现清晰斑点,并且甘草阴性对照溶液在该位置无斑点。因此该方法可以用来定性鉴别参术补钙颗粒中的甘草。
2.1.2 党参的薄层鉴别
2.1.2.1 供试品的制备 称取样品5.00 g,加水30 mL、盐酸3 mL,加热回流1 h,放凉后滤过,滤液用二氯甲烷提取三次,每次20 mL,合并二氯甲烷液,蒸干,残渣加1 mL甲醇溶解,作为供试品溶液。
2.1.2.2 阴性样品的制备 取缺党参的阴性样品,同供试品的方法制备。
2.1.2.3 对照药材的制备 称取对照品0.50 g,加水10 mL、盐酸1 mL,加热回流1 h,放凉后滤过,滤液用三氯甲烷提取三次,每次10 mL,合并三氯甲烷液,蒸干,残渣加0.5 mL甲醇溶解,作为对照药材溶液。
2.1.2.4 薄层鉴别 吸取上述溶液5 μL,分别点于同一硅胶G薄层板上,以甲苯∶乙酸乙酯∶甲酸(20∶8∶0.5)为展开剂中展开,取出,晾干。喷10%硫酸乙醇,105 ℃加热至样点清晰显现(图2)。
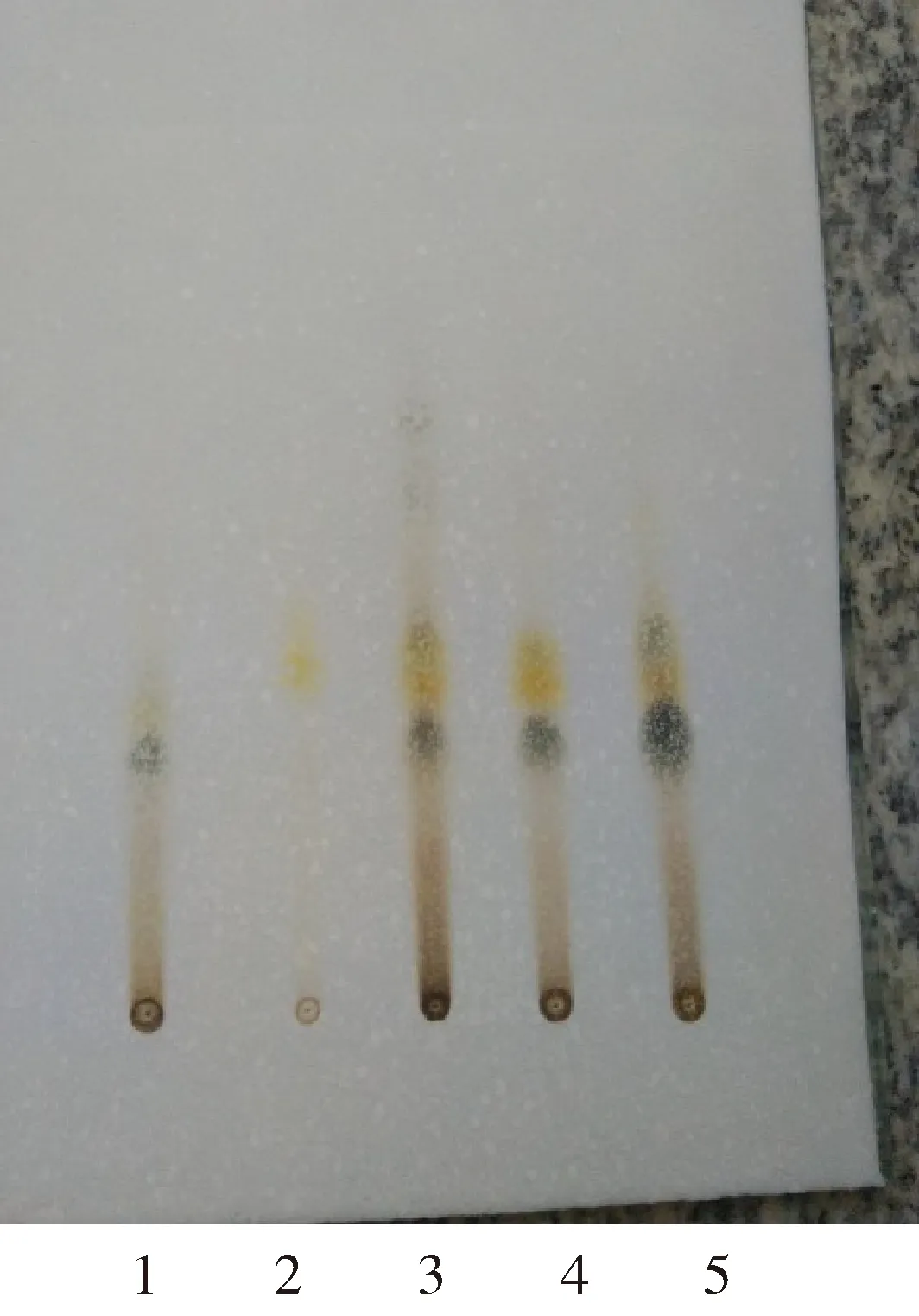
1、党参对照品溶液;2、缺党参阴性对照溶液;3-5二批、三批和四批供试品溶液1、Dangshen reference solution;2、Negative control solution of Codonopsis pilosula;3-5、Two,three and four batches of test solution图2 党参薄层鉴别色谱图谱Fig 2 TLC chromatogram of Codonopsis pilosula
薄层鉴别结果显示:在和党参对照药材相对应的位置,样品2、3、4均出现清晰斑点,并且党参阴性对照溶液在该位置无斑点。因此该方法可以用来定性鉴别参术补钙颗粒中的党参。
2.1.3 白术的薄层鉴别
2.1.3.1 供试品的制备 称取样品3.00 g,加水饱和过的正丁醇40 mL,超声30 min后过滤,滤液用水洗涤两次,每次20 mL,弃去水液,蒸干,残渣加1 mL丙酮溶解。
2.1.3.2 阴性对照的制备 取缺白术的阴性样品,同法制备阴性对照
2.1.3.3 对照品的制备 取白术的对照药材,按照供试品的前处理方法制备。
2.1.3.4 薄层鉴别 吸取上述样品溶液各5 μL,分别点于同一硅胶G薄层板上,以三氯甲烷:丙酮(19∶1)作为展开剂,展开,取出,晾干。置紫外365 nm下检视(图3)。

1、缺白术阴性对照溶液;2-4二批、三批和四批供试品溶液;5、白术对照药材溶液1、Negative control solution of Atractylodes macrocephala;2-4、Two,three and four batches of test solution;5、Atractylodes macrocephala reference solution图3 白术薄层鉴别色谱图谱(紫外365 nm)Fig 3 TLC chromatogram of Atractylodes macrocephala (UV 365 nm)
薄层鉴别结果显示:在和白术对照药材相对应的位置,样品2、3、4均出现清晰斑点,并且白术阴性对照溶液在该位置无斑点。因此该方法可以用来定性鉴别参术补钙颗粒中的白术。
2.2 含量测定
2.2.1 钙的含量测定
2.2.1.1 标准品溶液的制备 精密称取碳酸钙基准试剂60 mg于100 mL容量瓶,加10 mL水润湿,再用5 mL稀盐酸溶解后加水至刻度,摇匀,从中精密量取25 mL于100 mL容量瓶中,加水至刻度,摇匀,精密量取1.0、1.5、2.0、2、3.0 mL分别置于25 mL量瓶中,各加镧试液1 mL,加水至刻度后,摇匀,即得一系列不同浓度的对照品溶液。
2.2.1.2 供试品溶液和阴性对照溶液的制备 将参术补钙颗粒粉碎,阴性对照品(参术补钙颗粒缺钙)研细,过60目筛,精密称定0.5 g或0.3 g置100 mL容量瓶中,加10 mL水润湿,再用5 mL稀盐酸溶解,加水至刻度,摇匀,过滤,从续滤液中精密量取2 mL置于25 mL容量瓶中,加1 mL镧试液,加水至刻度,摇匀,得供试品溶液和阴性对照溶液。
2.2.1.3 空白对照溶液的制备 于100 mL容量瓶中加10 mL水,再加5 mL稀盐酸后加水至刻度,摇匀,从中精密量取2 mL置于25 mL容量瓶中,加镧试液1 mL,加水至刻度,摇匀,即得。
2.2.1.4 测定法 用火焰原子吸收分光光度计按照原子吸收分光光度法第一法标准曲线法在422.7 nm的波长处测定,即得。
2.2.1.5 标准曲线的制备 由上述标准品溶液的制备得到6、9、12、15、18 μg/mL一系列不同浓度的标准品溶液,再加上空白对照溶液,用原子吸收分光光度法,每个浓度平行测定3次,得标准曲线方程y=0.0177x+0.1072,r=0.999836,钙在0~18 μg/mL范围内线性关系良好。

图4 钙标准曲线Fig 4 Calcium standard curve
2.2.1.6 精密度的测定 取供试品溶液4的2号,连续测定6次,考察方法的精密度,RSD为2.75%。
2.2.1.7 重复性试验 精密称取同一批的参术补钙颗粒6份,按供试品溶液的制备方法处理,测定样品中钙的含量,结果平均含量为11.79 mg/g,RSD为2.13%。
2.2.1.8 样品中钙含量的测定 分别取8个批次的参术补钙颗粒,按照2.2.1.2项下供试品制备方法制备供试品溶液,每个批次平行处理两份。按照2.2.1.4项下测定方法分别测定可得样品中钙含量,结果见表1。

表1 钙标准曲线数据Tab 1 Calcium standard curve data
根据测定结果,取8个批次平均含量的80%做为定量限,参术补钙颗粒中所含钙的含量定为8.76 mg/g。
2.2.2 维生素D3的含量测定
2.2.2.1 色谱条件 流动相:甲醇∶水(98∶2);色谱柱:WAT054275 C18柱;检测波长:264 nm。
2.2.2.2 标准品溶液的制备 精密称取VD3标准品5 mg于5 mL容量瓶中,加正己烷溶解并稀释至刻度,摇匀,得C=1.0 mg/mL的VD3标准贮备液。从中精密量取1 mL置于蒸发皿中,使溶剂挥干,用甲醇溶解残渣转移至10 mL容量瓶中并稀释至刻度摇匀,得C=100 μg/mL的VD3标准工作液,从中精密量取1 mL置10 mL容量瓶中,用甲醇稀释至刻度,摇匀,得C=10 μg/mL的标准工作液。
2.2.2.3 原料药溶液的制备 精密称取VD3原料药1 g于具塞锥形瓶中,加25 mL正己烷,超声提取30 min,过滤至25 mL容量瓶中,用正己烷补足至刻度,摇匀,从中精密量取1 mL至蒸发皿中挥干,用甲醇溶解残渣转移至10 mL容量瓶中并稀释至刻度,摇匀。
2.2.2.4 供试品溶液及阴性对照品溶液的制备 称取阴性对照品(参术补钙颗粒缺VD3)20 g,样品50 g,分别置于具塞锥形瓶中,加正己烷150 mL,超声提取30 min,过滤至蒸发皿中,滤液挥干后用甲醇溶解残渣转移至5 mL容量瓶并稀释至刻度,摇匀,即得。
2.2.2.5 测定法 分别吸取VD3标准品、原料药、阴性对照品及供试品溶液,用0.22 μm微孔滤膜过滤上机检测,标准品和原料药进样10 μL,阴性及样品进样20 μL,测定,记录峰面积,即得。

图5 维生素D3标准品Fig 5 Vitamin D3 standard

图6 参术补钙颗粒维生素D3阴性Figure 6 Vitamin D3 of Shenzhu Calcium Supplem Granule was negative
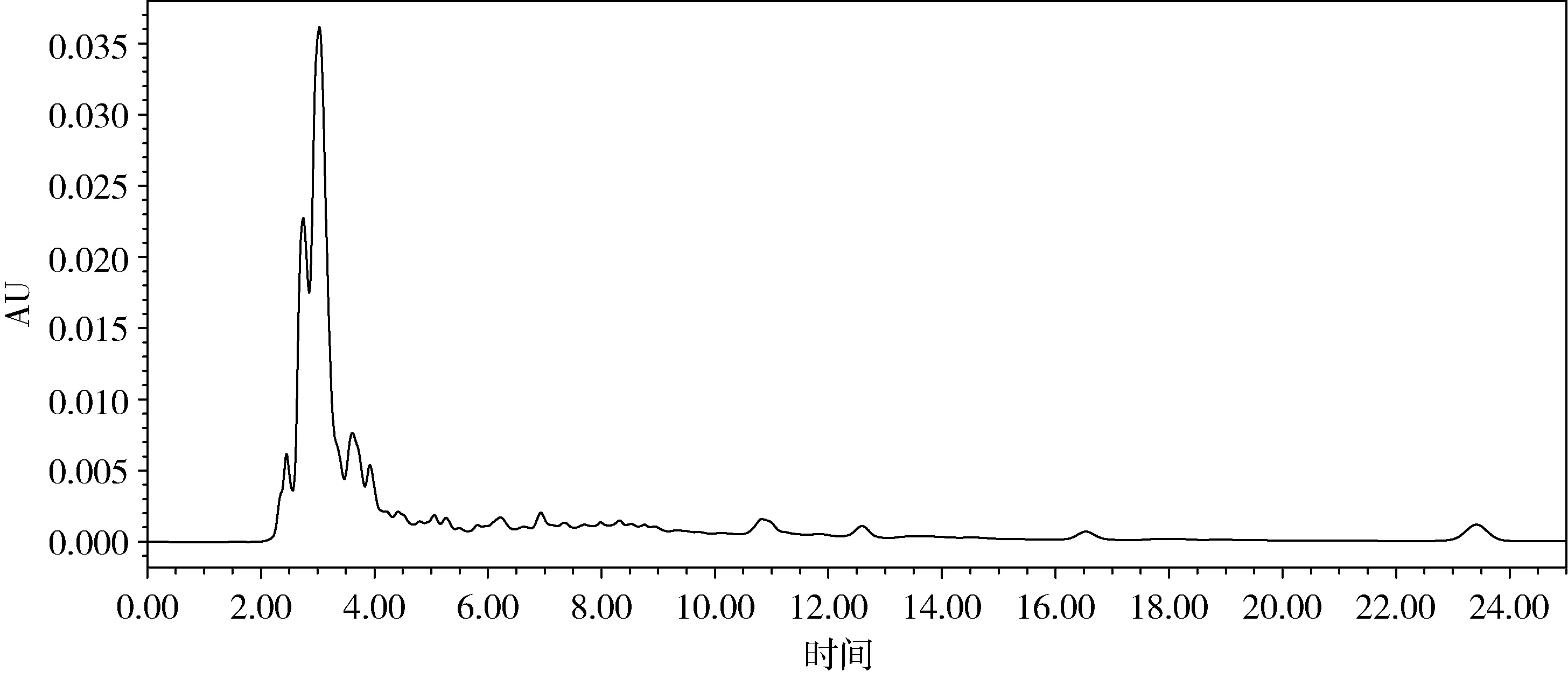
图7 参术补钙颗粒样品中维生素D3Fig 7 Vitamin D3 in Shenzhu Calcium Supplem Granule
2.2.2.6 标准曲线的制备 取上述C=100 μg/mL的VD3标准工作液,依次稀释得到50、25、12.5、6.25、3.125 μg/mL一系列不同浓度的标准品溶液,6个浓度的标准样分别进样10 uL,每个平行进两针,得标准曲线方程y=36300x-9110,r=0.999997,维生素D3在3.125~100 μg/mL范围内线性关系良好。
2.2.2.7 精密度的测定 取上述浓度为25 μg/mL对照品溶液,连续进样6次,每次10 μL,考察进样精密度,RSD为2.20%。
2.2.8 重复性试验 称取同一批的参术补钙颗粒样品6份,按照供试品品溶液的制备方法处理,测定样品中VD3的含量,结果平均含量为0.03067 μg/g,RSD为3.37%。
2.2.9 回收率的测定 称取同一批次已知含量的参术补钙颗粒(粉碎过60目筛)6份,每份50 g,然后分别按样品中维生素D3含量的大约80%、100%、120%的量加入维生素D3标准品,再按照供试品溶液的制备方法处理,进样20 μL,测峰面积。结果平均回收率为94.83%,RSD为2.77%。
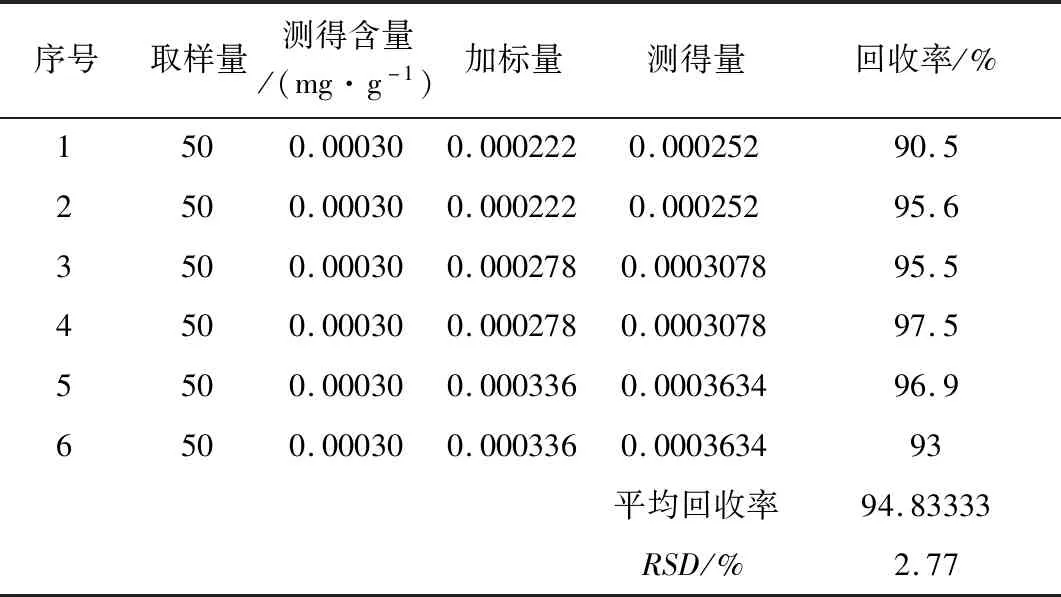
表3 维生素D3回收率的测定Tab 3 Determination of recovery rate of vitamin D3
2.2.10 样品中维生素D3的含量测定 分别称取8个不同批次的参术补钙颗粒,按照2.2.4项下制备供试品溶液的方法来处理,每个批次平行处理两份。按照2.2.1项下色谱条件测定,分别进样20 μL,记录峰面积,并计算供试品中维生素D3含量。结果见表2。

表2 不同批次参术补钙颗粒中钙的含量Tab 2 Contents of calcium in different batches of Shenzhu Calcium Supplem Granule

表4 不同批次参术补钙颗粒中维生素D3的含量Tab 4 Contents of vitamin D3 in different batches of Shenzhu Calcium Supplem Granule
根据测定结果,取8个批次平均含量的80%做为定量限,参术补钙颗粒中所含维生素D3的含量定为0.0248 μg/g。
3 讨论与结论
钙的含量测定方法很多,传统的EDTA络合滴定法样品用量大,前处理耗时长,终点不易判断,操作误差大并且灵敏度不高;高锰酸钾氧化还原滴定法得到的结果较准确,终点变化很明显便于观察,但操作过程中需要进行沉淀过滤,较为繁琐[5];还有离子色谱法、分光光度法。火焰原子吸收法测定范围宽[6]、操作简便、选择性好、结果准确可靠,所以实验中也选用了具有高灵敏度的火焰原子吸收法[7]。该方法操作简便,样品无需经过消化处理,能测出低含量的钙且得到结果的重现性较好,可以用来检验多批次的样品[8],可用于药物中钙的质量控制。
虽然已有不少文献中都采用HPLC法测定保健品以及制剂中维生素D3含量的方法[9-12],但多用正相色谱检测且样品前期处理较为复杂。本课题建立了参术补钙颗粒中维生素D3含量测定的反相高效液相色谱法,样品制备方法简单,直接用溶剂超声提取,免去了碱液皂化和反复提取的繁琐过程,降低了样品中维生素D3的损失。在检测过程中采用95%的甲醇作为流动相时,目标峰的保留时间太长;调整为纯甲醇时,出峰时间提前但目标峰与其前面的杂峰无法完全分离;采用98%的甲醇时,目标峰可与杂峰完全分离,保留时间也比用95%甲醇时短。经过方法学考察,精密度、重现性、回收率均良好,可用于参术补钙颗粒中维生素D3的质量控制。
该实验建立的参术补钙颗粒中定性鉴别和定量测定方法简便、准确、重复性好,可用于参术补钙颗粒的质量控制。

