白杨素衍生物的生物活性研究进展*
储丽莎, 彭 露, 黄伟军, 张亚林, 马春雨, 朱 伟, 闻 振
(安徽中医药大学药学院, 安徽 合肥 230031)
白杨素(Chrysin,图1)又称白杨黄素,其化学名为 5,7-二羟基黄酮。研究表明[1],抗肿瘤、改善体重和脂质代谢作用、抗抑郁、神经保护作用、治疗皮肤病等广泛的生理药理活性。最近几年人们对白杨素生物活性进行不断研究,如清除自由基、抗病毒等活性已被逐步揭示出来,新的结合位点和作用机制已经被发现并且公之于众。白杨素具有多种药理作用和低毒性,愈来愈受到科研人员的重视。但是白杨素的结构决定了其水溶性差,胃肠道吸收效果也不理想,口服给药时会产生严重的“首过效应”。为了充分利用白杨素的药理活性,提高其水溶性和代谢稳定性,科研工作者对其结构进行了大量的修饰研究,获得了大量白杨素衍生物。
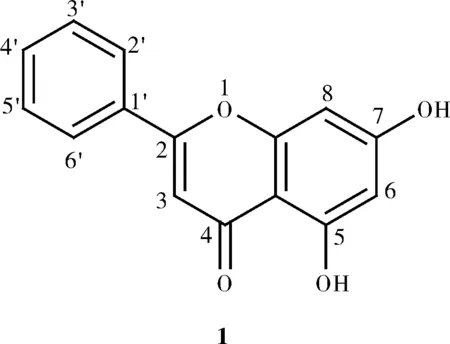
图1 白杨素的结构
1 白杨素的生物活性
1.1 白杨素的抗肿瘤活性
肿瘤的发生是细胞增殖与凋亡失衡的结果,细胞凋亡在肿瘤生长过程中起负调控作用,诱导细胞凋亡能阻碍肿瘤的恶性增殖,所以,目前大多数抗肿瘤治疗方法是诱导细胞凋亡。Saima等[2]研究发现,白杨素治疗(50 mg/kg体重)通过诱导小鼠B16F10黑色素瘤细胞G2/M期细胞周期阻滞和凋亡,显示出剂量依赖性抑制肿瘤细胞生长的作用。与抑制71%黑色素瘤生长的对照组相比,它在治疗14天后抑制了60%的黑色素瘤生长。此外,在Caco-2和SW480结直肠癌细胞中,通过给药白杨素,使巨噬细胞、CTL和NK的细胞的活性增加。
1.2 白杨素改善体重和脂质代谢作用
余松等[3]研究了白杨素对小鼠非酒精性脂肪肝(NAFLD)的影响。用缺乏蛋氨酸胆碱的饲料(MCD)建立NAFLD小鼠模型。白杨素可减轻MCD诱导的NAFLD小鼠肝脏脂肪堆积,增加极低密度脂蛋白(VLDL)分泌,降低肝脏氧化应激。白杨素抑制氧化应激或直接抑制蛋白激酶C(PKC)显著降低肝脏PKC活性,导致肝细胞核因子4α(HNF4α)抑制性磷酸化降低。HNF4α的激活导致载脂蛋白B的转录和VLDL的分泌。结果表明,白杨素通过靶向肝氧化应激/PKC/HNF4α信号通路有效地改善了MCD诱导的NAFLD小鼠脂肪肝。
1.3 白杨素的抗抑郁作用
Rashno等[4]研究的结果表明,白杨素能够改善与TBI相关的前庭运动功能障碍、认知记忆衰退和焦虑/抑郁样行为,至少部分归因于其能通过调节大脑皮层和海马DG区Bcl-2家族蛋白的表达,减轻神经炎症,预防神经元凋亡。在TBI后第3天,100 mg/kg的白杨素对神经炎症和神经细胞凋亡的抑制作用最强,但值得注意的是,三种剂量的白杨素均能改善行为缺陷。需要进一步的研究来详细探讨白杨素对TBI相关神经行为缺陷的作用机制,以及其在临床上的潜在应用。
1.4 白杨素的神经保护作用
Vandreza等[5]研究了白杨素对甲状腺功能减退小鼠记忆障碍的影响,采用了Morris水迷宫(MWM)实验、开放野试验(OFT)和被动回避实验。白杨素(20 mg/kg,10 mL/kg)在连续灌胃给药28天后,显示出神经保护作用。进一步研究表明,白杨素使海马谷氨酸水平和Na+, K+-ATP酶活性正常化,从而能够有效逆转甲状腺功能减退的小鼠表现出的记忆缺陷。
1.5 白杨素的治疗皮肤病作用
Li等[6]发现白杨素通过抑制表皮角质形成细胞中的下游反应,包括MAPK途径的磷酸化、NF-κB途径中IκBα的激活以及在蛋白质水平上触发JAK-STAT途径,能明显减轻咪喹莫特(IMQ)诱导的小鼠银屑病样皮肤损伤,改善咪喹莫特诱导的皮肤屏障破坏。白杨素减少了TNF-α、IL-17A和IL-22诱导的CCL20和表皮角质形成细胞释放的抗菌肽,具有治疗炎症性皮肤病的潜力。
2 白杨素的毒理性质
随着白杨素在食品中的应用越来越多,以及其潜在的健康益处,由于缺乏相关毒理学文献,迫切需要澄清其毒理学性质。在魏尧的研究中[7],我们通过对实验大鼠进行急性和亚慢性口服毒性(90天)研究,对白杨素进行了全面的安全性评价。研究发现,单次口服白杨素(1750 mg/kg)在14天内没有造成任何致死。然而,在5000 mg/kg体重的剂量下,白杨素造成了40%的死亡率。此外,雄性大鼠比雌性大鼠对白杨素更敏感,因为雄性大鼠的摄食量和肝脏重量比载体对照组显著降低。AOT研究结果表明,白杨素的半数致死量(MLD即LD50)为4350 mg/kg。
3 白杨素衍生物的生物活性
3.1 白杨素衍生物的抗肿瘤活性
Zhu等[8]分别在白杨素的5,7位羟基上进行了烷基化、乙酰化,苯甲酰化和羧甲基化的结构修饰改造,合成了9个5,7双取代或单取代的白杨素衍生物,并测试了该系列衍生物对H22细胞(小鼠肝癌H22肿瘤细胞系)的抗肿瘤活性的影响,实验结果显示,其中化合物2(图2)的活性最强,其IC50是141 μM。研究其机制发现化合物2与蛋白质有相互作用,影响细胞有丝分裂,使细胞生长周期停留在G2期。
因为白杨素的7位羟基具有很高的活性,任杰等[9]利用这一特性,将水溶性基团烷胺基引入C-7位,设计并合成了21种未见文献报道的含氮衍生物。当哌嗪取代基出现在第7位时,化合物3(图2)的抗肿瘤活性最强,其 IC50介于1.19~3.08 μΜ。所以这类药物有作为抗肿瘤新药的潜力。
Martins等[10]基于生物电子等排原理,用S和Se取代白杨素的4-羰基氧原子,合成了新的S代和Se代白杨素。相较于S代白杨素,Se代(化合物4,图2)有更好的抗肿瘤活性。
Zeng等[11]合成的白杨素镧配合物, 能插入DNA疏水区,从而改变DNA的复制,抑制肿瘤细胞的生长,从而具有较强的体外抗肿瘤活性。实验发现La(Ⅲ)配合物(化合物5,图2)对两种肿瘤细胞(A-549和P388)的抑制作用远大于白杨素,其抗肿瘤活性的强弱是由其分子结构对DNA分子亲和力的大小所决定的。化合物5和Chrysin与DNA结合的发射滴定曲线表明,白杨素的镧配合物插入DNA内部疏水环境的深度强于白杨素。
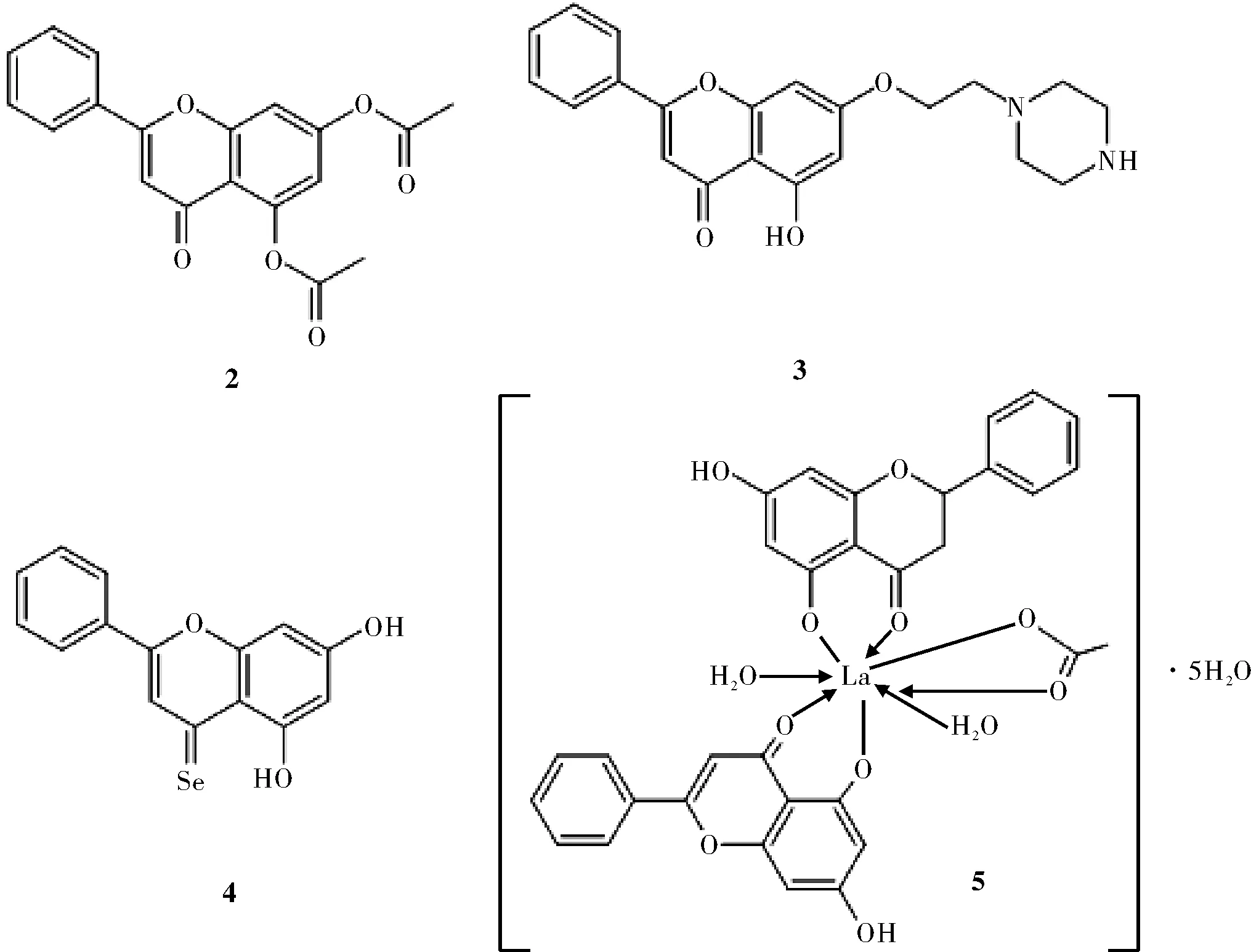
图2 具有抗肿瘤活性的白杨素衍生物的结构
3.2 白杨素衍生物的降血糖活性
基于药效团拼合的原理,Wang等[12]设计合成了15个白杨素偶联NO的衍生物(6.1-6.5a~c,图3),测试了该类化合物对α-葡萄糖苷酶的抑制活性及体外NO释放能力。结果表明,除化合物6.4a~c外,其余12个化合物对α-葡萄糖苷酶的抑制活性均强于阳性对照阿卡波糖和脱氧野尻霉素的活性,进一步构效关系研究发现,5-OH、疏水基团和羰基都能够增强抑制活性,这为糖尿病并发症的治疗研究提供了一个新思路。
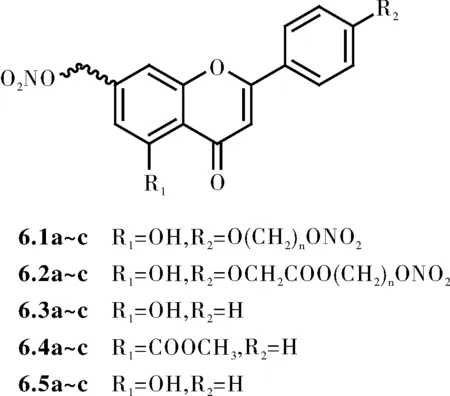
图3 具有降血糖活性的白杨素衍生物的结构
3.3 白杨素衍生物的抗菌活性
Babu等[13]制备了3个系列的白杨素7位羟基偶联的杂环衍生物(7a~c,图4),分别进行G+和G-菌的抑制试验,革兰氏阳性菌以枯草芽孢杆菌(MTCC 441)、球形芽孢杆菌(MTCC 11)和金黄色葡萄球菌(MTCC 96)为例,革兰氏阴性菌以紫色色杆菌(MTCC 2656)、克雷伯菌(MTCC 39)和铜绿假单胞菌(MTCC 741)为例,用MIC(最低抑菌浓度)值监测它们的抑菌活性,数据显示大部分衍生物具有适度的抑菌活性,其中含有4个C间隔的系列2化合物(n=2)显示出良好的生物活性。
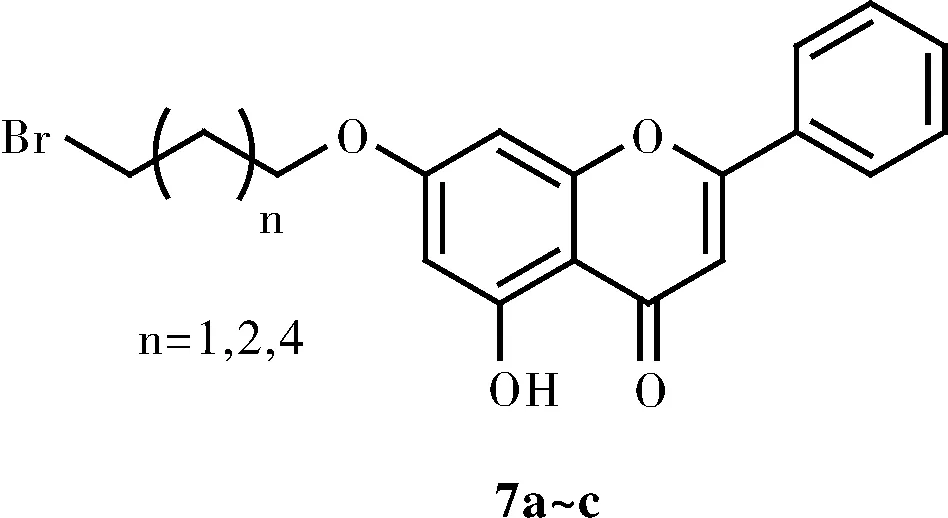
图4 具有抗菌活性的白杨素衍生物的结构
3.4 白杨素衍生物的抗炎作用
Song等[14]研究发现白杨素经γ射线照射会转化为一种新的羟乙基化产物,白杨素羟乙基衍生物对骨髓来源树突状细胞(BMDC)和葡聚糖钠盐(DSS)诱导的小鼠结肠炎有抗炎作用。与白杨素相比,白杨素羟乙基衍生物能更有效地抑制BMDC的成熟,而脂多糖刺激的BMDC中促炎细胞因子、表面分子抗原能力和T细胞增殖/活化水平的降低则恰恰证明了这一点。活化的BMDC通过产生大量促炎细胞因子来诱导炎症,而白杨素羟乙基衍生物能抑制脂多糖刺激的BMDC产生细胞因子,从而起到抗炎作用。
3.5 白杨素衍生物对血管的保护作用
Ravishankar等[15]合成了硫衍生物、钌配合物和硫钌白杨素衍生物,并评价了它们对血小板功能的调节作用。实验证明,在富含血小板的血浆和全血生理条件下,硫钌白杨素衍生物对血小板功能和血栓形成的抑制作用是白杨素的4倍。值得注意的是,硫钌白杨素衍生物对小鼠的止血作用与白杨素相似。与白杨素相比,钌硫白杨素的生物利用度和细胞通透性增加,是其活性增强的基础。这些结果表明,钌硫偶联的白杨素衍生物为研发新型抗血栓药物指明了方向。吴金华等[16]发现白杨素和羟乙基白杨素能够活化抗氧化酶,激活抗氧化体系,清除自由基,减轻脑缺血对神经细胞的损伤。白杨素和羟乙基白杨素减轻缺血损伤的效果可能是基于对Nr2-ARE信号通路的上调作用,且羟乙基白杨素的作用比白杨素更强,效果更好。导致其药效增强的原因是羟乙基水杨素的水溶性较白杨素有所改善,进入体内吸收率增加、分布情况改善,并且代谢清楚速率下降,延长了药物作用时间,使其对急慢性脑缺血的防治效果更加显著。
3.6 白杨素衍生物的抗高尿酸血活性
仲崇琳等[17]以天然产物白杨素为起始原料,选择性地引入含氟原子的活性官能团,如:氟苯基,二氟苯基,三氟苯基,氟苄胺等,最终合成了白杨素类衍生物(8a~b, 图5)。研究表明,氟取代药物能在很大程度上改变各种生物过程,从而改变药物的体内活性。比如说,氟原子和含氟基团被引入化合物后,改变了分子内部电子密度的分布,提高了化合物的脂溶性和渗透性,不仅有利于药物在生物体内的吸收和转运,还延缓了药物的代谢。并且氟取代药物能够通过电子的调节使药物和受体间的结合力加强。仲崇琳等通过对白杨素衍生物黄嘌呤氧化酶抑制活性的研究,发现合成的白杨素衍生物(8a、8b)对黄嘌呤氧化酶具有良好的抑制作用。通过实验研究白杨素及其衍生物对高尿酸小鼠血清尿素水平的影响,发现先导化合物白杨素的生理作用不明显,而大部分的白杨素衍生物在40 mg/kg剂量下可以明显降低高尿酸血症小鼠血清尿酸水平,甚至使动物模型小鼠的高尿素水平恢复到正常水平。
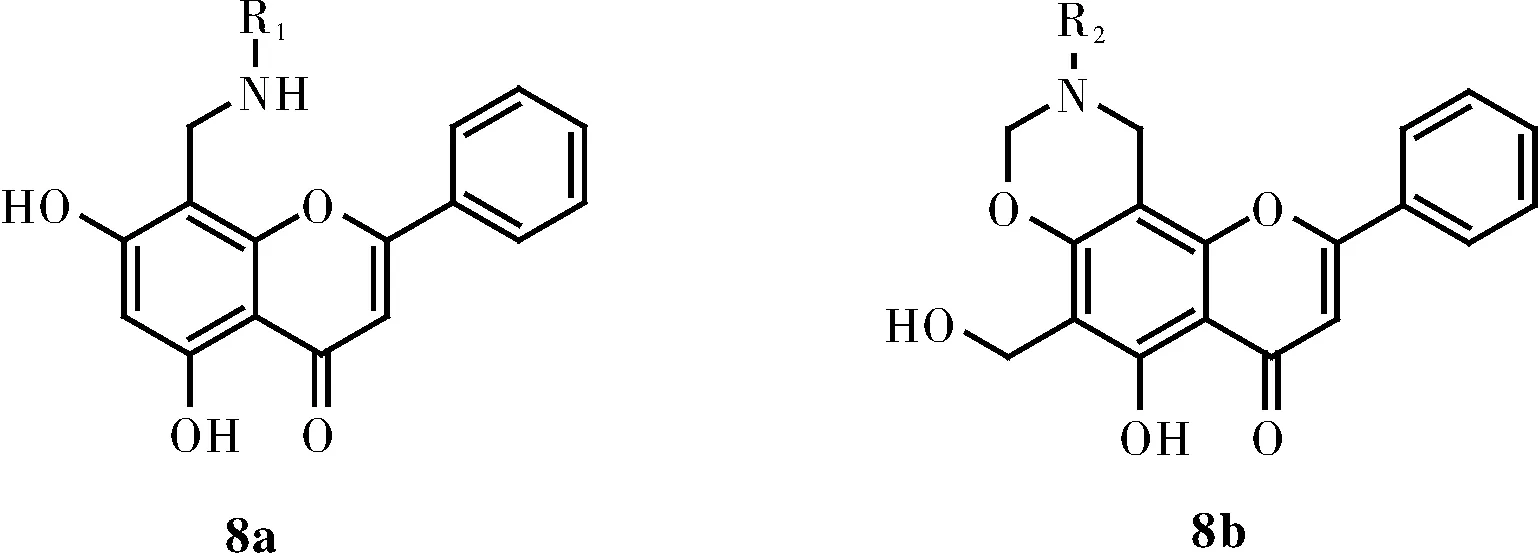
图5 具有抗高尿酸血活性的白杨素衍生物的结构
4 结 语
在全面掌握白杨素分子构效信息的基础上,增强其药理活性和减轻不良反应的结构修饰研究成为热点。目前现有技术中已经对白杨素衍生物做了大量研究,设计并合成了众多结构新颖、活性较强的白杨素衍生物。但衍生物仅限于白杨素磺化物、硝化物、烷基化、酯化、磷酰化、氨基化、甲基化、偶联杂环及一氧化氮供体衍生物的合成等,因此对于各种有效的化学修饰方法的研究还有待深入。
近年来,通过分子生物学的研究,人们也得到了一些关于白杨素衍生物的较深入的机制,如预防或治疗糖尿病并发症、治疗高尿酸血症、抗辐射损伤、抑制肿瘤细胞增殖、诱导肿瘤细胞凋亡和抗基因突变作用等,对以后白杨素的结构修饰和改造起到了重要的指导作用。相信随着定量构效关系分析技术的进一步发展,将会有更多具有潜在生物活性的白杨素衍生物被发现。

