困难胆囊切除术对患者术中和术后并发症的影响及其风险预测模型的建立
曹葆强,李敏,胡金龙,袁中旭,钟兴国,姚佳明,王润东
伴随微创技术在腹部外科的发展和进步,腹腔镜胆囊切除术(LC)因其创伤小、康复快、术后并发症少等特点已经成为胆囊良性病变的标准术式。然而,在某些情况下,LC的操作是十分困难的,并有可能中转开腹,给患者带来许多痛苦[1]。因此,术前对LC手术困难程度进行合理评估,对于保证手术安全性非常必要。本研究回顾性分析我院行胆囊切除术患者资料,对手术困难程度进行合理划分,分析各种因素和手术困难程度的关系,以期降低LC手术风险及中转开腹率。
1 对象与方法
1.1研究对象 收集安徽省第二人民医院2018年1月1日—2019年11月10日行胆囊切除术的患者共201例。纳入标准:(1)术前常规行肝、胆、胰、脾B超和磁共振胆胰管成像(MRCP)检查,明确诊断为胆囊结石或胆囊息肉。(2)胆囊结石≥2 cm或胆囊息肉直径≥1 cm。排除标准:(1)术前诊断不能排除胆囊恶性占位性病变。(2)合并肝内或肝外胆管结石,需行胆总管探查者。(3)术中麻醉效果不理想。(4)术中气腹建立不佳。(5)术中器械故障等。
1.2手术难度评估及分组 胆囊切除术作为常规开展的手术,对于技术成熟的外科医生来说,手术时长通常能够反映手术难度。参考陈蕾等[2]对人群中胰岛素抵抗的评估方法,笔者对纳入研究患者的手术时间进行统计和划分,将手术操作时间的第75百分位数(P75)作为分组依据,时长≥P75的患者归入困难胆囊切除术(DC)组,<P75的患者归入常规腹腔镜胆囊切除术(NLC)组。为进一步评价此方法划分手术难度的合理性和真实性,辅以患者主要结局指标,如术中出血量、中转开腹率、引流管置放率、术后24 h呕吐频次、术后肩痛发生率等作为评价依据。
1.3手术方法 所纳入的患者全部采用气管插管和全身麻醉,待患者麻醉、插管后,建立CO2气腹并维持压力12 mmHg(1 mmHg=0.133 kPa),由经验丰富且固定团队的外科医生进行常规三孔腹腔镜胆囊切除术,根据术中情况或改为四孔法。逐层钝性分离组织,仔细解剖胆囊三角,Hem-o-lok夹分别结扎胆囊动脉及胆囊管,根据难易程度进行胆囊顺行切除或逆行切除,清洗腹腔,酌情放置腹腔引流管,查无出血后缝合戳孔,结束手术。若术中见患者腹腔内广泛粘连、胆囊三角解剖极为不清、出血无法有效控制或可能出现意外胆管损伤等情况,及时给予腹腔镜中转开腹,保证手术安全。
1.4观察指标 根据临床经验选择术前即可评估的、可能影响LC手术操作的因素,如体质量指数(BMI)、白细胞计数(WBC)、近期胆囊炎发作频次、腹部手术史、经内镜逆行胰胆管造影(ERCP)手术史、胆囊穿刺术史、腹部炎症史等作为研究观察指标。以术中出血量、是否中转开腹、是否置放引流管、术后24 h呕吐频次、术后是否发生肩痛、术后首次排气时间以及住院时间作为主要结果指标。查阅患者原始病历资料并逐条登记、收录。所有资料搜集过程征求患者或家属意见,签署知情同意书。本研究经医院伦理委员会审核通过。
1.5统计学方法 运用SPSS 24.0软件对数据资料进行分析,采用四分位法划分手术难易程度,满足正态分布的计量资料用均数±标准差(±s)表示,组间比较采用成组t检验。非正态分布计量资料以M(P25,P75)表示,组间比较采用Mann-whitneyU检验。定性资料以例(%)表示,组间比较采用χ2检验或Fisher确切概率检验。先将多个观察指标进行单因素分析,选择单因素分析有意义的观察指标进行多因素非条件Logistic回归进一步筛选出独立危险因素,并构建其预测模型,采用Hosmer-lemeshow检验评价预测模型的拟合优度。绘制受试者工作特征(ROC)曲线并计算曲线下面积评价预测模型的效能。以P<0.05为差异有统计学意义。
2 结果
2.1 一般情况 201例患者的手术操作时间20~240 min,P75为70 min。遂将手术操作时间<70 min的患者归入NLC组,将手术时间≥70 min归入DC组。最终,NLC组纳入148例患者(均在腹腔镜下完成),年龄22~89岁,BMI 18.26~33.65 kg/m2;DC组纳入53例患者(腹腔镜下完成50例,中转开腹3例),年龄20~85岁,BMI 19.11~36.57 kg/m2。2组患者基线资料比较差异无统计学意义(P>0.05),见表1。
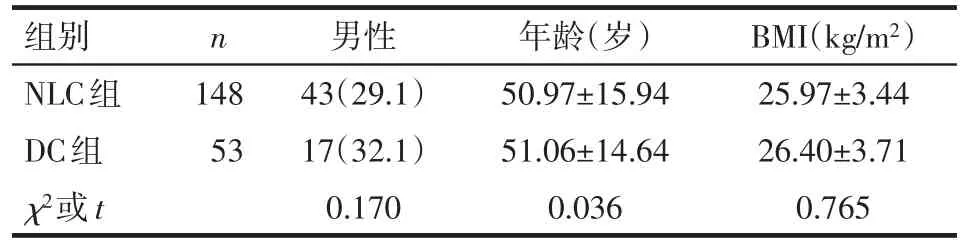
Tab.1 Comparison of basic data between NLC group and DC group表1 2组患者基线资料比较
2.2 2组患者围手术期情况 DC组与NLC组相比,术中出血量、术后24 h呕吐频次增加,中转开腹率、术后引流管置放率升高,术后首次排气时间及住院时间延长(P<0.05),2组术后肩痛发生率及切口感染率差异无统计学意义(P>0.05),见表2。
2.3 影响胆囊切除手术难度的单因素分析 结果显示,BMI>25 kg/m2、WBC>10×109L、胆囊穿刺术后、颈部结石嵌顿、近2个月胆囊炎发作>4次、胆囊壁厚度>0.5 cm、结石最大直径>2 cm在NLC和DC组间存在明显差异(P<0.05),见表3。
2.4 建立DC风险预测模型及模型评价 以胆囊切除手术困难与否(手术操作时间是否≥70 min)为因变量,以BMI、WBC、胆囊穿刺术后、胆囊颈部结石嵌顿、近2个月胆囊炎发作次数、胆囊壁厚度及结石最大直径为自变量,行Logistic回归分析,变量赋值见表 4。结果显示,回归方程:Logit(P)=-3.426+1.291X1+2.400X2+1.564X4+2.722X5+2.486X6+2.323X7。
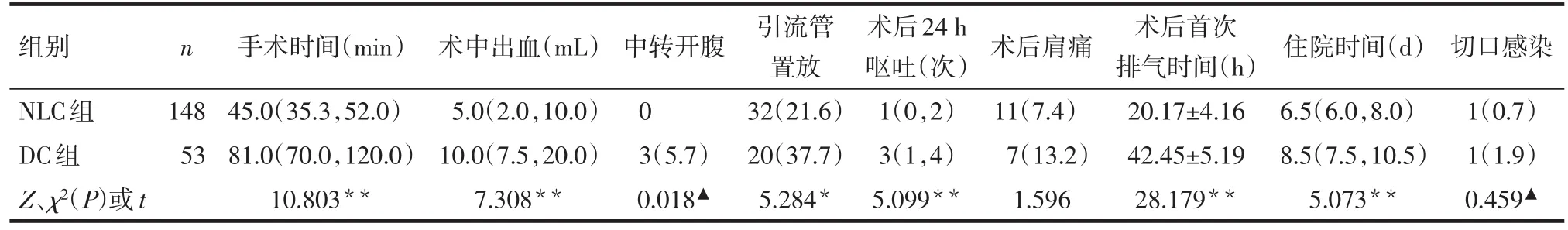
Tab.2 Comparison of perioperative indicators between the two groups表2 2组患者围手术期指标比较
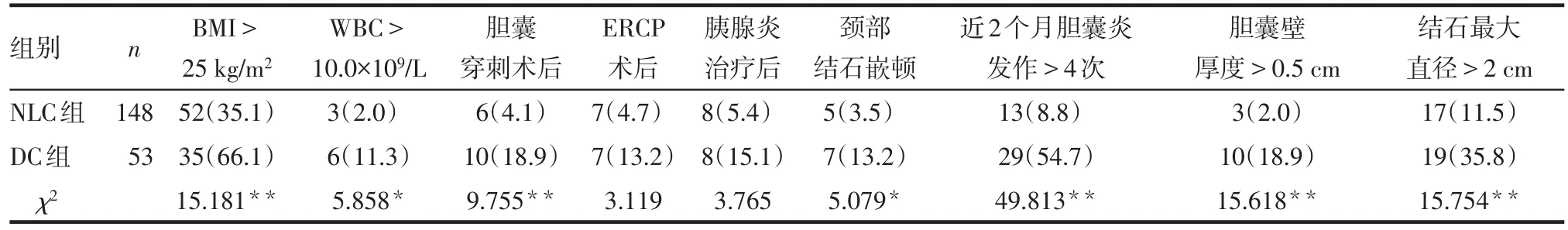
Tab.3 Results of univariate analysis on the difficulty of cholecystectomy表3 影响胆囊切除手术难度的单因素分析结果 例(%)
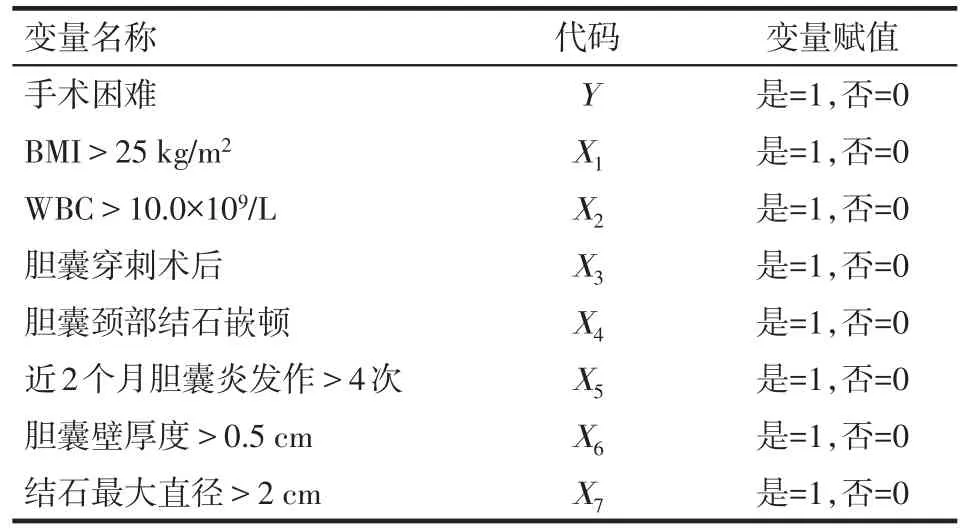
Tab.4 Variable assignment table of Logistic stepwiseregression analysis表4 多因素Logistic回归分析变量赋值表
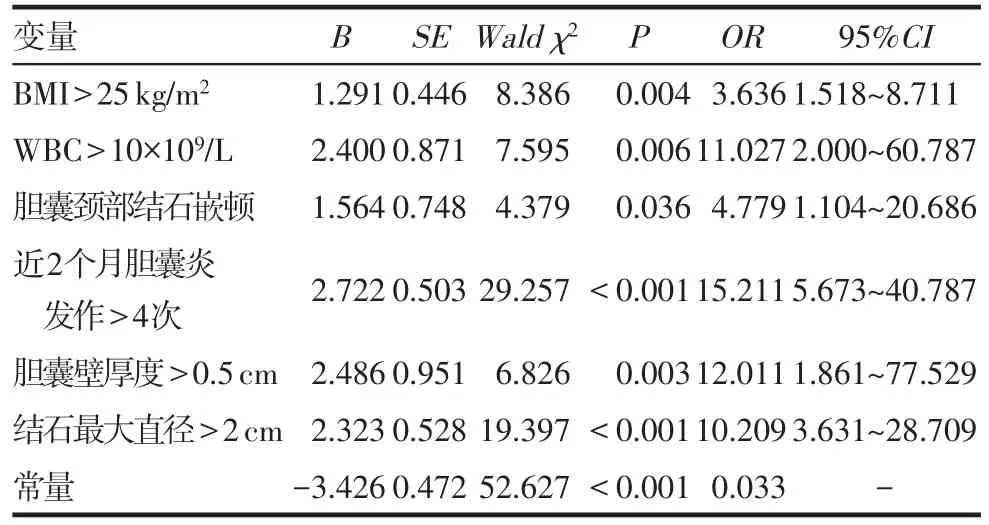
Tab.5 Multivariate analysis of risk factors in DC表5 困难胆囊切除术危险因素的多因素分析结果
采用Hosmer-lemeshow检验评价Logistic回归模型的拟合优度,结果显示该回归方程拟合优度较好(χ2=1.457,df=5,P>0.05)。计算患者的手术困难概率预测值P,绘制ROC曲线评价模型的预测效能,结果显示曲线下总面积为0.879,最佳临界值为0.686,敏感度为94.3%,特异度为52%,95%CI为0.822~0.933,P<0.01,认为此模型合理,适用于临床风险的预测,见图1。
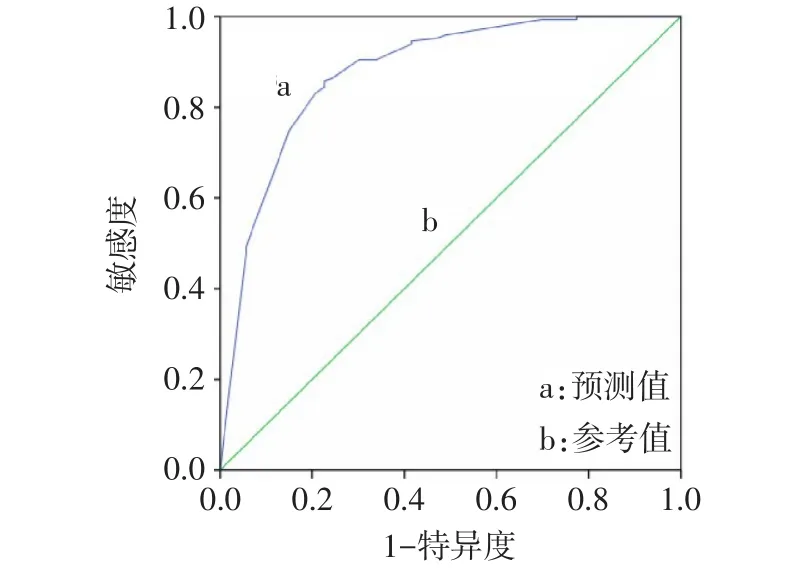
Fig.1 The ROC curves of difficult cholecystectomy图1 困难胆囊切除术预测模型的ROC曲线
3 讨论
LC作为一项成熟的技术,已经成为胆囊切除的标准术式,但术中、术后仍然可能出现胆道损伤[3]、胆瘘、腹腔感染等严重并发症[4]。既往有学者研究了LC中转开腹和LC术后严重并发症的相关危险因素[5],但其研究对象多为无法完成腹腔镜胆囊切除或已出现严重并发症的病例,往往忽略了那些手术难度大、手术时程长、手术风险大的LC术可能的风险因子。因此,如何在术前有效地预测、评估手术难度和风险,哪些指标改变能够让外科医生更具有警惕性,是本次研究的重点。本研究通过分析困难胆囊切除术的危险因素并构建预测模型,希望能够帮助临床医生更加安全、高效地开展LC。
3.1 手术时间划分手术难度的合理性 笔者采用手术操作时间的P75值作为DC和NLC的分割点进行分组研究,符合临床习惯,简便易行。研究结果显示,DC组与NLC组相比,术中出血量、术后24 h呕吐频次增加,中转开腹率、术后引流管置放率升高,术后首次排气时间以及住院时间延长,表明采用手术时间长短划分胆囊切除手术的难度有一定合理性。考虑到外科医生的手术经验往往会直接影响到整个手术的操作时间[6],本研究选择了经验丰富且固定的手术团队实施手术的病例资料,以此降低人为因素对手术操作时间的影响。此外,对于术中麻醉效果不理想、术中气腹建立不佳以及术中机器故障等可能影响手术操作时间的因素,均予以排除,以保证病例的选取的合理性。
3.2 LC手术影响因素分析 在尽量减少系统误差的基础上,笔者发现BMI>25 kg/m2、胆囊壁厚度>0.5 cm及近2个月胆囊炎发作>4次是手术时程、手术难度增加的独立危险因素。结合临床工作经验,笔者认为上述因素致手术操作困难的原因和可能的解决办法如下:(1)肥胖。过度肥胖患者腹壁脂肪层肥厚会导致常规的trocar因长度不够而难以抵进腹腔理想的位置,从而影响手术进程;肥胖患者常伴有肝脏尾状叶生理性增大和下坠以及胆囊三角脂肪组织堆积等情况,这也会造成操作难度提升、胆囊管和肝外胆管显露困难等问题[7]。因此,对于腹壁脂肪肥厚的患者应选用更长的trocar进行穿刺以利于术者进行腹腔操作;当尾状叶遮挡手术区域时,可以让助手利用无损伤钳挑起尾状叶;当胆囊三角脂肪堆积时,可先打开胆囊三角浆膜层,再使用电凝钩顺着管道走行方向反复、多次勾起小块组织进行分离,并配合吸引器轻柔推剥周围组织,直至充分暴露出胆囊管、胆总管、肝总管之间的关系,仔细甄别后再行钳夹和离断。(2)胆囊壁增厚。除了长期反复的慢性炎症刺激以及胆囊萎缩会引起胆囊壁增生、增厚以外,急性炎症的患者也会出现胆囊壁不同程度的水肿、增厚[8],胆囊壁增厚会增加钳抓胆囊的难度,故需要选用带齿抓钳抓取胆囊或者电凝切开胆囊壁后,将抓钳伸进胆囊内进行钳抓。(3)胆囊炎反复发作使得胆囊与周围组织粘连致密,组织难以剥离,解剖关系难辨,更易误伤胆管[9]。当出现类似情况时,仍然要以充分游离胆囊前、后三角,充分显露胆囊三角为目标,如术中发现结肠、十二指肠粘连时,可以更多地采用吸引器推拨等钝性方法进行分离。
本研究中也发现WBC>10×109/L、结石最大直径>2 cm,胆囊颈部结石嵌顿是胆囊切除术变得困难的独立危险因素。分析原因,笔者认为:(1)白细胞升高往往表明患者处于急性炎症期,而胆囊在胆囊炎急性发作期内会呈现不同程度的充血水肿、胆囊壁增厚,并且随着急性炎症期的发展,胆囊壁以及三角区域组织充血水肿进一步加重,这些改变可使胆囊三角区域解剖难以区分,容易误伤肝外胆管,给腹腔镜手术造成极大的困扰[10]。因此,需要合理应用抗生素控制胆囊急性炎症,急性炎症72 h内手术治疗,急诊手术中亦可采用前述方法谨慎处理胆囊水肿、胆囊壁增厚、胆囊三角解剖不清等问题;超过窗口期的采用保守治疗或先行经皮经肝胆囊穿刺引流术(PTGBD)穿刺引流,待炎症完全控制后再择期行手术治疗。(2)当胆囊内结石较大,尤其是较大的结石发生嵌顿时,手术难度和风险也会随之提升,这主要是因为颈部结石嵌顿会使胆囊管变短或消失,胆囊管无法充分显露,如若强行剥离可致胆总管损伤等问题[11]。针对此类问题,术中可先利用分离钳将嵌顿结石挤回胆囊体部,或者电凝切开近壶腹部胆囊颈管取出结石,再进行胆囊管的分离与结扎。
本研究与既往研究观点[12]不同的是,胆囊穿刺引流术、ERCP术、胰腺炎治疗并不增加患者行LC的难度。笔者认为:(1)胆囊穿刺引流术能够有效地减少急性化脓性胆囊炎、急性重症胆囊炎、胆囊肿大对LC造成的困难。(2)ERCP术及胰腺炎治疗不增加LC的难度,可能与我院ERCP术后、胰腺炎治疗后行LC的间隔时间短有关,短期内安全地实施LC手术能够及早解决大多数胆总管结石及胆源性胰腺炎的根本诱因,并且减少胆囊三角及周围组织炎症水肿、炎性粘连对手术的影响。
3.3 术前回归方程对评价手术难度的参考价值 为更好地明确影响因素对评价胆囊切除手术难度的临床价值,笔者先对模型进行拟合优度评价,再采用ROC分析法[13]评价模型的预测效能,最终结果表明回归方程Logit(P)预测LC手术难度有一定临床参考价值。
综上所述,影响LC手术难度的危险因素主要有BMI>25 kg/m2、WBC>10×109/L、近2个月胆囊炎发作>4次、胆囊壁厚度>0.5 cm、结石最大直径>2cm及胆囊颈部结石嵌顿。术前通过回归方程Logit(P)预测胆囊切除的困难性,将有助于指导临床医生更加安全、高效地开展LC,更好地为患者提供精准的个体化优质诊疗服务。

