儿童混合型淋巴管畸形1例
周少余 郑惠文 李云玲 金国信 虞培珍
淋巴管畸形(lymphatic malformations,LMs)是淋巴管的良性增生,而非肿瘤性改变。该病多发生于2岁以前的儿童,2岁以后发病者少见。根据病变内淋巴管囊腔的大小,可将LMs分为巨囊型、微囊型和混合型[1],其中混合型LMs较为少见。浙江大学医学院附属儿童医院于2019年8月22日收治了1例混合型LMs患儿,现将诊治经过报道如下。
患儿女,6岁。左背部肿块伴水疱样皮疹7个月余。不痛、不痒。查体:左背部可见一包块,约3.3 cm×2.5 cm×0.5 cm,质软,界清,无压痛,表面散在两处粟粒至绿豆大小水疱样改变,无破溃。水疱呈透明乳白色或淡黄色,表面光滑发亮,如蛙卵状外观。部分水疱呈暗红色。基底为正常肤色,无红晕,见图1(插页)。实验室检查:血、尿、大便常规及肝肾功能、血糖、血脂、电解质、凝血谱等均无异常。胸部X线片及心电图检查亦无异常。浅表B超检查:背部皮下脂肪层内可探及无回声区及2.5 cm×2.5 cm×0.5 cm的低回声区,边界清,内部透声尚可,内可见多个分隔,后方回声增强,包块内分隔处可见血流信号。考虑LMs可能。结合患儿病史、查体及辅助检查,临床诊断:左背部混合型LMs。鉴于该患儿皮损较为表浅、局限,予以全麻下经皮背部淋巴管瘤体内聚桂醇注射治疗。聚桂醇注射液(批号:20181207,10 ml∶100 mg,陕西天宇制药有限公司)与空气按1∶3比例混合制成泡沫制剂备用。在B超引导下,分别于病灶上、下两极经皮穿刺,穿刺针进入病灶囊腔回抽有淡黄色清亮淋巴液,经上极穿刺部位注入聚桂醇泡沫制剂,此时病灶内弥漫性高亮气体影,由下极可回抽出泡沫制剂,多点穿刺共注入聚桂醇3 ml,压迫针眼止血,术后待患儿苏醒后返回病房。术后3 d患儿病情平稳,无明显不良反应,予出院门诊随访。术后3个月随访,浅表B超检查:背部皮下脂肪层内可探及1.5 cm×0.7 cm×0.3 cm的等回声区,边界欠清,内部回声均匀,未见明显异常血流信号。肉眼观察左背部,发现肿块已消退,皮下畸形面积明显缩小,皮损部分结痂脱落,未见复发,见图2(插页)。讨论 LMs是儿童常见的一种先天性脉管畸形疾病,多数学者认为是淋巴管的先天性发育畸形或某些原因引起发病部位淋巴液排出障碍,造成淋巴液潴留,导致淋巴管扩张、增生而形成[2]。该病好发于头颈部、腋窝、四肢关节、腹壁、腹腔及腹股沟等处。根据病变内淋巴管囊腔的大小,可分为巨囊型、微囊型和混合型。巨囊型LMs由1个或多个体积≥2 cm3的囊腔构成,微囊型LMs由1个或多个体积<2 cm3的囊腔构成,两者兼有为混合型LMs[3]。根据本例患儿的临床表现及辅助检查结果(背部包块为体积>2 cm3的囊腔,周边有水疱样皮疹,系小囊腔,存在无回声区和低回声区),再结合术中穿刺可见淡黄色清亮淋巴液,故临床诊断为背部混合型LMs。
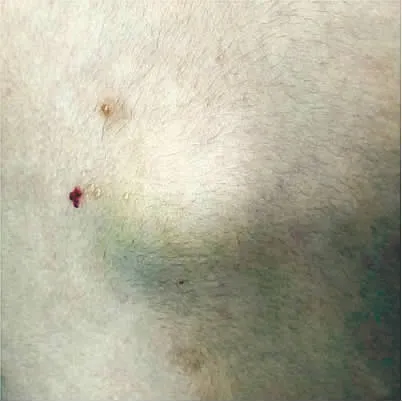
图1 术前左背部肿块伴皮疹
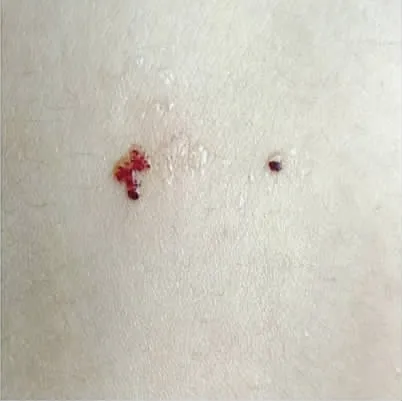
图2 术后左背部肿块已消失
LMs一般不会自行消退,畸形瘤体随时间逐渐增大。在遭受创伤、感染或发生囊内出血、接受不适当治疗后,瘤体常常突然增大。若LMs长在某些特殊部位,可能导致毁容、畸形,甚至压迫重要器官而引起功能障碍,危及生命[4]。目前,治疗LMs的方法很多,包括手术切除、硬化剂注射治疗、二氧化碳激光治疗[5]、口服西罗莫司治疗[6]、等离子消融[7]等。根据LMs分型、发病部位的不同,应选择不同的治疗方式。过去,手术治疗是LMs首选方法,但是单纯手术治疗的创伤较大,难以完全切除病灶,复发率高,且遗留瘢痕影响美观。硬化剂注射治疗是通过化学物质破坏囊肿壁内皮细胞,产生无菌性炎症,导致局部的成纤维细胞和胶原纤维增殖,使囊腔凝固、硬化、粘连、闭合,具有创伤小、治疗周期短、治愈率高、复发率低、不遗留手术瘢痕等优点,已逐步取代了手术治疗。常用的硬化剂包括OK-432、平阳霉素[8]、聚桂醇及聚多卡醇、博来霉素[9]等,临床上对于哪种疗效更佳并无一致的结论。王立丹等[10]研究表明,对于儿童复杂及难治型LMs,囊内硬化治疗具有安全、可靠、可重复、最大限度保护容貌等优势,建议在充分认识疾病临床特点后采取合理的硬化剂治疗方案。本例患儿为混合型LMs,行聚桂醇注射术治疗后3个月,背部肿块消退,皮下LMs面积明显缩小,未见复发,提示硬化剂注射治疗LMs有效。然而,硬化剂治疗也可能导致肺炎样病变或肺纤维化等不良反应,但目前尚无关于相关严重不良反应的个案报道。因此,仍需要大样本、多中心的研究及长期随访进一步研究证实。

