微球形Bi2WO6催化剂的制备及其光催化性能
王 艳,白风荣,周 佳,王洪亮,陆津津
(内蒙古化工职业学院,内蒙古 呼和浩特 010010)
苯甲醛是有机合成中一种重要的中间体,在农药、染料、香料、化妆品和制药等领域被大量的应用[1-4]。苯甲醛的生产工艺主要有甲苯氧化法和苯甲醇直接氧化法[5]。甲苯氧化法生产苯甲醛产品收率低,副产物多,限制了其工业化应用。苯甲醇直接氧化法生产苯甲醛,工艺简单,环境友好,表现出较好的应用前景,但是氧化反应时常用贵金属做催化剂,如Au/沸石,Pd-Co/Al2O3[6-7],通常需要在高温下进行,反应条件要求较高、能耗大、催化剂成本也相对较高。所以开发半导体光催化剂用来光催化苯甲醇液相氧化生产苯甲醛,绿色、环保、条件温和、成本低备受人们关注。
Bi2WO6属于简单的Aurivillius型氧化物,是钙钛矿层状结构,由Bi2O2层和WO6八面体结构片层构成,具有优异的物理和化学性能,另外带隙较窄(禁带宽度约为2.69 eV),能吸收紫外光和可见光,可以吸收更多的光量子用于光催化。近年来,Bi2WO6已作为一种新型可见光催化材料引起广泛的关注,但大部分合成出的Bi2WO6应用于光降解,很少用于光催化有机合成反应。本工作选用Bi(NO3)3·5H2O和Na2WO4·2H2O作为前驱体,采用水热法制备出Bi2WO6微球,在可见光照射下,将其用于苯甲醇催化氧化生产苯甲醛,苯甲醛获得较高产率,并根据表征分析及实验结果,进一步推测了该反应可能的光催化机理。
1 实 验
1.1 Bi2WO6光催化剂的制备
按比例分别称取一定量的Bi(NO3)3·5H2O(天津市永晟化学试剂厂,分析纯)和Na2WO4·2H2O(天津市化学试剂四厂,分析纯),将称量的Bi(NO3)3·5H2O溶解于0.5 mol/L的硝酸溶液中经磁力搅拌得到溶液A,Na2WO4·2H2O完全溶解于二次去离子水中得到溶液B。室温下,将溶液B逐滴加入至溶液A中,并将二者搅拌混合均匀得到混合溶液,用硝酸溶液和氢氧化钠溶液调节混合溶液pH值至合适范围,混合溶液继续磁力搅拌1 h,然后将混合溶液移到高压反应釜中,密封后放入马弗炉,设定水热反应温度和时间,反应结束后反应釜自然冷却至室温得到沉淀物。用去离子水和无水乙醇各洗涤沉淀物3次,在60 ℃下将固体产物干燥12 h,即得到淡黄色Bi2WO6粉末,研磨贮存待用。
1.2 催化剂表征方法
采用RIGAKU公司的D/MAX-2500型X射线衍射仪对催化剂试样进行XRD表征(测试条件:尾管电压40 kV,管电流100 mA,利用铜靶作为金属靶(λ=1.540 5×10-10m),扫描范围为5°~80°,扫描速度为5 (°)/min);采用日本Hitachi公司U-390型固体紫外-可见吸收光谱仪对催化剂试样进行UV-vis DRS表征;采用日本Hitachi公司S-4800扫描电子显微镜对催化剂试样进行SEM表征;催化剂试样的比表面由Quantachrome公司的比表面仪测试得到,以N2为分析气,浴温为77.35 K。
1.3 催化苯甲醇氧化反应
称取一定量Bi2WO6催化剂和碱放入50 mL圆底烧瓶中,然后量取5.0 mL溶剂和1.0 mmol反应物苯甲醇加入上述圆底烧瓶,磁力搅拌圆底烧瓶中的溶液。光催化反应时,用LED灯(500 W,波长为200~800 nm)作为照射光源,LED灯距离反应装置圆底烧瓶20 m,空气气氛下,反应时间12 h,反应温度为(35±3) ℃。为对比光催化反应效果,与此同时进行暗反应,暗反应实验操作过程、实验条件与光催化时相同,但在进行暗反应时装有反应试样的烧瓶用锡纸包裹紧密,不被光照射。反应结束后,分别对光催化反应和暗反应的试样用气相色谱(GC)进行测试分析。
2 结果与讨论
2.1 催化剂的表征
2.1.1 X射线衍射(XRD)
图1为Bi2WO6催化剂试样的XRD谱线。由图1可见,催化剂试样在2θ=28.40°、33.06°、47.28°、56.00°、58.76°、76.16°和 78.40°处均出现了Bi2WO6的特征峰。各衍射峰与JCPDS标准卡片(No.79—2381)完全吻合,没有出现杂质相,所制得的试样属于钨铋矿结构的Bi2WO6,并且水热法制备出的Bi2WO6光催化剂结晶度良好,没发生晶相转变。

图1 Bi2WO6催化剂的XRD谱线
2.1.2 UV-vis DRS
半导体光催化剂的活性很大程度上取决于半导体禁带宽度,禁带宽度值越小,吸收太阳能的波长会向长波长的方向移动,对可见光的利用率就会提高,光催化活性也响应会变好。图2为Bi2WO6催化剂试样的UV-vis DRS谱。由图2可见,纯的Bi2WO6在可见光范围具有一定的吸收强度。所以Bi2WO6催化剂具有光催化效果,归因于Bi2WO6在紫外和可见光区有吸收。
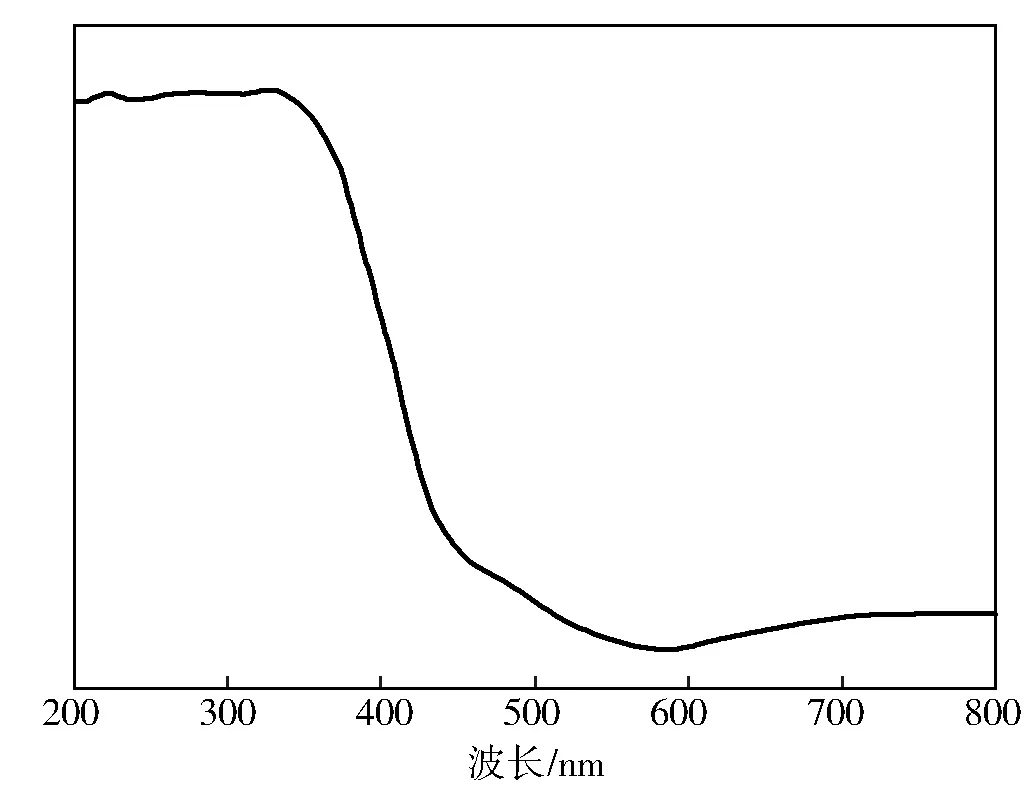
图2 Bi2WO6催化剂的UV-vis DRS谱
2.1.3 比表面(BET)
图3、图4分别为Bi2WO6催化剂试样的N2吸附-脱附等温线和粒径分布曲线。
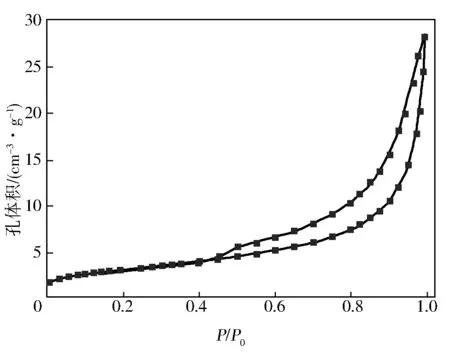
图3 Bi2WO6催化剂的N2吸附-脱附等温线

图4 Bi2WO6催化剂的粒径分布曲线
由图3可见,等温线属于IUPAC分类中的Ⅳ类吸附曲线。等温线在P/P0为0.45~1.0内显示明显的滞后回线,说明所制备的Bi2WO6催化剂试样属于典型介孔结构,由测试表明试样中有较大介孔结构存在,大孔的形成主要原因应该是Bi2WO6片状结构交叉形成的空隙[8]。由图7可知,孔尺寸大多集中在240 nm左右,孔径较大,与等温线上获得的信息几乎一致。介孔结构可以为催化反应时提供较多活性位点,制备的Bi2WO6催化剂试样的比表面为12.01 m2/g。
2.1.4 扫描电子显微镜(SEM)
图5为Bi2WO6催化剂试样的SEM照片。由图5可以看出,实验所得试样Bi2WO6是多孔微球型,微球由众多厚度约为170 nm的纳米片交叉组装而成,粒度均匀,粒径大约6 um。

图5 Bi2WO6催化剂的SEM照片
2.2 光催化苯甲醇氧化反应
2.2.1 溶剂对苯甲醇氧化反应的影响
在反应物1.0 mmol苯甲醇、反应时间12 h、反应温度(35±3) ℃、0.5 mmol NaOH为碱,催化剂Bi2WO6用量50 mg的条件下,考察不同溶剂时苯甲醇氧化反应生成苯甲醛的影响,结果见表1。

表1 不同溶剂对苯甲醇催化氧化反应的影响
由表1可知,Bi2WO6催化氧化苯甲醇反应时,不同溶剂,苯甲醛产率有较大差别,溶剂为异丙醇时,苯甲醛产率最高,可达68.5%。极性较大的DMF为溶剂时,苯甲醛产率最低,其原因可能是溶剂极性过强,催化剂稳定性降低导致[9]。
2.2.2 碱的种类和用量对苯甲醇氧化反应的影响
反应物苯甲醇1.0 mmol、反应时间12 h、反应温度(35±3) ℃、溶剂为异丙醇,催化剂Bi2WO6用量50 mg的条件下,考察碱的种类和用量对苯甲醇氧化反应生成苯甲醛的影响,结果见表2。

表2 碱的种类及量对苯甲醇催化氧化反应的影响
由表2可见,Bi2WO6催化氧化苯甲醇反应时,采用强碱NaOH时,苯甲醛产率较高,采用弱碱CsCO3、Na2CO3时,苯甲醛产率较低,其原因可能是反应物对强碱更敏感[10]。另外,随碱用量增加,苯甲醛收率呈增加趋势,但在本实验中当NaOH用量从0.8 mmol增加到1.0 mmol时,苯甲醛产率增加幅度不大,原因是碱量偏高,出现过量颗粒屏蔽效应,造成体系中光分散和光通路被堵塞[11],所以后续实验中碱的适宜用量是0.8 mmol。
2.2.3 波长对苯甲醛氧化反应的影响
为证明Bi2WO6催化剂对苯甲醇氧化反应是光催化反应,通过滤波片变化照射光的波长范围,考察不同光照波长下苯甲醛的产率,结果见图6。

图6 不同波长范围对苯甲醇氧化反应的影响
由图5可见,随波长范围减小,苯甲醛产率减少,当波长范围达到400~800 nm时,苯甲醛产率最高,可达80.8%,当波长范围450~800 nm和510~800 nm时,苯甲醛产率下降较多,可能是Bi2WO6的吸收波长小于460 nm造成的。
2.3 催化反应机理
基于Bi2WO6光催化苯甲醇的反应结果并结合文献[12],可见光照射时,苯甲醇在Bi2WO6催化剂作用下,氧化为苯甲醛的可能反应机理如图6所示,其过程为:1)可见光照射下,Bi2WO6价带的电子(e-)受到激发跃迁至导带,空穴(h+)留在价带;2)在催化剂表面苯甲醇与空穴h+作用形成苯甲醇自由基和H+,苯甲醇自由基在进一步和空穴h+作用,形成苯甲醛和H+;3)氧气与Bi2WO6导带e-作用形成O-;4)H+和O-生成H2O。在光催化反应过程中,光照射产生的空穴h+起主要作用。

图6 Bi2WO6催化苯甲醇氧化反应的机理
3 结 论
以Bi(NO3)3·5H2O和Na2WO4·2H2O作为前驱体,采用水热法制备出Bi2WO6催化剂,在制备过程中,通过改变制备过程中的温度、酸碱度及制备方法等,得到不同形貌、不同比表面、不同催化性能的具有介孔结构的微球型Bi2WO6催化剂,提高了其光催化活性;Bi2WO6作为催化剂,前人主要将其用于光降解污染物,而将Bi2WO6用于光催化苯甲醇氧化生成苯甲醛有机合成反应中,获得了较好光催化效果,为今后苯甲醇催化氧化生产苯甲醛提供了一种高效、绿色、有发展前景的技术可能。

