洗碗机用洗涤剂理化指标检测方法探讨
吴其文 徐艳丽
(上海和黄白猫有限公司,上海,200231)
随着洗碗机在家庭生活中的逐渐应用,洗碗专用洗涤剂市场也日渐红火。国内洗碗机普及较晚,目前洗碗机用洗涤剂还没有国家标准和行业标准。洗碗机用洗涤剂,不同于手洗餐具洗涤剂,不能借鉴它的检测方法。
目前常见的洗碗机用洗涤剂呈粉状、块状。研究选取了国内外知名品牌的洗碗粉、洗碗块,其主要标识成分为:表面活性剂、碳酸钠、碳酸氢钠、过氧化物(过碳酸钠或过硼酸钠)、 螯合剂(柠檬酸钠)、偏硅酸钠、酶(蛋白酶、淀粉酶)、填充剂硫酸钠及微量添加剂,包括氧活化剂、改性聚羧酸盐、香精、抗再沉积剂、纤维素胶体等[1]。现对上述主要成分的含量测定、产品理化指标的检测方法和检测过程中发现的问题进行探讨。
洗碗粉是通过混合复配的方式制备的,原料之间的比重有一定的差异,造成粉体不均匀,普通的取样方式不具有代表性,所以检测过程以分样后得到的最小数量为取样量。对洗碗块以压碎后分样,依据GB/T 13173-2008《表面活性剂 洗涤剂实验方法》第四章 样品的分样中4.2.1 “粉状样品分样”的要求进行分样[2]。
1 主要成分的测定
1.1 表面活性剂含量的测定
表面活性剂在洗碗粉中用量较少,其主要作用是润湿和帮助污垢分散,并防止污垢再沉积到餐具表面,使用的表面活性剂通常是低泡和耐氧化的非离子表面活性剂。洗碗粉的主成分是各种碱性助洗剂,这些碱性助剂在95%乙醇中有一定的溶解度,所以按GB/T 13173-2008(7)中的方法,用95%乙醇萃取法测定总活性物含量来表示表面活性剂含量时,总活性物含量测定结果会偏高,相对误差比较大。如将标准中所用的95%乙醇改用无水乙醇,就大大降低了各种碱性助洗剂的溶解度,结果更接近真实值。本研究分别用95%乙醇和无水乙醇萃取,按GB/T 13173-2008 7 洗涤剂中总活性物含量的测定方法对市售的6种洗碗粉进行测定,结果见表1。
对6种洗碗粉、洗碗块测定结果显示,用95%乙醇作为萃取剂测得的结果均高于用无水乙醇作为萃取剂测得的结果,所以在总活性物测定过程中,可以用无水乙醇作为表面活性剂的萃取剂,这样测得的结果更具真实性。
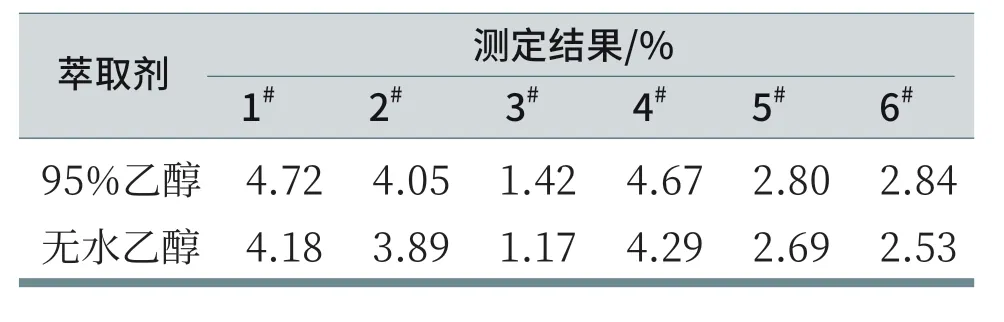
表1 用95%乙醇和无水乙醇萃取测定结果
1.2 活性氧含量的测定
依据GB/T 13173-2008《表面活性剂 洗涤剂实验方法》第十六章 洗涤剂中活性氧含量的测定方法,经过多次实验发现,柠檬酸钠、甜橙油对该测定方法有很大的干扰,它们和过氧化氢(过碳酸钠或过硼酸钠在酸性条件下释放出过氧化氢)一样,在此反应中作为还原剂,均能使高锰酸钾褪色,滴定终点难判断,影响结果的准确性。该方法不适用于洗碗粉或洗碗块中活性氧含量的测定。所以实验采用了碘量法[3],在碘量法中过氧化氢作为氧化剂,经过了多次实验,测定过程无干扰,测定终点明确。
1.2.1 原理
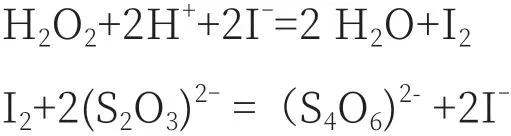
1.2.2 方法步骤
将分样所得样品,加蒸馏水溶解定容,吸取一定量于碘量瓶中,加入10%的硫酸10 mL,10%的碘化钾10 mL,立即加盖水封平摇混匀,暗处放置5~6 min,用0.1 mol/L硫代硫酸钠标准溶液滴定,近终点加入1%的淀粉溶液2 mL,滴定至蓝紫色消失为终点,记录滴定消耗硫代硫酸钠标准溶液的体积V。
1.2.3 结果计算
活性氧含量以质量分数X1表示,用式(1)计算:
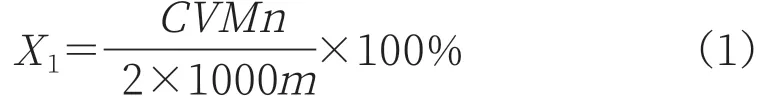
式中:
V—滴定消耗硫代硫酸钠标准溶液的体积,mL;
C—硫代硫酸钠标准溶液的浓度,mol/L;
m—称取试样的质量,g;
n—稀释倍数;
M—活性氧的摩尔质量,16.0 g/mol。
对6种市场样进行了测定,结果见表2。测定过程中发现,因洗碗块中含有一定量的增稠剂,生成的碘会和增稠剂凝聚,黏附在碘量瓶底部,所以在用硫代硫酸钠滴定至近终点时应充分振摇,防止凝聚,使反应完全。

表2 活性氧含量测定结果
1.3 碳酸钠含量的测定
1.3.1 原理
碳酸钠和盐酸反应生成二氧化碳,通过酸和碱二次滴定,可定量从第一等电点到碳酸氢钠完全反应生成二氧化碳所消耗的盐酸,从而计算出碳酸钠含量[4]。
1.3.2 方法步骤
准确称量分样后的样品,溶解并定容,移取一定量滤液至烧杯中,插入事先校正过的pH电极,用0.1 mol/L的盐酸调节溶液的pH=8.4,然后用0.1 mol/L的盐酸标准溶液滴定至pH 3.7~3.9,记录消耗的盐酸的体积V1,取出电极,将烧杯置于天平上称重并记录,然后再置于电炉上微沸5~7 min,以除去溶解的二氧化碳,冷却后,再置于天平上补充无二氧化碳的蒸馏水至上述重量,插入电极,用0.1 mol/L氢氧化钠标准溶液返滴定至pH=8.4,记入消耗的氢氧化钠的体积V2。
1.3.3 结果计算
碳酸盐含量以碳酸钠计,以质量分数X2表示,用式(2)计算:

式中:C1—盐酸标准溶液的浓度,mol/L;V1—耗用盐酸标准溶液的体积,mL;
C2—氢氧化钠标准溶液的浓度,mol/L;
V2—耗用氢氧化钠标准溶液的体积,mL;m—称取试样的质量,g;
n—稀释倍数;
M—碳酸钠的摩尔质量,106 g/mol。
为验证方法的准确性,在含有过碳酸钠样品中精确加入质量分数为39.35%碳酸钠,按上述方法测定其回收率,结果见表3。
经查阅资料[5-6],在GB/T 27404-2008 附录F(资料性附录)中,检测方法确认的技术要求见表4。

表4 附录F(资料性附录)检测方法确认的技术要求
本实验加标样品的量,换算成上述单位,应大于100 mg/kg,对应上表,回收率应达到90%~110%,本实验计算出的回收率在99.21%~101.27%之间,均满足此要求。
1.3.4 注意事项
a)用盐酸滴定时的测定终点设定为pH=3.7~3.9,确保碳酸氢钠全部转化生成二氧化碳。
b)补充蒸馏水是为消除因水分蒸发对pH的影响。
c)如样品中已含有过碳酸钠,样品中实际碳酸钠的质量分数X按式(3)计算。
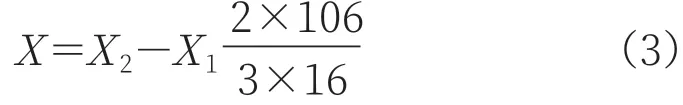
式中:
X2— 样品测定中总碳酸钠含量;X1— 活性氧含量;碳酸钠和活性氧摩尔质量之比。
1.4 硫酸钠含量的测定
1.4.1 原理

表3 碳酸钠含量测定结果和回收率
1.4.2 方法步骤
1.4.3 结果计算
样品中硫酸钠的质量分数X按式(4)计算:
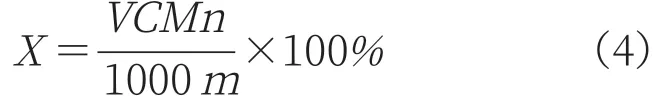
式中:
V—滴定消耗氯化钡标准溶液的体积,mL;
C—氯化钡标准溶液的浓度,mol/L;
M—硫酸钠的摩尔质量,g/mol;
n—稀释倍数;
软件功能模块主要包括数据获取模块和数据显示模块。其中,数据获取模块负责获取Bmob后端云数据库上更新的昆虫生境数据,数据显示模块负责将获取到的数据显示在昆虫生境移动监测软件的用户界面上。软件系统的功能模块设计见图2。
m—称样量,g。
对6种市场样中硫酸钠含量进行了测定,结果见表5。
测定过程中为消除干扰,在试样中加盐酸酸解,使碳酸盐分解成二氧化碳,硅酸盐生成不溶解的硅酸,过氧化物完全分解成氧气和二氧化碳,从而消除这些因素对测定的影响。经酸解后的上述样品的测定终点明确。
1.5 柠檬酸钠含量的测定
柠檬酸钠易生物降解,是环保型络合剂,有软化水质,预防水垢的作用,可使餐具表面无痕,大部分洗碗粉中均加入了一定量的柠檬酸钠。采用离子色谱法,测定了洗碗粉、洗碗块中的柠檬酸钠含量,结果见表6。
2 理化指标测定
2.1 pH的测定
洗碗机用洗涤剂的主要组成为各种碱性无机盐,在水中,各种碱性盐混合成的碱度对洗涤起乳化作用,但过高的碱性对洗碗机有一定的损伤,所以在洗碗粉配方中必须控制好产品的pH。一款好的产品不应该有过高的pH,但必须在洗涤过程中保持相对稳定的pH缓冲效应,而且在一定pH范围内有较强的活性碱。
建议机用洗碗粉中pH的测定分两个浓度,1%和1‰,以此来界定产品的缓冲体系。
在测定过程中,如分样后得到的样品量较大,先将分样得到的样品配制成10%的溶液,再稀至1﹪和1‰溶液,然后按GB/T 6368-2008标准对6种市场样进行测定,结果见表7。

表5 硫酸钠含量测定结果

表6 柠檬酸钠含量测定结果
2.2 游离碱含量测定
通过对洗碗粉(块)中游离碱的含量进行测定,并结合其pH,是评价产品内在质量的一个方面,在合理的pH范围内,缓冲效应越好,相对游离碱含量也就越高。游离碱含量的测定按GB/T 13171.1《洗衣粉(含磷型)》附录A测定。样品测定结果见表8。
通过对上述6种市场样的测定结果可知,5号样品其1%的pH不高,但其缓冲效应最好,碱的活性也最高,意味着在合理的pH条件下,其乳化洗涤作用发挥的最好。而6号样品pH最高,但其碱的活性却远小于5号样品。
2.3 钙螯合值测定
洗碗粉(块)中加入了螯合剂,能有效地抑制金属离子(如钙、镁离子)发生沉淀,使餐具更加光亮;其次,螯合剂除具有一定的分散能力,还能有效地抑制金属离子过早对过碳酸钠的催化分解。
2.3.1 原理
在pH为11的含碳酸钠的溶液中,螯合剂和钙离子螯合,当溶液出现混浊不消失时,定量样品的钙螯合值。
2.3.2 方法步骤
将分样得到的样品定容,吸取50 mL纯清滤液置于250 mL烧杯中,加入10 mL 20 g/L的碳酸钠溶液,插入校正好的pH计电极,滴加40 g/L氢氧化钠溶液至pH为11,加入四氟搅拌珠,在磁力搅拌下用0.1 mol/L的乙酸钙标准溶液滴定(滴定速度约为3 s/滴),边滴定边滴加氢氧化钠溶液,维持溶液的pH为11,滴定至溶液出现混浊且不消失为止,记录消耗的乙酸钙标准溶液体积。
2.3.3 结果计算
钙螯合值以mg/g计,用X表示,按式(5)计算:

式中:
C—乙酸钙标准溶液的浓度,mol/L;
V—滴定样品消耗乙酸钙标准溶液体积,mL;
M—碳酸钙摩尔质量,100.8 g/mol;
m—试样质量,g。
对6种市场样进行了测定,结果见表9。
2.4 氯离子含量的测定
在洗涤过程中,如果溶液中氯离子含量过高,会导致电化学反应速度加快,特别在加热的流动状态下,会加速洗碗机的金属表面孔蚀和应力腐蚀开裂的倾向,而在配制洗碗粉的原料中,会带入一定量的氯离子,也不排除加入低价的氯化钠作为填充剂。Cl-含量的测定如下。
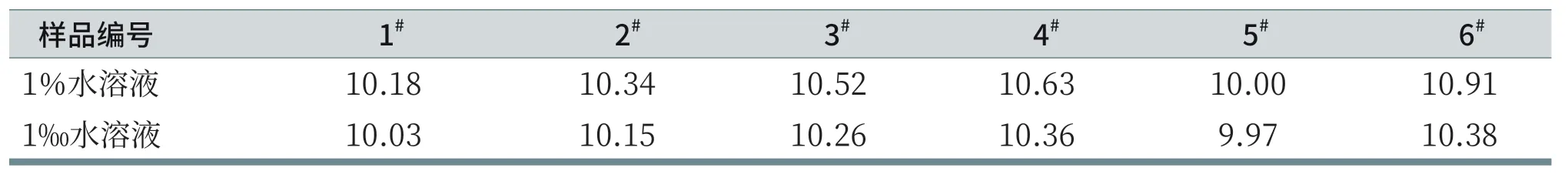
表7 pH测定结果

表8 活性碱测定结果
2.4.1 原理
在酸性条件下,Cl-和Ag+生成白色沉淀AgCl。
2.4.2 方法步骤
准确称量分样后的样品,溶解并定容,移取一定量滤液至烧杯中,调节溶液的pH为3.5~3.8,置于电炉上加热微沸5~6 min,冷却后加入5%铬酸钾溶液,用0.1 mol/L AgNO3标准溶液滴定至砖红色为终点,记录消耗硝酸银标准溶液的体积V。
2.4.3 结果计算
样品中的Cl-按氯化钠计,以质量分数X表示,按式(6)计算:

式中:
V—滴定消耗硝酸银标准溶液的体积,mL;
C—硝酸银标准溶液的浓度,mol/L;
M—氯化钠的摩尔质量,58.5 g/mol;
m—称样量,g;
n—稀释倍数。
2.4.4 方法讨论
在用AgNO3标准溶液测定洗碗粉中Cl-时,溶液中一般还含有大量的CO32-、SO42-,而Ksp(AgCl)=1.8×10-10,Ksp(Ag2CO3)=8.1×10-12,Ksp(Ag2SO4)=1.4×10-5,Ksp(Ag2CrO4)为1.1×10-12。根据Ksp可以计算出这些难溶盐中Ag+的浓度,其大小顺序是Ag2SO4>Ag2CO3>Ag2CrO4>AgCl,用铬酸钾作为指示剂,理论上CO32-、SO42-对测定无影响。考虑到Ag2CO3和Ag2CrO4两者的浓度积常数比较接近,而且当溶液中CO32-浓度过高时,Ag2CO3会先于Ag2CrO4产生沉淀,使终点无法判定。解决的方法是在测定过程中,提高指示剂铬酸钾的加入量。也就是说在测定过程中如发现终点无法确定时,在进行重新实验时增加指示剂的量,一般碳酸盐在30%左右时,指示剂铬酸钾的加入量为3 mL。
在高含量的碳酸钠、过碳酸钠、硫酸钠的溶液中定量加入氯化钠,实验过程中指示剂铬酸钾的加入量为3 mL,测定氯化钠回收率,结果见表10。
从测定结果看,适当增加铬酸钾的用量完全能克服高含量碳酸盐和硫酸盐对测定Cl-时的影响。
3 总结
洗碗机用洗涤剂作为现今洗涤剂行业的一员,正在不断发展和壮大,需要建立一个完善的检测方法系统,来确保产品的质量和性能,以此推动洗碗机用洗涤剂产品的良性发展,得到更多消费者的认可和 青睐。根据洗碗机用洗涤剂的要求、性能、组成和特点,建立和优化了相关的检测方法,并对各个测定方法中关键的切入点进行了说明论证,并以实验结果加以证实,来确保方法的准确性、有效性。

表9 螯合值测定结果
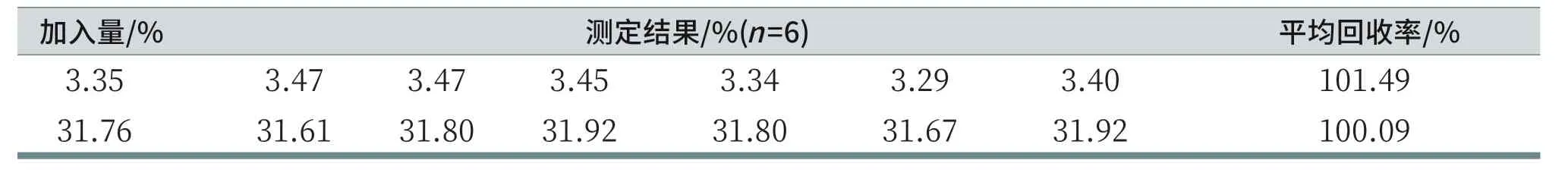
表10 在含有CO32-、SO42-溶液中氯化钠的回收率


