微波场下的钒渣氯化动力学
谭 博,王丽君,闫柏军,周国治
1) 北京科技大学钢铁共性技术协同创新中心,北京 100083 2) 北京科技大学钢铁冶金新技术国家重点实验室,北京 100083 3) 北京科技大学冶金与生态工程学院,北京 100083✉通信作者,E-mail:lijunwang@ustb.edu.cn
钒渣主要来源于钒钛磁铁矿冶炼工艺的含钒铁水吹炼过程,它含有钒、铬、锰、铁和钛五种有价元素. 目前,中国的钒渣产量已经达到了40万吨[1]. 钒渣主要以钒铁尖晶石、硅酸盐相和钛磁铁矿相以及金属铁互包裹复合形式存在,不同地域的钒渣物相有所差别[2−3],一般很难采用物理方法破坏其紧密共生的尖晶石−硅酸盐结构,实现有价元素富集.
钒渣提取的传统方法主要有钠化焙烧法、钙化焙烧法、亚熔盐法以及直接合金化[3−6],都对钒渣的有价元素提取和利用做出了有益的尝试. 钠化焙烧工艺一般是在钒渣中混合Na2SO4、Na2CO3等钠盐后焙烧,其中有价金属钒和铬被氧化为六价,再与钠盐结合为水溶性的钒酸盐,钠离子加快了尖晶石相的分解;钙化焙烧是将CaO、CaCO3与钒渣混合后焙烧,三价有价金属被氧化为六价,生成酸溶性的钒酸钙,钙离子的加入,减小了钠盐的消耗,降低了经济成本[3−6]. 直接合金化是直接将钒渣中的金属钒铁还原为合金,流程较短,但能耗较高,且未能实现钒渣中其他有价金属元素的综合利用.
最近,本课题组提出采用选择性氯化的方法[7−8],保持有价元素原有价态提取钒渣中Fe、Mn、Cr、V和Ti,并制备了高附加值材料[9−10]. 考虑到常规加热中存在AlCl3(180 ℃开始挥发)和氯化物的挥发性问题,在综合考察了钒渣物料的微波介电特性后,以及微波加热物料的快速升温,加速元素迁移等优势,本文引入微波外场来强化钒渣的氯化过程.
微波能是一种清洁能源,因为其快速加热、选择性加热、非热效应等优势[11−13],广泛应用于生物、化学、材料、冶金等领域. 基于以上优点,常利用微波进行强化磨矿、强化浸出、碳热还原、熔盐合成以及干燥等冶金过程[14−16]. 在微波场中,微波选择性加热不同吸波性能的矿物成分,会导致矿物热应力开裂[17],微波可以改善材料的表面性质,降低熔盐合成温度和缩短时间[18−19]. 微波焙烧可以改变钒渣的尖晶石结构,提高钒渣的反应性,降低钒的浸出温度敏感性[20]. 本研究在研究微波加热氯化钒渣的基础上,用非等温动力学的方法具体研究了微波加热提取钒渣有价金属的物相变化和强化机理.
1 实验材料和方法
1.1 实验材料
实验原料钒渣取自国内某钢厂,它的主要化学成分经X射线荧光光谱分析如表1所示. 经过破碎、研磨后,钒渣筛分成粒度大小为 < 0.075 mm粒级. X射线衍射分析表明,钒渣的主要物相包括铁硅橄榄石、锰硅橄榄石((Fe,Mn)2SiO4)、铁钒尖晶石((Mn,Fe)(V,Cr)2O4)和钛磁铁矿(Fe2.5Ti0.5O4),结果如图1所示.

表 1 钒渣的化学组成 (质量分数)Table 1 Chemical composition of the V-slag %
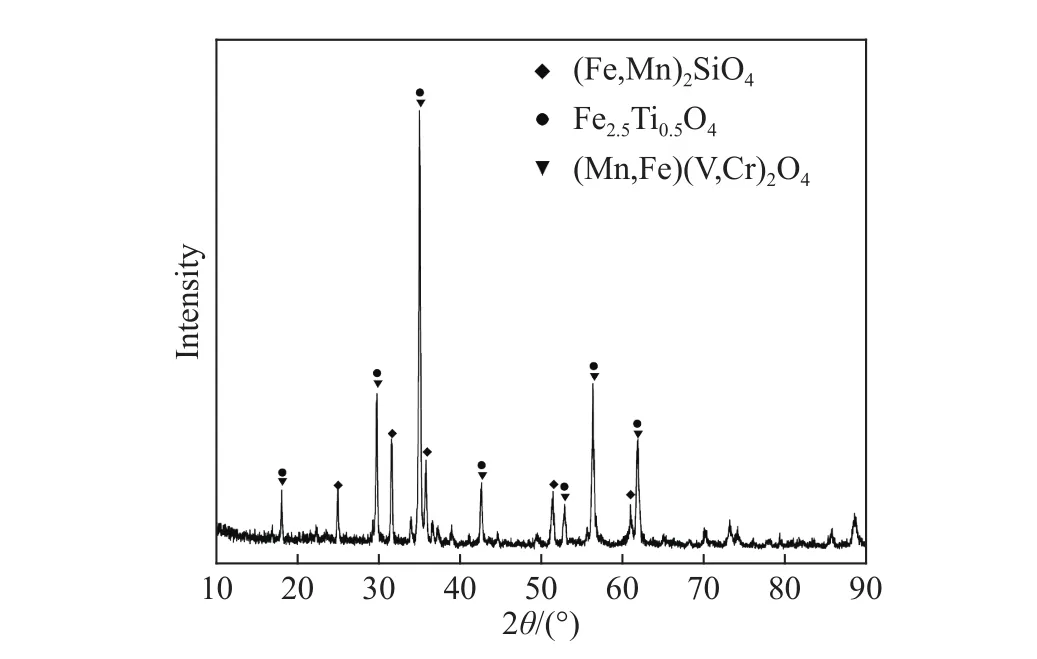
图1 原钒渣的 X 射线衍射图Fig.1 X-ray diffraction pattern of the original vanadium slag
分析纯的无水 AlCl3(99%),NaCl(99.5%),KCl(99.5%)购自中国医药集团公司,均在 105 ℃下干燥12 h后备用.
1.2 实验过程
实验采用竖式Mobilelab-T系列微波材料学工作站(唐山微波纳源有限公司),其结构示意图如图2所示. 工作站的工作频率为2.45 GHz,功率在0~4 kW可调. 坩埚材质采用微波透明材料—石英,尺寸为 ϕ50 mm×50 mm. 将在 105 ℃ 下干燥12 h 的 10 g 钒渣、25 g(NaCl-KCl)和 15 g AlCl3混合后,放入有开孔盖子密闭的石英坩埚,坩埚置于带有保温材料(保温材料不吸波)的微波加热腔中. 采用带有金属屏蔽罩的K型热电偶置于物料中间,连接设备测量温度. 微波功率设置为2 kW,实验过程中通入纯度为99.9%的氩气作为保护气体.
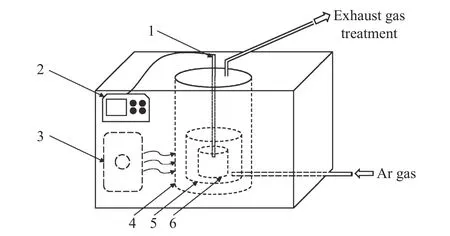
图2 Mobilelab-T 系列微波工作站结构图Fig.2 Microwave workstation structure of the Mobilelab-T series
根据方程(1)计算钒渣氯化产物中Fe、Mn、V和Cr的提取率:

式中:η(V, Cr, Mn, Fe)是钒渣中各元素(V、Cr、Mn 和Fe)的提取率;c(V, Cr, Mn, Fe)是通过 ICP-AES 测量的液相产物中有价金属离子(V、Cr、Mn和Fe)的质量浓度,mg·L−1;V是去离子水的体积,L;M(V, Cr, Mn, Fe)是钒渣中有价金属的初始质量,mg.
1.3 实验表征
通过 X 射线衍射分析(Rigaku TTRIII,Rigaku,Japan)氯化产物物相. 电感耦合等离子体原子发射光谱法(Varian715-ES,Varian,USA)分析氯化产物中Fe、Mn、V和Cr离子浓度. X射线荧光光谱分析(AxiosmAX,Axios,Netherlands)原钒渣各元素含量. 通过扫描电镜(Quanta250,FEI,Netherlands)分析氯化产物形貌.
2 实验结果和讨论
2.1 AlCl3 氯化可行性分析
从热力学角度考察氯化反应发生的可能性,三氯化铝可与钒渣中各物质反生如下反应


通过Factsage7.0软件计算400~800 ℃各氯化反应的吉布斯自由能,结果如图3所示. 在相同温度下,吉布斯自由能的大小为在 400~ 800 ℃,反应(2)~(9)的标准吉布斯自由能皆为负值,说明在热力学条件上反应均能发生,且橄榄石比尖晶石更容易发生氯化.

图3 方程(2)~(9)中标准吉布斯自由能随温度变化的曲线图(1 mol AlCl3标准化)Fig.3 Plots of standard Gibbs free energy as a function of temperature in Equations (2)-(9) (normalized by 1 mol AlCl3)
通过圆柱形谐振腔微扰法测试物料的介电性能,考察微波加热钒渣的可行性. 在常温下,粒径<0.075 mm钒渣的复介电常数ε可以表示为
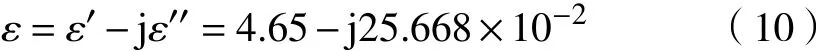
式中,ε′为复介电常数实部,ε′′为复介电常数虚部,反应物料吸波能力的介电损耗tanδ可以表示为
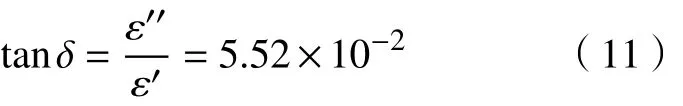
结果显示,在常温下,105 ℃干燥 12 h粒径<0.075 mm 的钒渣损耗角正切为 5.52×10−2. 通常冶金物料的介电损耗在0.01以上可以称为吸波物料,所以钒渣物料本身具有良好的吸波能力,可以在微波场中吸波实现快速升温.
2.2 NaCl–KCl熔盐配比选择
NaCl–KCl熔盐可以与AlCl3形成三元系熔盐,相图如图4所示. 三元系熔盐可以稳定180 ℃开始挥发的AlCl3,提高参与氯化反应的氯化剂含量,且生成的氯化产物可以在熔盐介质中溶解. 在本项工作中,AlCl3/钒渣质量比为1.5,微波加热至600和900 ℃保温 30 min,研究不同熔盐配比对有价金属提取率的影响. (NaCl-KCl)/AlCl3熔盐质量比分别设置为0.61∶1(A点)、1.11∶1(B点)、1.66∶1(C点).

图4 AlCl3–KCl–NaCl三元相图Fig.4 AlCl3–KCl–NaCl phase diagram
表2为有价金属Fe、Mn、V和Cr的提取率,结果表明Fe和Mn的提取率高于V和Cr,在高温度下的有价金属提取率高于低温度,这可能与钒渣中尖晶石相和橄榄石相的反应顺序有关. 600 ℃时,橄榄石相先于尖晶石相反生反应,较低的反应温度不利于尖晶石的氯化;在A、B点的的V、Cr提取率低于C点,表明低熔点的熔盐配比不利于有价金属的氯化.

表 2 不同熔盐配比的有价金属提取率Table 2 Valuable metal extraction rate of different molten salt ratios
2.3 AlCl3/钒渣质量比对提取率的影响
微波加热至 800 ℃ 保温 30 min,在 AlCl3/(NaCl–KCl)质量比为1.66,研究AlCl3/钒渣对有价金属提取率的影响. 采用反应(2)~(6)计算恰好完全反应的AlCl3质量为钒渣的1.17倍,考虑三氯化铝的挥发,AlCl3与钒渣的质量比设置为1.2、1.3、1.4、1.5和2.0,氯化产物的提取率采用电感耦合等离子体原子发射光谱法测量结果如图5所示.

图5 AlCl3/钒渣质量比对有价金属氯化的影响Fig.5 Effect of mass ratio of AlCl3/vanadium slag on chlorination of valuable metals
结果表明,随着AlCl3/钒渣质量比的升高,有价金属的提取率呈先升高后降低的趋势. 在AlCl3/钒渣质量比为1.5时,有价金属的提取率达到最佳,Fe、Mn、V和Cr的提取率分别为91.66%、92.96%、82.67%和75.82%. 随着AlCl3/钒渣的质量比增加至2.0,提取率开始降低. 提取率降低的原因可能是过量AlCl3不能在熔盐中固定,导致了氯化物的大量挥发. 在本项工作中,三氯化铝的挥发是影响氯化的主要原因,AlCl3与钒渣质量的最佳配比为1.5.
2.4 微波加热氯化钒渣的变温动力学
微波加热具有即时加热的特点,样品不能在恒定温度放入微波加热腔内. 本研究采用变温动力学方法研究了微波与熔盐氯化钒渣中有价金属的氯化动力学过程. 对不同氯化时间(350~650 s)的产物水洗后进行物相分析. 不同氯化时间产物的X射线衍射图如图6所示,图7为氯化产物的扫描电镜图.
样品温度逐渐升高,350 s样品温度升至507.9 ℃,图6(a)显示氯化产物中存在反式尖晶石相,电感耦合等离子体原子发射光谱法测量结果(表3)显示V和Cr的提取率分别为2.3%和1.9%,图7(a)能谱图显示尖晶石相和橄榄石相还呈互相包裹的形态,Al、Si和O并未覆盖在有价元素V、Cr和Ti的表面,较低的提取率表明尖晶石相没有大量发生氯化反应,出现反式尖晶石相的原因可能是氯化产物在较低温度取出过程中被氧化[21];同时,Fe和Mn的提取率都达到45%以上,表明橄榄石相更容易发生氯化反应. 500 s样品温度升至686.3 ℃,图 6(b)中尖晶石峰相强度继续降低,表明尖晶石相继续反应,且Al−Si−O复合物峰相强度增加,Fe和Mn提取率也达到73.4%和68.1%,图7(b)能谱显示V、Cr和Ti元素均存在,Fe、Mn 和Ca元素也分布在尖晶石表面,尖晶石和橄榄石两相互相包裹的现象消失. 650 s样品温度升至 795.6 ℃,图 6(c)显示尖晶石相的峰位消失,但图 7(c)能谱显示还有尖晶石物相的组成元素,可能是由于Al−Si−O复合物对有价元素的包裹,X射线衍射图并没有显示出尖晶石相峰位. 因此,尖晶石相中的V和Cr需要更长的反应时间实现提取. 不同氯化时间下有价金属提取率如表3所示,升温过程T/t关系曲线如图8所示.

图6 不同氯化时间下氯化产物的 X 射线衍射图. (a) 350 s;(b) 500 s;(c) 650 s;(d) 原钒渣Fig.6 X-ray diffraction patterns of products with different chlorination time: (a) 350 s; (b) 500 s; (c) 650 s; (d) original vanadium slag
熔盐氯化钒渣过程可以用液固未反应收缩核模型来描述[2,9]. 在本实验条件下,确保了熔盐中AlCl3是过量的,考虑到熔盐中计算AlCl3浓度比较复杂,所以用质量分数代替浓度. 通过表3元素提取率和反应方程(2)~(9)计算AlCl3的消耗量约为3.4 g,AlCl3的初始质量分数为37.5%,而动力学研究终点AlCl3的质量分数为31.6%,在反应过程中采用AlCl3浓度近似不变方法处理动力学方程. 如果扩散为氯化钒渣过程的控速步骤,对于不可逆反应,颗粒物表面的质量分数cs=cs′≈0(cs′为反应剂反应界面的质量分数),反应物在边界层的传质速率等于未反应核界面消耗物的速率,非等温过程传质系数可以由公式Arrhenius表示,动力学方程可以表示为

式中,T为绝对温度,x为有价金属的提取率,ρ为钒渣的密度,β为样品加热速率,r0为钒渣颗粒半径,ΔE1为液相边界层的扩散活化能,为与材料本身性质有关的扩散系数,M为钒渣的摩尔质量,R为气体常数,b为AlCl3系数,c0为AlCl3初始质量分数.
如果内扩散为氯化钒渣过程的控速步骤,cs=c0,对于不可逆反应,cs′≈0,固体消耗速率与反应物扩散通量成正比,非等温过程传质系数可以由公式Arrhenius表示,内扩散控制的非等温动力学可以描述为
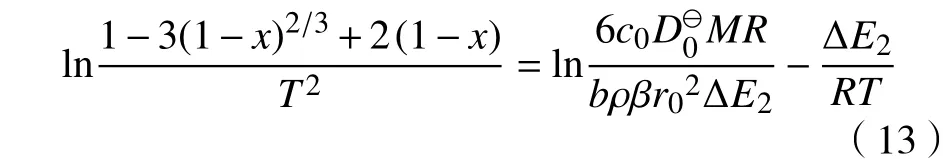
式中,ΔE2是固体产物层的扩散活化能.
如果氯化钒渣过程控速步骤为界面化学反应,可用方程(14)表示[22−23]:

式中,Ea是有价金属的表观活化能,A是指前因子.
将V、Cr、Mn和Fe在800 ℃下的氯化数据拟合,结果如表 4 所示. 对于 Fe、Mn,方程(13)表现出更高的先关系数值,表明速控环节为扩散步骤;对于V、Cr,方程(14)表现出更高的相关系数值,在外扩散环节时,AlCl3浓度较高不会成为控制环节,但内扩散环节相关系数同样较高,表明对于V、Cr可能是化学反应与内扩散环节共同控制,这与钒渣中橄榄石相与尖晶石相先后反应机制吻合.

图7 微波加热不同时间氯化产物的扫描电镜‒能谱图. (a) 350 s;(b) 500 s;(c) 650 sFig.7 SEM-EDS morphologies of products by microwave heating for differnet time: (a) 350 s; (b) 500 s; (c) 650 s

表 3 微波加热不同时间氯化产物中有价金属的提取率Table 3 Chlorination rate of valuable metals in samples by microwave heating for various time

图8 样品升温过程温度/时间关系Fig.8 T/t relationship of sample heating process
微波加热过程中,高效氯化钒渣的机理可以解释如下:(ⅰ)增强扩散作用. 在微波加热和常规加热过程中,Fe和Mn的速率控制步骤都为扩散步骤控制,微波加热并没有实质改变氯化过程的速控步骤,微波交变电场和磁场在分子水平上直
接与钒渣作用,并和熔盐介质发生耦合,增强了离子的扩散. (ⅱ)局部高温效应. 钒渣中的V和Fe作为良好的微波吸收材料成分可以在微波选择性加热特点下吸波升温[20]. 在微波加热熔盐氯化钒渣过程中,可以观察到火花或电弧现象. 这些火花或电弧可以被视为微观水平的微等离子体[24],微波等离子体可能导致局部高温促进有价金属的氯化[25].

图9 (b)与 1/T 的关系Fig.9 Relationship between (b) with 1/T

表 4 动力学方程的相关系数Table 4 Correlation coefficient of the kinetic equation
3 结论
(1)微波加热在 800 ℃ 保温 30 min 条件下,(NaCl‒KCl)/AlCl3熔盐质量比 1.66∶1,AlCl3与钒渣质量比为1.5,Fe、Mn、V和Cr的提取率分别为91.66%、92.96%、82.67%和75.82%. 与常规加热相比,微波加热可以缩短熔盐氯化的时间,减小AlCl3和样品的挥发.
(2)钒渣中的橄榄石相优先于尖晶石相发生反应,V和Cr对时间的敏感性高于Fe和Mn,延长氯化时间,有利于V和Cr的氯化.
(3)微波与熔盐氯化钒渣非等温动力学过程,V和Cr的限制性环节为化学反应环节,Fe和Mn为扩散环节. 采用方程描述V和Cr的氯化反应,V和Cr的表观活化能分别为 40.00 和 50.92 kJ·mol−1,采用 方程描述Fe和Mn的氯化反应,Fe和Mn非等温动力学扩散活化能为 17.02 和 17.10 kJ·mol−1.

