万古霉素人工抗原的制备及鉴定
李玉静,刘鹏茹,刘静静,李春生
(1.河北交通职业技术学院,河北 石家庄 050035;2.河北省科学院生物研究所,河北 石家庄 050081)
万古霉素分子量1485.72,是一种糖肽类抗生素,可用于多种耐药性葡萄球菌如耐甲氧西林金黄色葡萄球菌引发的感染,如脑膜炎、感染性心内膜炎、骨髓炎、肺炎、关节炎等,及手术、创伤引起的继发感染[1,2]。万古霉素对多重耐药G+菌敏感性高,但其副作用也比较明显,如耳肾毒性、红人综合征等[3,4]。有研究结果显示,万古霉素耳肾毒性的发生与其血药浓度有关,当达到20μg/mL以上时,出现不良反应的概率升高[5,6]。万古霉素的给药剂量与血药浓度,在肾功能正常的成年人中存在良好的线性关系,但在儿科群体中还不能肯定[7,8]。因其安全浓度范围窄、个体用药差别大、且有副作用,在使用万古霉素治疗时,有必要进行血药浓度监测(TDM)[1,9],以提高治疗效果并减少不良反应。
万古霉素血药浓度的测定,目前多采用色谱法和免疫学方法[10,11]。液质联用(HPLC-MS/MS)检测限低、结果可靠,但是其操作繁琐、耗时长[12]。免疫学方法主要是化学发光微粒子免疫检测法(CMIA),具有特异性好、操作简单等特点,适于快速检测[13]。本研究合成了万古霉素的人工抗原并进行鉴定,为万古霉素的免疫学方法研究制备了原料。
1 材料与方法
1.1 主要试剂
万古霉素(vancomycin,VCM),中国食品药品检定研究院;弗氏完全佐剂,弗氏不完全佐剂,牛血清白蛋白(BSA),鸡卵清白蛋白(OVA),三羟甲基氨基甲烷(Tris) ,丙烯酰胺(Acr) ,亚甲基双丙烯酰胺(Bis),均购自Sigma;辣根过氧化物酶标记山羊抗小鼠IgG(二抗),北京中杉金桥;四甲基乙二胺(TEMED),美国BBI公司;其他试剂均为国产分析纯。
1.2 主要仪器
移液器,ND2000超微量核酸蛋白测定仪,德国Thermo;酶标仪,美国Bio-TEK;90-2型磁力搅拌器,上海浦江分析仪器厂;微量震荡器,金业仪器有限公司。
1.3 实验方法
1.3.1 万古霉素半抗原的制备
称取万古霉素25 mg、琥珀酸酐20 mg,用二甲基亚砜0.6 mL 溶解,加入吡啶0.2 mL,80℃搅拌反应4h,37℃烘干,固体为半抗原。
1.3.2 免疫原的制备
取20 mg半抗原,溶于2 mL N,N-二甲基甲酰胺中,取碳二亚胺和N-羟基琥珀酰亚胺各30 mg,用0.2 mL 0.01 M的PBS溶解后加入半抗原溶液中,室温搅拌24h,得到反应液Ⅰ。称取牛血清白蛋白50 mg,溶解在3 mL 0.01M的PBS中,然后滴加入反应液Ⅰ中,室温搅拌24h,用0.01 M的PBS 4℃透析3d,分装,-20℃保存。得到免疫原VCM-BSA。
1.3.3 包被原的制备
用卵清白蛋白40mg代替牛血清白蛋白,其他步骤同1.2.2。得到包被原VCM-OVA。
1.3.4 人工抗原的鉴定
(1)紫外分光光度法鉴定。用PBS稀释VCM、VCM-BSA、BSA至相同浓度,进行紫外全波长(220~700 nm)扫描,计算BSA与万古霉素的分子偶联比[14]。
(2)SDS-PAGE鉴定。按照常规SDS-PAGE方法,配制12%分离胶,5%浓缩胶,电压30V至蛋白条带进入分离胶后,调节电压90V继续电泳约2h。经染色、脱色处理后拍照。
(3)动物免疫。取3只5周龄的Balb/c小鼠,背部皮下多点注射,免疫剂量VCM-BSA 40μg/只,每隔2周免疫一次,共4次。4次免疫后7-10天断尾取血,分别检测小鼠血清抗体效价和抑制率。
(4)血清效价测定。采用间接ELISA法,具体步骤如下:VCM-OVA浓度为2μg/ml,100μl/孔,4℃包被过夜;洗涤、拍干,加200 μl/孔封闭液(小牛血清:洗涤液=1∶9),37℃放置1h;洗涤、拍干,待测血清以1∶200、1∶400、1∶800…倍比稀释,100 μL/孔,设置洗液为空白对照、阴性血清为阴性孔,37℃反应45 min;洗涤、拍干,加入100μl/孔的1∶10000稀释的二抗,37℃反应30min;洗涤,拍干,加显色液37℃显色10 min,终止反应。测定A450nm值。阴性对照孔A450nm值为N,阳性为P,以P/N≧2.1时为抗体效价。
(5)血清敏感性测定结果。采用间接ELISA法测定,步骤同1.3.4中(4),加待测血清改为加待测血清和标准品:将标准品稀释成50 μg/L、25 μg/L、12.5 μg/L、6.25 μg/L、3.125 μg/L, 50 μl/孔,再加入稀释的阳性血清50 μl,50 μl阴性血清+50 μl PBS作为阴性对照,37℃放置45 min。
2 结果分析
2.1 合成抗原蛋白浓度的测定结果
合成的抗原用超微量核酸蛋白测定仪测定,浓度分别为VCM-BSA为4.4 mg/mL,VCM-OVA为12 mg/mL。
2.2 紫外光谱扫描结果
紫外扫描结果显示,BSA的特征吸收峰在278 nm处,VCM的特征吸收峰在282 nm处,二者合成产物的吸收峰在278~280 nm之间,且峰形与BSA更接近。因此可初步判定免疫原VCM-BSA合成成功。
2.3 SDS-PAGE 鉴定结果
由图2可以看出,偶联产物与BSA有明显差别,带宽且有拖尾,初步判定VCM-BSA偶联成功。
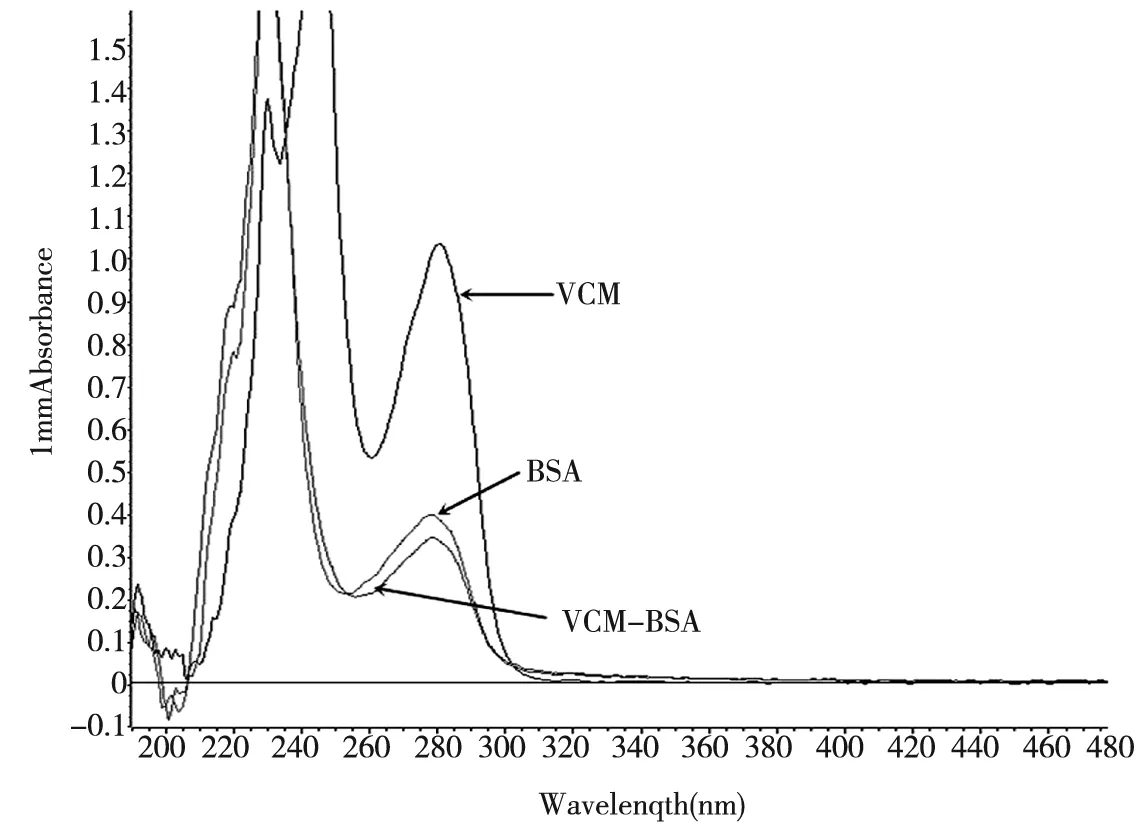
图1 VCM-BSA紫外扫描图谱

1.蛋白marker;2.BSA;3.VCM-BSA图2 VCM-BSA 凝胶电泳结果
2.4 小鼠抗血清效价测定结果
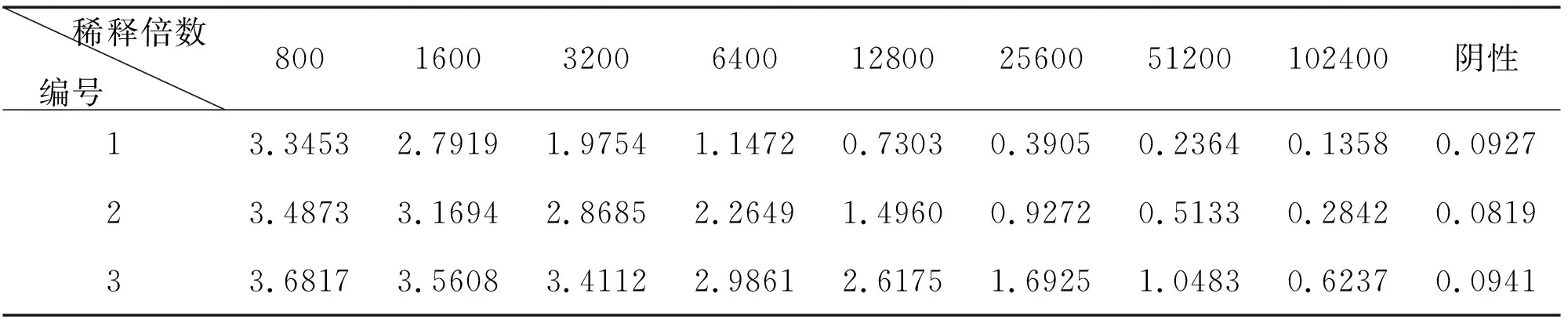
表1 间接ELISA测定小鼠血清效价
表1为第4次免疫后7d小鼠的血清效价。由表1可知,1号小鼠效价为1∶51200,2号和3号小鼠血清效价较高,均在1∶102400以上,可以判定抗原偶联成功。
2.5 小鼠抗血清敏感性测定结果

图3 小鼠血清敏感性测定结果
用竞争ELISA测定。以B/B0(B代表标准品A450nm,B0代表阴性对照A450nm)为纵坐标,以各标准品的浓度的对数值为横坐标,绘制标准曲线,并计算半数抑制质量浓度(IC50),IC50值越低则敏感性越好。图3所示为免疫小鼠血清敏感性结果,各小鼠的IC50值均在20μg/L以下,血清敏感性较好。
3 总结
本研究先将万古霉素与琥珀酸酐反应得到半抗原,再用碳二亚胺法将半抗原与载体蛋白偶联制备包被原和免疫原,再分别经紫外扫描法、SDS-PAGE电泳和免疫学方法对两种抗原进行检测,结果显示人工抗原的紫外吸收峰位移、及分子量发生变化,从化学结构的变化初步判定抗原合成成功。免疫小鼠血清检测结果显示效价高、敏感性好,从抗原抗体的特异性反应判定抗原合成成功。本研究成功制备了万古霉素人工抗原,免疫了实验动物,可以用于后续制备单克隆抗体,作为免疫学检测方法研究的实验原料。

