个体化泪点成形术治疗获得性泪点狭窄
张俊鸽 明帅 周钟强 祝磊 庆惠玲 王莉红 柳晓辉
泪点狭窄是眼科常见且易被忽视的泪器疾病,是导致溢泪的常见因素之一。泪点狭窄可分为先天性和获得性,获得性泪点狭窄的发生与许多因素有关,如感染、炎症、全身性疾病、药物、年龄等[1]。目前,临床常用治疗泪点狭窄的方法有传统剪式(一至四剪式)泪点切开术[2-6]、泪点扩张[2]、360°泪点切除术[7]、使用小梁咬切器的泪点成形术[8-10];为预防术后泪点再次狭窄而置入不同支撑材料,如带孔的泪点塞[11-12]、微型单管支撑管[2-3]、双泪小管支撑管[5,11]等,以及抗代谢药物丝裂霉素C的应用[10-12]等。传统的剪式,尤其是四剪式,是相对成熟的获得性泪点狭窄的治疗术式,可以取得较好的功能成功率。但近年来更多术者开始关注手术的解剖成功率,即重视泪点在维持泪道系统泵正常功能的重要性,希望以更微创的手术方式治疗泪点狭窄[8,13]。
裂隙灯显微镜下检查发现,与正常泪点相比,狭窄的泪点在大小和形状上有明显差异。因泪点狭窄的类型有其自身特点,传统的四剪式治疗不同类型的泪点狭窄其效果可能并不完全理想。我们根据泪点狭窄的不同形态,采用个体化泪点成形术治疗,取得较好疗效,现报告如下。
1 资料与方法
1.1 一般资料选取2013年1月至2018年6月在我院诊断为获得性泪点狭窄并行泪点切开成形术的患者纳入研究。纳入标准:(1)患者主要症状为持续性溢泪;(2)裂隙灯显微镜下检查确诊为单纯泪点狭窄,即泪点小于正常,被增生膜或纤维化覆盖,或仅见泪点痕迹甚至完全闭锁消失;(3)荧光素清除试验提示泪液清除延迟,但泪点扩张后,泪道冲洗通畅;(4)行两次泪点扩张治疗后,泪点狭窄无改善,溢泪症状不减轻;(5)患者依从性好,能够配合治疗和随访,术后随访时间至少6个月。
排除标准:(1)先天性无泪点者;(2)泪点或眼睑位置异常及泪阜肥大者;(3)泪点或其周围长有肿物;(4)泪道冲洗检查显示泪小管、泪总管、泪囊、鼻泪管狭窄或阻塞;(5)未治愈的结膜炎、睑缘炎,或因倒睫、角膜炎症等刺激因素导致的流泪;(6)术前泪液分泌试验异常及睑板腺功能障碍者;(7)合并鼻腔病变者,如鼻窦炎及鼻腔占位性病变等;(8)眼轮匝肌松弛导致的功能性溢泪。本研究严格遵守赫尔辛基宣言,所有患者均知情同意,并签署知情同意书。
1.2 方法
1.2.1 观察指标将溢泪情况、泪点大小、泪液排出功能作为主要观察指标,参照Ozgur等[11]的分级标准分别对其详细分级,具体见表1。根据术后溢泪和泪点分级,以术后解剖成功率和功能成功率作为评价指标。解剖成功率:泪点大小分级为3级,即正常大小。功能成功率:溢泪分级为0级或1级,即无溢泪或偶在室外迎风时溢泪。泪液排出功能评价采用荧光素清除试验:将20 g·L-1的荧光素滴入结膜囊内,3 min后开始观察,若染料在结膜囊内完全消失而出现在鼻腔,说明泪道通畅,排出功能良好;若5 min后染料仍停留在结膜囊内不出现在鼻腔,说明泪道阻塞。

表1 获得性泪点狭窄患者观察指标及分级
1.2.2 分组及手术方法根据手术方式不同分组,试验组参照Hur等[5]对泪点狭窄类型的描述,根据泪点狭窄的不同形态采用个体化泪点成形术;对照组参照Kim等[6]的方法行传统的四剪式泪点切开成形术。所有患眼均使用表面麻醉及筛前神经、眶下神经阻滞麻醉,由同一位眼科泪器病专业医师在高倍手术显微镜下完成手术。
试验组:(1)膜状/裂隙状泪点行环形泪点切开并置管:泪点严重被增生膜覆盖,无法看到泪点轮廓,呈闭锁状态(图1A),或增生膜从泪点结膜面和睑缘面长入,开口呈裂隙状(图1B),则环形切除泪点增生部分并置管。具体步骤为:泪点扩大器扩张狭窄的泪点,用显微有齿镊夹取泪点增生膜边缘,用显微剪(小梁剪)环形剪除增生膜,并留取组织行HE染色。剪除增生膜时沿泪点边缘弧形剪取,边界不超过泪点周围结缔组织环,深度不超过泪小管垂直部管壁黏膜,保持泪点形状呈圆形或类圆形并处在正常位置。泪点切开成形后,通过带记忆针芯的泪道探针,从上下泪点置入外径0.8 mm环形硅胶管,将硅胶管两端打结留置于下鼻道内。(2)马蹄状泪点行泪点增生膜切除:增生膜从泪点结膜面长入、覆盖泪点,带蒂,呈舌状或圆盖状(图1C),其头部与泪点边缘留有间隙,呈游离状。手术步骤为:用显微小梁镊夹取增生膜的游离缘,显微小梁剪弧形剪除基底部,同样边界不超过泪点周围结缔组织透明环,保持泪点形状呈圆形或类圆形,并留取组织行HE染色。泪点成形后,用Fox980泪道激光,使光纤露出探针0.5~1.0 mm,将激光能量调小,对出血点进行间断发射1~2次,凝固止血,无需置管。(3)针尖状泪点行泪点扩张并置管:泪点口与纤维组织收缩并出现点状开口,泪点扩张器扩张狭窄的泪点后直接置入外径0.8 mm环形硅胶管。
对照组:所有形状狭窄的泪点均行四剪式切开,具体步骤为:扩张器扩张狭窄的泪点后,使用显微剪做第一个垂直切口剪到泪小管壶腹(垂直睑缘向结膜面方向剪开);沿泪小管顶部水平(平行睑缘方向)切开长约2 mm,再从第二个切口的止端边缘进行第三个垂直切口(垂直睑缘向结膜面方向剪开),以创建一个皮瓣,最后剪除皮瓣底部,并留取组织行HE染色。

图1 不同泪点形态A:上泪点被增生膜完全覆盖;B:增生膜从结膜面长入下泪点,开口呈裂隙状;C:马蹄状下泪点,增生膜基底窄
1.2.3 术后处理及随访术后常规用抗生素眼液滴眼,分别于术后1个月、3个月、6个月复查,有置管的患者3个月后常规取管。术后定期检查患者视力、眼压及眼前节情况,如出现并发症及时处理。每次随访均询问患者术后溢泪情况,记录裂隙灯显微镜下观察到的泪点形态、位置及周围组织情况,对置入硅胶管的耐受情况,泪液排出功能检查结果等。
1.3 统计学方法应用SPSS 19.0统计学软件进行统计学处理和分析,连续变量采用均数±标准差表示,分类变量采用频数及构成比(%)表示。术前与术后不同时间点观察指标的比较采用配对Wilcoxon秩和U检验;两组术后不同时点观察指标的比较,采用两独立样本Wilcoxon秩和检验;两组术后不同时间点解剖成功率、功能成功率的比较采用卡方检验,必要时进行连续性校正。检验水准:α=0.05。
2 结果
2.1 术前基线资料试验组共纳入48例57眼患者,其中女30例(62.5%),男18例(37.5%);年龄(50.5±13.2)岁,以膜状/裂隙状泪点为主(38眼,66.7%)。对照组共纳入30例33眼患者,其中女20例(66.7%),男10例(33.3%);年龄(50.9±11.9)岁,以膜状/裂隙状泪点为主(19眼,57.6%)。两组患者间年龄、性别构成比差异均无统计学意义(均为P>0.05)。两组患眼溢泪病史为0.5~10.0 a,两组患眼间溢泪情况分级、荧光素清除试验分级、泪点大小分级及各形状泪点眼的构成等基线资料差异均无统计学意义(均为P>0.05)(见表2)。
2.2 两组功能成功率试验组和对照组术后1个月、3个月、6个月时均无3级溢泪,0级和1级溢泪比例均较术前明显提高,溢泪分级构成均较术前明显好转(均为P<0.001);术后1个月、3个月、6个月,试验组与对照组间溢泪分级构成差异均有统计学意义(均为P<0.01)(见表3)。术后1个月、3个月、6个月,试验组的功能成功率(0级和1级溢泪的比例)逐渐增长,分别为93.0%、96.5%和98.2%,对照组则呈增长后略有下降趋势,分别为75.8%、90.9%和 87.9%,两组功能成功率仅在术后1个月时差异有统计学意义(P=0.046)。
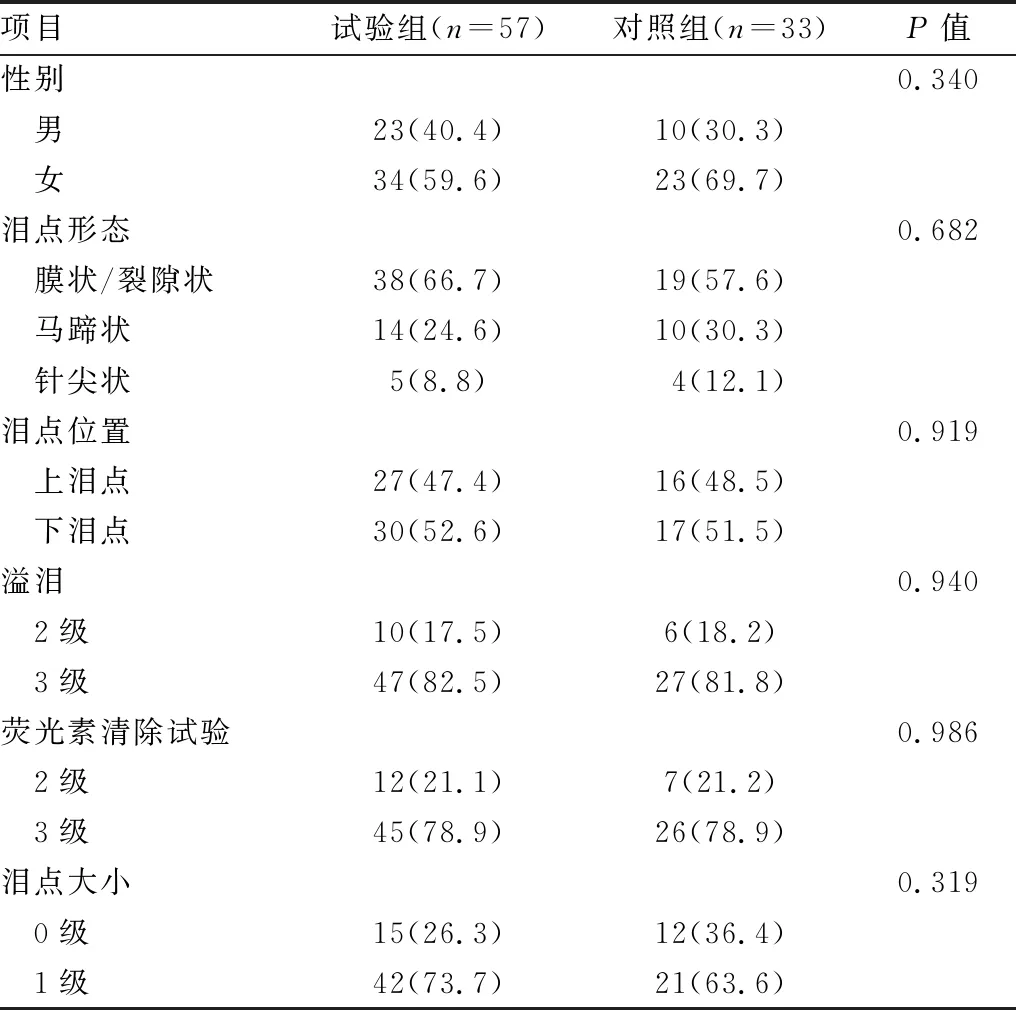
表2 两组患者术前基线资料(眼/%)
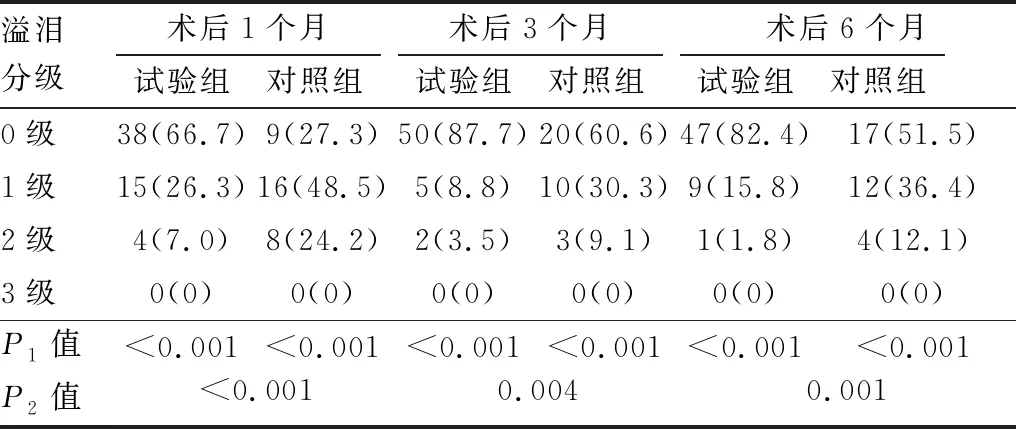
表3 两组术后不同时间点溢泪分级(眼/%)
2.3 两组荧光素清除试验结果术后1个月、3个月、6个月,两组荧光素清除试验分级构成均较术前有所改善(均为P<0.001),且两组间荧光素清除试验分级构成差异均有统计学意义(均为P<0.05)。术后1个月、3个月、6个月,试验组荧光素清除试验1级的比例分别为56.1%、87.7%和 86.0%,高于对照组的39.4%、66.7%和63.6%,差异均有统计学意义(P=0.038、0.013、0.009)(见表4)。
2.4 两组解剖成功率术后1个月、3个月、6个月,两组泪点大小分级的构成均较术前改善(均为P<0.001),且术后1个月、3个月,两组间泪点大小分级构成差异均有统计学意义(均为P<0.05)。试验组术后1个月时解剖成功率达到100.0%,高于对照组的51.5%(P<0.001);试验组术后3个月时解剖成功率有所下降,为89.5%,但仍然高于对照组的72.7%(P=0.040);术后6个月时两组解剖成功率相比差异无统计意义(P=0.075)(见表5)。试验组患眼术后3个月时,置管取出前、后及未置管泪点的解剖形态见图2。
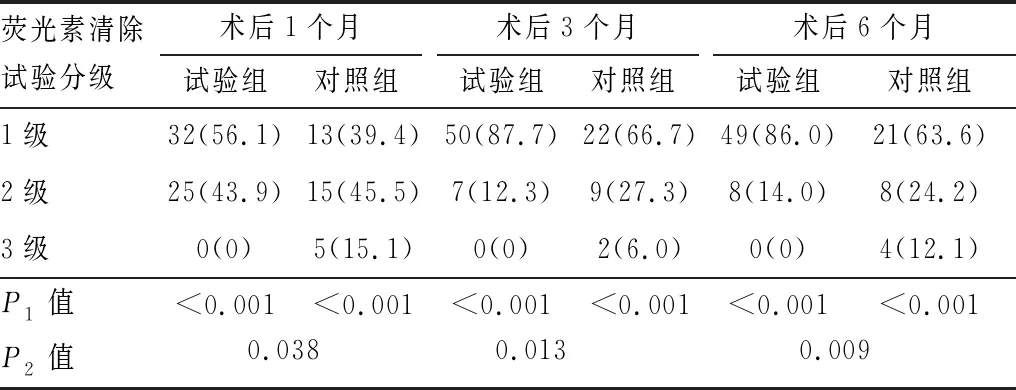
表4 两组术后不同时间荧光素清除试验分级(眼/%)
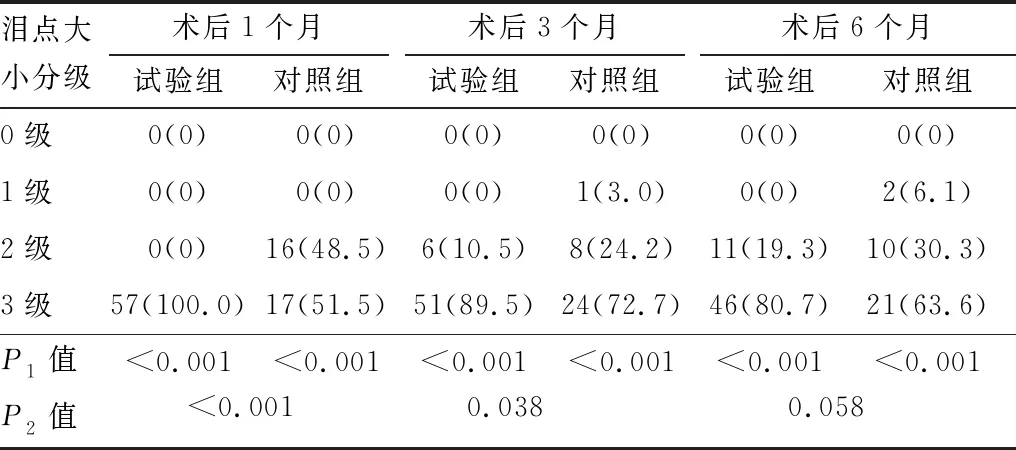
表5 两组术后不同时间泪点大小分级(眼/%)
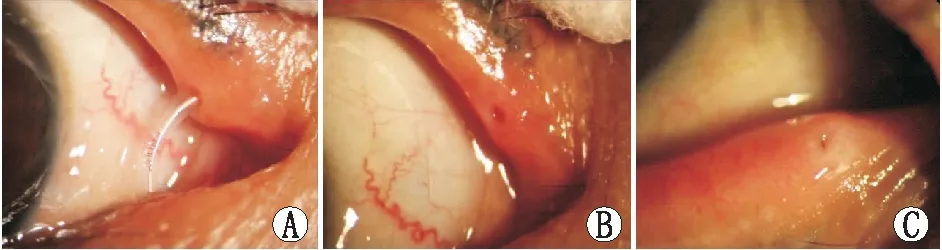
图2 试验组患眼术后3个月典型图像A:图1A患眼术后3个月对置管耐受好;B:图1A患眼术后3个月取管后,泪点正常(3级);C:图1C患者未置管,术后泪点正常(3级)
2.5 HE染色结果试验组HE染色结果显示,泪点的胶原纤维结缔组织内可见毛细血管充血,鳞状上皮细胞增生,其间可见杯状细胞和少量淋巴细胞浸润。对照组HE染色结果显示,泪点的胶原纤维结缔组织内可见毛细血管增生,成纤维细胞增生,其间可见肌纤维组织及淋巴细胞和中性粒细胞浸润。
3 讨论
个体间泪点正常解剖结构差异较大,直径为0.2~0.5 mm[1,14]。当患者有溢泪症状,且裂隙灯下检查泪点直径小于0.2 mm时,即可诊断为泪点狭窄[1]。与正常泪点相比,狭窄泪点的形态有明显差异,Hur等[5]将裂隙灯下的泪点狭窄分为四种类型:膜状、裂隙状、马蹄状和针尖状;对标本的病理学分析发现,不同狭窄类型有其自身的组织病理学特征。张敬先等[15]提出,结合泪点解剖形态改变的不同特征,对临床诊断分类和分型,有利于指导临床设计适合的泪点成形术,进行个体化治疗。
本研究中,试验组行个体化泪点成形术后患者泪点形状、泪液排出功能、溢泪症状均得到明显改善,与传统的四剪式泪点成形术相比,在术后1个月同时获得了更好的功能和解剖成功率。在术后3个月及6个月时,两组虽然功能成功率差异没有统计学意义,但个体化泪点成形术后解剖成功率总体高于四剪式。以上结果表明,个体化泪点成形术在改善泪点狭窄患眼泪液排出和溢泪症状的同时,可维持患者泪点的生理结构,且见效速度更快。
膜状泪点的泪点处覆着带血管的黏膜组织和结膜化生,周围有黏膜下结缔组织和少量肌纤维,而裂隙状和马蹄状泪点均未见明显的结膜化生或肌纤维[5]。个体化泪点成形术将膜状闭锁的泪点或有较宽基底增生膜的泪点(裂隙状)采用环形切除泪点增生部分并置入硅胶管,而对增生膜基底部较窄的马蹄状泪点,则直接从基底部剪除增生膜且不置管。针尖状泪点是纤维组织收缩形成,周围显示出高密度的肌肉纤维(即Riolan肌)[5,14,16],因此,个体化泪点成形术中仅在扩张泪点后置入环形硅胶管,从而维持原有泪点口。这种根据泪点狭窄的形态针对性地设计术式,避免了传统采用一种术式解决所有类型泪点狭窄的缺陷,提高了手术成功率。
高倍显微镜下,个体化泪点成形术利用青光眼术中用到的显微器械小梁镊和小梁剪,以更精细地夹持和切除泪点的增生部分,比传统剪式术式更微创。炎症和纤维化会致泪点孔径变小或闭塞[17],小梁镊和小梁剪对泪点周围组织的接触面小,且操作可控,沿泪点边缘弧形剪取,可使术后泪点形状恢复至生理圆形或类圆形,而传统泪点切开术,如剪式手术,术后泪点多呈角状。本研究也验证了采用四剪式泪点切开术的患者,因伤口愈合和瘢痕形成过程中对邻近结缔组织的牵拉,使术后泪点形状从边角清晰的长方形变成相对平坦的钝角方形,因此降低了解剖成功率。
本研究HE染色结果发现,个体化泪点成形术切除组织可见胶原纤维结缔组织内毛细血管充血,鳞状上皮细胞增生,其间可见杯状细胞,均未发现肌纤维组织,说明该术式不伤及泪点外围的Riolan肌和Horner肌,而本研究对照组泪点送检组织中发现有肌纤维组织。传统剪式手术会不同程度破坏泪小管的垂直部、水平部以及泪小管壶腹,影响了泪点的虹吸功能,使得术后泪液排出不畅[18]。有研究表明,泪点膜状闭锁的形成与覆盖泪小管的上皮破坏或泪道始端部分管道化失败有关[5,19]。泪点或泪小管结构的破坏,还会造成复发性泪点狭窄闭锁。Singh等[2]也认为,剪式泪点切开术损伤近端泪小管和泪液引流系统,且损伤不可逆。而本研究个体化设计的泪点成形术只切除了泪点边缘增生的多余病变组织,最大程度保存了泪点的虹吸功能,疗效更好。
因正常泪点周围有弹性纤维和结缔组织束,直径可扩张至正常的3倍,为了保持术后扩大的泪点形状,本研究有选择地在术中置入外径0.8 mm环形硅胶管,在泪点创面愈合过程中起到很好的支撑和塑形作用。且硅胶管两端留置在鼻腔内,伴随眨眼和呼吸可带动硅胶管在泪点处轻微活动,减少硅胶管对泪点的刺激,同时泪液及空气仍可由管壁与泪点间隙进入泪道排出。增生膜的基底大小决定是否置入硅胶管,若基底是较小的蒂,切除后创面也较小,则无需置管。
本研究有部分局限性:(1)为回顾性研究,提供的证据强度不如前瞻性随机对照试验,未来仍有待进一步的临床试验对本研究结论加以验证;(2)四剪式病例较难收集,故两组样本量不够均衡,可能会降低统计学效力;(3)评价指标缺乏统一标准:本研究参照已有文献对泪点大小、溢泪情况及泪液排出功能进行分级,对解剖和功能成功率进行定义,但国际上尚无明确的统一标准,类似的文献结果可能因参照标准的不同而存在差异,希望本研究结果能对未来统一标准的制定提供参考。
综上,根据泪点狭窄类型,个体化选择泪点成形术可有效治疗获得性泪点狭窄,且与传统四剪式手术相比,术后泪点更容易维持正常的解剖形态,在解剖学和功能上的治疗效果均良好。本研究为获得性泪点狭窄实现微创、精准手术提供一种新的治疗理念。

