蜂王浆蛋白肽的制备及其降血糖和抗氧化活性研究
朱作艺,张 玉,王君虹,李 雪,王 伟,*
(1.浙江省农业科学院农产品质量标准研究所,浙江杭州 310021;2.农业农村部创意农业重点实验室,浙江杭州 310021)
蜂王浆(Royal Jelly),又称蜂皇浆,是青年工蜂咽下腺和上颚腺分泌的浆状物质,是蜂王终身的食物[1]。蜂王浆具有众多营养保健功能,具有调节免疫力[2]、抗菌消炎[3-4]、抗衰老[5]、抗肿瘤[6]、降血压[7]、降血糖[8]和促进细胞生长等功能[9]。另外,蜂王浆还具有抗疲劳、降血脂、改善睡眠、保护肝脏、护肤养颜等作用,是一种珍贵的天然食物,被称为“液体黄金”[10]。
我国是世界上生产和输出蜂王浆最多的国家,大部分蜂王浆产品均为原料产品,但蜂王浆本身口感辛辣,粘稠,溶解性欠佳,这些感官和理化特性制约了蜂王浆的市场空间和经济价值。蜂王浆中富含蛋白质,其蛋白含量约占蜂王浆干物质的30%~50%[11]。从营养学角度,蜂王浆作为原料产品也严重制约了其蛋白质的利用价值,从蜂王浆中提取分离出的大部分成分为大分子量的蛋白质,不能直接被人体吸收,在体内的作用机制存在一定的模糊性。生物活性肽是源于蛋白质的具有生理作用的肽类化合物,具有多种人体代谢和生理调节功能,比原料蛋白更容易消化吸收,具有更优异的理化特性、营养特性和生物学活性。除此之外,生物活性肽的食用安全性高,近年来,国内外学者开展了一系列天然动、植物蛋白源多肽的分离纯化、结构鉴定和功能活性研究[12-15]。目前,针对蜂王浆,研究较多的是蜂王浆蛋白的鉴定和生物学活性,而针对其蜂王浆蛋白酶水解后的产物则研究较少,尤其是对蜂王浆蛋白酶解产物的结构组成和降血糖活性研究更少。
因此,本实验拟提取鲜蜂王浆蛋白质在蛋白酶的作用下进行酶解,制得蜂王浆蛋白源活性肽,并研究蜂王浆蛋白活性肽的氨基酸组成、相对分子质量分布情况,以及制备的蜂王浆蛋白肽对α-葡萄糖苷酶的抑制作用和其对ABTS自由基、羟基自由基、超氧阴离子自由基及DPPH自由基的清除能力,以期为研制具有降血糖及抗氧化功能的蜂王浆制品提供一定的理论依据。
1 材料与方法
1.1 材料与仪器
蜂王浆 2017年3月生产于安徽宿松的油菜花期蜂王浆;木瓜蛋白酶(800 U/mg)、酸性蛋白酶(50 U/mg)、中性蛋白酶(100 U/mg)、碱性蛋白酶(200 U/mg)、菠萝蛋白酶(300 U/mg)、风味蛋白酶(20 U/mg) 上海源叶生物科技有限公司;二苯基-2-苦肼基自由基(DPPH)(>97%)、α-葡萄糖苷酶(Intestinal acetone powders from rat)、4-硝基苯基-α-D-呋喃葡萄糖苷(PNPG)(>99%) 美国Sigma公司;阿卡波糖 德国拜耳医药保健有限公司;总抗氧化能力(T-AOC)检测试剂盒(ABTS法)、羟自由基测试试剂盒及抑制与产生超氧阴离子自由基测定试剂盒 南京建成生物工程研究所;其他试剂(均为分析纯) 上海凌峰化学试剂有限公司。
PHS-3C pH计 瑞士梅特勒-托利多仪器有限公司;AMR-100全自动酶标分析仪 杭州奥盛仪器有限公司;EZ-2真空浓缩工作站 美国Genevac公司;N5000紫外-可见光分光光度计 上海佑科仪器仪表有限公司;TDL-60B低速台式离心机 上海安亭设备有限公司;SHZ-82A型水浴恒温振荡器 上海福玛实验设备有限公司;Waters e2695高效液相色谱仪 美国Waters公司;SYCOM型S-433D氨基酸分析仪 德国SYKAM公司;TSKgel G2000SWXL凝胶色谱柱(7.8 mm×300 mm) 日本TOSOH公司;冷冻干燥机 上海皓庄仪器有限公司。
1.2 实验方法
1.2.1 蜂王浆蛋白提取 取一定量的鲜蜂王浆,参照文献[16]采用碱提酸沉法进行蜂王浆蛋白提取。碱提酸沉法的最佳工艺参数(蛋白质等电点pH4.0)为:抽提pH10,料液比1∶4(质量比),抽提温度35 ℃,抽提时间2 h,沉淀时间1 h,沉淀温度5 ℃,沉淀后4000 r/min离心15 min,去清液后得到的沉淀为蜂王浆蛋白。
1.2.2 蛋白酶的选择 称取一定量的蜂王浆蛋白,加入不同蛋白酶进行酶解,酶解条件见表1。酶解结束后,沸水浴灭酶10 min,7500 r/min离心10 min,取上清液测定α-葡萄糖苷酶抑制率和ABTS自由基清除率,筛选出最佳蛋白酶。

表1 6种蛋白酶的最优酶解条件
1.2.3 蜂王浆蛋白肽的制备 称取蜂王浆蛋白100 g,按照料液比1∶10加入去离子水,总加酶量为6000 U/g,调pH为4.0,采用酸性蛋白酶酶解4 h,酶解温度43 ℃,经90 ℃高温灭酶15 min,4000 r/min转速下离心15 min,取上清液冷冻干燥后制得蜂王浆蛋白肽。
1.2.4 蜂王浆蛋白肽氨基酸组成的测定 准确称取0.1 g蜂王浆蛋白肽,加入10 mL 6 mol/L HCl水解22 h,用氨基酸自动分析仪分析其氨基酸组成和含量[17]。
1.2.5 蜂王浆蛋白肽分子量大小及分布 准确称取10 mg蜂王浆蛋白肽,加入去离子水定容至10 mL,溶液经0.45 μm滤膜过滤后,采用凝胶过滤色谱法分析制备的蜂王浆蛋白肽的分子量分布[18]。色谱条件为:色谱柱为TSKgel G2000SWXL(7.8 mm×300 mm);流动相为乙腈/超纯水/三氟乙酸=45/55/0.1(V/V);流速0.5 mL/min;柱温30 ℃;检测波长220 nm。选用胰岛素(MW=5807 Da)、杆菌肽(MW=1450 Da)、甘氨酸-甘氨酸-色氨酸-精氨酸(MW=451 Da)和甘氨酸-甘氨酸-甘氨酸(MW=189 Da)为分子量校正曲线所用标准品,以出峰时间为横坐标,相对分子质量的对数值(lg)为纵坐标,制作校正曲线。
1.2.6 蜂王浆蛋白肽对α-葡糖糖苷酶抑制活性的测定 参照Boath等[19]和Raju等[20]的测定方法,分别配制0.1 mol/L pH6.9 的磷酸缓冲液,5 mg/mL的α-葡糖糖苷酶溶液,5 mmol/L的PNPG溶液和0.67 mol/L的Na2CO3溶液,反应试剂按表2依次添加,待添加完100 μLα-葡糖糖苷酶溶液后,混匀,于25 ℃反应10 min;再添加PNPG溶液和缓冲溶液,混匀,于37 ℃反应10 min;最后加入Na2CO3溶液,混匀后利用酶标仪测定405 nm波长处吸光值,并按公式计算抑制率。阿卡波糖是常见的α-葡萄糖苷酶抑制剂,本试验以阿卡波糖为阳性对照,对不同浓度(0.1~20 mg/mL)蜂王浆蛋白肽对α-葡萄糖苷酶的抑制率进行测定,并计算相应的半抑制浓度(IC50),评价其降血糖活性。

表2 α-葡糖糖苷酶活性测定体系的组成成分

1.2.7 蜂王浆蛋白肽体外抗氧化活性的测定
1.2.7.1 ABTS自由基清除能力测定 参照文献[21]测定。分别量取25 mL 7.4 mmol/L ABTS溶液和25 mL 2.6 mmol/L K2S2O8溶液,等体积混匀后,室温避光反应12~16 h,然后取一定体积上述混合液,再用无水乙醇稀释40~50倍,室温避光后放置30 min后,在734 nm处测定其吸光度为0.70±0.02,制备得到ABTS工作液。取20 μL待测样品液(浓度范围为0.1~20 mg/mL)和280 μL ABTS工作液于96孔酶标板,734 nm处测定吸光值A1,以去离子水代替样品液的吸光值为A2,并以维生素C(VC)为阳性对照。ABTS自由基清除率计算公式如下:清除率(%)=(A2-A1)/A2×100。
1.2.7.2 羟自由基清除能力测定 参照文献[22]测定。取1.0 mL待测样品液(浓度范围为0.1~20 mg/mL)依次加入2.0 mL 1.8 mmol/L FeSO4,1.5 mL 1.8 mmol/L水杨酸-乙醇和0.1 mL 8.8 mmol/L H2O2,37 ℃水浴 30 min。反应结束后取200 μL混合液于96孔酶标板,510 nm处测定吸光值A1,以去离子水代替样品液的吸光值为A2。以VC为阳性对照。羟自由基清除率计算公式如下:清除率(%)=(A2-A1)/A2×100。
1.2.7.3 超氧阴离子自由基清除能力测定 参照文献[23]测定。吸取4.5 mL 50 mmol/L的Tris-HCl缓冲液(pH8.2)于试管中,再吸取2.0 mL蒸馏水于试管中,然后吸取1.0 mL待测样品(浓度范围为0.1~20 mg/mL)液于试管中,将其充分混匀后,放置在25 ℃水浴锅中,放置20 min后,吸取0.5 mL 3.0 mol/L的邻苯三酚溶液于该试管中,迅速摇匀,用蒸馏水调零,利用紫外分光光度计于波长325 nm处测吸光度A1,以去离子水代替样品液的吸光值为A2。以VC为阳性对照。超氧阴离子自由基清除率计算公式如下:清除率(%)=(A2-A1)/A2×100。
1.2.7.4 DPPH自由基清除能力测定 DPPH自由基清除率测定参照文献[24]:取100 μL待测样品液(浓度范围为0.1~20 mg/mL)与100 μL DPPH(95%乙醇配制)溶液均匀混合,室温条件下避光反应30 min,在517 nm处测吸光度值A1。100 μL DPPH溶液与100 μL去离子水反应为对照组(A2),100 μL 95%乙醇与100 μL去离子水反应为空白组(A0)。以VC为阳性对照。DPPH自由基清除率公式如下:清除率(%)=(A2-A1)/(A2-A0)×100。
1.3 数据处理
所有实验均重复3次,结果取平均值,实验结果由平均值±SD 表示。采用SPSS 20.0软件进行分析,组间差异比较采用One-way ANOVA 检验来比较其差异显著性。
2 结果与分析
2.1 蛋白酶的筛选
本实验选择了6种常见的蛋白酶,6种蛋白酶均在其最佳酶解条件(温度和pH)下,以相同的酶活力、酶解时间及料液比条件(见表1),对提取的蜂王浆蛋白进行酶解,然后分别测定酶解后上清液的α-葡萄糖苷酶抑制率和总ABTS自由基清除率。由图1A可知,6种蛋白酶中以风味蛋白酶制备的蜂王浆蛋白肽具有最高的α-葡萄糖苷酶抑制能力,抑制率达到52.09%,其后依次是酸性蛋白酶(46.45%)、碱性蛋白酶(40.11%)、菠萝蛋白酶(35.79%)、木瓜蛋白酶(33.88%)和中性蛋白酶(18.85%)。从图1B中可以看出,酸性蛋白酶水解液的ABTS自由基清除率最高,为64.64%,其次是中性蛋白酶(52.07%)、风味蛋白酶(36.66%)、碱性蛋白酶(33.55%)、木瓜蛋白酶(22.93%)和菠萝蛋白酶(4.27%)。综合考虑,由酸性蛋白酶酶解制备得到的多肽兼具较强的降血糖和抗氧化活性,同时蜂王浆pH在3.5~4.0之间,呈弱酸性,与酸性蛋白酶的酶解条件相匹配,因此,本研究选择酸性蛋白酶为制备蜂王浆肽的最佳蛋白酶。
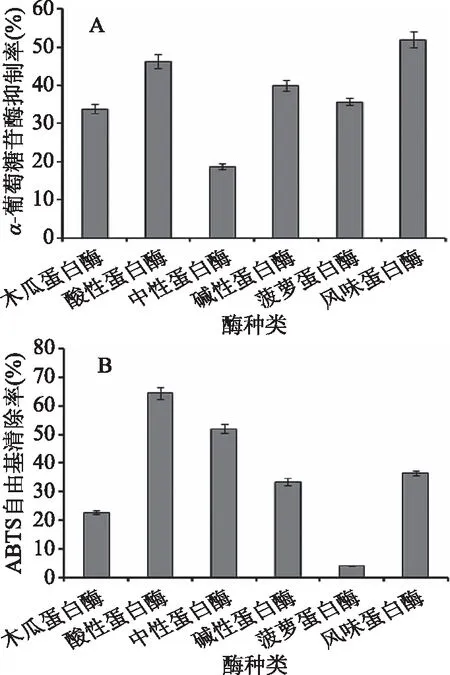
图1 不同蛋白酶酶解对蜂王浆肽的α-葡萄糖苷酶抑制率(A)及ABTS自由基清除率(B)的影响
2.2 蜂王浆蛋白肽氨基酸组成
本实验制备的蜂王浆蛋白肽经氨基酸仪分析,其氨基酸组成及含量如表3所示,氨基酸的总量为82.19%,其中含量最高的氨基酸为天门冬氨酸(15.15%),其次是谷氨酸(10.36%)和亮氨酸(7.00%)。生物活性肽的氨基酸组成与其活性密切相关,有研究者从动物蛋白中分离得到一系列抗氧化多肽,通过对这些多肽的氨基酸序列进行分析发现,这些抗氧化多肽的末端多为酪氨酸、苯丙氨酸、脯氨酸、丙氨酸、组氨酸和亮氨酸,占总氨基酸的30%左右[25-27]。由表3可知,针对蜂王浆蛋白肽,上述6种氨基酸占其氨基酸总量的28.80%,其中亮氨酸含量为7.00%,苯丙氨酸含量为4.19%,这些氨基酸的存在可能直接影响着蜂王浆蛋白肽的抗氧化活性。

表3 蜂王浆蛋白肽氨基酸组成
2.3 蜂王浆蛋白肽分子量分布
由图2可以看出,制备的蜂王浆蛋白肽通过凝胶色谱柱的出峰时间大部分集中在18~21 min内,通过分子量校正曲线(lgMw=-0.2554tR+7.5677,R2=0.9894,Mw为相对分子质量,tR为保留时间)计算分子量大小,由表4可知,酶解后的蜂王浆蛋白肽相对分子质量集中在1000 Da以下。相对分子质量在 400~1000 Da左右的多肽组分峰面积占总面积的14.3%,180~400 Da左右的多肽组分含量最多,占78.9%,这些多肽可能基本以二肽、三肽和四肽为主;还有6.8%左右的组分相对分子质量小于180 Da,基本为游离氨基酸和水解过度的氨基酸残基[28-29]。酶解后的多肽分子量与蛋白酶种类和酶解时间相关,酶解度不同,所形成的肽类化合物的分子量大小和结构也不同,这将直接影响酶解产物的活性。因此,今后针对不同活性需求的蜂王浆多肽优化其酶解程度,将能更好地发挥蜂王浆的营养功效。

表4 蜂王浆蛋白肽分子量分布
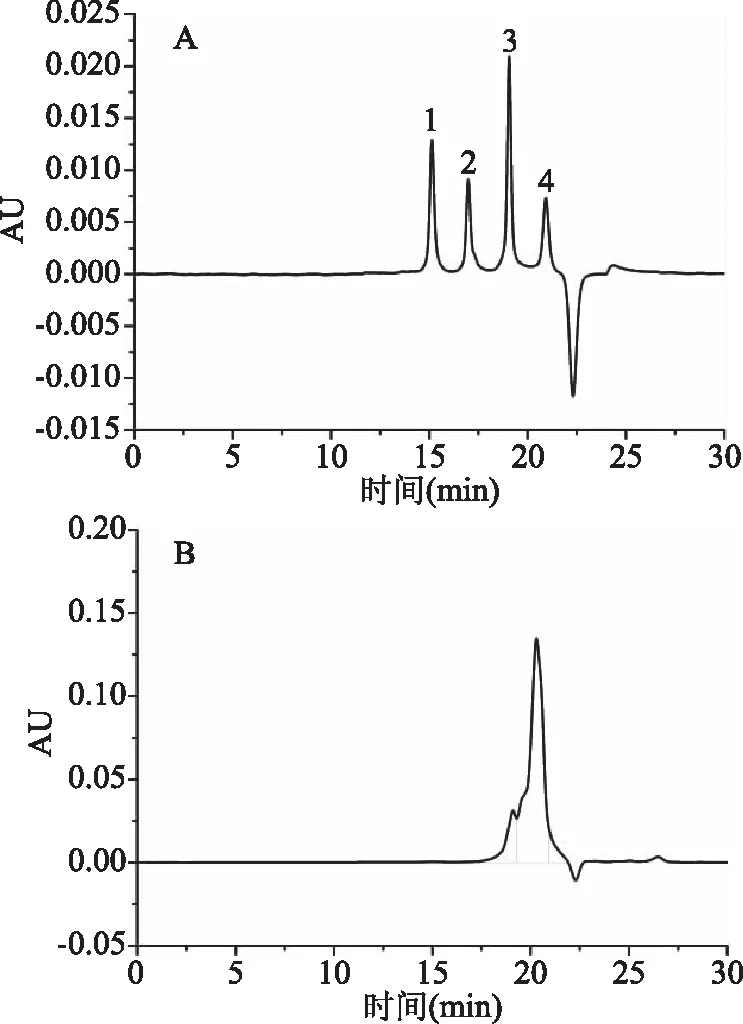
图2 分子量标准(A)及蜂王浆蛋白肽(B)的凝胶过滤色谱图
2.4 蜂王浆蛋白肽对α-葡萄糖苷酶的抑制能力
从图3可知,在0~2 mg/mL浓度范围内,蜂王浆蛋白肽对α-葡萄糖苷酶的抑制率随着浓度增大而升高,2 mg/mL后升高缓慢,浓度为20 mg/mL时,抑制率为63.86%,其IC50值为6.94 mg/mL。而阿卡波糖浓度为5 mg/mL时,其对α-葡萄糖苷酶的抑制率高达95.14%。试验结果表明,蜂王浆蛋白肽具有一定的降血糖活性,其活性低于阳性对照药物阿卡波糖,这可能是因为蜂王浆蛋白肽是粗酶解产物,未经进一步的分离纯化。药物阿卡波糖虽然能较好地控制血糖,但长期服用容易产生耐药性,同时会伴随着许多不良反应和副作用。蜂王浆蛋白肽作为天然产物,食用安全性高,目前尚未见有关于抑制α-葡萄糖苷酶活性的蜂王浆蛋白肽报道。因此,基于本实验研究的蜂王浆蛋白酶解产物具有一定的α-葡萄糖苷酶抑制活性,可进一步对酶解产物进行分离纯化,筛选出高活性的多肽单一组分,对于糖尿病的治疗具有重要的意义。

图3 蜂王浆蛋白肽对α-葡萄糖苷酶的抑制能力
2.5 蜂王浆蛋白肽体外抗氧化活性
2.5.1 ABTS自由基清除能力 从图4A可知,不同质量浓度的蜂王浆蛋白肽和VC对ABTS自由基的清除率随着质量浓度的增大而增加,呈现出一定的剂量依赖效应。在0~2.0 mg/mL浓度范围内,VC对ABTS自由基的清除率随着浓度增大而迅速升高;浓度为2.0 mg/mL时,其ABTS自由基清除率高达88.91%。相同质量浓度情况下,蜂王浆蛋白肽对ABTS自由基的清除率低于VC,尤其当浓度大于5 mg/mL时,升高缓慢。蜂王浆蛋白肽浓度为20.0 mg/mL时,其清除率为54.03%,对ABTS自由基清除能力的IC50值为14.18 mg/mL。
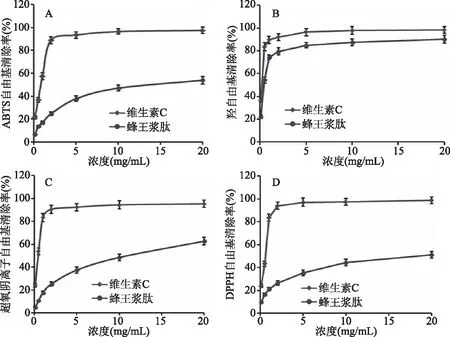
图4 蜂王浆蛋白肽对ABTS自由基(A)、羟自由基(B)、超氧阴离子自由基(C)和DPPH自由基(D)的清除能力
2.5.2 羟自由基清除能力 由图4B可知,在0~1.0 mg/mL浓度范围内,蜂王浆蛋白肽与VC的羟自由基清除能力与质量浓度之间存在明显的线性关系;质量浓度为1.0 mg/mL时,蜂王浆蛋白肽对羟自由基的清除率高达74.24%,相同浓度下VC的清除率为89.53%。当浓度大于1.0 mg/mL时,两者对羟自由基的清除率均升高缓慢,蜂王浆蛋白肽清除羟自由基能力的IC50值为0.45 mg/mL,显著低于文献报道的鳀鱼酶解肽[29]及鲍鱼蛋白肽[30]对羟自由基的清除能力。一般认为某种物质的IC50低于10.0 mg/mL时,说明其具有良好的抗氧化性[31]。
2.5.3 超氧阴离子和DPPH自由基清除能力 不同质量浓度的蜂王浆蛋白肽对超氧阴离子和DPPH自由基清除能力的影响趋势(图4C和4D),类似于对ABTS自由基的清除效果,蜂王浆蛋白肽浓度为20.0 mg/mL时,对超氧阴离子和DPPH自由基的清除率分别为62.79%和51.10%,IC50值分别为11.02和18.38 mg/mL,远高于文献报道的鳀鱼酶解肽[29]及鲍鱼蛋白肽[30]对DPPH、超氧阴离子自由基等的清除能力。蜂王浆蛋白肽对ABTS、超氧阴离子和DPPH自由基具有类似的清除效果,而对羟自由基清除能力呈现不一样的影响趋势,这可能是由于对ABTS、超氧阴离子和DPPH自由基的清除是基于电子传递方法,而对羟自由基的清除是基于氢传递方法导致的[33]。
以上结果表明,蜂王浆蛋白肽对羟自由基具有较强的清除能力,同时还具有一定的ABTS、超氧阴离子和DPPH自由基清除能力。多肽的抗氧化活性同样与其氨基酸序列有关,有研究表明由2~4个氨基酸分子组成的小肽,当其C-端氨基酸残基多为芳香族氨基酸(Trp、Tyr)和Pro、His,同时N-端多含疏水性氨基酸Val、Leu、Ile、Ala、Lys时,其抗氧化活性尤其高[32]。由此可知,蜂王浆原蛋白本不具抗氧化活性,通过蛋白酶的水解,可以释放出具有类似以上结构特征的小分子肽类化合物,从而产生抗氧化活性。
3 结论
蜂王浆中富含蛋白质,本研究筛选了制备蜂王浆降血糖及抗氧化活性肽的最佳蛋白酶,酶解工艺条件为:酸性蛋白酶,酶添加量为6000 U/g,酶解温度为43 ℃,酶解pH为4.0,酶解时间为4 h,料液比为1∶10。体外降血糖及抗氧化活性实验结果表明,蜂王浆蛋白肽具有一定的抑制α-葡萄糖苷酶能力和清除ABTS自由基、DPPH自由基和超氧阴离子能力及较强的羟基自由基清除能力。由于本研究制备的蜂王浆蛋白肽是粗酶解物,因此对于蜂王浆蛋白肽的分离纯化、结构功能鉴定等方面还有待于今后的进一步研究,深入挖掘高活性的蜂王浆蛋白肽组分,发挥蜂王浆的营养功效。

