二维超声联合超微血管成像技术在宫颈癌术前分期诊断中的价值*
韦玲华,凌冰,肖艳菊
(广西壮族自治区人民医院,广西 南宁 530021)
宫颈癌为全球女性常见的第三大癌症,多数新发及死亡病例是因为没有进行疾病筛查,尤其是在发展中国家,发病率及死亡率更高[1]。宫颈癌的治疗、预后与分期关系密切,所以对疾病进行正确的诊断及分期意义重大。有研究指出,磁共振成像(magnetic resonance image,MRI)对明确宫颈癌分期有较高的应用价值[2],在宫颈癌的诊断中超声可以提供与MRI 相似的临床信息,且具备可重复性、动态监测及低成本等优势。超微血管成像(superb microvascular imaging,SMI)作为一种新型的多普勒超声血管显像技术,能够区分机体中、低速血流信号与组织信号所产生的多普勒信号,敏感性高,对乳腺肿瘤的鉴别有着极高的应用价值[3]。然而SMI 在宫颈癌的临床应用报道较少。本文对二维超声联合SMI 诊断早期宫颈癌术前分期的价值进行分析,旨在探索一种经济、方便的技术辅助宫颈癌分期,现报道如下。
1 资料与方法
1.1 临床资料
选取2018年11月—2019年12月广西壮族自治区人民医院收治的经病理检查确诊为宫颈癌拟手术治疗的76 例患者。其中,年龄34 ~67 岁,平均(51.37±3.86)岁;体重指数19 ~27 kg/m2,平均(22.36±2.64)kg/m2;组织类型: 鳞癌53 例,腺癌17 例,其他6 例;分化程度: 中、高分化9 例,中分化24 例,低分化43 例。本研究经医院伦理委员会审批通过。
纳入标准: ①符合第9 版《妇产科学》相关诊断标准[4],术前均进行二维超声联合SMI 及MRI 检查;②年龄18 ~80 岁;③患者及其家属均知情同意。排除标准: ①严重心、肝、肾等脏器功能障碍;②合并其他恶性肿瘤疾病和严重内科疾病;③感染性疾病或盆腔手术史;④合并其他宫颈疾病;⑤智力缺陷或精神障碍不能配合临床工作。
1.2 方法
1.2.1 超声检查采用Aplio500 多普勒彩色超声诊断仪(日本佳能医疗系统株式会社),首先行阴道超声检查,频率3 ~11 MHz,扫描角度180 °。患者检查前排空膀胱,取屈膝仰卧位,探头经阴道进入,行二维超声、彩色多普勒超声和SMI 检查,先观察子宫附件情况,重点观察宫颈形态、大小、部位、范围、与边缘的距离及总浸润深度等,探查范围由膀胱颈至直肠窝及宫颈韧带区域。开启灰阶超微血流成像模式,调节取样框大小,流速设置为1 ~2 cm/s。监测宫颈病灶及周围组织血流情况,探头定位在血流显示最清晰的切面处保存图像。
1.2.2 MRI采用标准化MRI,包含矢状及轴向斜面T2加权序列和轴向T1加权序列。为了更好地评估肿瘤大小、部位及向宫旁浸润的情况,采取2 个正交平面,即矢状与轴向倾斜序列或者轴向序列上的T2加权图像。所有患者注射螯合物,扫查肿瘤大小、部位、范围、与边缘的距离及总浸润深度。
1.2.3 病理检查手术后由病理医师对标本进行病理组织学检查。
1.2.4 宫颈癌分期根据2018年国际妇产科联盟(International Federation of Gynecology and Obstetrics,FIGO)分期标准进行评估,具体见表1。
1.3 评价方法
所有病例由2 位高年资的妇科肿瘤医师进行妇科检查,术后由病理医师对标本进行评价。评价内容包含肿瘤的大小、病变部位、涉及范围、与边缘的距离及总浸润深度等,同时借助显微镜检查确定分期。以宫颈癌FIGO 分期标准分组,分别用二维超声联合SMI、单独MRI 测量肿瘤的大小、阴道受累及宫旁浸润情况,进行术前分期,评估各期诊断的敏感性、特异性、阳性预测值及阴性预测值。
1.4 统计学方法
数据分析采用SPSS 22.0 统计软件。计数资料以率(%)表示,比较用χ2检验,P<0.05 为差异有统计学意义。
2 结果
2.1 宫颈癌超声结果
二维超声扫描显示患者宫颈有不均匀低回声,内见多个点状强回声(见图1)。二维超声联合SMI 结果显示低回声区及宫颈前壁肌层有丰富的较杂乱血流信号(见图1)。苏木精-伊红(HE)染色可见宫颈鳞状细胞癌(见图2)。。

表1 宫颈癌FIGO 分期
2.2 分期诊断结果
二维超声联合SMI 诊断宫颈癌分期总的准确率为77.6%(59/76),MRI 为73.7%(56/76),经χ2检验,差异无统计学意义(χ2=0.322,P=0.571)。二维超声联合SMI 与单独MRI 诊断宫颈癌ⅠB1、ⅠB2 期的准确率比较,差异有统计学意义(P<0.05);其他分期的准确率比较,差异无统计学意义(P>0.05)。见表2。
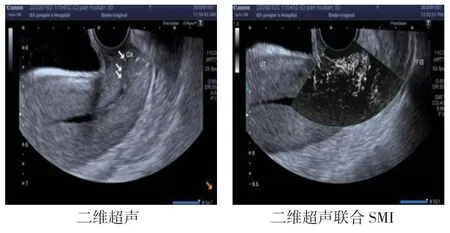
图1 二维超声单独或联合SMI 检查
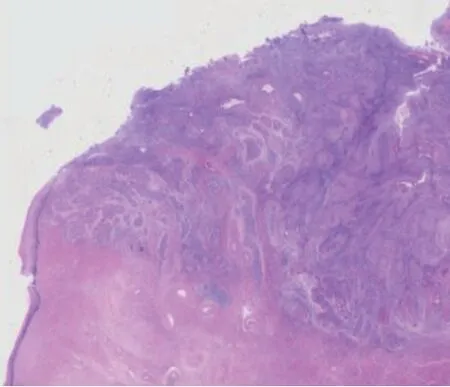
图2 宫颈鳞状细胞癌 (HE×400)
2.3 肿瘤大小、浸润情况的诊断价值
肿瘤直径<2 cm、2 ~<4 cm 时,二维超声联合SMI 与单独MRI 的诊断敏感性比较,差异有统计学意义(P<0.05),二维超声联合SMI 较高。肿瘤直径≥4 cm、阴道受累时,2 种技术的诊断敏感性比较,差异有统计学意义(P<0.05),MRI 较高。肿瘤直径<2 cm、2 ~<4 cm、≥4 cm 和阴道受累时,2 种技术的诊断特异性比较,差异无统计学意义(P>0.05)。见表3。
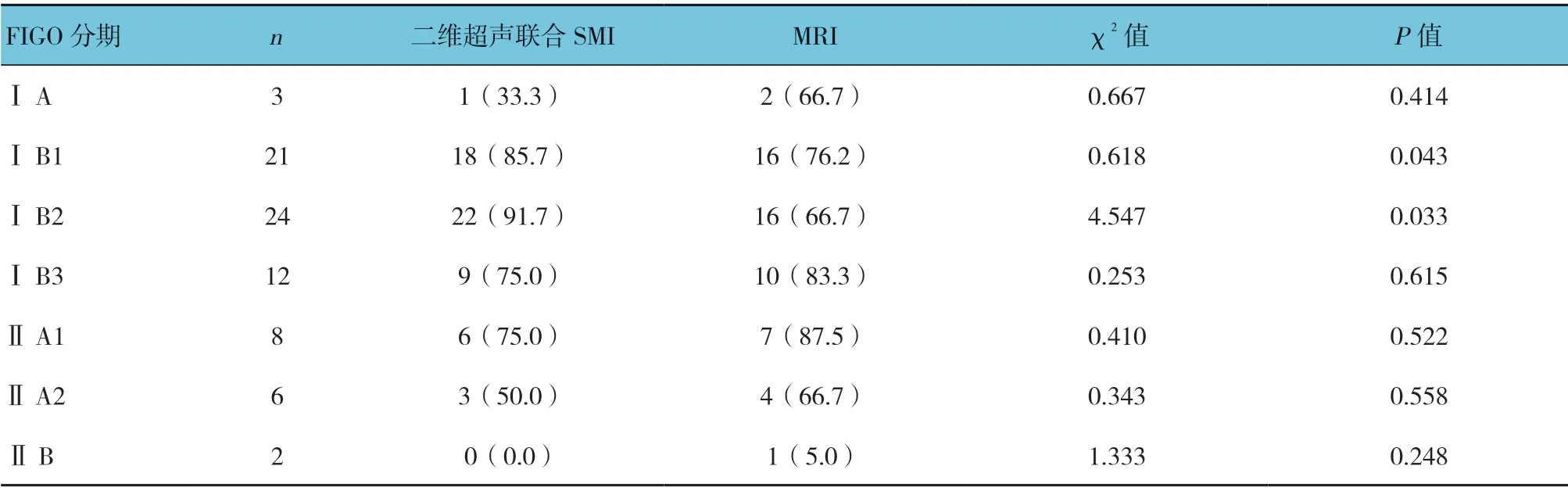
表2 二维超声联合SMI 与单独MRI 诊断宫颈癌分期的准确率 例(%)
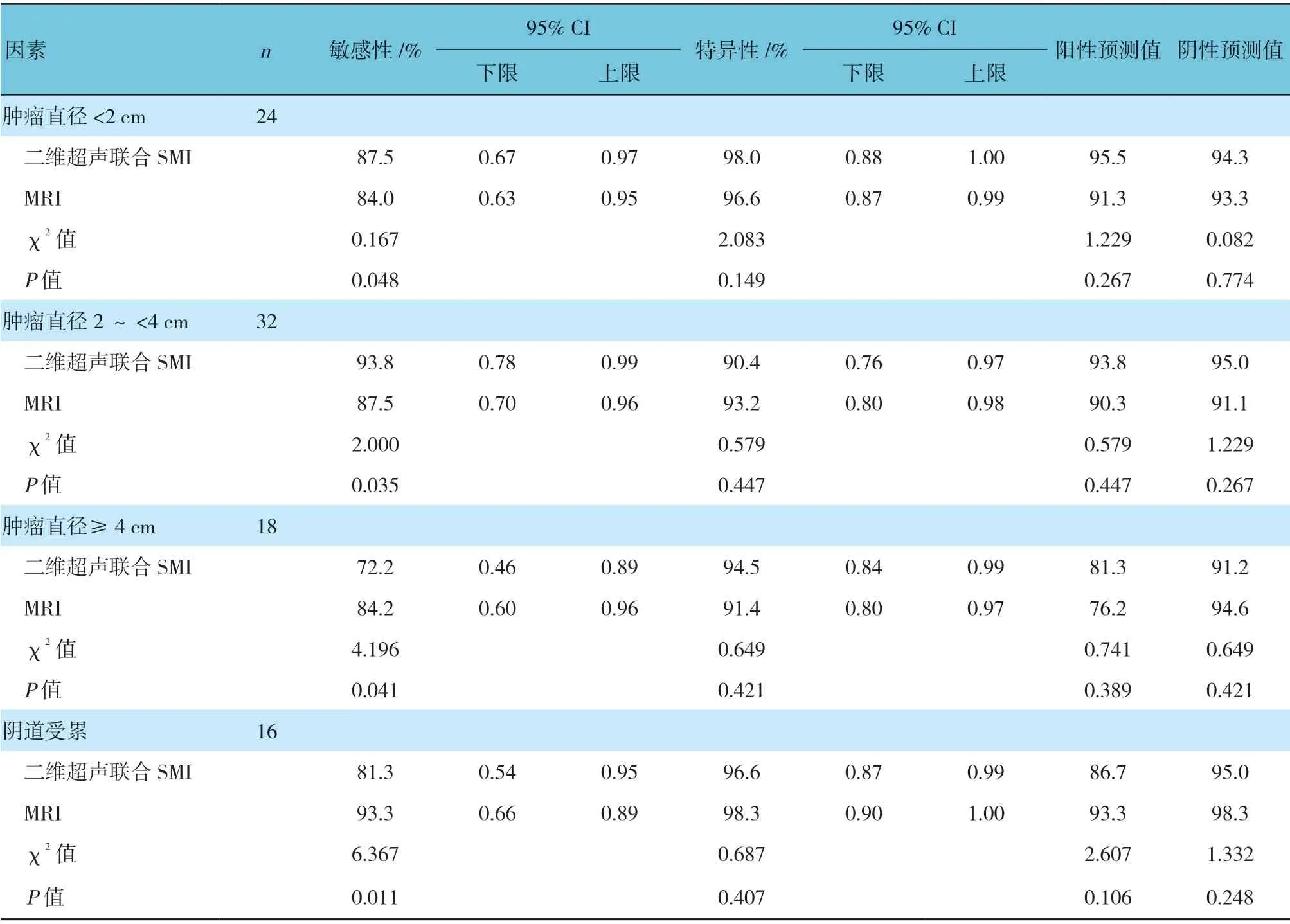
表3 二维超声联合SMI 和单独MRI 对肿瘤大小、浸润情况的诊断价值 例(%)
3 讨论
宫颈癌的预后与临床分期关系密切,不同分期宫颈癌患者治疗方案也有所不同,其中Ⅰ、Ⅱ期多行根治手术治疗,Ⅲ、Ⅳ期多予以根治术放化疗及综合治疗,因此明确宫颈癌分期,对于制定有效的治疗方案和改善预后意义重大。在疾病分期方面,临床分期与术中或组织学评估之间存在差异。实际上,妇科检查分别导致40%和64%的低估和高估误差[5]。基于此,FIGO 在2018年更新了宫颈癌分期,允许依据辅助检查的评估结果来修正初始临床分期,因此临床还需寻找能辅助宫颈癌准确分期的检查方法[6]。
宫颈癌有多种检查方法,MRI 是目前最受推崇的一种宫颈癌影像学分期诊断方法,其最大的优势是可以实现大视野扫描和高空间分辨率显像,从而将子宫壁的各层结构清晰地显示出来。MRI 在宫颈癌分期尤其是晚期宫颈癌分期的评价上有较大优势,但在术前分期上也会出现假阴性和假阳性情况,加上其可见低信号宫颈基质环完整但不均,所以在病理活检时可观察到宫旁有MRI 无法显示的微小癌巢[7-8]。肿瘤大小是为癌症患者制定治疗方案的重要标准之一。MRI 对肿瘤大小的评估存在一定的局限性,尤其是肿瘤处于宫颈内位置时,MRI 难以显示微小病变[9]。MRI 价格昂贵不易普及也限制其广泛应用。
二维超声在宫颈癌的诊断及分期应用中比较常见。有研究认为,普通超声在宫颈癌诊断及其分期中虽然有一定优势,但是其诊断准确率还需进一步提高,表现为缺乏清晰包膜,与正常组织的声阻抗不明显,无法形成鲜明回声对比,对邻近正常组织界限的准确分辨有一定难度,对较小病灶的诊断也比较困难[10]。二维超声检查可见子宫颈增大,形态多不规则,局部低回声且不均匀,病灶边缘和浸润范围均显示比较模糊,对宫颈癌早期诊断容易出现误诊、漏诊[11]。SMI是一种基于高分辨率的多普勒技术,利用Aplio 系列的高端超声波诊断装置构架实时应用平台和高密度波束形成器,从而用更高帧速率对低流速血流进行成像[12]。SMI 能够显示低速微小血管的血流,对血流信号的捕捉具有高度敏感性,加上SMI 成本低、操作简单、无创性及可重复检查等特点,通过自适应图像处理手段,以自适应算法提取微血管中的血流信号,并保留最细微低速血流信息,以此提高显示微细血管的敏感性,弥补二维超声的不足[13]。SMI 能够清晰地显示出血流分布及走行,以减少二维超声检查时低血流和无血流检测漏诊现象,理论上对提高宫颈癌分期的诊断准确率有重要意义。本研究结果提示,二维超声联合SMI 诊断ⅠB1、ⅠB2 期宫颈癌的准确率均高于MRI;肿瘤直径<2 cm、2 ~<4 cm 时,二维超声联合SMI 诊断敏感性为87.5%和93.8%,优于MRI 的84.0%和87.5%。SOZZI 等[14]研究显示,二维超声检查与麻醉下的检查、MRI 相比,诊断性能更好,尤其是对于直径2 ~<4 cm 的肿瘤。由此可见,二维超声联合SMI 在早期宫颈癌术前分期诊断中有一定优势。
除肿瘤的大小外,宫旁组织浸润及阴道受累也是影响宫颈癌分期和治疗的重要指标。既往文献中少有数据报道阴道受累情况,但通常发现超声检查和MRI准确率均低[15]。本研究结果提示阴道受累方面二维超声联合SMI、单独MRI 的诊断敏感性分别为81.3%和93.3%,MRI 优于二维超声联合SMI,不排除样本量较少所致。由于ⅡB 期宫颈癌患者的主要治疗方法为根治性放化疗,因此ⅡB 期纳入仅2 例,且为术后病理发现,因此本研究中这2 种方法鉴别宫旁组织浸润依据欠充分。既往研究表明,MRI 对宫颈癌宫旁侵犯的诊断准确率显著高于超声[16]。还有研究提示MRI联合经阴道彩超可有效判断肿瘤直径、临床分期、间质及阴道浸润、宫旁受累及淋巴结转移情况,其诊断效能显著高于MRI 与经阴道彩超单独检测[17]。另外,在SMI 操作过程中,要注意SMI 以检测低速血流信号为主,速度标尺一般在1.0 ~1.4 cm/s 时为稳定性和敏感性最好的范围;对彩色增益进行适当调整,过高可能无法显示部分低速血流,过低则可能增加运动伪像;操作过程探头尽量保持稳定,切忌大幅度快速移动,以免速度过快或波动过大造成误差;适当调节SMI 的频率,先以低频率观察,再调整高频率,保证观察范围内远场及近场的血流显示,如患者呼吸幅度大时,嘱患者屏住呼吸以减少伪像。
综上所述,二维超声联合SMI 对早期宫颈癌术前分期诊断具有价格低廉、可反复操作、无创等优势,可为宫颈癌治疗方案的制订提供重要依据。但由于本研究收集的数据和纳入的病例数有限,仍需进行前瞻性及更大规模的研究加以验证。

