放射治疗前使用氨磷汀对头颈部癌症患者口干症等干预效果的Meta分析和GRADE评价
卫彬彬 胡慧维 刘玉娟 孙哲 衣玉丽
1.南昌大学护理学院 南昌 330006;
2.南昌大学第一附属医院肿瘤科 南昌 330006
2017年有数据[1]显示全球每年约有70万新确诊的头颈部癌症病例,放射治疗是该类肿瘤一种常用且有效的治疗方式,但头颈部区域解剖结构复杂,包括唾液腺在内的正常组织也不可避免地受到了辐射,产生口腔干燥等放射性毒性反应。口干症(或称口干)的定义为“口腔干燥的主观感觉”,头颈部放射治疗后唾液腺功能障碍、唾液分泌减少,即称为放射性口干,是放射治疗后一种主要的甚至是永久性的毒性反应[2]。急性期口干发生在放射治疗过程中或放射治疗结束后3个月内,晚期口干发生在放射治疗结束3个月以后或更晚,即使是采用最新的现代放射治疗技术,头颈部癌症患者中重度(≥2级)晚期口干的发生率仍可达40%[3]。口干的发生会引发诸多并发症如语言障碍、口腔感染、龋齿、咀嚼和吞咽困难、味觉缺失、睡眠障碍等,使患者的生活质量急剧下降[4-5]。
氨磷汀是美国食品药品管理局(Food and Drug Administration,FDA)批准上市的泛细胞保护剂,但其作为口腔干燥预防剂的使用一直饱受争议,尤其是在肿瘤保护、药物不良反应、成本效益等方面[5]。
有研究[6]指出氨磷汀可有效预防或减轻肿瘤治疗引起的涎腺功能低下和口干,但另有研究[2]称当前支持氨磷汀减少放射性口干的证据质量均较低,还有待于进一步的研究。
因此,本研究继续探索氨磷汀对头颈部肿瘤放射治疗后口干的效果,以期为临床的应用提供参考。
1 材料和方法
1.1 文献纳入与排除标准
纳入标准:本文采用PICOS格式界定纳入标准。1)S(研究设计类型,study design):为随机对照试验(randomized controlled trial,RCT)。2)P(研究对象,population):经细胞学或病理学检查确诊为头颈部癌症且接受放射治疗的患者,年龄满18周岁,语种为中文或英文,不限性别、病程。3)I(干预措施,intervention):在每次放射治疗开始前15~30 min内应用氨磷汀。4)C(对照措施,control):安慰剂、空白对照及常规预防口干的其他药物。5)O(结局指标,outcome):①2级以上急性口干;②2级以上晚期口干;③放射治疗结束后腺体功能指标;④急性黏膜炎;⑤恶心呕吐;⑥低血压;⑦过敏反应;⑧肿瘤局部区域控制;⑨总体生存。
排除标准:重复发表的文献、非RCT类型的文献、非头颈部癌症患者、非放射治疗前使用氨磷汀、研究结局指标无口干、非中文或英文文献。
1.2 文献检索策略
计算机检索中国知网(China National Knowledge Infrastructure,CNKI)、万方数据知识服务平台(WanFang Data Knowledge Service Platform)、中国生物医学文献数据库(China Biology Medicine disc,CBMdisc)、维普中文科技期刊数据库(VIP Database for Chinese Technical Periodicals,VIP)、PubMed、Cochrane Library、EMbase、Medline,检索时限从建库至2019年7月,检索策略为主题词和自由词间相组合。
中文检索词以(氨磷汀OR阿米福汀)、(头颈部肿瘤OR头颈部癌症OR头颈部鳞癌)、(放疗OR放射疗法OR放射治疗)、(口干OR口腔干燥)进行检索。英文检索词以(amifostine)、(head and neck tumor OR head and neck cancer OR head and neck neoplasms OR squamous cell carcinoma of head and neck)、(radiotherapy OR radiation)、(xerostomia OR thirst OR polydipsia OR dry mouth)进行检索。
1.3 文献筛选、资料提取
由2名评价员通过阅读题目和摘要,对可能符合纳入标准的文献进一步查阅全文,如遇到分歧,进行讨论或咨询第三方。对纳入的文献以表格的形式列出提取的信息。包括作者、发表年份、研究所属国家、样本量、研究对象基线特征、干预措施以及结局指标等。
1.4 纳入研究的方法学质量评价
偏倚风险由2名评价员根据Cochrane手册5.1.0版提出的评价RCT方法进行评价,如遇到分歧,进行讨论或咨询第三方,最终达成共识,以表格列出方法学质量评价结果。
1.5 GRADE证据质量评价
根据GRADE证据分级系统对结局指标的证据质量进行评价[7],并通过GRADE profiler3.6软件实现。
1.6 统计学方法
采用RevMan5.3软件进行数据处理。计数资料以相对危险度(relative risk,RR)或比值比(odds ratio,OR)作为效应指标;计量资料以均数差(mean deviation,MD)作为本研究的效应指标,各效应量均以95%置信区间(confidence interval,CI)表示。采用χ2检验对各研究结果进行异质性检验,当P≥0.10,I2≤50%时,采用固定效应模型进行Meta分析;反之,则采用随机效应模型进行Meta分析,检验水准α=0.05。若数据无法合并则行描述性分析。
2 结果
2.1 文献检索结果
初步检索出635篇文献,经逐层筛选最终确定纳入9篇文献[8-16],中文4篇,英文5篇。文献筛选流程图见图1。

图1 文献筛选流程图Fig 1 Literature screening procedure
2.2 纳入研究的基本特征
纳入9篇文献,共计948例头颈部癌症患者,其中实验组470例、对照组478例。各研究基本特征见表1。
2.3 纳入研究的方法学质量评价
对各研究是否存在选择偏倚、实施偏倚、测量偏倚、失访偏倚、发表偏倚及其他偏倚进行评价,评价结果见表2。
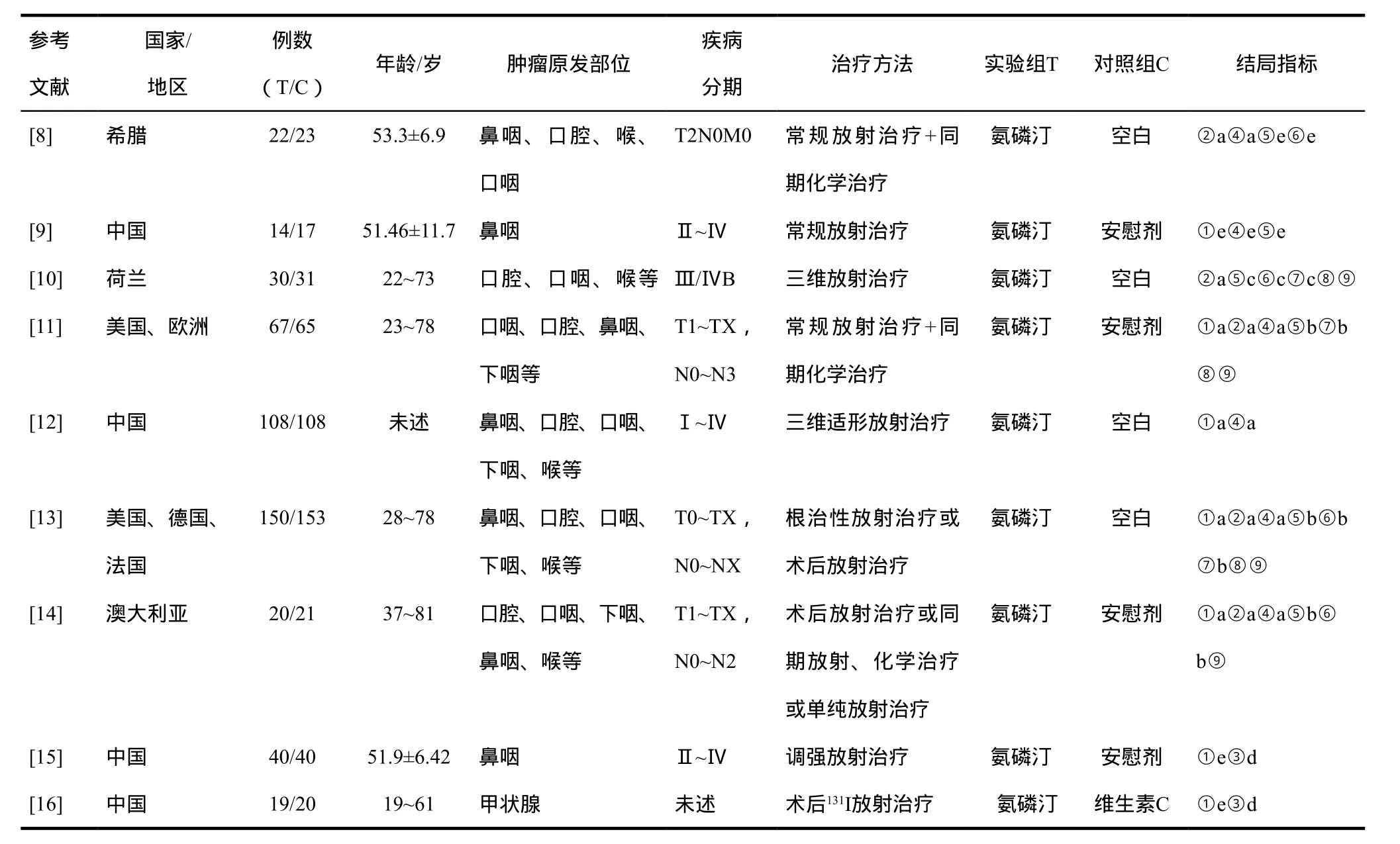
表1 纳入研究的基本特征Tab 1 General characteristics of included studies
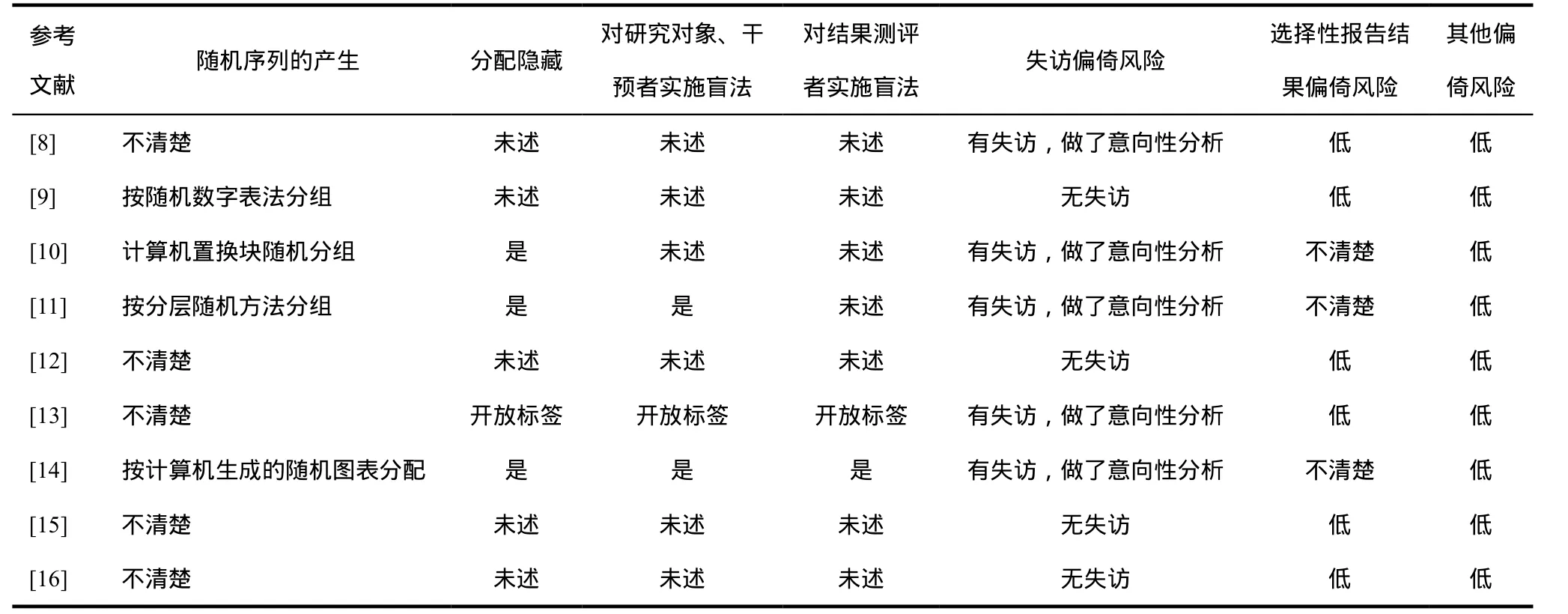
表2 纳入研究的方法学质量评价结果Tab 2 Methodological quality evaluation of included studies
2.4 Meta分析结果
2.4.1 2级以上急性口干的发生率 7篇研究[9,11-16]报告了2级以上急性口干的发生率,共纳入835例患者。两组间的异质性检验显示I2=81%,故采用随机效应模型分析,结果显示氨磷汀组降低2级以上口干的效果优于对照组[RR=0.62,95% CI(0.44,0.87),P=0.005],差异有统计学意义(图2)。
2.4.2 2级以上晚期口干的发生率 5篇研究[8,10-11,13-14]报告了2级以上晚期口干的发生率。根据随访时间(放射治疗后6个月、放射治疗后12个月、放射治疗后24个月)进行亚组分析(图3)。
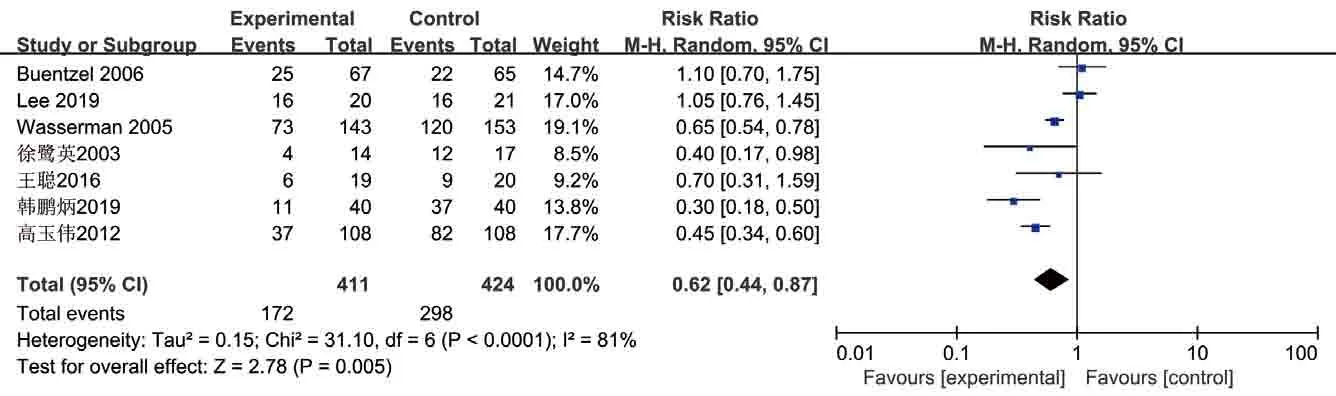
图2 氨磷汀组与对照组2级以上急性口干的Meta分析Fig 2 Meta-analysis of acute xerostomia above grade 2 in amifostine group and control group
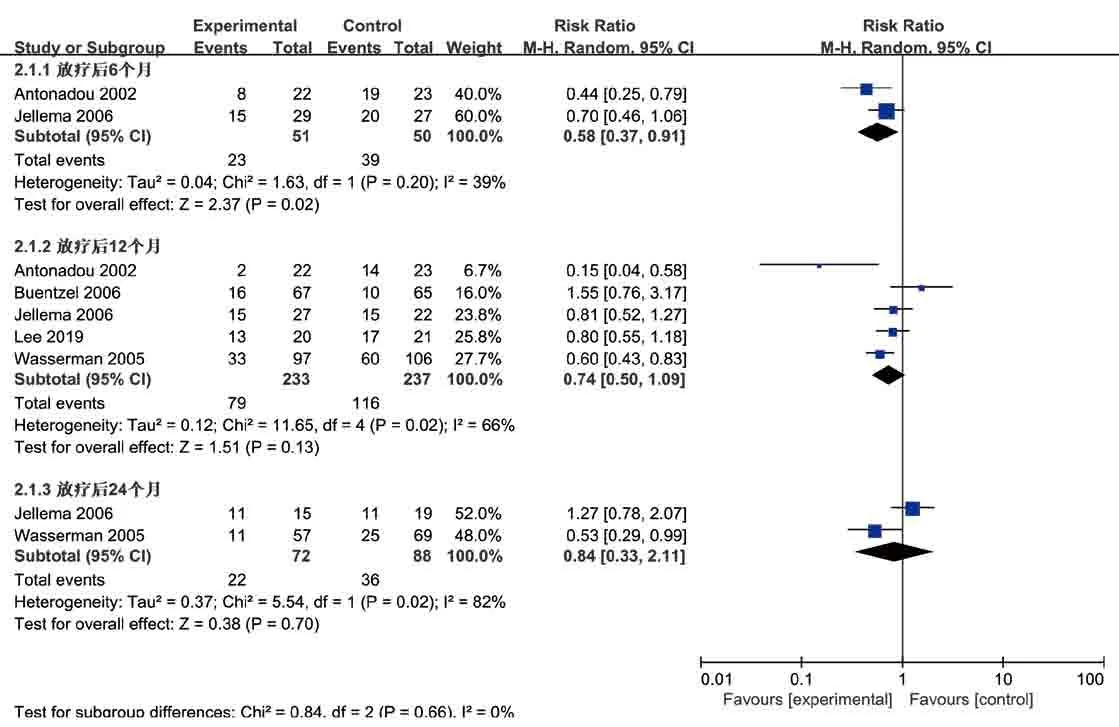
图3 氨磷汀组与对照组2级以上晚期口干的Meta分析Fig 3 Meta-analysis of advanced xerostomia above grade 2 in amifostine group and control group
1)放射治疗后6个月2级以上口干的情况:2篇文献[8,10]共纳入101例患者,两组间的异质性检验显示I2=39%,仍采用随机效应模型分析,结果显示氨磷汀组降低2级以上口干的效果优于对照组[RR=0.58,95% CI(0.37,0.91),P=0.02],差异有统计学意义。
2)放射治疗后12个月2级以上口干的情况:5篇文献[8,10-11,13-14]共纳入470例患者,两组间的异质性检验显示I2=66%,采用随机效应模型分析,结果显示氨磷汀组与对照组在该时间点差异无统计学意义[RR=0.74,95% CI(0.50,1.09),P=0.13]。
3)放射治疗后24个月2级以上口干的情况:2篇文献[10,13]共纳入160例患者,两组间的异质性检验显示I2=82%,采用随机效应模型分析,结果显示氨磷汀组与对照组在该时间点差异无统计学意义[RR=0.84,95% CI(0.33,2.11),P=0.70]。
2.4.3 治疗后腺体功能指标 2篇研究[15-16]报告了放射治疗后腺体功能指标,根据测试部位(腮腺、颌下腺)进行亚组分析(图4、5)。
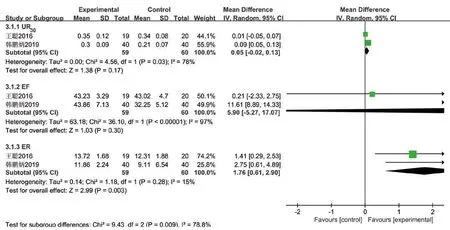
图4 氨磷汀组与对照组放射治疗后腮腺功能指标的Meta分析Fig 4 Meta-analysis of parotid gland function index after radiotherapy in amifostine group and control group
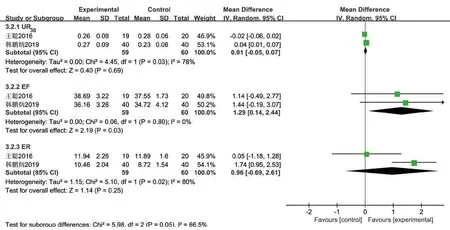
图5 氨磷汀组与对照组放射治疗后颌下腺功能指标的Meta分析Fig 5 Meta-analysis of salivary gland function index after radiotherapy in amifostine group and control group
1)腮腺。2篇研究[15-16]共纳入357例患者,两组间腺体的30 min摄取分数(uptake ratio of 30 min,UR30)、排泌分数(excretion fraction,EF)、排泌率(excretion ratio,ER)的异质性I2分别为78%、97%、15%,采用随机效应模型分析,结果显示氨磷汀组仅在腺体功能指标ER上明显优于对照组[MD=1.76,95% CI(0.61,2.90),P=0.003],差异有统计学意义;氨磷汀组在腺体功能指标UR30、EF上的优势不明显[MD=0.05,95% CI(-0.02,0.13),P=0.17]、[MD=5.90,95% CI(-5.27,17.07),P=0.30],差异无统计学意义。为检验合并结果的稳定性,采用固定效应模型再次合并,结果氨磷汀组在3项指标上均明显优于对照组,提示结果不稳健,必须审慎地看待本结论。
2)颌下腺。2篇研究[15-16]共纳入357例患者,两组间UR30、EF、ER的异质性I2分别为78%、0%、80%,采用随机效应模型分析,结果显示氨磷汀组仅在腺体功能指标EF上明显优于对照组[MD=1.29,95% CI(0.14,2.44),P=0.03],差异有统计学意义;氨磷汀组在腺体功能指标ER上的优势和在UR30上的劣势不明显[MD=0.96,95%CI(-0.69,2.61),P=0.25]、 [MD=0.01,95% CI(-0.05,0.07),P=0.69],差异无统计学意义。为检验合并结果的稳定性,采用固定效应模型再次合并,结果氨磷汀组在指标EF、ER上明显优于对照组,提示结果不稳健,必须审慎地看待本结论。
2.4.4 急性黏膜炎的发生率 6篇研究[8-9,11-14]报告了急性黏膜炎的发生率,共纳入763例患者,根据严重程度进行亚组分析,两组间急性黏膜炎、3级以上急性黏膜炎的异质性I2分别为77%、65%,采用随机效应模型分析,结果显示氨磷汀组与对照组在减少急性黏膜炎、3级以上急性黏膜炎方面差异均无统计学意义[RR=0.97,95% CI(0.92,1.02),P=0.29]、[RR=0.96,95% CI(0.74,1.24),P=0.73](图6)。

图6 氨磷汀组与对照组放疗后急性黏膜炎的Meta分析Fig 6 Meta-analysis of acute mucositis after radiotherapy in amifostine group and control group
2.4.5 次要结局指标 在恶心、呕吐症状方面,Meta分析结果显示:氨磷汀组恶心、呕吐症状的总体发生率和严重程度均明显高于对照组,差异均有统计学意义。
在低血压和过敏反应方面,Meta分析结果显示:氨磷汀组低血压和过敏反应的总体发生率均明显高于对照组,差异有统计学意义;两组间3级以上(≥3级)低血压、过敏反应的发生率差异无统计学意义。
在患者肿瘤局部区域控制和总体生存方面,Meta分析结果显示:氨磷汀组和对照组的1、2年局部区域控制率和总体生存率差异均无统计学意义。仅有1项研究[14]报告了4年总体生存率,两组间差异仍无统计学意义。各次要结局指标见表3。
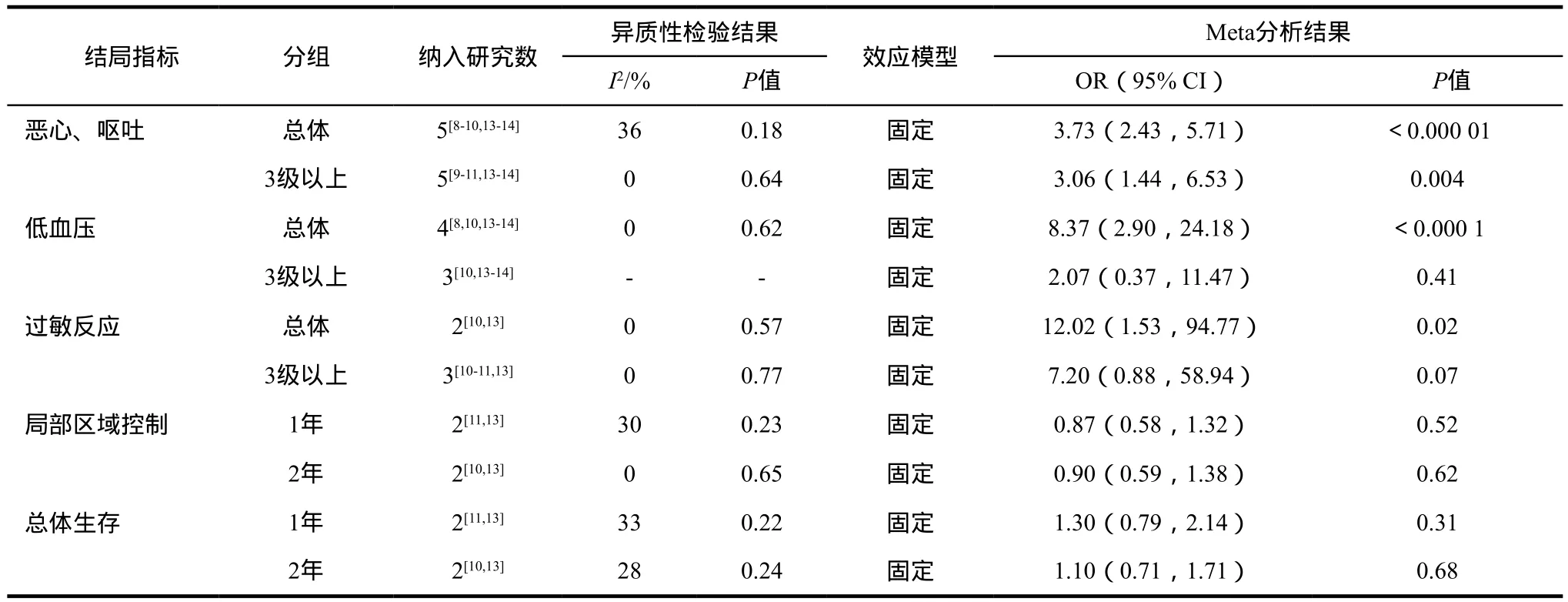
表3 次要结局指标的Meta分析Tab 3 Meta analysis of secondary outcomes
2.5 GRADE证据分级评价结果
对各结局指标进行GRADE评价,其中2级以上急性口干发生率、恶心呕吐发生率、过敏反应发生率、局部区域控制率、总体生存率为中等质量证据,2级以上晚期口干发生率、急性黏膜炎发生率、低血压发生率为低质量证据,而腺体功能指标为极低质量证据。证据降级的主要原因为原始研究存在随机化、盲法缺失嫌疑等(表4)。

表4 结局指标的GRADE证据评级Tab 4 Outcomes of GRADE evidence evaluation
3 讨论
经放射治疗联合(或不联合)化学治疗、手术的头颈部癌症患者生存率高,即使是晚期,其5年无转移生存率约为50%[4],而人乳头瘤病毒(human papilloma virus,HPV)相关的晚期头颈部癌症患者5年生存率高达90%,放射治疗后口干可为永久性的,是大多数幸存患者的主要问题[17],可多方面降低患者的生活质量,尤其对夜间睡眠和口腔健康会产生灾难性的影响[17-18],因此通过改善口干提高患者生存质量是亟待解决的问题。氨磷汀(WR-2721)是一种理论上使正常组织免受放化疗影响而不保护肿瘤组织的细胞保护剂,1996年经美国FDA批准上市[12],2002年美国临床肿瘤学会专家小组指出可考虑将其用于降低头颈部癌症患者放射治疗后急性和晚期口干[19],但自该药开发以来,其有效性和安全性一直在广泛热议中,尚无定论,故本研究继续就氨磷汀对头颈部癌症放射治疗后口干、黏膜炎、不良反应等方面进行探讨。
本研究结果表明氨磷汀可减少头颈部癌症患者放射治疗后中重度口干,但效果仅体现在放射治疗急性期和放射治疗结束后6个月,在放射治疗结束后12个月、24个月的时间点上则无优势,这与Cochrane图书馆2017年发布的系统评价[2]结果“氨磷汀可能减少了放射治疗结束至3个月的中重度口干,但无足够证据表明这种作用能持续到12个月”基本一致;Ma等[20]的系统评价则指出氨磷汀可降低长期口干的风险,但并未指出具体时间。在放射性黏膜炎方面,本研究发现氨磷汀似有减少急性黏膜发生及缓解黏膜炎严重程度的倾向,但无统计学意义。Sasse等[21]的研究指出氨磷汀可减少放射治疗期间黏膜炎的发生,Gu等[22]的研究指出氨磷汀可减少头颈部鳞状细胞癌患者放射性重度黏膜炎的发生,也有研究[23]指出没有足够的证据表明氨磷汀能减少放射性黏膜炎的发生。氨磷汀对放射性毒性反应的干预作用一直存有争议,目前对该药减少口干和黏膜炎的作用机制不明,似乎是因为唾液腺等正常组织对该药物及其代谢产物的更高吸收和保留而免受放射、化学治疗影响,且可清除放射治疗时体内过多的自由基,加快DNA修复、逆转细胞损害。
本研究显示氨磷汀对减少放射治疗结束6个月内的口干有效,但在腺体功能指标上的优势并无统计学意义,这是因为唾液腺功能障碍主观表现为口干感觉,客观表现为唾液腺功能减退(唾液流量减少),但口干表现与唾液腺功能减退表现并不一定对等[2],头颈部癌症患者放射治疗后唾液量在前3个月内下降最多,改善时间长达36个月以上[18]。
氨磷汀最常见的不良反应为恶心呕吐、短暂性低血压、过敏反应,一般通过药物控制可得到有效控制,本研究与以往的研究[20,22]结果相似,显示氨磷汀组和对照组这3种不良反应的发生率分别为45.8%、20.4%,12.6%、1.3%,5.6%、0%,其中3级以上不良反应的发生率分别为9.6%、3.5%,2%、0%,2.4%、0%,但氨磷汀不良反应仍会导致患者中断或退出原治疗计划,由于文献对该方面数据记录不详,本研究没有进行定量分析,另外3级以上不良反应并不能杜绝,临床使用需谨慎。
氨磷汀的细胞保护作用具有高选择性,主要分布在正常组织中而不易进入肿瘤组织,本研究与以往研究[24]结果相似,均表明氨磷汀对肿瘤组织无保护作用、不影响患者的生存率。
本研究的局限性:1)检索策略较完善,但仅纳入已发表的中、英文文献,且个别文献[10,13]提取的数据是通过间接转化而得,可能存在一定偏倚;2)研究对象肿瘤原发部位、进展程度、放射治疗方式等不一致,可能存在纳入研究基线不一致的情况;3)纳入9项研究,数量较少未予漏斗图评价发表偏倚,且关键结局指标的证据质量为中、低等。
综上所述,当前证据表明放射治疗前注射氨磷汀可减少头颈部癌症患者放射治疗结束后6个月内的中重度口干的发生,但对放射治疗后腺体功能、12个月之后的口干症和急性黏膜炎、肿瘤治疗效果无明显改善,且其不良反应值得关注,尚不支持临床推广应用。基于GRADE分级系统对证据质量的评价,本研究证据整体评价不高,还需更大样本、设计良好的临床研究来验证本结论。

