吉西他滨在胰腺癌联合治疗方案中的研究进展
石雪英 赵金
[摘要] 胰腺癌是目前恶性程度极高的肿瘤之一,因其发病隐匿,多数患者确诊时已发展为晚期,失去手术机会,因此,化疗成为晚期胰腺癌主要治疗措施。吉西他滨以其作用机制独特,毒性反应低,与其他化疗药物联合使用无交叉耐药等优点成为胰腺癌一线化疗药物。由于吉西他滨单药疗效有限,且存在大剂量使用出现毒副作用和耐药性等问题,国内外学者不断探索吉西他滨联合用药以及吉西他滨纳米载体药物递送等技术,以提高胰腺癌患者的生存期和生存质量。
[关键词] 吉西他滨;胰腺癌;联合化疗
[中图分类号] R453 [文献标识码] A [文章编号] 1673-7210(2020)07(c)-0050-04
Research progress of Gemcitabine in combined therapy of pancreatic cancer
SHI Xueying ZHAO Jin
Department of General Surgery, Baogang Hospital of Inner Mongolia, Inner Mongolia Autonomous Region, Baotou 014010, China
[Abstract] Pancreatic cancer is one of the most aggressive tumors at present. Because of its occult incidence, most patients have been diagnosed as advanced stage and lost the opportunity of operation. Therefore, chemotherapy has become the main treatment for advanced pancreatic cancer. Gemcitabine has become the first-line chemotherapy drug for pancreatic cancer because of its unique mechanism, low toxicity, and no cross resistance when combined with other chemotherapy drugs. Due to the limited efficacy of Gemcitabine alone, and the problems of large dose use of side effects and drug resistance, domestic and foreign scholars continue to explore the combination of Gemcitabine and Gemcitabine nano carrier drug delivery technology for improving the survival period and quality of life of patients with pancreatic cancer.
[Key words] Gemcitabine; Pancreatic cancer; Combined chemotherapy
胰腺癌是目前惡性程度极高的肿瘤之一,位居世界癌症相关死亡第四位,目前最佳的治疗手段是手术切除、化疗和放疗辅助治疗,然而因其发病隐匿,发展速度快,80%以上患者就诊时已发展为晚期,手术预后不理想或失去手术价值,因此更多的研究者把重心集中在化疗药物开发、联合应用方案和抗耐药性的研究上。吉西他滨作为癌症一线化疗药物,在胰腺癌治疗方案中被广泛应用,疗效优于其他化疗药物,备受肿瘤研究者关注。
1 吉西他滨结构及作用机制
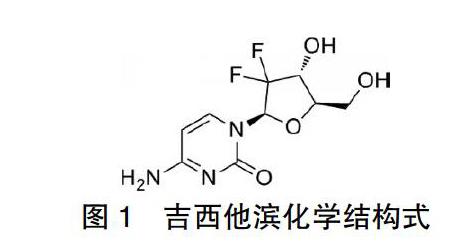
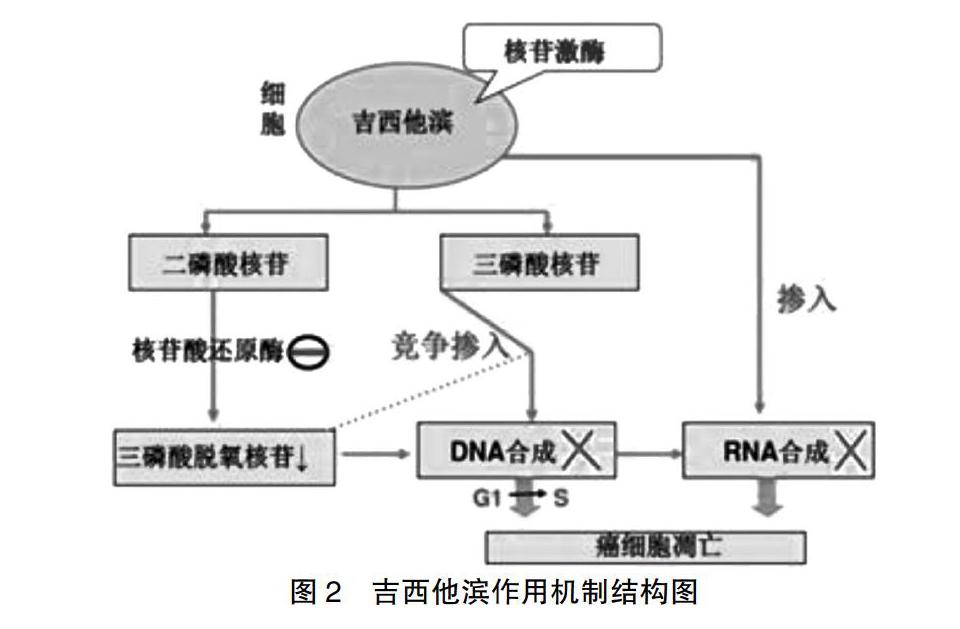
吉西他滨是近年来人工合成的嘧啶核苷衍生物,属于二氟核苷类抗代谢水溶性药物,分子式为C9H11F2N3O4(图1),吉西他滨的主要作用机制是诱导DNA损伤和抑制DNA合成。吉西他滨作为前体药物进入细胞后经过两次磷酸化,其代谢产物二磷酸盐和三磷酸盐在细胞内积聚并竞争性渗入DNA双链,且主要作用于G1/S期,抑制DNA复制,而DNA合成所需的DNA解旋酶继续向前解旋,导致双链DNA变成单链DNA,单链DNA失去保护引起DNA损伤,最终导致细胞死亡(图2)。同时吉西他滨代谢产物可抑制核苷酸还原酶,降低细胞内脱氧核苷三磷酸酯生成,此外代谢产物还可抑制脱氧胞嘧啶脱氨酶,使细胞内代谢物降解降低,达到抗肿瘤的目的,对多种实体瘤均有效[1-2]。因其作用机制独特、毒性反应低、与其他化疗药物联合使用无交叉耐药性且毒副作用无累加等特点,成为20世纪90年代末多种恶性肿瘤辅助化疗方案的金标准药物[3]。
2 吉西他滨在胰腺癌治疗中的研究进展
2.1 吉西他滨在胰腺癌治疗中的优势和不足
吉西他滨是由美国Lily公司在1983年研发,1996年美国食品药品管理局批准该药投入临床使用,1999年正式进入中国,目前是许多实体瘤如非小细胞肺癌、胰腺癌、乳腺癌、膀胱癌等一线化疗药物。由于吉西他滨在肿瘤治疗中效果优于其他种类的化疗药,近30年来,吉西他滨逐渐成为国内外肿瘤研究学者关注的热点。1990年,Lilly研究实验室Hertel LW报道吉西他滨对各种恶性肿瘤均有疗效,是恶性肿瘤治疗的优选药物;1997年美国癌症治疗中心Burris在临床研究中比较吉西他滨与传统化疗药5-氟尿嘧啶(5-Fu)对胰腺癌治疗效果发现,临床受益率(包括体力状况上升、体重增加、疼痛减轻)分别是23.8%和4.8%,中位生存期分别为5.65个月和4.41个月,中位无进展生存期分别为2.33个月和0.92个月,1年生存期分别为18%和2%[4]。鉴于吉西他滨治疗晚期胰腺癌优势明显,美国食品药品管理局批准吉西他滨作为胰腺癌的一线化疗用药。
3 吉西他滨在胰腺癌术前新辅助治疗(NAT)中的应用
吉西他滨不仅在非手术治疗中发挥重要作用,而且在目前越来越被国际重视的NAT中至关重要。业内研究者普遍认为胰腺癌术前NAT主要有以下作用[23]:①控制肿瘤发展速度,缩小瘤荷,提高手术切除成功率;②通过评估术前化疗效果,预测患者手术结果,对术后预后可能极差的患者停止手术治疗方案;③降低肿瘤发展期,提高手术治疗的机会[24]。美国国家肿瘤数据回顾性分析(2004—2012年非转移性胰腺癌手术治疗)发现,在Ⅲ期胰腺癌中,基于吉西他滨联合化疗的术前新辅助治疗可明显改善中位生存期[25]。吉西他滨联合顺铂的新辅助化疗可改善患者的生活质量和营养状态,患者的无瘤生存期及总生存期均良好。2014年,一项美国癌症中心的前瞻性研究发现,應用吉西他滨联合奥沙利铂作为新辅助化疗方案,38例可切除胰腺癌患者的中位生存期达30.6个月[13]。日本东北大学的临床研究发现,吉西他滨联合替吉奥口服,中位生存期达34.7个月[24]。胰腺癌NAT化疗方案不断优化改良,寻找高等级循证医学证据和最佳治疗方案,到目前为止吉西他滨在多数NAT方案中发挥重要作用。
4 应用前景展望
吉西他滨自问世以来,由于其良好的广谱抗癌作用成为癌症治疗的一线药物,特别是对化疗不敏感的晚期和转移性胰腺癌效果较好,备受癌症治疗者的青睐和关注。在临床实践研究中不断优化治疗方案,从最初的单药治疗到联合治疗方案,癌症术前NAT,再到研发吉西他滨共载制剂,不断推动胰腺癌的治疗进程,提高胰腺癌患者生存时间和生存质量。相信不久的将来一定会开发出毒性低、治疗效果好、半衰期长的吉西他滨合成制剂,在抗癌一线发挥更好的作用。特别是近年来正在研究的Gem纳米共载技术将不断克服其毒性作用,势必为胰腺癌患者带来更加安全有效的治疗方案。
[参考文献]
[1] 陈煜.吉西他滨与多西他赛对老年晚期非小细胞肺癌的治疗效果分析[J].中外医学研究,2019,17(12):11-13.
[2] 王大志,陈娜,郭成业.GP与TP方案治疗晚期老年非小细胞肺癌的临床对比研究[J].中国医药指南,2014,12(21):134-136.
[3] Kamisawa T,Wood LD,Itoi T,et al. Pancreatic cancer [J]. Lancet,2016,388(10039):73-85.
[4] Parhi P,Mohanty C,Sahoo SK. Nanotechnology-based combinational drug delivery: an emerging approach for cancer therapy [J]. Drug Discov Today,2012,17(17/18):1044-1052.
[5] 罗芳,王丹,夏桂民.抗癌药物吉西他滨纳米递送系统研究进展[J].中国医药生物技术,2019,14(1):83-88.
[6] 张彩霞,林能明.吉西他滨药代动力学研究进展[J].肿瘤学杂志,2004,10(4):271-274.
[7] 谢燕鸣,王连心,王永炎.临床联合用药机制研究探讨[J].中国中药杂志,2014,39(18):3424-3426.
[8] Maksimenko A,Caron J,Mougin J,et al. Gemcitabine based therapy for pancreatic cancer using the squalenoyl nucleoside monophosphate nanoassemblies [J]. Int J Pharm,2015, 482(1/2):38-46.
[9] 王琳,秦叔逵,邵志坚.吉西他滨治疗晚期癌症[J].南京军医学院学报,2002,24(2):144-145.
[10] 石海峰,金征宇,周智强,等.经动脉灌注盐酸盐酸吉西他滨和5-氟尿嘧啶治疗中晚期胰腺癌的疗效分析[J].中华放射学杂志,2002,36(12):1072-1074.
[11] 束永前,刘凌翔,黄普文,等.盐酸吉西他滨联合顺铂或氟尿嘧啶治疗晚期胰腺癌临床疗效的比较[J].实用癌症杂志,2003(5):527-530.
[12] 丁昂,童赛雄,靳大勇,等.125Ⅰ粒子和125Ⅰ+盐酸吉西他滨在治疗局部进展期胰腺癌中的比较[J].肝胆胰外科杂志,2004(1):19-22.
[13] Sahoo RK,Kumar L. Albumin-bound paclitaxel plus gemcitabine in pancreatic cancer [J]. N Engl J Med,2014,370(5):479.
[14] Goldenstein D,El-Maraghi RH,Hammel P,et al. Nab-paclitaxel plus gemcitabine for metastatic pancreatic cancer:long-term survival from a phase Ⅲ trial [J]. J Natl Cancer Inst,2015,107(2):dju413.
[15] 梁延波.胰腺癌新辅助治疗的现状与展望[J].临床肝胆病杂志,2019,35(5):946-952.
[16] 刘元芬,周咏梅.紫杉醇与吉西他滨联合抗肿瘤作用机制及共载给药系统的研究进展[J].中国新药杂志,2019, 28(9):1081-1086.
[17] Takahata T,Sato A,Yu C,et al. Retrospective Analysis of Weekly Paclitaxel Chemotherapy for Gemcitabine-and S-1-Resistant Pancreatic Cancer [J]. Gan To Kagaku Ryoho,2018,45(5):817-821.
[18] 刘芸云.吉西他滨+替吉奧共同治疗晚期胰腺癌的临床分析[J].临床医药文献电子杂志,2019,6(39):64.
[19] 张波,张娜.纳米载体共递送化疗药物用于肿瘤联合治疗的研究进展[J].中国新药杂志,2014,23(21):2514-2520.
[20] Poon C,He C,Liu D,et al. Self-assembled nanoscale coordination polymers carrying oxaliplatin and gemcitabine for synergistic combination therapy of pancreatic cancer [J]. Control Release,2015,201:90-99.
[21] Saneja A,Dubey RD,Alam N,et al. Co-formulation of p-glycoprotein substrate and inhibitor in nanocarriers: an emerging strategy for cancer chemotherapy [J]. Curr Cancer Drug Targets,2014,14(5):419-433.
[22] Zhao X,Li F,Li Y,et al. Co-delivery of HIF1α siRNA and gemcitabine via biocompatible lipid-polymer hybrid nan-oparticles for effective treatment of pancreatic cancer [J]. Biomaterials,2015,46:13-25.
[23] Du L,Wang-Gillam A. Trends in neoadjuvant approaches in pancreatic cancer [J]. J Natl Compr Canc Netw,2017,15(8):1070-1077.
[24] Heinrich S,Pestalozzi BC,Sch?覿fer M,et al. Prospective phase Ⅱ trial of neoadjuvant chemotherapy with gemcitabine and cisplatin for resectable adenocarcinoma of the pancreatic head [J]. J Clin Oncol,2008,26(15):2526-2531.
[25] de Geus SW,Eskander MF,Bliss LA,et al. Neoadjuvant therapy versus upfront surgery for resected pancreatic adenocarcinoma A nationwide propensity score matched analysis [J]. Surgery,2017,161(3):592-601.
(收稿日期:2019-12-03)

