酒精性肾损伤的发病机制
张历涵 综述 付 平 审校
酒精(乙醇)是一种被普遍滥用的物质,已有多项研究证明酒精会导致多种器官和组织损伤。2016年行为健康统计和质量中心数据显示,在美国12岁及以上人群中有1 570万受到其影响[1]。此外,世界卫生组织的数据显示,2016年,依赖和过量使用酒精导致全球约300万人死亡(占所有死亡人数的5.3%),经年龄调整的酒精导致的死亡人数为38.8人/10万人口[2]。美国CDC的数据显示,2017年,由酒精导致的死亡率在1999年~2017年期间达到最高比率,为9.6人/10万人口。45~64岁年龄组的酒精引起的死亡率从1999年的17.3人/10万人口上升到2017年的26.0人/10万人口[3]。
现有证据表明,酒精与肝硬化、肝癌、胰腺炎和心血管并发症的发病率和死亡率增加相关。然而到目前为止,还没有足够的流行病学证据将酒精与慢性肾脏疾病(chronic kidney disease,CKD)联系起来。一些临床前研究表明,饮酒对肾脏有很大影响,主要表现为肾小球滤过率下降,血清肌酐及尿素氮升高以及蛋白尿[2],并提出可能存在一个独立的病理类型,称之为“酒精性肾损伤”。
在其他器官和组织中完成的研究表明,酒精可能会通过某些特定机制导致肾功能障碍,例如可能与乙醇诱导的氧化应激和促炎改变有关。此外,肾脏和其他器官(包括肝脏、肠道、骨骼肌和心血管系统)之间的相互作用可能会使情况变得更加复杂(图1)。本文简要回顾了支持这些假说的证据。
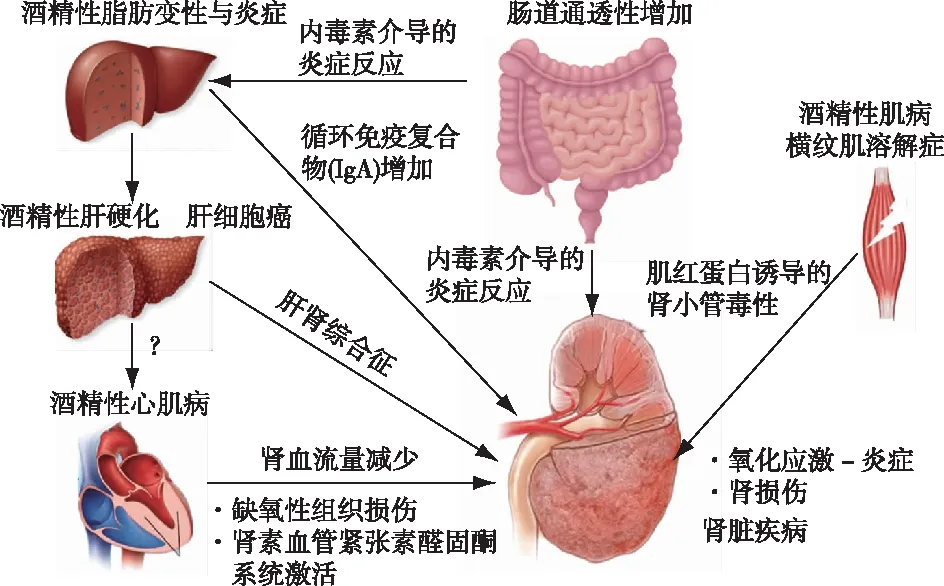
图1 酒精性肾损伤的可能机制
酒精与肾脏疾病:流行病学的证据
流行病学表明,长期饮用大量酒精的人比少量饮用酒精的人发生心脏病的风险更高,而心血管疾病又是CKD发展的主要危险因素之一。也就是说,饮酒与CKD之间可能存在一定关系,然而流行病学数据尚未证实。一项Meta分析[4]的结果就与该观点不符。该研究纳入了20项研究,共292 431例患者。结果显示,在大量饮酒的患者中,CKD、蛋白尿和终末期肾脏疾病的汇集风险比分别为0.83、0.85和1.00,这表明重度酒精消费者发生肾脏疾病的风险降低或没有风险。其他研究也报告了类似的结果,表明重度饮酒者(每周饮酒超过210g)的肾病发病率与适度饮酒者(每周饮酒70~210g)相当,甚至更低[5]。在东南亚人口中也观察到了类似结果,在日本身体健康的男性中,饮酒频率与CKD发生率呈负相关[6]。另一项日本研究表明每天<19g的饮酒会降低蛋白尿的风险[7]。
相反,另一些研究发现,大量饮酒可能预示着CKD患者的预后较差。例如,White等[8]报告称,酗酒者(每周饮酒超过30g)发生蛋白尿的风险更高。日本学者Yamagata等[9]和意大利学者Buja等[10]进行的队列研究显示,饮酒和蛋白尿发病率之间呈U型关系。台湾的一项队列研究显示长期酒精摄入与CKD发生的风险增加相关(HR=1.62,95%CI 1.46~1.81)。这些矛盾的发现可能是由于不同类型的酒精饮料对肾脏影响不同,也可能是不同国家饮酒模式存在差异的结果。
酒精性肾损伤的直接机制:实验研究的启示
饮酒导致肾脏疾病的机制尚不明确,但现有一些研究为其可能的机制提供了相应的证据。酒精本身可能会导致肾脏疾病,也可能是细胞分解(或代谢)酒精时形成的过量中间产物引起的,包括乙醛、还原型辅酶Ⅰ(nicotinamide adenine dinucleotide,NADH)和自由基。这些与酒精相关的细胞病理生理变化与许多器官的损伤有关,并可能在肾脏损伤中发挥作用。此外,器官之间复杂的相互作用可能会使过量饮酒的患者的肾脏病状进一步复杂化和加重。
氧化应激自由基也称为活性氧簇(reactive oxygen species,ROS),是酒精代谢的副产物之一,会导致细胞损伤。当人体无法迅速地清除过量生成的自由基时,就会发生氧化应激,这在引发酒精相关的组织损伤中起着关键作用。研究表明,酒精可通过多种机制在受损害器官(如肝脏、心脏和肾脏)中产生ROS,包括非酶机制(如线粒体电子传递链功能异常)[11]以及酶机制[如NADPH氧化酶和细胞色素P4502E1酶( CYP2E1)]。
乙醇在体内通过三条途径代谢,分别是乙醇脱氢酶、乙醛脱氢酶和CYP2E1。长期摄入酒精的患者体内乙醇氧化酶系统会发生重构,CYP2E1代谢途径逐渐占主导地位。乙醇在CYP2E1的作用下,会大量生成氧活性自由基,如超氧阴离子自由基和过氧化氢等,这是引发组织氧化应激和损伤的重要途径[12]。 CYP2E1主要在肝脏中表达,但在慢性乙醇消耗期间,乙醇也会诱导肾脏表达CYP2E1。有趣的是,研究发现,乙醇对肾脏表达CYP2E1的诱导作用比其对肝脏的作用更强[13]。CYP2E1在肾脏的大量表达会导致氧化应激,从而改变了细胞膜上磷脂的结构。这种修饰过的磷脂可能会激活中性粒细胞,进一步加剧氧化应激,形成恶性循环[12]。Latchoumycandane等[14]报道CYP2E1对乙醇的氧化会产生足够的ROS,进而成为血小板活化因子受体(platelet-activating Factor receptor,PTAFR)激动剂。肾脏大量表达PTAFR与肾损伤和纤维化密切相关。
研究表明,乙醇的摄入可能增加肾脏其他潜在自由基的表达,与一氧化氮合酶的酶家族有关[15]。一氧化氮合酶促进一氧化氮的产生,如果产生过量,则可以与其他分子发生反应并产生自由基,从而触发肾脏的组织损伤[16]。Tirapelli等[15]研究发现,酒精增加了两种一氧化氮合酶的表达,促进氮氧化物及其活性代谢物过氧亚硝酸盐(ONOO-)通过阴离子通道穿过细胞膜,并通过酪氨酸硝化使许多重要的蛋白质和酶失活。然而,目前还不清楚乙醇是如何上调一氧化氮合酶的。一种可能的机制是乙醇增加肠道通透性,使内毒素从肠道释放到血液循环中,并激活了一氧化氮合酶的表达。另一种理论表明,由于氧化或缺乏关键的辅酶(例如四氢生物蝶呤),两种一氧化氮合酶都可能经历解偶联过程。解偶联最终产生破坏性的活性氧,如超氧阴离子,而非维持肾脏正常血液流动的血管松弛剂一氧化氮。
酒精代谢衍生中间体除了氧化应激,越来越多的证据表明,一些非氧化机制也会导致酒精相关的器官损伤。具体地说,乙醇会在不同的器官中代谢产生脂肪酸乙酯,从而引起器官损伤,主要表现为抑制细胞生长及蛋白质合成,诱导细胞凋亡等方面。Loftus等[17]使用液相色谱-串联质谱法进行代谢组学分析发现,与对照组相比,酒精处理的小鼠和大鼠样品的肝脂质谱有显著差异,主要是脂肪酸乙酯,脂肪酰基,甘油脂和磷脂酰乙醇同系物。
乙醇的新陈代谢会产生大量的醋酸盐,然后并入乙酰辅酶A,这是一种参与蛋白质、脂质和碳水化合物新陈代谢的分子。这会导致系统新陈代谢的重新编程。蛋白质乙酰化(在蛋白质上添加乙酰基)是调节线粒体控制的过程中不可或缺的部分,包括脂肪酸代谢和抗氧化防御[18]。我们目前的理解是,关键蛋白如线粒体生物发生的主要调节者过氧化物酶体增殖物激活受体γ共激活因子1α(peroxisome proliferator activated receptor γ coactivator-1α,PGC-1α)的赖氨酸乙酰化和去乙酰化的平衡至少部分地触发了转换营养失衡情况下的代谢状态[19]。Harris等[20]研究表明,乙醇诱导肾脏线粒体蛋白过度乙酰化(通过蛋白质赖氨酸残基的乙酰化过度修饰),这可能会干扰某些参与酒精代谢或防御氧化应激的线粒体蛋白的功能(如超氧化物歧化酶2、乙醛脱氢酶2、谷胱甘肽过氧化物酶)。这也可能是导致乙醇诱导的肾脏线粒体功能障碍的另一个重要因素。
酒精性肾损伤的间接机制:其他器官损伤
肠道损伤酒精性肠道损伤和黏膜细菌内毒素(LPS)移位增加在酒精性肝损伤的发生、发展以及其他酒精相关疾病的发病机制中起着至关重要的作用[21]。Liangpunsakul等[22]的研究表明,与对照组相比,饮酒过量的人群的循环内毒素水平更高。LPS是脓毒症最重要的来源之一,可导致“细胞因子风暴”,氧化应激加剧,肾灌注不足,血压降低,并最终逐渐降低肾功能[23]。此外通过肠道释放的内毒素引起的固有免疫系统的激活也可能在肾脏损害的发展中起着核心作用[22]。
大量的实验和临床证据表明,过量饮酒引起的肠道通透性增加和内毒素释放会导致循环IgA水平升高[24],IgA是一种对黏膜免疫反应至关重要的抗体。肾脏对的IgA负荷增加特别敏感。事实上,IgA肾病是全世界最常见的原发性肾小球肾炎类型之一。研究表明,饮酒史与IgA肾病患者进展成为终末期肾病的风险增加独立相关(OR 1.32,P<0.05)[25]。
也有证据表明,酒精对肝脏的损害,特别是晚期肝硬化,会导致肝肾综合征(HRS),这是一种与循环障碍有关的肾功能恶化。尽管血管收缩剂和血管扩张剂因子之间的平衡改变可能起着重要作用,但涉及HRS发生和发展的潜在机制尚不完全清楚。
骨骼肌病过量饮酒通常与各种急性或慢性肌肉症状相关。急性酒精性肌病的特征是受累肌肉无力,疼痛,压痛和肿胀等,它通常是由于一次性过量饮酒,血液中的酒精水平达到0.08 g/dl或更高而引起的。相反,慢性酒精性肌病的最常见表现为数周至数月的进行性近端肌无力。在慢性酒精性肌病中,一个人的整体肌肉质量可能会减少多达三分之一,也是工业化国家中最常见的骨骼肌疾病,以不同的严重程度表现在大约一半的酗酒者中[26]。迄今为止,还没有研究证实急性酒精性肌病和肾脏损伤之间是否有直接联系,但目前存在几项研究表明两者之间可能是有关联的。
尽管酒精性肌病的机制还不完全清楚,但线粒体相关能量稳态的破坏很可能是促进肌细胞损伤的重要因素[27]。在极少数营养不良的慢性酒精中毒的病例中,也可能发生急性酒精性肌病,即急性酒精性坏死性肌病或酒精性横纹肌溶解症[28]。
一些研究已经将横纹肌溶解和肌红蛋白毒性与急性肾损伤联系起来,支持饮酒、酒精相关的急性肌病和肾损害之间可能存在联系。例如,Belliere等[29]表明横纹肌溶解和肾脏中过度的巨噬细胞浸润之间存在联系,这反过来又导致促炎标记物的表达进而造成组织损伤。Plotnikov等[30]另一项研究显示,从大鼠肾脏分离的线粒体在与肌红蛋白中孵育时会受到氧化应激的破坏。这一发现表明横纹肌溶解和肌红蛋白毒性可能通过线粒体损伤引发肾脏的氧化应激。
心肌病几项流行病学研究表明,轻度饮酒可以降低冠心病的风险,从而有益于心血管健康[31]。相反,大量饮酒会导致非缺血性扩张型心肌病的发生,并显著增加心脏性猝死的风险[32]。有研究表明,酒精代谢产生的大量活性氧及活性氮物质会导致心肌细胞中参与心肌收缩、代谢、抗氧化防御等关键蛋白氧化或硝化,并通过激活炎症反应诱导心肌肥厚、纤维化,或通过诱导凋亡和自噬失调等机制导致心肌细胞死亡。
慢性或急性心力衰竭可导致肾脏慢性或急性功能障碍,称为心肾综合征(CRS)。复杂的肾脏病理生理反应导致组织内液体堆积、缺血性损伤、外周血管收缩,以及肾素-血管紧张素-醛固酮系统(RAAS)的激活[33]。RAAS的过度激活有助于激活NADPH氧化酶和其他代谢氧化酶,产生超氧阴离子和其他自由基,进一步加剧了慢性酒精中毒的氧化应激[34]。
其他酒精性肾脏损伤还可能会对机体代谢产生多种负面影响,如随着肾脏滤过率的下降,患者体内的致动脉粥样硬化性脂蛋白(如载脂蛋白A)增加,并形成更致密的胆固醇分子,降低脂蛋白脂肪酶活性,进而加剧脂质在肝脏的堆积[35]。
此外,长期摄入乙醇会导致肾脏合成1,25-二羟维生素D3的功能受损或其降解速率增加,进而影响其他多个器官的功能,例如增加癌症风险,免疫功能障碍等,形成恶性循环。
酒精性肾损伤的治疗
尽管临床前和人体研究都强调了氧化应激和炎症在触发和推动与酒精性肾损伤相关的病理过程中的中心作用,但针对酒精性肾损伤的治疗在很大程度上仍然是对症治疗。对该疾病的早期诊断和严格戒酒对于减缓疾病的进展和恢复肾功能非常重要。
小结:如上所述,关于酒精性肾病及酒精导致多个器官之间的复杂相互作用,仍然有很多需要深入了解之处。尽管研究表明酒精可能存在直接或间接影响肾脏的多种潜在机制,但仍有待进一步验证。未来的研究有望探索这些假说,以更好地理解酒精性肾损伤。

