温敏性水凝胶抑制间充质干细胞凋亡并促进旁分泌及过表达FTH的细胞MRI的实验研究
赖丽莎?郭媛?梁莹莹?胡晓俊?卢雄

【摘要】目的 探討过表达铁蛋白重链(FTH)的间充质干细胞(UE7T-13)进行体外MRI的可行性,并验证温敏性水凝胶HA-F127复合UE7T-13是否可抑制其凋亡、促进细胞因子分泌。方法 构建携带FTH-绿色荧光蛋白(GFP)基因的慢病毒载体并感染UE7T-13,检测感染后的GFP阳性率及FTH表达水平。同时,HA-F127复合FTH/UE7T-13,细胞计数试剂盒(CCK8法)检测FTH慢病毒载体感染后和(或)水凝胶复合后的UE7T-13细胞增殖能力,并进行HA-F127复合FTH/UE7T-13的MRI。检测HA-F127复合对过氧化氢(H2O2) 诱导UE7T-13细胞凋亡的影响,ELISA检测IL-10、HGF含量。结果 FTH-GFP慢病毒载体可成功感染UE7T-13,48 h荧光显微镜观察GFP表达率几乎100%,FTH mRNA表达提高了3倍,FTH蛋白可随着时间延长表达增多并至5 d仍稳定高效表达。FTH感染或HA-F127复合均不影响UE7T-13增殖能力,不影响骨髓间充质干细胞的体外MRI。HA-F127复合UE7T-13可抑制H2O2介导的细胞凋亡,并促进IL-10、HGF细胞因子分泌。结论 过表达FTH实现UE7T-13的MRI示踪功能,温敏性水凝胶HA-F127可在过氧化损伤环境下抑制FTH/UE7T-13的凋亡,并促进其分泌IL-10、HGF,可为下一步实验奠定基础。
【关键词】骨髓间充质干细胞;铁蛋白重链;水凝胶;磁共振成像;凋亡
Experimental study of role of thermo-sensitive hydrogel in inhibiting apoptosis and promoting paracrine function of MSC and MRI of MSC overexpressing FTH Lai Lisha, Guo Yuan, Liang Yingying, Hu Xiaojun, Lu Xiong. Department of Radiology, Guangzhou First Peoples Hospital, School of Medicine, South China University of Technology, Guangzhou 510180, China
Corresponding author, Lu Xiong, E-mail: 122055667@ qq. com
【Abstract】Objective To explore the feasibility of in-vitro magnetic resonance imaging (MRI) for UE7T-13 overexpressing ferritin heavy chain (FTH), and investigate the role of thermo-sensitive hydrogel (HA-F127) in suppressing apoptosis and promoting paracrine function of UE7T-13. Methods Lentiviral vectors carrying FTH-GFP gene were established and transfected into UE7T-13. The positive rate of GFP expression and FTH expression level in FTH/UE7T-13 cells were evaluated. FTH/UE7T-13 was encapsulated in HA-F127. Cell Counting Kit-8 (CCK-8) was used to detect the cell proliferation of UE7T-13 after transfection and encapsulation. MRI of the HA-F127-encapsulated FTH/UE7T-13 was performed. The effect of HA-F127 upon the H2O2-induced UE7T-13 apoptosis was evaluated. The contents of IL-10 and HGF were quantitatively measured by using ELISA. Results Lentiviral vectors carrying FTH-GFP gene were successfully transfected into UE7T-13. Fluorescent microscope revealed that the GFP expression rate was almost 100% at 48 hours and the expression level of FTH mRNA was up-regulated by three times. The expression of FTH protein was up-regulated over time and stably expressed for 5 days after transfection. FTH transfection and HA-F127 encapsulation exerted no effect on the proliferation ability of UE7T-13 or the MRI of mesenchymal stem cell. HA-F127 encapsulation could inhibit cell apoptosis induced by H2O2 and promote HGF and IL-10 secretion. Conclusions FTH over-expression can realize in-vitro MRI of UE7T-13. Thermo-sensitive hydrogel HA-F127 encapsulation can inhibit the apoptosis and enhance the HGF and IL-10 secretion of FTH/UE7T-13, which lay a basis for subsequent experiment.
【Key words】Mesenchymal stem cell;Ferritin heavy chain;Hydrogel;Magnetic resonance;
Apoptosis
我国慢性乙型肝炎患者约2000万,每年死于肝纤维化和肝癌的患者高达50万,是全球晚期肝病发病率最高的地区[1]。目前尚无有效治疗肝纤维化的临床方法,间充质干细胞(MSC)被认为具有修复肝纤维化的潜能[2]。前期实验表明,体内微环境影响MSC存活率,并且缺乏活体监测MSC的有效手段是阻碍MSC治疗从基础研究向临床移植治疗转化的关键[3-4]。本研究拟构建可活体MRI显像的过表达铁蛋白重链(FTH)的MSC(FTH/MSC),并体外证实其可实现MSC的MRI示踪功能,同时,通过构建功能化水凝胶(HA-F127)改善细胞外微环境,以提高MSC的存活率及旁分泌功能,为下一步实验奠定基础。
材料与方法
一、主要试剂和仪器
DMEM-LG 培养基(GIBCO),FTH基因质粒(广州永诺生物科技有限公司),CCK-8细胞计数试剂盒(日本同仁化学研究所),HGF、IL-10 ELISA试剂盒(RD公司),兔抗人FTH单克隆抗体、兔抗人GAPDH单克隆抗体(武汉博士德公司)。荧光显微镜(奥特BDS200-FL),酶标仪(Diatek公司),冷冻高速离心机(Hema TGL-16R),1.5T 磁共振成像仪(Signa Infinity Twinspeed,GE公司)。人永生化骨髓MSC UE7T-13(日本Mori等[5]惠赠):5%二氧化碳(CO2),37℃环境下,低糖DMEM培养基(含10%胎牛血清)培养(图1)。
二、慢病毒载体构建、病毒感染及基因表达检测
通过PCR进行FTH基因和IRES-绿色荧光蛋白(GFP)基因扩增,将二者连接后,与慢病毒载体LV003相连,构建LV003-FTH-IRES-GFP慢病毒载体进行测序鉴定;同时构建GFP慢病毒载体作为阴性对照(FTH/UE7T-13及GFP/UE7T-13)。采用脂质体法将重组载体感染人胚肾细胞293A(HEK-293A)进行包装,检测病毒滴度(TU/ml)。
将5×105 UE7T-13接种至6孔板,感染前更换新鲜培养液,根据预实验获得的最佳感染复数(3000 pfu/细胞)加入病毒液,混匀后置于细胞培养;于6 h更换新鲜培养液,每隔24 h观察细胞状态。
病毒感染后48 h,采用荧光显微镜观察GFP表达情况;定量PCR(Q-PCR)方法检测FTH mRNA水平,引物如下(FTH1-F:GACTCAGAG
GCCGCCATCAA;FTH1-R:AAGATTCGGCCA CCTCGTTG),使用2-ΔΔCt法[ΔCt = Ct(FTH) -Ct(GAPDH),△△Ct = Ct(FTH/UE7T-13) -Ct(UE7T-13)];采用蛋白免疫印迹法检测FTH慢病毒感染UE7T-13后1、2、3、5 d的FTH蛋白表达。
三、体外細胞MRI
分别将不同数量(1×103、1×104、1×105、1× 106、1×107、1×108)FTH/UE7T-13细胞进行体外MRI扫描。扫描方案:1.5 TMR,并采用内径12.7 cm的表面线圈,进行SE序列T2W扫描,参数:重复时间= 400 ms,回波时间= 100 ms,带宽20.83,NEX = 2.0,FOV = 20 cm×20 cm,层厚2 mm,矩阵384×256。
四、温敏水凝胶透明质酸(HA) -F127的制备、鉴定并复合FTH/UE7T-13
称取0.9 g的普朗尼克(Pluronic)F127分别和0.05、0.1、0.15、0.2、0.25 g 透明质酸钠混合,配制成质量分数为18%及分别含有不同浓度(1%、2%、2.3%、2.5%、3%、4%、5%)HA-F127溶液,使其可在37℃凝胶,成胶后采用扫描电镜观察凝胶(HA-F127)的三维结构。
收集生长状态良好的第3 ~ 5代慢病毒感染后UE7T-13,消化、离心后,用未凝固的水凝胶混合液重悬细胞沉淀,UE7T-13与HA-F127充分混合后,置于5% CO2、37℃细胞培养箱内,待凝固成胶体后,每孔再添加 200 μl含10%胎牛血清和1% 链霉素的 DMEM 细胞培养基。
细胞实验根据处理情况共分4组:A组(UE7T- 13),未感染的UE7T-13;B组(GFP/UE7T-13),空白载体载GFP感染的UE7T-13;C组(FTH/UE7T-13),FTH慢病毒感染的UE7T-13;D组(GEL-FTH/UE7T-13),HA-F127复合的FTH/UE7T-13,即凝胶组。
五、HA-F127复合及FTH感染对UE7T-13的成脂成骨分化能力检测
D组(GEL-FTH/UE7T-13)需先放入4℃冰箱中溶解凝胶,凝胶溶解后去除,并使用预冷的磷酸盐缓冲液(PBS)进行清洗,分别向培养板内加入成脂、成骨诱导分化培养基,分别采用油红O染色、茜素红染色,显微镜下观察标记后MSC的成脂、成骨分化情况。
六、CCK-8检测HA-F127复合FTH/UE7T-13的增殖率
4个处理组各取5×103个细胞,均匀接种于96孔板,于接种后第3日进行CCK-8,检测细胞增殖情况,以A组(UE7T-13)作为对照组,每次每组设3个复孔,取平均值。
七、HA-F127复合FTH/UE7T-13抗过氧化氢(H2O2)诱导细胞凋亡及促进细胞因子释放的检测
将C、D组细胞接种于6孔板,24 h后加入H2O2(50 μmol/L),调整终浓度为50 μmol/L,继续培养12 h;培养结束后,收集细胞进行流式凋亡检测。采用ELISA检测C组及D组上清液的肝细胞生长因子(HGF)、IL-10浓度:分别将2组5×105个细胞接种于6孔板,24 h后加入H2O2(50 μmol/L),继续培养12 h,取细胞上清液检测HGF、IL-10水平。
八、统计学处理
采用SPSS 19.0进行统计分析,数据以表示。两独立样本采用t检验进行组间比较。多组比较采用单因素方差分析。P < 0.05为差异有统计学意义。
结果
一、成功构建LV003-FTH-IRES-GFP慢病毒载体并转染UE7T-13
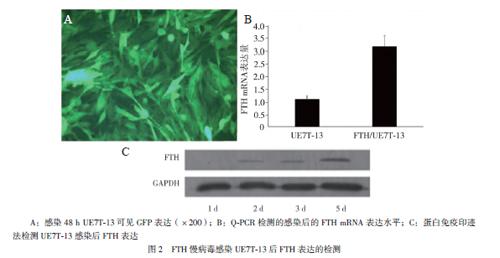
LV003-FTH-IRES-GFP慢病毒载体,并成功感染UE7T-13。感染293A 48 h后,细胞免疫法检测病毒滴度为1×109 TU/ml。FTH慢病毒感染UE7T-13 48 h后荧光显微镜下观察,GFP表达阳性率几乎100%(图2A);Q-PCR证实FTH慢病毒感染UE7T-13 48 h后FTH mRNA表达水平提高了3倍(P < 0.001);FTH慢病毒感染UE7T-13,FTH蛋白表达随着感染時间延长增多。
二、HA-F127可成功复合MSC,不影响细胞增殖能力
当F127浓度为18%,HA浓度为2.3%,HA-F127可在37℃凝固成胶(图3A)。CCK-8显示,4组细胞生长增殖情况比较差异无统计学意义(P = 0.809,图3B)。HA质量分数与凝胶化温度的关系见表1。
三、HA-F127复合FTH/UE7T-13的MRI
HA-F127复合FTH/UE7T-13后,利用FTH的T2负性对比效应,可检测MSC的T2负性对比,在磁共振T2加权图像上呈低信号。并且随着细胞数量的增加,MRI标准化信号强度逐渐降低(图4)。
四、HA-F127复合FTH/UE7T-13不影响其成骨成脂分化能力
水凝胶包裹FTH/UE7T-13洗脱后进行成骨成脂诱导:①茜素红染色显示FTH/UE7T-13大片深红色化合物,聚集部可见斑片状橘红色钙盐沉积(图5A);②油红O染色显示FTH/UE7T-13体积增大,胞浆内可见串珠状红色脂滴(图5B)。上述证明成骨成脂诱导成功。
五、HA-F127复合可抑制UE7T-13凋亡,并促进HGF及IL-10的旁分泌
经H2O2处理12 h后,D组细胞早期凋亡率为5.7%,晚期凋亡率为13.9%,C组细胞早期凋亡率为7.2%,晚期凋亡率为21.7%,D组细胞凋亡数量少于C组(图6A)。ELISA实验证实,D组的上清液中HGF及IL-10分泌较C组增加(HGF:148.4±15.9 vs. 42.9±3.9,t = -11.1,P < 0.001;IL-10:49.51±5.4 vs. 21.2±2.6,t = -5.7,P = 0.005;图6B)。
讨论
干细胞移植治疗终末期肝病越来越受到人们的关注[2]。然而,仍有研究指出MSC移植不能改善,甚至是促进肝纤维化,可能是肝纤维化体内微环境导致MSC活性降低或者死亡[6-7]。因此,如何改善移植后微环境,提高MSC存活率及增强旁分泌能力,可能是提高MSC移植治疗肝纤维化疗效的关键。因此本研究采用HA-F127复合MSC改善细胞生长微环境,增强MSC在H2O2过氧化损伤环境中的存活及旁分泌功能;同时,通过MRI分子影像技术,实现MSC的活体示踪的目的。
本实验使用人永生化骨髓MSC(UE7T-13),具有无限增殖能力并维持良好的细胞状态和功能,且同MSC一样易于接受外源性基因的导入[5]。本研究选择FTH的MRI报告基因实现MSC活体示踪的目的,因为其可利用内源性铁离子进行MRI,不依赖外源性铁剂,具有相对更高的MRI灵敏度[8]。细胞基因导入的转运载体选择非常重要,本研究选择慢病毒载体,可将大片段的目的基因整合靶细胞DNA,并使目的基因长时间稳定表达,同时,其引起的免疫反应小[9-10]。构建的LV003-FTH-IRES-GFP慢病毒表达载体感染UE7T-13 48 h后,可同时表达FTH和GFP,荧光显微镜下可见GFP表达几乎达100%,Q-PCR检测提示感染细胞中FTH mRNA的表达提高了3倍,蛋白免疫印迹法显示感染细胞中FTH可随着时间延长表达增多,并至5 d仍稳定高效表达,并被证实可用于MSC的体外MRI,这为下一步动物实验提供成像基础。
有研究者指出MSC治疗肝纤维化疗效欠佳,可能与肝纤维化微环境中存在的大量炎症因子,直接导致移植的MSC大量逃逸和死亡有关[3-4, 6-7]。HA和Pluronic F127制备的水凝胶(HA-F127)不仅具有良好的生物相容性和安全性,还具有温度敏感性,可用于常温下注射,并在37℃呈凝胶状,注射后能够构建MSC移植后生存的微环境,促进其滞留、存活及旁分泌等功能[11-13]。本研究证实,HA-F127在体外不影响FTH/UE7T-13的增殖能力,且不影响MSC的成脂成骨能力。
在H2O2诱导凋亡情况下,D组细胞凋亡率低于C组;同时证实在过氧化损伤情况下,D组细胞上清液中HGF及IL-10分泌较C组明显增多。上述结果可能与HA-F127改善细胞存在的微环境,促进MSC的存活而进一步增加其旁分泌功能有关,同时,HGF及IL-10作为抗凋亡及抗炎因子也发挥了抗过氧化而减少细胞损伤作用[14-15]。
综上所述,表达LV003-FTH-IRES-GFP慢病毒感染UE7T-13后可稳定高效表达FTH,可用于MSC的体外MRI,而且不影响UE7T-13分化增殖能力;同时,HA-F127可通过改善UE7T-13的微环境从而抑制MSC凋亡,提高旁分泌能力。该结果为本课题组进一步开展水凝胶复合MSC治疗肝纤维化提供了研究基础。
参 考 文 献
[1] Soriano V, Young B, Reau N. Report from the international Conference on Viral Hepatitis-2017. AIDS Rev,2018,20(1):58-70.
[2] Guo Y, Chen B, Chen LJ, Zhang CF, Xiang C. Current status and future prospects of mesenchymal stem cell therapy for liver fibrosis. J Zhejiang Univ Sci B,2016,17(11):831-841.
[3] Lai L, Chen J, Wei X, Huang M, Hu X, Yang R, Jiang X, Shan H. Transplantation of MSCs overexpressing HGF into a rat model of liver fibrosis. Mol Imaging Biol,2016,18(1):43-51.
[4] Carvalho AB, Quintanilha LF, Dias JV, Paredes BD, Mann-heimer EG, Carvalho FG, Asensi KD, Gutfilen B, Fonseca LM, Resende CM, Rezende GF, Takiya CM, de Carvalho AC, Goldenberg RC. Bone marrow multipotent mesenchymal stromal cells do not reduce fibrosis or improve function in a rat model of severe chronic liver injury. Stem Cells,2008,26(5):1307-1314.
[5] Mori T, Kiyono T, Imabayashi H, Takeda Y, Tsuchiya K, Miyoshi S, Makino H, Matsumoto K, Saito H, Ogawa S, Sakamoto M, Hata J, Umezawa A. Combination of hTERT and bmi-1, E6, or E7 induces prolongation of the life span of bone marrow stromal cells from an elderly donor without affecting their neurogenic potential. Mol Cell Biol,2005,25(12):5183-5195.
[6] Russo FP, Alison MR, Bigger BW, Amofah E, Florou A, Amin F, Bou-Gharios G, Jeffery R, Iredale JP, Forbes SJ. The bone marrow functionally contributes to liver fibrosis. Gastroenterology,2006,130(6):1807-1821.
[7] Mohamadnejad M, Alimoghaddam K, Bagheri M, Ashrafi M, Abdollahzadeh L, Akhlaghpoor S, Bashtar M, Ghavamzadeh A, Malekzadeh R. Randomized placebo-controlled trial of mesenchymal stem cell transplantation in decompensated cirrhosis. Liver Int,2013,33(10):1490-1496.
[8] Vandsburger MH, Radoul M, Cohen B, Neeman M. MRI reporter genes: applications for imaging of cell survival, proliferation, migration and differentiation. NMR Biomed,2013,26(7):872-884.
[9] Lundstrom K. Latest development in viral vectors for gene therapy. Trends Biotechnol,2003,21(3):117-122.
[10] Vigna E, Naldini L. Lentiviral vectors: excellent tools for experimental gene transfer and promising candidates for gene therapy. J Gene Med,2000,2(5):308-316.
[11] Ballios BG, Cooke MJ, Donaldson L, Coles BL, Morshead CM, van der Kooy D, Shoichet MS. A hyaluronan-based injectable hydrogel improves the survival and integration of stem cell progeny following transplantation. Stem Cell Reports, 2015,4(6):1031-1045.
[12] Bumgardner GL, Gao D, Li J, Baskin JH, Heininger M, Orosz CG. Rejection responses to allogeneic hepatocytes by reconstituted SCID mice, CD4, KO, and CD8 KO mice. Trans-plantation,2000,70(12):1771-1780.
[13] Hamrah P, Haskova Z, Taylor AW, Zhang Q, Ksander BR, Dana MR. Local treatment with alpha-melanocyte stimulating hormone reduces corneal allorejection. Transplantation,2009,88(2):180-187.
[14] Thompson K, Maltby J, Fallowfield J, McAulay M, Millward-Sadler H, Sheron N. Interleukin-10 expression and function in experimental murine liver inflammation and fibrosis. Hepatology,1998,28(6):1597-1606.
[15] T?gel F, Weiss K, Yang Y, Hu Z, Zhang P, Westenfelder C. Vasculotropic, paracrine actions of infused mesenchymal stem cells are important to the recovery from acute kidney injury. Am J Physiol Renal Physiol,2007,292(5):F1626-F1635.
(收稿日期:2020-03-18)
(本文編辑:杨江瑜)

