水菱镁矿制备不同形貌纳米氧化镁的研究
黄建翠,凌观爽,宗 俊
(华东师范大学化学与分子工程学院,上海 200241)
1 前言
纳米氧化镁(MgO)是一种新型高功能精细无机材料,由于纳米材料的表面效应、体积效应、量子尺寸效应和宏观量子隧道效应等特殊效应,而具备一些不同于本体的光、热、电、磁、机械和化学等特性[1-3],近年来在抗菌剂[4-5]、催化剂[6-7]、吸附剂[8-10]、高级陶瓷[11]、光电材料[12]、耐火材料[13]、填料[14]、医药[15]等领域有着重要的应用。纳米氧化镁通常具有不同的形态特征,而不同的形态特征导致了不同的性能,其主要形态有粉体、薄膜、片、棒、管、丝等,还有一些特殊形貌[2]。目前报道的纳米氧化镁的制备方法主要分为气相法、固相法、液相法[16],其中固相法、液相法最为常见,固相法主要有矿物煅烧法[17]、机械粉碎法、固相化学反应法[18],液相法主要有沉淀法[19]、溶胶—凝胶法[20]、电化学方法[21]、金属醇盐水解法[22]、水热法[23]、白云石碳化法[24]、微波法[25]、微乳液法[26]等。其中,矿物煅烧法由于原料丰富、成本低廉是常用的大规模制备氧化镁的方法之一,但是常用的矿物一般是菱镁矿,在煅烧前通常需要进行复杂的预处理过程,且生产出的大多为低端氧化镁。而液相法中虽然生产的氧化镁质量较高,但该方法需要大量的化学试剂,甚至引入有机杂质造成污染,且对设备要求高,成本高,工业化生产面临挑战。因此,寻找成本低、无污染、适合工业化生产优质氧化镁产品的方法是当前的重要任务。
水菱镁矿是一种储量丰富的天然碱式碳酸盐矿物。20世纪50年代后期,郑绵平[27]等在西藏班戈湖等地区首次发现该矿物。我国现已探明的水菱镁矿资源含量超过1亿t,是罕见的大型矿床,主要分布于北部西藏盐湖地区以及青海的一些盐湖地带[28]。水菱镁矿质地纯净,色泽洁白,有“snow-white”或“white-flower”之称,其化学式为4MgCO3·Mg(OH)2·4H2O[29],其中CaO等杂质含量低,对一般性应用影响很小,是制备阻燃剂、活性氧化镁、重质碱式碳酸镁、纳米氢氧化镁等镁质产品的优质矿产原料[30-32]。然而,由于地域、交通等因素的限制,并未对其进行较好的开发利用,关于以水菱镁矿制备不同特性纳米氧化镁的研究更未见报道。
基于此,文章提出了以水菱镁矿为原料,采用“煅烧—水化—煅烧”的工艺路线制备不同特性的纳米氧化镁。探究了不同煅烧温度和时间对氧化镁形貌、结晶度、晶粒尺寸、比表面积的影响以及二次“水化+煅烧”对氧化镁形貌的影响。
2 实验部分
2.1 实验原料
天然水菱镁矿(4MgCO3·Mg(OH)2·4H2O)源自西藏班戈湖那曲;无水乙醇(分析纯)购自国药集团化学试剂有限公司(中国,上海);去离子水实验室自制。所有试剂无需进一步纯化即可使用。
2.2 纳米氧化镁的制备方法
2.2.1 煅烧
将适量水菱镁矿石放入坩埚中,一同放入马弗炉中煅烧。设置煅烧温度650 ℃,煅烧时间30 min,升温速率10 ℃/min。冷却到室温后,将其研磨成粉末并使用0.074 mm筛子过筛,得到白色粉末,命名为M1。
2.2.2 水化
将去离子水加入到三颈烧瓶中,在磁力搅拌器中水浴加热至80 ℃,称取一定量的上步制备的M1,在剧烈搅拌下缓慢加入到三颈烧瓶中,保持固液比为1 ∶30,水浴回流反应2 h。反应结束后,悬浊液陈化30 min,进行抽滤,并依次用去离子水、无水乙醇洗涤滤饼3次。将滤饼放置在150 ℃鼓风干燥箱中烘干3 h,研磨得白色粉末,并命名为MH1。
2.2.3 煅烧
将MH1放入坩埚中,置于马弗炉中煅烧,在10 ℃/min的升温速率下分别于不同温度下保温不同时间,分析产物粒径、形貌、比表面积变化。
2.2.4 二次“水化+煅烧”
将上步在650 ℃下煅烧1 h所制备的氧化镁再次重复水化和煅烧步骤。煅烧条件定为650 ℃和850 ℃分别煅烧1 h,分析氧化镁形貌变化。
2.3 表征方法
用X射线粉末衍射仪(型号:SmartLab SE,Rigaku公司,日本)进行物相分析,参数设置(CuKα 辐射,λ=1.541 8 Å,镍滤光片,25 mA,35 kV,扫速30°/min);用差热热重分析仪(型号:TGA/SDTA851e,梅特勒—托利多仪器公司,瑞士)分析水菱镁矿的热分解过程,参数设置(温度范围:室温~800 ℃,升温速率10 ℃/min,N2氛);用场发射扫描电子显微镜(型号:Quanta FEG 250,FEI公司,美国)和场发射透射电子显微镜(型号:JEOL JEM-2100F-AH,JEOL JEM公司,日本)观察产物形貌。
3 结果与讨论
3.1 水菱镁矿原料的表征
3.1.1 水菱镁矿的XRD分析
天然水菱镁矿的XRD图谱如图1所示,主要衍射峰与4MgCO3·Mg(OH)2·4H2O (JCPDS 70-0361)和CaCO3(JCPDS 41-1475)的峰位置几乎一致,证明主要矿物组成是水菱镁矿(4MgCO3·Mg(OH)2·4H2O)和文石(CaCO3)。样品经化学分析,测得其中氧化镁含量为41.59%,氧化钙含量为1.30%,其他杂质含量较少。
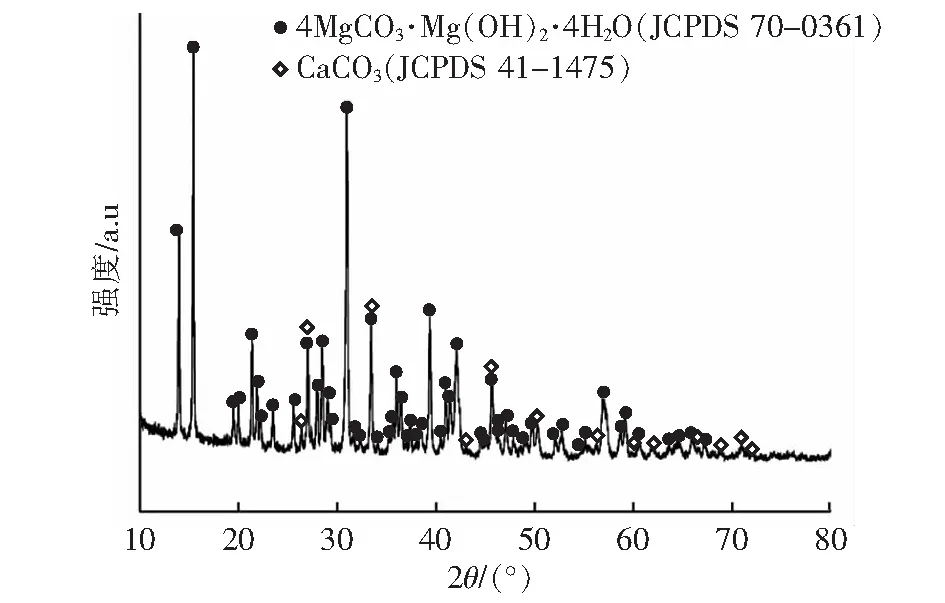
图1 水菱镁矿的XRD图Fig.1 XRD pattern of hydromagnesite
3.1.2 水菱镁矿的TG-DTG分析
水菱镁矿(4MgCO3·Mg(OH)2·4H2O)在800 ℃氮气气氛中热分解,得到图2的TG-DTG曲线。TG曲线表明,样品初始分解温度在150 ℃左右,分解完全的温度在680 ℃附近。根据TG曲线的质量损失台阶可将样品的质量损失分解过程分为四个区间:150 ℃~350 ℃、350 ℃~480 ℃、480 ℃~560 ℃、560 ℃~680 ℃。由DTG曲线可以看出,各阶段的质量损失速率不同,四个温度区间的质量损失分别为13.33 %、29.28 %、8.28 %和3.51 %,总的分解率为54.40 %,其总吸热反应分解的方程式[29]为(1),因此,在650 ℃煅烧基本可以完全分解。
4MgCO3·Mg(OH)2·4H2O → 5MgO+4CO2+5H2O
(1)
3.2 过程产物表征
3.2.1 XRD分析
图3(a)、图3(b)表示的是水菱镁矿第一次煅烧后产物M1和M1进行水化反应所得水化产物MH1的XRD图谱。从图3(a)可以看出,经历煅烧后已经观察不到水菱镁矿的特征峰,此时衍射峰主要位于2θ为36.9 °(111晶面)、42.9 °(200晶面)、62.3 °(220晶面)、74.7 °(311晶面)、78.6 °(222晶面),与MgO (JCPDS 89-4248)的峰完全符合,说明煅烧产物为MgO。从图3(b)可以看出,水化产物的衍射峰主要位于2θ为18.58 °、32.84 °、37.96 °、50.88 °、58.70 °、62.14 °、68.10 °、72.16 °,与Mg(OH)2(JCPDS 44-1482)的峰完全吻合,说明水化产物是Mg(OH)2,MgO基本反应完全,另外,产物中还存在一些杂质CaCO3。
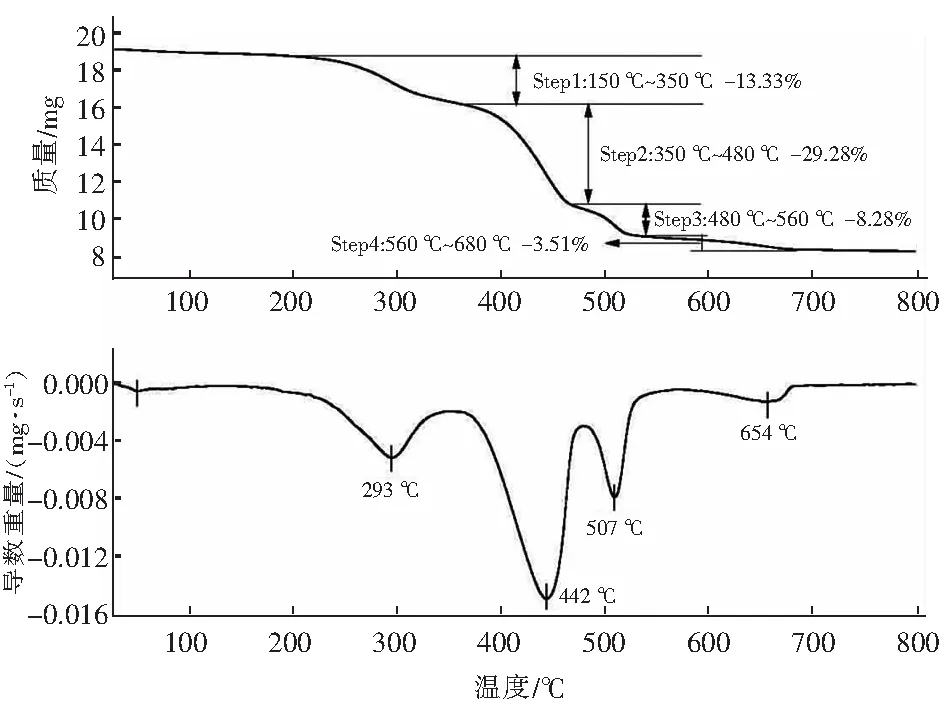
图2 水菱镁矿的TG-DTG图Fig.2 TG-DTG diagram of hydromagnesite
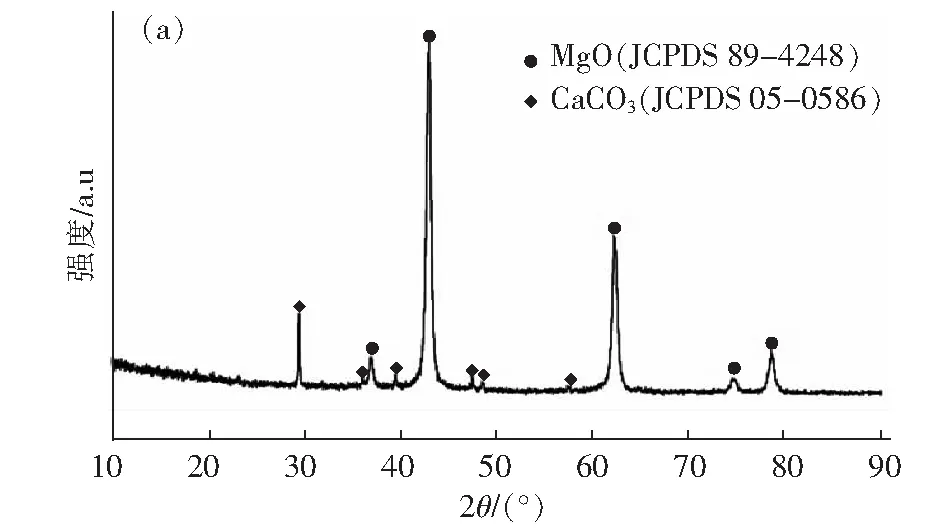
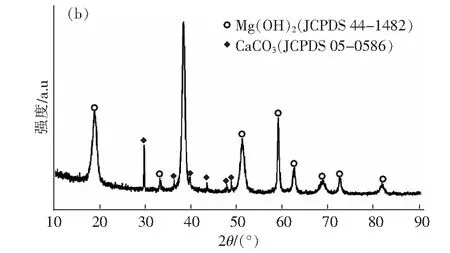
图3 (a)第一次煅烧后产物M1的XRD图;(b)M1水化后产物MH1的XRD图Fig.3 (a)XRD pattern of product M1 after the first calcination; (b) XRD pattern of product MH1 after M1 hydration
3.2.2 SEM分析
图4(a)、图4(b)表示的是水菱镁矿第一次煅烧后产物M1和M1进行水化反应所得水化产物MH1的SEM图,可以看出,水菱镁矿第一次煅烧后的产物呈现不规则的大的块状体,并没有特定形貌。而在其进行水化反应后,形貌发生了很大改变。可以看出,水化产物呈薄片状,片与片之间交叉生长,形成了类似“卡房”的结构。

图4 (a)第一次煅烧后产物M1的SEM图;(b)M1水化后产物MH1的SEM图Fig.4 (a)SEM image of product M1 after the first calcination;(b)SEM image of product MH1 after M1 hydration
3.3 纳米氧化镁的表征
3.3.1 XRD分析
将水化产物MH1分别在500 ℃、550 ℃、600 ℃、650 ℃、700 ℃、750 ℃、800 ℃、850 ℃下煅烧1 h所得产物的XRD图如图5所示,由图5可知,衍射峰均与MgO(JCPDS 89-4248)的峰位置基本一致,是稳定的立方相,说明MH1煅烧后的产物为MgO。另外,我们仍可以观察到产物中含有少量杂质,在煅烧温度低于650 ℃时,杂质为CaCO3,超过650 ℃时,产物的杂质变为了CaO,这是由于在较高的温度下,CaCO3发生了分解,释放了CO2的缘故(由于氧化镁中杂质含量较少,且对一般性应用影响较小,考虑到利于工业化生产的经济要求,我们暂时不对杂质进行去除)。
通过比较可观察到,随着煅烧温度的升高,MgO特征峰的强度逐渐增大,半峰宽逐渐减小,这说明在较高温度下MgO的结晶度较高。不同煅烧温度下纳米氧化镁的晶粒尺寸见表1。由表1可以看出,随着温度的升高,平均粒径逐渐增大。这可能是由于煅烧温度可以提供热驱动力,使得晶粒之间的界面产生迁移,从而引起晶粒的生长。
纳米氧化镁的晶粒尺寸可根据Debye-Scherrer[3]公式(2)计算得到:
(2)
式中:K——Scherrer常数,K=0.89;D——晶粒尺寸,nm;λ——X射线波长,λ=0.154 056 nm;β——MgO(200)衍射峰校正后的半峰宽;θ——衍射角。Gaussian-Gaussian关系式用于修正仪器误差:
β2=B2-b2
(3)
式中:B——测试样品的半高宽;b——标准硅的半高宽。
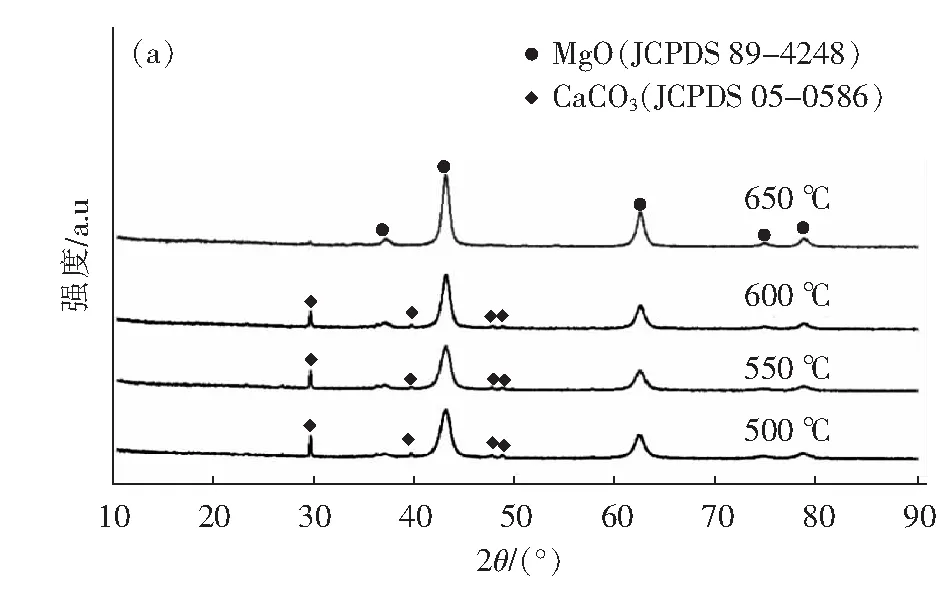
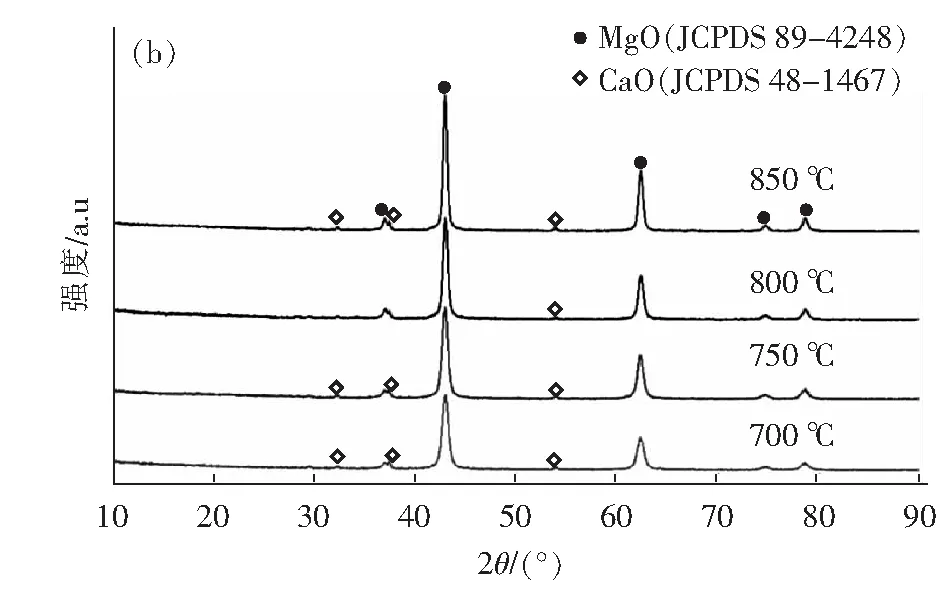
图5 不同温度下第二次煅烧后产物的XRD图Fig.5 XRD patterns of products after second calcination at different temperatures

表1 煅烧温度对纳米氧化镁晶粒尺寸的影响Tab.1 Effect of calcination temperature on grain size of nanometer magnesium oxide
将水化产物MH1在850 ℃下分别煅烧1 h、2 h、3 h、4 h所得产物的XRD图如图6 (a)所示,由图可知,随着煅烧时间的延长,MgO特征峰变得更加尖锐,半峰宽变得更窄,这说明延长煅烧时间,也可增强MgO的结晶性,促进MgO晶粒生长。不同煅烧时间下纳米氧化镁的晶粒尺寸见表2。纳米氧化镁的平均粒径随着煅烧时间的延长而逐渐增大,这是因为前驱体在经历升温、恒温过程后,发生了再结晶和晶粒长大等变化,表明煅烧时间的延长是纳米氧化镁晶粒缓慢增长的过程。
图6(b)显示了水化前后两次650 ℃下煅烧1 h所得产物的XRD对比图。可以看出,第一次煅烧后产物峰形尖锐,杂质峰较为明显,第二次煅烧后产物峰形有所宽化,杂质峰也被大大弱化,根据MgO(200)衍射峰的半峰宽(FWHM),使用Debye-Scherrer方程确定了第一次煅烧和第二次煅烧的平均粒径分别为16.66 nm和12.12 nm,证明在650 ℃的条件下煅烧,第二次煅烧后产物比第一次煅烧后产物纯度更高,且具有更小的晶粒尺寸。
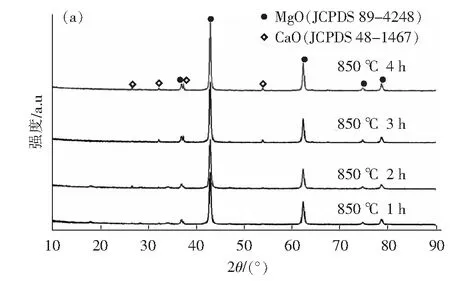
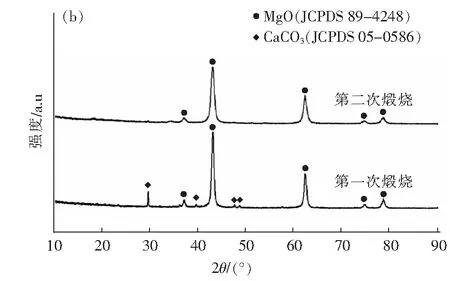
图6 (a)不同时间下第二次煅烧后产物的XRD图;(b)水化前后两次650 ℃煅烧XRD图Fig.6 (a) XRD patterns of products after second calcination at different times; (b)XRD pattern of twice calcination at 650 ℃ before and after hydration
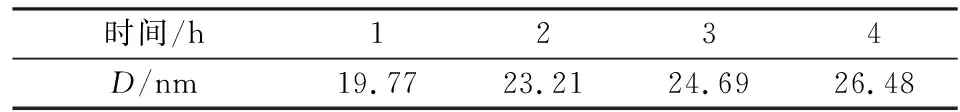
表2 煅烧时间对纳米氧化镁晶粒尺寸的影响Tab.2 Effect of calcination time on grain size of nanometer magnesium oxide
3.3.2 SEM分析
为了研究纳米氧化镁形貌的变化,对典型的650 ℃和850 ℃下煅烧的产物进行了SEM表征。图7(a)、图7(b)、图7(c)、图7(d)、图7(e)、分别为在650 ℃下煅烧1 h以及在850 ℃煅烧1 h、2 h、3 h、4 h的SEM图。由图7(a)可知,在650 ℃下煅烧1 h得到的产物是由厚度约为15 nm的交叉的纳米片构成,其基本上保持了前驱体的结构,而每一片纳米片上由于Mg(OH)2脱水又形成了介孔网状结构。由图7 (b)可知,在850 ℃下煅烧1 h得到的产物基本还能维持原来的交叉片状结构,但相比650 ℃下煅烧1 h的产物,该温度下片层厚度明显增加,纳米片上的纳米颗粒尺寸也明显变大。由图7 (c)可知,在850 ℃下煅烧2 h得到的产物交叉片状结构开始坍塌,纳米MgO颗粒逐渐生长。由图7(d)、图7 (e)可知,继续延长煅烧时间,交叉片状结构逐渐解体,介孔网状结构也逐渐消失,纳米MgO颗粒则继续生长,最终形成了尺寸在50 nm~60 nm之间,具有棒状、哑铃状的MgO纳米颗粒。这是在较高温及较长保温时间过程中,纳米片溶解并重结晶为纳米颗粒,这与XRD分析结果相一致。说明控制不同的煅烧温度和时间可以控制产物的粒径,得到具有不同形貌的纳米氧化镁。

图7 第二次煅烧后产物的SEM图(a)650 ℃ 1 h;(b)850 ℃ 1 h;(c)850 ℃ 2 h;(d)850 ℃ 3 h;(e) 850 ℃ 4 hFig.7 SEM image of the product after the second calcination(a)650 ℃ for 1 h; (b)850 ℃ 1 h; (c) 850 ℃ 2 h; (d)850 ℃ 3 h; (e)850 ℃ 4 h
3.3.3 比表面积和孔结构分析
由SEM分析结果可知,在一定煅烧温度下,可得到具有丰富的交叉片层、介孔网状结构的氧化镁,这种特殊结构可能提供大的比表面积。因此,对650 ℃和850 ℃下煅烧1 h得到的介孔网状纳米氧化镁进行了N2吸脱附分析,样品的吸附等温线如图8(a)所示。样品均表现出具有H3磁滞回线的Ⅳ型等温线,这主要见于层状结构的聚集体产生狭缝的介孔或大孔材料,表明了材料的介孔性质[33],从图8中可以看出,相比850 ℃,在650 ℃下煅烧得到的介孔网状纳米氧化镁具有更高的N2吸附量。经BET计算,结果表明,在650 ℃的煅烧温度下,样品的比表面积高达188.3 m2/g(该值远高于其他报道中MgO样品的比表面积值,具体见表3);在850 ℃的煅烧温度下,样品的比表面积为71.7 m2/g。因此,MgO纳米材料的比表面积的变化趋势表现为随煅烧温度的升高而逐渐减小,这是由于较高的温度下氧化镁的形貌发生了从薄片介孔网状结构向纳米颗粒的转变。
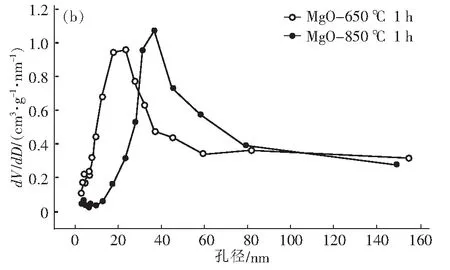
图8 (a)氧化镁的N2吸附-脱附等温线;(b)氧化镁的孔径分布图Fig.8 (a)N2 adsorption-desorption isotherm of magnesium oxide;(b) Pore size distribution of magnesium oxide
通过BJH计算分析两种温度下的孔径分布,结果如图8(b)所示。两种温度下的孔径均显示为较均匀的单峰分布,但孔径大小存在较大差异。在650 ℃的煅烧温度下,样品的平均孔径为12.33 nm,孔体积为0.85 cm3/g;在850 ℃的煅烧温度下,样品的平均孔径增加到31.31 nm,而孔体积减小到0.56 cm3/g。
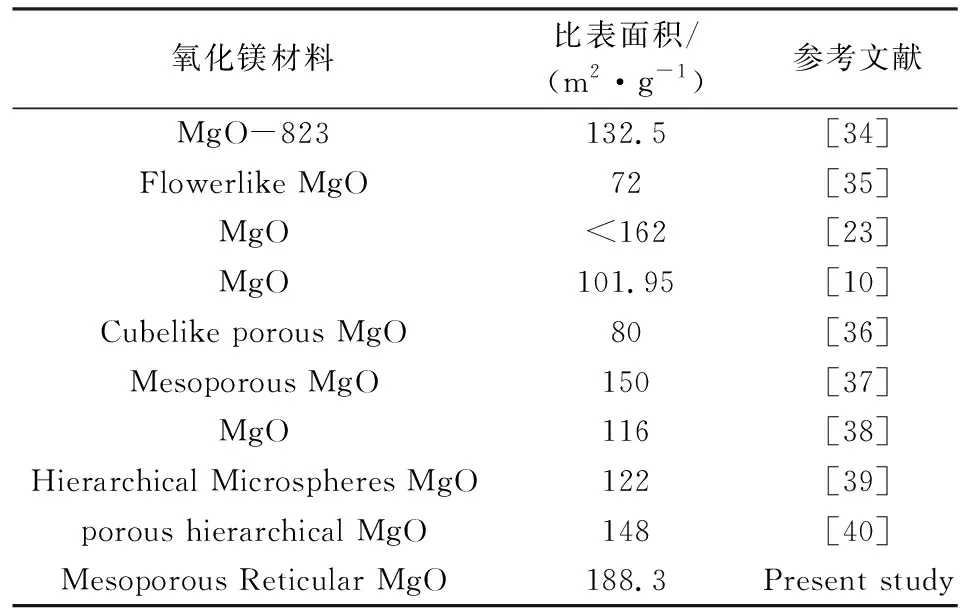
表3 其他文献报道氧化镁材料的比表面积Tab.3 Other literature reports on specific surface area of magnesium oxide materials
以上结果表明,在650 ℃下煅烧1 h可得到具有高比表面积的介孔网状纳米氧化镁。
3.3.4 二次“水化+煅烧”产物表征
为了进一步制备其他形貌的纳米氧化镁,将在650 ℃下煅烧1 h制备的高比表面积介孔网状氧化镁再次重复水化和煅烧步骤,并对产物进行了XRD、SEM和TEM表征。图9为第一次水化与第二次水化产物的XRD图,可以看出在同样的水化条件下,经历二次水化后的样品衍射峰强度大大增加,半峰宽也变得很窄,说明重复水化步骤,可以显著提高样品的结晶度,促进晶体生长。
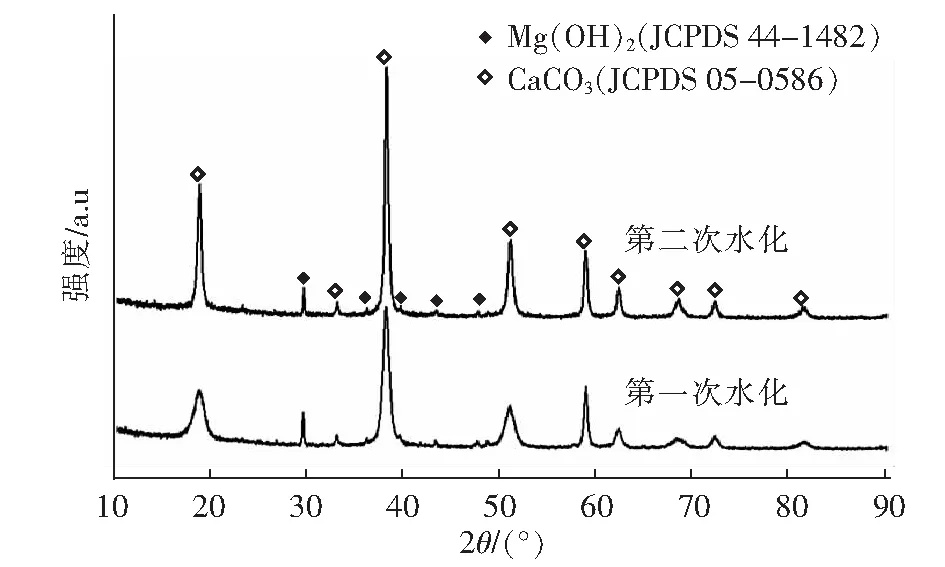
图9 第一次水化与第二次水化的XRD图Fig.9 XRD patterns of first hydration and second hydration
图10(a)为二次水化后所得Mg(OH)2的SEM图,可以看到,反应前后产物的形貌也发生了明显的改变,反应前是非常薄的交叉片层介孔网状结构,而反应后变成了边界清晰、厚度在30 nm~40 nm之间的较规则的六角片状Mg(OH)2纳米粒子,这印证了XRD的分析结果。
图10(b)、图10(c)为在650 ℃、850 ℃下煅烧1 h所获产物的SEM图。可以看出,650 ℃下煅烧得到的产物保持了前驱体的结构,形成了六角片状的氧化镁。850 ℃下煅烧得到的产物,在保持了前驱体片状结构的基础上,又在片内部形成了大量的介孔。这是因为较高温下样品失去结晶水,而产生的孔道。图10(d)为850 ℃下煅烧所得产物的TEM图,可以明显看到介孔结构。
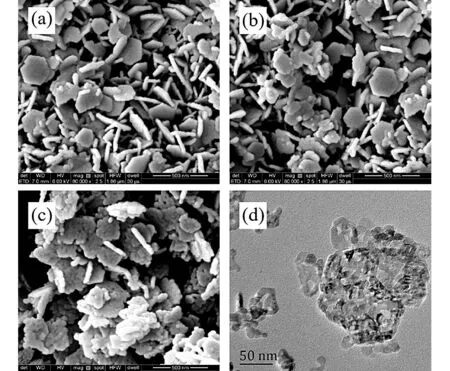
图10 二次“水化+煅烧”产物的SEM与TEM图(a)二次水化(SEM);(b)650 ℃ 1 h(SEM);(c)850 ℃ 1 h(SEM);(d)850 ℃ 1 h(TEM)Fig.10 SEM and TEM images of secondary “hydration+calcination” products(a) secondary hydration(SEM); (b)650 ℃ 1 h(SEM); (c)850 ℃ 1 h(SEM); (d)850 ℃ 1 h(TEM)
3.4 反应机理
在以水菱镁矿为原料,采用“煅烧—水化—煅烧”工艺路线制备纳米氧化镁过程中发生的化学反应及机理如下:
煅烧。水菱镁矿在大约650 ℃的温度范围内吸热分解,释放出水和二氧化碳。
4MgCO3·Mg(OH)2·4H2O→5MgO+4CO2+5H2O
(1)
水化。水化反应体系中可能遵循“溶解—沉淀”[41]的反应机理,水化反应的具体反应如下:
(1)溶解。MgO 在水中提供电子,生成OH-,OH-吸附在带正电荷的固体表面,OH-从表面解吸进入溶液中,同时释放出Mg2+。
(4)
(5)
(6)
(2)沉淀。离子浓度增大形成过饱和溶液,生成氢氧化镁沉淀。
(7)
煅烧。在一定温度下,氢氧化镁热分解失去结晶水,得到氧化镁。
Mg(OH)2(s)→MgO(s)+H2O(g)
(8)
4 结论
1)以水菱镁矿为原料,采用“煅烧—水化—煅烧”的简单工艺路线制备出了具有不同形貌的纳米氧化镁,且过程中无需加入任何其他试剂。
2)实验探究了煅烧条件对样品形貌、结晶度、晶粒尺寸及比表面积的影响,结果表明,温度的升高或煅烧时间的延长有助于提高氧化镁的结晶度,促进晶体生长,减小比表面积。实验最终得出:在650 ℃下煅烧1 h,可得到比表面积高达188.3 m2/g的介孔网状氧化镁;在850 ℃下煅烧4 h,可得到棒状、哑铃状的MgO纳米颗粒。
3)将实验所得的高比表面积介孔网状氧化镁重复“水化+煅烧”实验,结果表明,重复水化步骤,可提高氢氧化镁样品的结晶度,促进晶粒生长,煅烧后的氧化镁基本能保持前驱体的结构。实验结果:二次水化可得到具有六角片状的纳米氢氧化镁,将其在650 ℃下煅烧1 h,可得到六角片状纳米氧化镁;在850 ℃下煅烧1 h,可得片状介孔纳米氧化镁。

