响应面法优化阴阳极同时作用电化学法处理染料废水
班福忱,郑雪婷,姜亚玲
(沈阳建筑大学 市政与环境工程学院,辽宁 沈阳 110168)
染料废水具有水质复杂、毒性大、色度高、可生化降解性差等特点[1-3],传统的废水处理技术很难使染料废水处理后达到排放标准[4],有些工艺虽处理效果较好,但存在能耗高、产生二次污染等问题[5]。
电催化高级氧化技术(AEOP)具有工艺简单、操作简便、环保且能耗低等优点,已被广泛应用于染料废水处理领域[6-8]。该工艺原理为选择具有催化氧化作用的活性电极,在极板上生成能降解有机物的强氧化物质。RAUF等[9]以Bi2O5-PbO2为阳极降解氯酚,可有效抑制析氧副反应的发生,电流效率明显提高。SAHINKAYA等[10]自制Ti/SnO2电极电解氧化酚,其降解效率超过Pt电极5倍以上。袁松虎等[11-12]研究发现,电解过程中阴极上还原生成H2O2,阳极上生成Cl2,进而转化为HClO,H2O2和HClO都是强氧化物,可氧化降解苯酚、硝基苯等。单独的阳极氧化、阴极催化氧化均能降解有机物,但每一极都有副反应与限制条件。
本实验将阳极氧化与阴极催化氧化联合使用,并通过Box-Behnken Design响应面法,以甲基橙模拟染料废水脱色率为考察指标,探讨Fe3+浓度、Cl-浓度、电流密度等影响因素之间的相关性,优化阴阳极同时作用电化学法处理甲基橙模拟染料废水的工艺条件,为实现AEOP在废水处理中的应用奠定基础。
1 实验部分
1.1 实验装置及方法
实验装置示意图见图1。实验所用试剂均为分析纯。
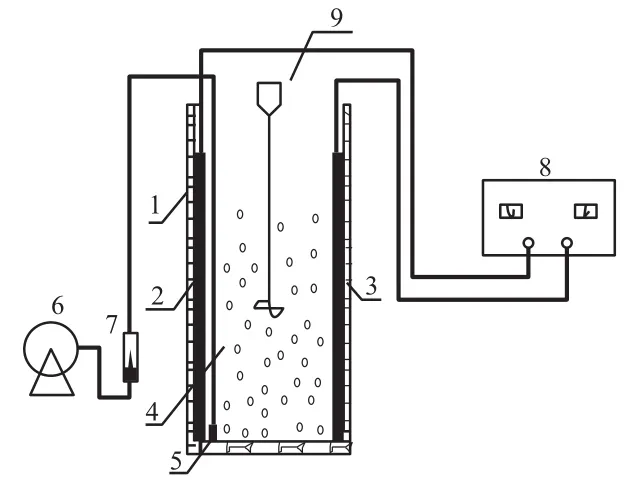
图1 实验装置示意图
1.2 实验方法
将3 500 mL质量浓度为200 mg/L的甲基橙溶液加入电解槽中,投加1 g/L的电解质Na2SO4,再加入一定浓度的NaCl溶液和Fe2(SO4)3溶液,用稀硫酸调节体系pH,通入压缩空气进行曝气,通过转子流量计调节曝气量,接通直流稳压电源,使反应在一定的电流密度下进行,定时取样在最大吸收波长460 nm处测定染料废水吸光度,计算废水脱色率。
1.3 分析方法
采用756CRT型紫外-可见分光光度计(上海菁华科技仪器有限公司)测定废水吸光度;采用B-212型酸度计(日本HORIBA公司)测定废水pH。
2 结果与讨论
2.1 单因素对废水脱色率的影响
2.1.1 体系pH
在Fe3+浓度为1 mmol/L、Cl-浓度为11 mmol/L、电流密度为7.5 mA/cm2、曝气量为1.5 L/min、电解时间为90 min的条件下,体系pH对废水脱色率的影响见图2。由图2可知:体系pH为3时,废水脱色率最高;体系pH升高,废水脱色率明显降低。这是因为,在酸性条件下阴极表面会生成·OH和H2O2,而升高pH会发生副反应。故本实验体系pH为3较适宜。
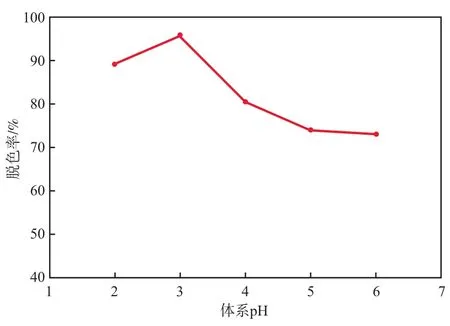
图2 体系pH对废水脱色率的影响
2.1.2 Cl-浓度
在Fe3+浓度为1 mmol/L、电流密度为7.5 mA/cm2、体系pH为3、曝气量为1.5 L/min、电解时间为90 min的条件下,Cl-浓度对废水脱色率的影响见图3。由图3可见:加入Cl-后,废水脱色率提高,因为Cl-在阳极上产生Cl2,Cl2在水溶液中反应生成HClO[13-14];当Cl-浓度超过11 mmol/L时废水脱色率下降,因为过量的Cl-会与溶液中的·OH发生副反应生成ClOH-,ClOH-与Fe2+反应生成其他物质,这不仅使HClO的量减少还会降低·OH的量[15],从而降低废水脱色率。故本实验适宜的Cl-浓度为11 mmol/L。
2.1.3 电流密度
在Fe3+浓度为1 mmol/L、Cl-浓度为11 mmol/L、体系pH为3、曝气量为1.5 L/min、电解时间为90 min的条件下,电流密度对废水脱色率的影响见图4。由图4可见,随电流密度增大,废水脱色率逐渐升高。电流密度增大会产生更多的电子,使阳极产生更多的·OH,阴极上还原更多的氧气,促进溶液中化学反应的进行。但随着电流密度继续增大,能耗增大,极板间电压增大,促进了析氧副反应的发生,因此废水脱色率升高缓慢。综合考虑,本实验选择电流密度为7.5 mA/cm2较适宜。
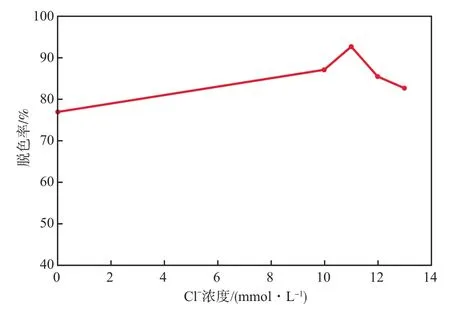
图3 Cl-浓度对废水脱色率的影响
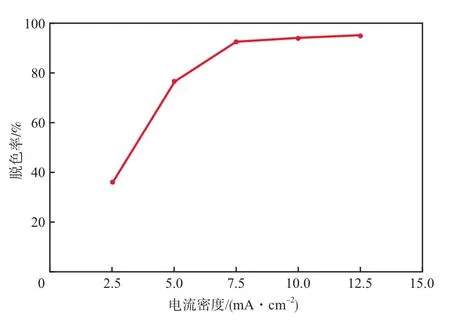
图4 电流密度对废水脱色率的影响
2.1.4 Fe3+浓度
在Cl-浓度为11 mmol/L、电流密度为7.5 mA/cm2、体系pH为3、曝气量为1.5 L/min、电解时间为90 min的条件下,Fe3+浓度对废水脱色率的影响见图5。

图5 Fe3+浓度对废水脱色率的影响
由图5可见:废水脱色率随Fe3+浓度增加呈先升后降趋势,这是因为随着Fe3+浓度的增加,Fe3+还原产生Fe2+催化水解生成的H2O2产生·OH,这时溶液中的电极、HClO、Fenton试剂共同作用降解甲基橙;但当Fe3+浓度过大时,溶液中会产生副反应消耗H2O2生成HO2·,从而降低了体系的氧化能力[16]。故本实验选择Fe3+浓度为1 mmol/L较适宜。
2.1.5 曝气量
在Fe3+浓度为1mmol/L、Cl-浓度为11 mmol/L、电流密度为7.5 mA/cm2、体系pH为3、电解时间为90 min的条件下,曝气量对废水脱色率的影响见图6。由图6可见:废水脱色率随曝气量增加呈先升后降趋势;当曝气量很低时不能满足电极反应和类Fenton反应所需的氧气,脱色率较低;曝气量提高后O2在阴极上还原产生H2O2从而产生·OH,为类Fenton反应提供了条件;但曝气量超过1.5 L/min后脱色率开始下降,这是因为曝气量过高导致传质速率过快,新生成的H2O2和·OH来不及氧化有机物就离开。综合考虑,本实验选择曝气量为1.5 L/min。
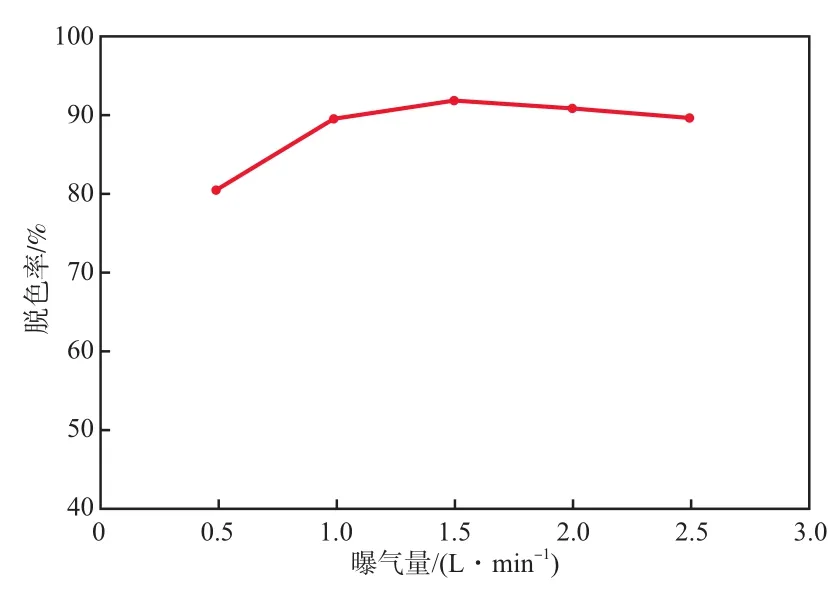
图6 曝气量对废水脱色率的影响
2.1.6 电解时间
在Fe3+浓度为1 mmol/L、Cl-浓度为11 mmol/L、电流密度为7.5 mA/cm2、体系pH为3、曝气量为1.5 L/min的条件下,电解时间对废水脱色率的影响见图7。

图7 电解时间对废水脱色率的影响
由图7可见:反应初期,甲基橙与电极接触充分,阴阳极快速产生大量的·OH和ClOH-,能快速降解甲基橙,故废水脱色率迅速提高;当反应时间超过90 min后,·OH和ClOH-的量逐渐减少,又发生析氢析氧等副反应,废水脱色率升高趋势缓慢。故本实验选择电解时间为90 min较适宜。
2.2 方案设计及结果
选取影响废水脱色率最大的3个因素:Fe3+浓度、Cl-浓度和电流密度,分别记为变量X1,X2,X3,响应值Y为废水脱色率。采用响应面法中的Box-Behnken Design模型设计为3因素3水平实验。设计因素编码与水平见表1,响应面实验设计及结果见表2。
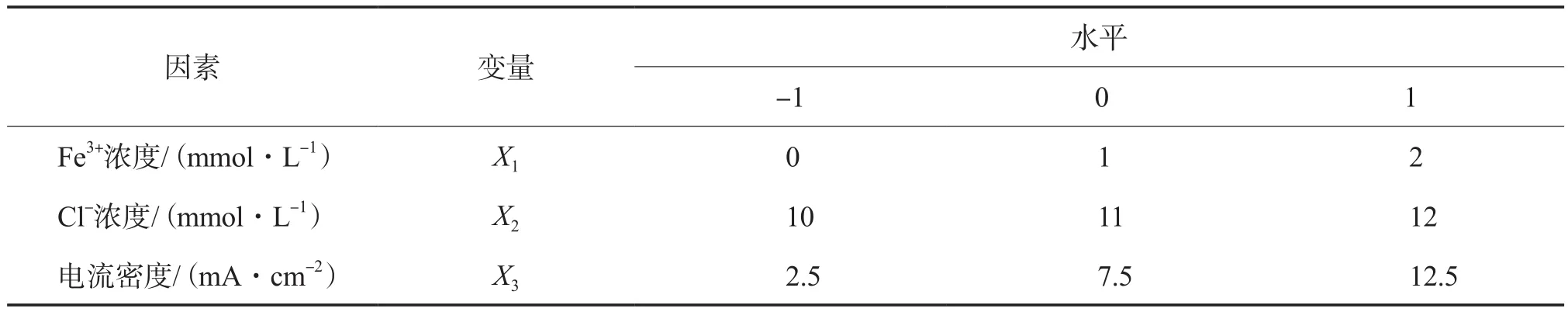
表1 设计因素编码与水平
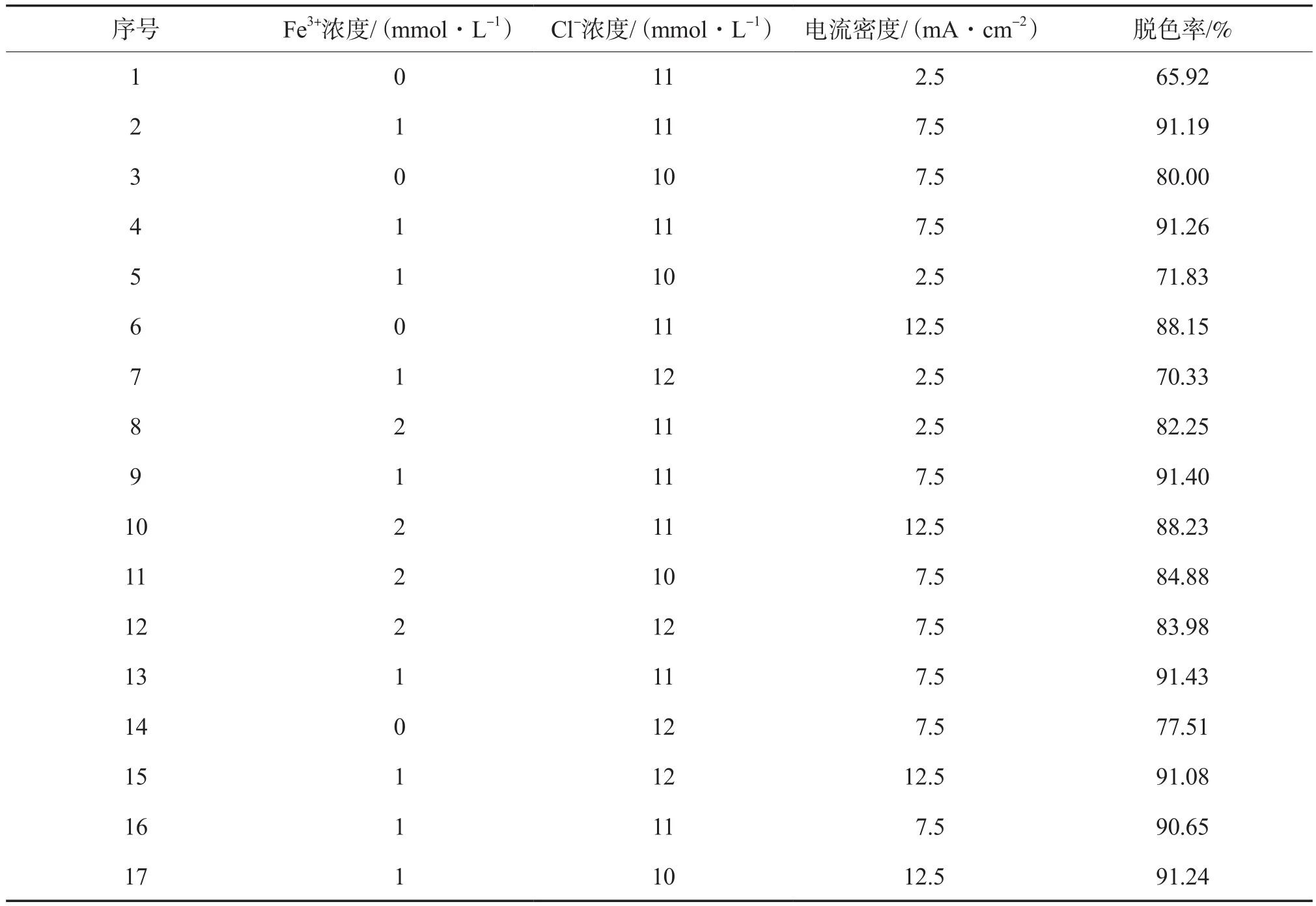
表2 响应面实验设计及结果
运用Design-Expert软件,回归模型和废水脱色率的方差分析结果见表3和表4。经过数据分析得到因素与响应值间的多元二次回归方程如下。
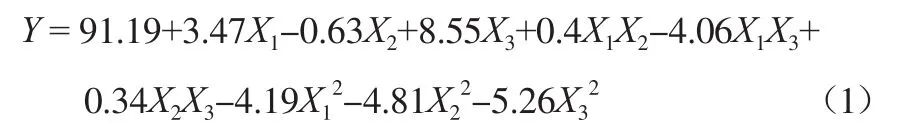
由表3可知:模型的相关系数R2=0.980 5,实验误差较小;即校正系数与预测系数仅相差6.22%,说明该模型预测值与实际情况拟合程度较好;离散系数CV=2.10%,实验的可靠性较高。
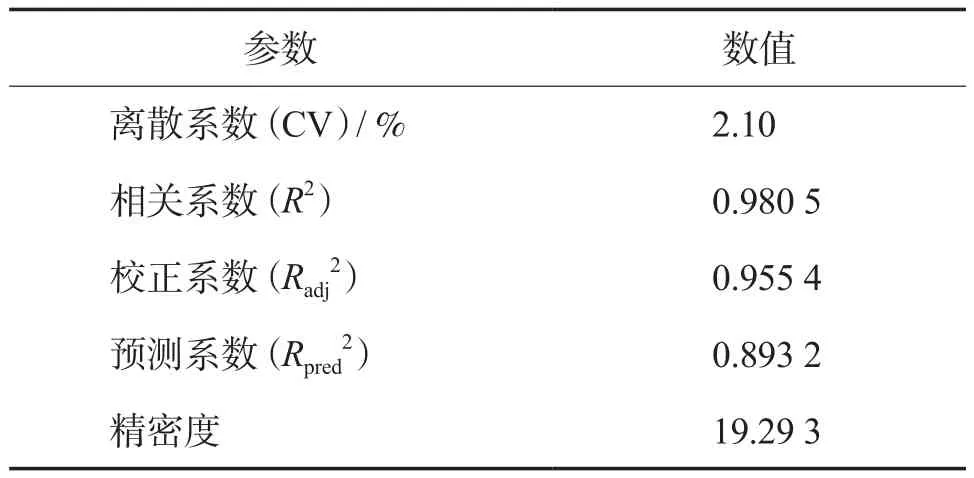
表3 回归模型的方差分析结果
由表4可知:模型的F值为39.12,该模型是显著的。另外,由F值的大小可得影响废水脱色率的3个因素的影响大小顺序为:电流密度>Fe3+浓度>Cl-浓度,模型p值<0.000 1,具有高度的显著性,说明使用该模型预测废水脱色率是可靠的。
2.3 双因子交互效应分析
影响废水脱色率的3个因素之间相互作用的等高线和响应曲面分别见图8~图10。在等高线图中,其中心位置呈椭圆形说明两因素交互作用显著,中心越圆说明两因素交互作用越弱;在响应曲面图中,响应面坡度陡峭说明反应条件变化时响应值随之改变较灵敏,图中颜色越深说明响应值越大,降解效果越好。

表4 废水脱色率的方差分析结果
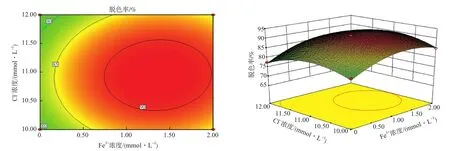
图8 Fe3+浓度和Cl-浓度交互作用的等高线和响应曲面
图8反映了Fe3+浓度和Cl-浓度的交互作用对废水脱色率的影响。从等高线图中可以看出,图形成微椭圆状即两因素间交互作用不明显;从响应曲面图中可以看到两者相互作用对废水脱色率影响相对较弱,Fe3+浓度的影响效果大于Cl-浓度。当Fe3+浓度为1 mmol/L、Cl-浓度为11 mmol/L浓度时,废水脱色率达到该实验最大值91.26%。这是因为,随着Fe3+浓度和Cl-浓度的升高,溶液中产生·OH形成类Fenton反应,Cl-反应生成强氧化剂HClO,二者共同作用氧化降解甲基橙。但随着Fe3+浓度和Cl-浓度继续升高,容易产生HO2·、ClOH-等副产物阻碍甲基橙的降解,因此废水脱色率随Fe3+浓度和Cl-浓度的升高先增大后减小。
图9反映了Fe3+浓度和电流密度的交互作用对废水脱色率的影响。从等高线图中可以看出两因素间交互作用显著;从响应曲面图可以看出废水脱色率对两者的变化极其灵敏,且电流密度的影响要大于Fe3+浓度的影响。当Fe3+浓度为1 mmol/L、电流密度为12.5 mA/cm2时脱色率达到最大值92.14%。随着电流密度的增加能促进产生更多的电子,促进Fe3+转化成Fe2+的还原反应,进而加快Fe2+催化H2O2使阳极产生更多的·OH而阴极上还原更多的氧气,促进甲基橙降解。但随着Fe3+浓度和电流密度不断增加,促进了阴极析氢副反应和阳极析氧副反应的发生,导致废水脱色率增加趋势变缓。
图10反映了Cl-浓度和电流密度的交互作用对废水脱色率的影响。从等高线图中可以看出两者的交互作用较明显;从响应曲面图中可以看出两因素的交互作用对废水脱色率的影响较大。当Cl-浓度为11 mmol/L、电流密度为7.5 mA/cm2时,废水脱色率达到最大值91.43%。随着电流密度的升高,产生的电子促进Cl-在阳极产生Cl2进而生成HClO,同时又有·OH产生,共同氧化降解甲基橙。但继续增加Cl-浓度和电流密度,会产生ClOH-、析氢、析氧等副反应从而影响甲基橙降解。
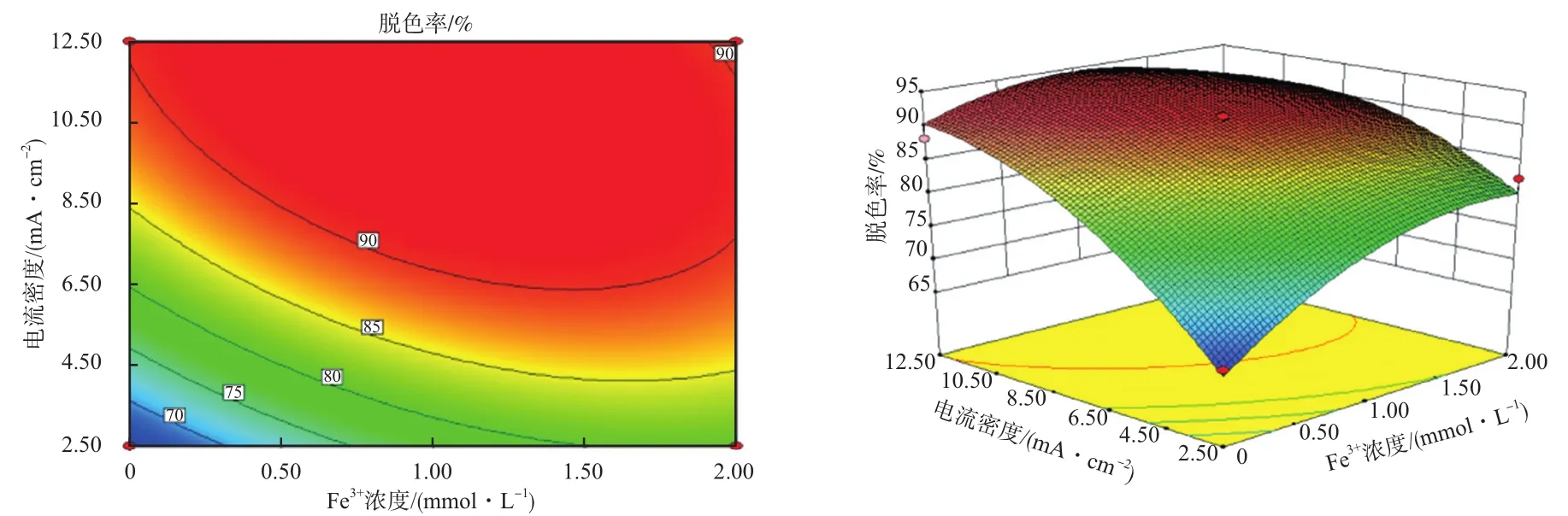
图9 Fe3+浓度和电流密度交互作用的等高线和响应曲面
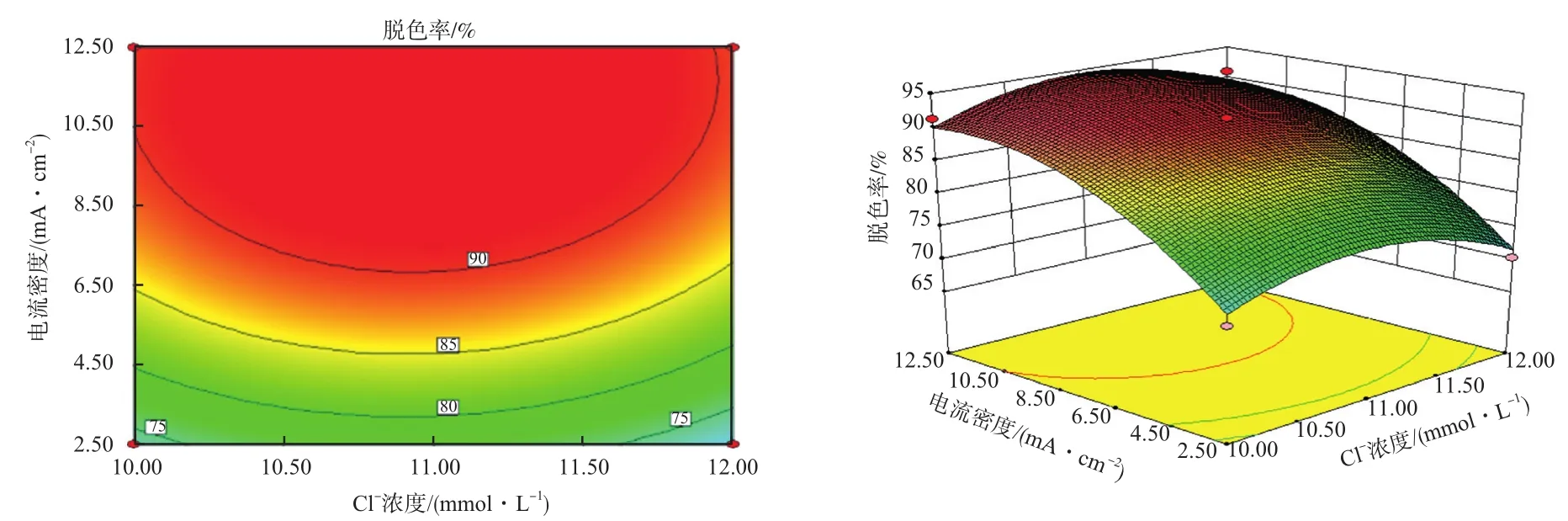
图10 Cl-浓度和电流密度交互作用的等高线和响应曲面
2.4 最优结果分析
通过Design Expert软件分析得到最优响应值Y=94.67%,即最高废水脱色率为94.67%。此时3个主要因素的最优量分别为:Fe3+浓度1.02 mmol/L、Cl-浓度10.96 mmol/L、电流密度11.52 mA/cm2。
3 结论
a)通过Box-Behnken Design响应面优化分析,得到阴阳极同时作用电化学法处理甲基橙废水的模型回归方程为:Y= 91.19+3.47X1-0.63X2+8.55X3+
b)各因素对废水脱色率影响的大小顺序为:电流密度>Fe3+浓度>Cl-浓度。通过等高线及响应面分析得出,各因素之间的交互作用对废水脱色率影响的大小顺序为:电流密度和Fe3+浓度>电流密度和Cl-浓度>Fe3+浓度和Cl-浓度。
c)3个主要因素的最优量分别为:Fe3+浓度1.02 mmol/L、Cl-浓度10.96 mmol/L、电流密度11.52 mA/cm2,最优脱色率为94.67%。该模型对处理甲基橙模拟染料废水的预测效果较好。

