Alamine336对低浓度模拟含硝酸废水的萃取分离
孙广垠,张 恒,,丁尚坤,王 朵,王 勇
(1. 河北工程大学 能源与环境工程学院,河北 邯郸 056038;2. 中国科学院 过程工程研究所,北京 100190;3. 阿尔伯塔大学 化学材料工程学院,加拿大 埃德蒙顿)
在很多工业生产(如采矿、化肥合成、冶金等)过程中,会排放大量的含硝酸废水[1],若直接排入自然水体会严重破坏环境[2],且造成资源浪费。进入自然水体的硝酸与水体中其他离子相互作用,转化为硝酸盐。硝酸盐进入人体后,经硝酸盐还原菌作用生成亚硝酸盐,并进一步转化为具有高度致癌、致畸、致突变性的亚硝基胺和亚硝基酰胺[3]。我国《生活饮用水水源水质标准》(CJ 3020—1993)中规定[4],硝酸盐质量浓度不得超过10.0 mg/L。
目前,含硝酸废水的处理方法主要有生物反硝化法、化学还原法和中和法等[5-7]。其中:生物反硝化法普遍存在不完全硝化过程、释放N2O造成二次污染、污泥减量化和处置等问题[8];化学还原法或电化学法处理硝酸盐氮,需要消耗大量化学药剂,还原生成的氨态氮需特殊工艺进一步处理,且存在操作流程复杂、生产成本较高等问题[9];中和法是根据常规的酸碱反应处理废水,实际操作过程简便,但会产生大量污泥。
溶剂萃取法是一种重要的分离手段,具有选择性高、分离效果好、适应性强等特点[10],且通过萃取-反萃取全流程控制,可实现有机溶剂的循环利用,具有很高的经济性[11]。JIA等[12]使用叔胺类萃取剂三辛胺(TOA)实现了H2O-H3PO4-HNO3体系中10.0%(w)高浓度硝酸与磷酸根的分离。CHEN等[13]以87.5%(φ)甲基异丁基酮和12.5%(φ)三辛癸烷基叔胺为萃取剂,选择性萃取分离模拟刻蚀废酸中的硝酸和乙酸,二者的萃取率分别为85%和75%,但甲基异丁基酮具有水溶性大、闪点低、挥发损失大等问题。
研究发现,不同硝酸浓度下的溶剂萃取机理不同,且会对萃取工艺产生影响[14-15]。工业生产过程所排放的含硝酸废水浓度范围较大[16-17],已有研究主要针对高浓度(>10 g/L)硝酸废水[18-19],而针对排放量更大的低浓度硝酸废水的研究还较少。
本研究以模拟低浓度含硝酸废水为研究对象,以煤油为稀释剂,考察了萃取剂种类、萃取剂浓度、有机相与水相的体积比等工艺条件对硝酸萃取和反萃效果的影响,并对相应的萃取机理进行了探讨,为回收低浓度硝酸和处理工业含硝酸盐废水提供理论依据和工艺基础。
1 实验部分
1.1 试剂和仪器
硝酸,分析纯,北京化工集团有限公司;磺化煤油,工业级,重庆康普化学工业股份有限公司;氢氧化钠,分析纯,天津光复化学试剂有限公司;Alamine336(TOA,纯度99.0%)、磷酸三丁酯(TBP,纯度99.0%)、Cyanex923(三烷基氧化膦混合物,纯度98.0%),北京化工集团有限公司;仲辛醇,纯度99.0%,上海阿拉丁生化科技股份有限公司;去离子水。
使用去离子水和纯硝酸配制模拟废水,通过计算将硝酸稀释至所需浓度备用。
紫外-可见分光光度计,LebTech-UV-9100型,北京莱伯泰科仪器有限公司;傅里叶变换红外光谱仪,Institute-DRIFT-TENSOR型,德国布鲁克公司;电动搅拌器,HD2004型,上海恒勤仪器设备有限公司;控温电热套,98-I-C型,天津泰斯特仪器有限公司。
1.2 实验方法
萃取实验:将一定量经过预热达到反应温度的模拟废水和经磺化煤油稀释的萃取剂加入萃取器中,用电动搅拌器进行充分搅拌,通过水浴加热保持设定的反应温度(±1 K);待萃取反应结束后,将混合液转移至分液漏斗中静置分层;取萃余液测定硝酸质量浓度,计算分配系数和萃取率,并对负载有机相进行FTIR分析。
反萃实验:将负载有机相与一定量去离子水或氢氧化钠溶液加入萃取器中,常温(298 K)下进行充分搅拌;待反萃结束后,将混合液转移至分液漏斗中静置分层;取水相测定硝酸质量浓度,计算反萃率。
为保证实验数据的准确性,不同条件下的每个萃取和反萃实验均重复3次,取平均值。
1.3 分析方法
采用紫外-可见分光光度计测定水样的硝酸质量浓度;采用傅里叶变换红外光谱仪对萃取前后的有机相进行红外光谱检测。
采用质量平衡法计算有机相中硝酸浓度。按式(1)计算硝酸的萃取率(E,%),按式(2)计算硝酸的分配系数(D),按式(3)计算硝酸的反萃率(SE,%)。
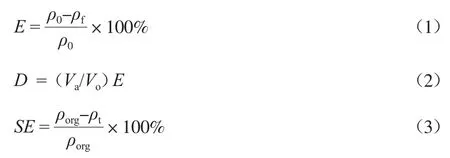
式中:ρ0和ρf分别为水相初始和萃取后的硝酸质量浓度,g/L;Va和Vo分别为水相体积和有机相体积,mL;ρorg和ρt分别为负载有机相和反萃后有机相中的硝酸质量浓度,g/L。
2 结果与讨论
2.1 硝酸萃取
2.1.1 萃取剂的选择
针对硝酸的Lewis酸碱特性,考察了4种不同结构类型的萃取剂对硝酸的萃取性能,即Alamine336、TBP、Cyanex923和仲辛醇。在初始硝酸质量浓度为0.93 g/L、Vo∶Va为1∶1、萃取温度为298 K、萃取时间为300 s的条件下,萃取剂对硝酸萃取效果的影响如图1所示。萃取剂Alamine336对硝酸的萃取能力明显优于其他3种萃取剂;当有机相中萃取剂体积分数从0增至10.0%时,硝酸的萃取率从0升至81.66%;继续增加萃取剂体积分数至20.0%时,硝酸萃取率升至87.18%。综合考虑生产成本和萃取剂浓度因素的影响,选择体积分数为10.0%的Alamine 336为最佳萃取剂较适宜。
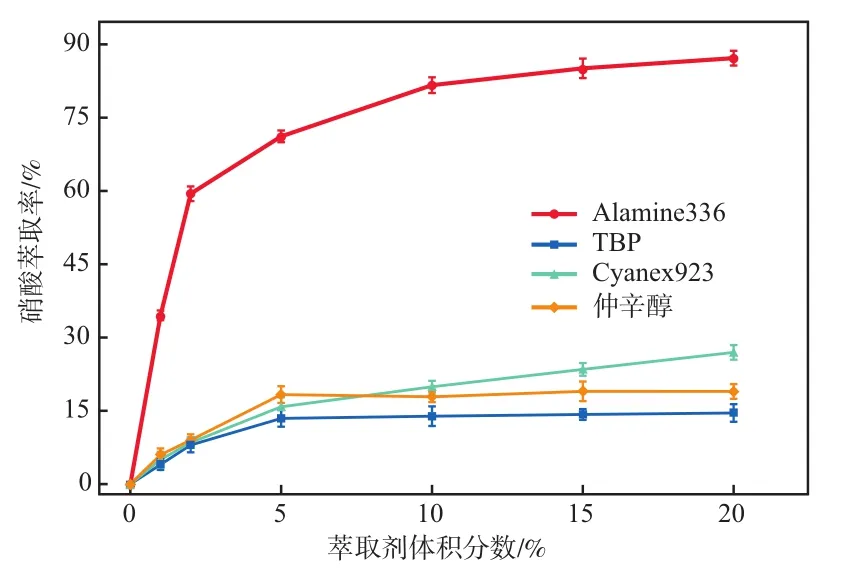
图1 萃取剂对硝酸萃取效果的影响
2.1.2 萃取时间
在初始硝酸质量浓度为0.93 g/L、Vo∶Va为1∶1、萃取温度为298 K的条件下,不同Alamine336浓度下,萃取时间对硝酸萃取率的影响如图2所示。当Alamine336体积为数为2.0%、萃取时间为60 s时,硝酸的萃取基本达到平衡;当Alamine336体积分数升至5.0%和10.0%后,得到的实验结果与2.0%时一致,即萃取时间超过60 s后,萃取率基本不变。为了确保萃取达到平衡,在后续实验中设定萃取时间为120 s。
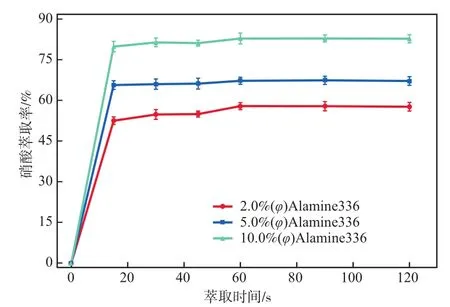
图2 硝酸萃取率随萃取反应时间的变化
2.1.3 初始硝酸浓度
物料相(水相)中待萃物初始浓度对萃取效率有很大影响[13]。在Vo∶Va为1∶1、萃取温度为298 K、萃取时间为120 s的条件下,初始硝酸质量浓度对其萃取率的影响如图3所示。随着初始硝酸浓度的增加,Alamine336萃取硝酸的萃取率显著升高;当初始硝酸质量浓度为2.28 g/L时,萃取率可达93.04%。这可能与Alamine336萃取硝酸的机理有关,不同萃取剂浓度与硝酸初始浓度的比例会导致络合物组成不同[19]。
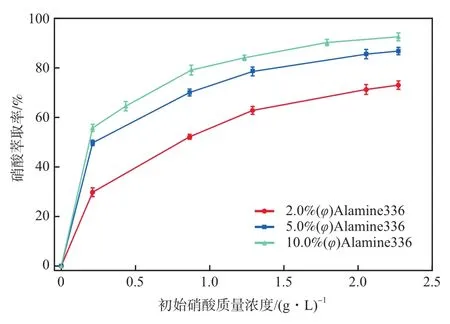
图3 初始硝酸质量浓度对硝酸萃取率的影响
2.1.4 有机相与水相的体积比
有机相与水相的体积比是萃取工艺中的重要参数。在初始硝酸质量浓度为0.93 g/L、萃取温度为298 K、萃取时间为120 s的条件下,Vo∶Va对硝酸萃取率的影响如图4所示。
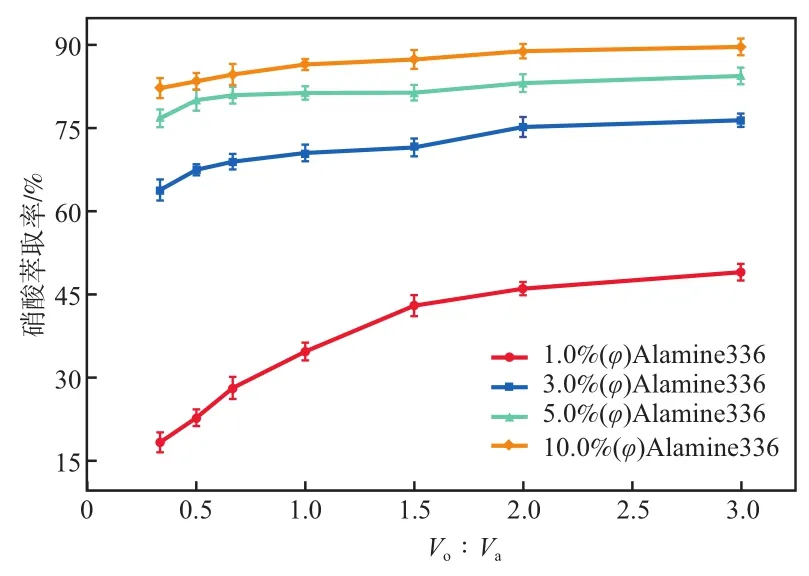
图4 Vo∶Va对硝酸萃取率的影响
提高有机相与水相的体积比,硝酸的萃取率随之增加。当萃取剂浓度较低时(1.0%(φ)Alamine336),萃取率随Vo∶Va的增大而明显增加;当萃取剂浓度较高时,Vo∶Va对萃取率的影响减弱。Vo∶Va较大时,有机萃取剂的利用率较低,实际运行过程中会降低工艺流程的处理能力,导致运行成本增加。
在初始硝酸质量浓度为1.01 g/L、萃取温度为298 K的条件下,用10.0%(φ)Alamine336的有机相与含硝酸的水相在不同相比下进行萃取,通过测定硝酸在两相中的平衡浓度,得到硝酸的萃取平衡曲线。根据萃取平衡曲线和操作线(Vo∶Va为1∶2)绘制McCabe Thiele图,结果如图5所示。对于初始硝酸质量浓度为2.00 g/L的废水,通过两级逆流萃取操作后,理论上硝酸残余量可小于15 mg/L,达到我国《污水综合排放标准》(GB 8987—1996)[20]中硝酸盐氮的一级排放标准(15.0 mg/L)。
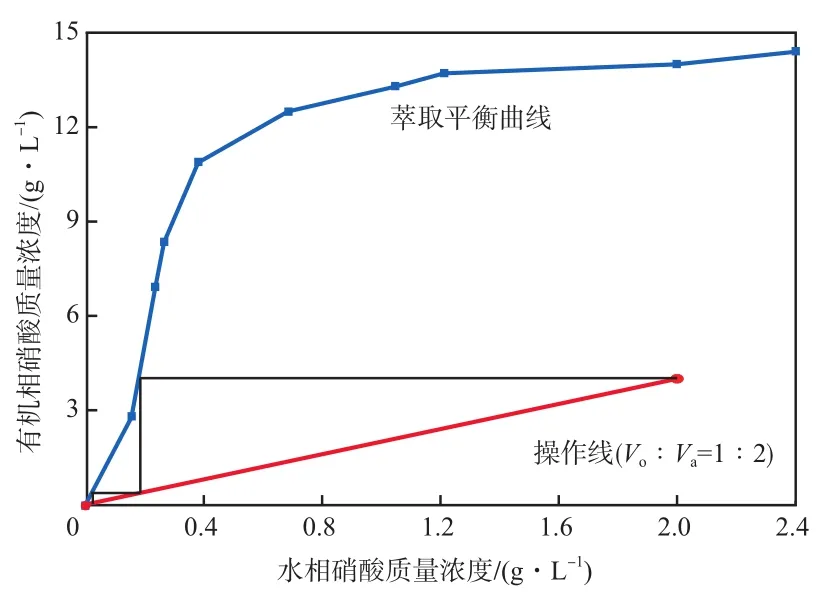
图5 硝酸萃取的McCabe Thiele图
2.1.5 萃取温度
萃取温度通过影响萃取平衡常数和萃合物在两相中的分配比而影响萃取率。在初始硝酸质量浓度为0.93 g/L、Vo∶Va为1∶1、萃取时间为120 s的条件下,以10.0%(φ)Alamine336为萃取剂,萃取温度对硝酸分配系数的影响如图6所示。随着萃取温度的升高,硝酸的分配系数逐渐减小。
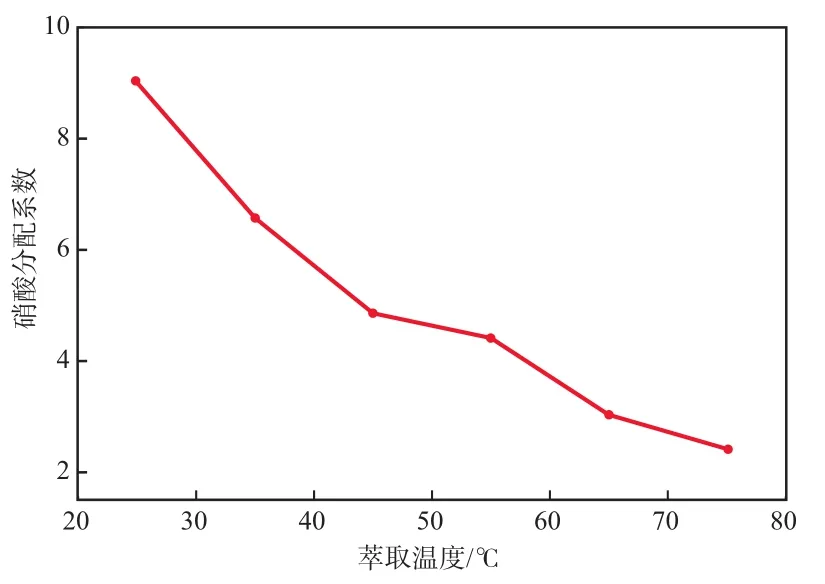
图6 萃取温度对硝酸分配系数的影响
萃取反应的焓变∆H可以通过Van’t Hoff方程按式(4)求得[21]。以lgD对1/T做图,通过拟合直线的斜率计算可得,∆H为-22.530 kJ/mol,说明Alamine336萃取硝酸为放热反应。若萃取温度过高,则不利于硝酸的萃取[12],且会促进有机溶剂的溶解。但过低的温度会使萃取剂黏度增加,不利于相间传质。因此,选择萃取温度为298 K较适宜。

式中:R为摩尔气体常数,8.314 47 J·(mol·K)-1;T为萃取温度,K;C为该体系中与初始条件相关的常数。
2.2 硝酸反萃
Alamine336在萃取硝酸后需要进行反萃再生,由于Alamine336通过离子对缔和机制萃取硝酸,故使用碱性反萃剂破坏离子对结构进行反萃。NaOH为最常见的碱性物质,故使用NaOH溶液作为反萃剂对负载于有机相中的硝酸进行反萃。
2.2.1 NaOH浓度对反萃率的影响
在硝酸负载量为1.42 g/L、反萃有机相与水相的体积比(Vo'∶Va')为1∶1、反萃温度为298 K、反萃时间为300 s的条件下,NaOH浓度对反萃率的影响如图7所示。随着反萃剂中NaOH浓度的增加,硝酸反萃率明显提高;当NaOH浓度达到0.05 mol/L时,硝酸反萃率可达80.88%。实验中持续增加反萃相中NaOH浓度时,反萃效果并未得到较大提升。
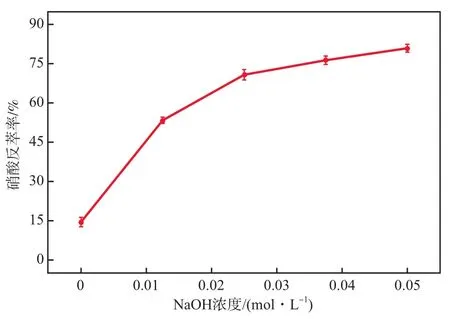
图7 NaOH浓度对硝酸反萃取率的影响
2.2.2 有机相与水相的体积比对反萃率的影响
在硝酸负载量为1.42 g/L、NaOH浓度为0.05 mol/L、反萃温度为298 K、反萃时间为300 s的条件下,探究Vo'∶Va'对反萃效果的影响,结果如图8所示。随着Vo'∶Va'的降低,有机溶剂中硝酸的反萃率逐渐增加,当Vo'∶Va'为1∶2(0.5)时,反萃率达到85.80%;进一步降低Vo'∶Va',反萃率上升减缓,且会促进有机相在水相中的溶解。因此,选择Vo'∶Va'为1∶2、NaOH浓度为0.05 mol/L较适宜。
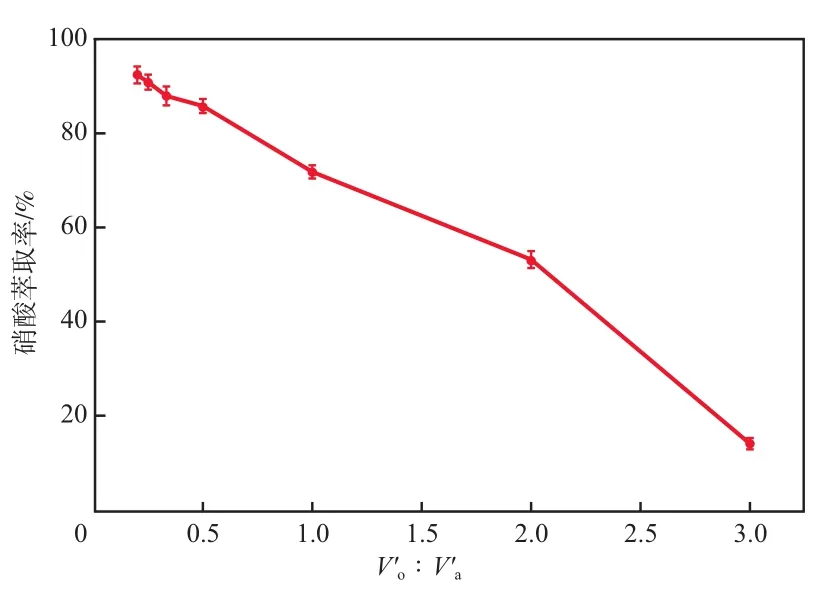
图8 Vo'∶Va' 对硝酸反萃率的影响
使用0.05 mol/L的NaOH溶液在298 K下对硝酸负载量为1.50 g/L的有机相进行不同相比的反萃实验,通过测定硝酸在两相中的平衡浓度,得到反萃平衡曲线(图9)。当Vo'∶Va'为1∶2时,绘制McCabe Thiele图(见图9)。通过两级反萃后,理论上硝酸反萃率大于96.70%,有机相中的硝酸残余量小于0.005 g/L。
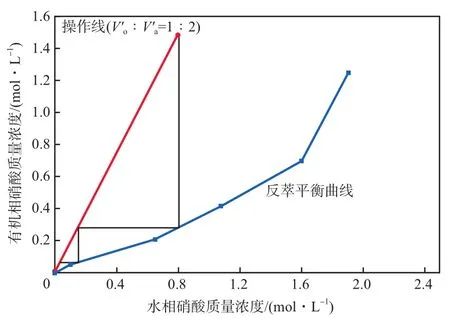
图9 硝酸反萃的McCabe Thiele图
2.3 萃取机理分析
本实验通过推算硝酸与萃取剂的配合物组成比[22]对Alamine336萃取硝酸的反应机理进行探究。假设萃取剂Alamine336与硝酸的反应式为:
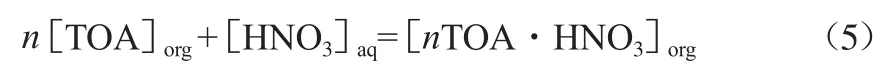
式中:n为化学计量比;下标org和aq分别代表有机相和水相;[ ]代表平衡浓度。
萃取平衡常数(Kex)为:

分配系数为:

则有:
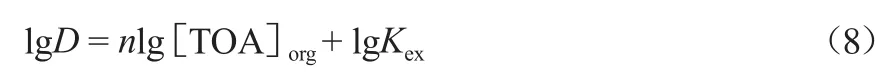
当萃取剂Alamine336浓度大于硝酸浓度时,可假设Alamine336的平衡浓度[TOA]org等于其初始浓度[TOA]0。此时,将D与[TOA]org在不同萃取剂初始浓度下的实验数据(298 K)进行双对数坐标系拟合,由直线斜率可得n值,如图10所示。
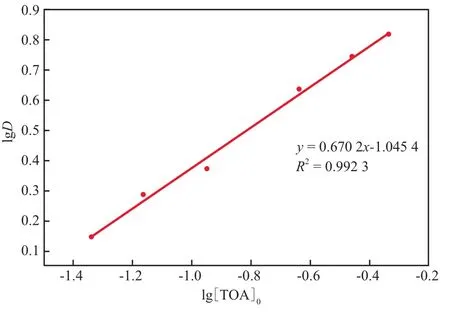
图10 Alamine336萃取硝酸的lgD~lg[TOA]0关系图
根据图10,n接近2/3,故萃取剂与硝酸的反应式可能为:
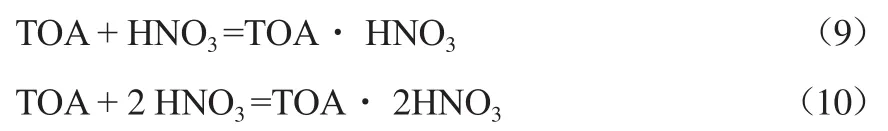
秦启宗等[14]认为,萃取剂Alamine336在萃取硝酸时分为3种状态:1)低酸浓度状态。Alamine 336具有弱碱性,物料相中酸度浓度低于Alamine 336浓度时,萃取是通过中和反应实现的;2)中酸浓度状态。当物料相中硝酸浓度大于Alamine 336浓度时,物料相中的硝酸持续被萃取,直至完全生成一硝酸盐[R·HNO3]org;3)高酸浓度状态。生成的一硝酸盐进一步与物料相中的硝酸发生反应,生成[R·nHNO3]org[23]。但也有研究者认为高浓度硝酸是通过物理分配的形式进入有机相的[20]。
为了进一步研究硝酸的萃取机理,分别对萃取前后的有机相进行FTIR扫描,结果见图11。
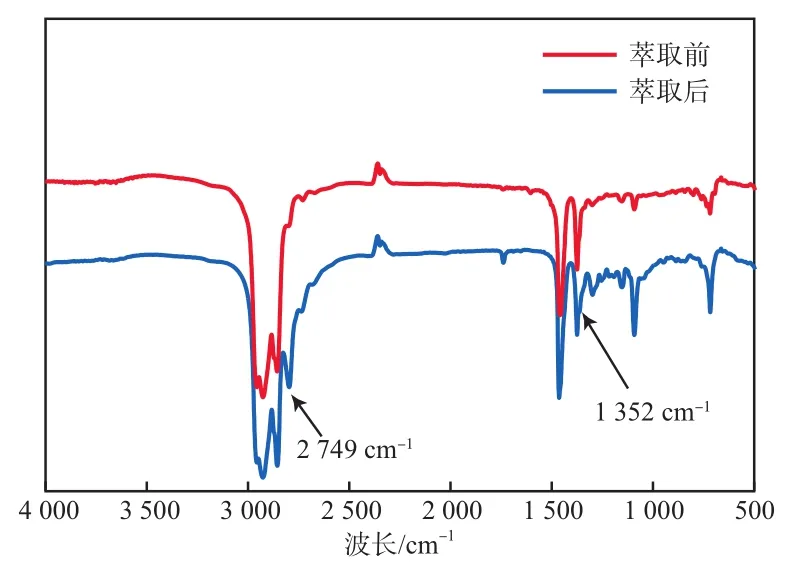
图11 萃取前后有机相的FTIR谱图
由图11可见,负载有机相在2 749 cm-1和1 352 cm-1处出现新的吸收峰,这可能是硝酸根的氮氧键反对称拉伸振动引起的。叔胺中氮原子由于存在孤对电子,可以与无机酸中游离的氢离子形成氢键[24],说明Alamine336通过与硝酸形成离子对络合物来萃取硝酸[25-26]。
3 结论
a)通过比较确定了Alamine336为低浓度硝酸萃取分离的萃取剂,随着萃取剂浓度和水相中硝酸浓度的增加,硝酸萃取率逐渐增加。
b)以10.0%(φ)Alamine336为萃取剂,在Vo∶Va为1∶2、萃取温度为298 K的条件下,对初始硝酸质量浓度为2.00 g/L的含硝酸废水进行两级逆流萃取操作后,理论上水相硝酸质量浓度低于15 mg/L,达到《污水综合排放标准》(GB 8987—1996)中的一级标准。
c)以0.05 mol/L氢氧化钠溶液为反萃剂,在Vo'∶Va'为1∶2、反萃温度为298 K的条件下,对硝酸负载量为1.50 g/L的有机相进行两级反萃后,理论上有机相硝酸残余量小于0.005 g/L。
d)Alamine336通过与硝酸形成离子对络合物来萃取硝酸。不同酸度下硝酸在有机相中的存在形式分别为TOA∙HNO3和TOA∙2HNO3。

