双重超声造影对胃癌术前T分期诊断的价值
杜润家 管玲 韩飞容 王卫丽 陈晓亮
甘肃省肿瘤医院,甘肃 兰州730050
胃癌是最常见的消化道恶性肿瘤之一,2010年WHO公布的全球统计报告显示,胃癌年发病率为213.86/10万,仅次于肺癌,居恶性肿瘤第二位[1]。胃癌患者早期临床症状表现不明显,少数患者存在恶心、呕吐或类似溃疡等上消化道反应症状,而进展期患者多以胃部疼痛、体重减轻等症状为主[2]。胃癌患者临床治疗中,术前病症分期是进行合理治疗方案的制定和预后判断的重要前提,对患者治疗及预后都存在较大的影响,目前常见的术前诊断方式包括超声、CT以及核磁共振、腹腔镜等,其在临床应用中均具有各自的特征优势和不足[3]。本研究探讨两种超声造影方式对胃癌手术患者术前超声T分期检查及诊断的价值,报告如下。
1 资料与方法
1.1 一般资料 选取我院2018年3月至11月收治的50例胃癌手术患者,其中男性31例,女性19例,年龄25~70岁,平均(51.6±10.2)岁,体重41~65kg,平均(52.7±8.6)kg,病变部位包含贲门6例、胃底部8例、胃体部20例以及胃窦部16例。
1.2 纳入与排除标准 纳入标准:①经胃镜组织病理证实的胃癌患者;②首诊入院并直接手术的患者;③年龄为20~70岁患者;④心肺功能正常的患者。排除标准:①既往有浅表性胃炎、慢性胃炎病史的患者;②新辅助化疗的患者;③因其他病史进行化疗或服用生物制剂的患者;④心肺功能异常的患者。
1.3 方法 所有患者于术前分别实施胃窗超声造影与双重超声造影检查,并以患者手术病理检查结果为金标准,对患者术前T分期诊断的价值进行对比研究。方法如下:取速溶胃肠超声助影剂(湖州东亚医药用品有限公司,规格:50g)50g,倒入杯中,用90~100℃开水冲泡至500~600mL,迅速搅拌成均匀糊状,冷却至适宜温度(一般控制在30~50℃)口服。检查前患者需禁食8小时以上,一次性喝完调制好的胃窗助影剂溶液5~10分钟后,取平卧位、侧卧位多切面多角度进行扫查,动态的观察从贲门至胃底、胃体、胃窦部、胃周及其周围组织结构和脏器情况,仔细观察肿瘤的部位、大小和形态及侵犯胃壁的层次、范围和程度,同时了解胃周淋巴结、邻近和远处器官转移状况,进行T分期判断。双重超声造影时开启造影CPS模式,图像调节成造影状态,患者平静呼吸,从肘静脉迅速注射SonoVue造影剂六氟化硫SF6微泡2.4mL(意大利Bracco公司,规格:59mg),继续观察肿瘤病变大小、范围和侵犯胃壁的深度有无改变以及血流微循环的灌注、是否伴有坏死液化等情况,根据造影的显示再次分析,对T分期进行进一步的修正。上述检查使用仪器为GE Logiq9/E8型彩色多普勒超声诊断仪,超声诊断系统和声学定量分析软件、CPS成像技术,频率为3.5~5.0MHz的腹部探头。
1.4 分期判断标准 胃癌T分期按照美国癌症联合委员会胃癌TNM分期标准进行判断,T1期:肿瘤对黏膜肌层或黏膜下层造成侵犯;T2期:肿瘤侵犯超过黏膜下层,但局限于固有肌层;T3期:肿瘤穿破固有肌层到达浆膜下的结缔组织,但并未对脏层的腹膜及其邻近结构造成侵犯;T4期:肿瘤对浆膜(即脏层腹膜)或者是邻近结构造成侵犯。超声造影检查的胃癌T分期,根据上述分期标准,分析肿瘤组织动脉期“正性显影区”与静脉期“负性显影区”特征,结合显影区累及范围对T分期进行判断[4]。
1.5 统计学分析 采用SPSS16.0统计软件进行数据分析,计数资料采用χ2检验,P<0.05为差异有统计学意义。
2 结果
2.1 术后病理情况50例胃癌手术患者,单发癌变患者47例,多发癌变患者3例,癌变病灶为2~4个。患者癌变病灶T分期诊断显示,T2期患者11例,表现为肿瘤病变影响到肌层组织,且动脉期整体出现增强变化,静脉期对黏膜、黏膜下层、固有肌层造成浸润;T3期患者31例,表现为动脉期“正性显影区”浸润变化达到浆膜层;T4期患者8例,包含累及食管患者2例、肝脏患者2例、胃周及腹腔淋巴结患者4例。
2.2 两种超声方式术前T分期准确率比较 双重超声造影在患者术前T分期判断的准确率较胃窗超声造影高,差异有统计学意义(P<0.05)。见表1。
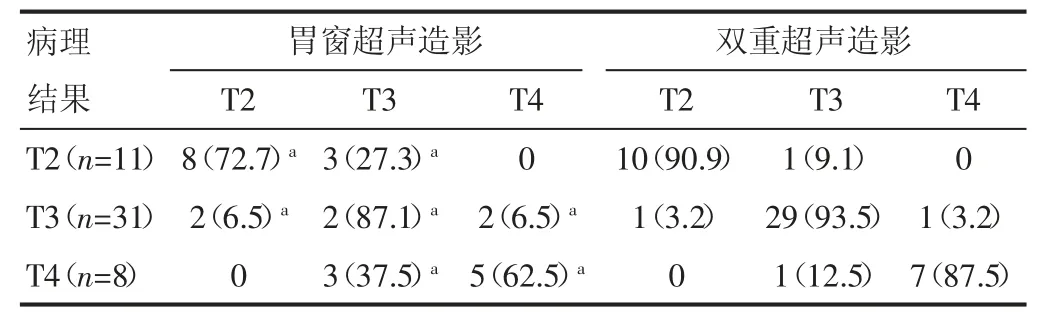
表1胃窗超声造影与双重超声造影在胃癌术前T分期诊断结果对比[例(%)]
3 讨论
胃癌是常见的消化系统恶性肿瘤,早期症状表现不明显,导致其临床诊断与发现难度较大。有研究显示,早期胃癌患者的临床治愈率相对较高,患者癌变发生后如果能早期诊断,生存周期可持续为2~3年[5]。由此可见,临床中胃癌患者的病症早期发现并准确诊断,将明显提升患者的临床治疗及预后效果,减少病症对患者的危害。近年来,随着我国医学影像技术的不断发展与应用,胃癌的诊断率有明显提升,正确的诊断及准确的术前分期,选择手术方案、判断预后和术后随访对患者都具有重要临床意义。临床中对胃癌的检查诊断方式和手段较多,如CT、超声以及核磁共振、超声内镜及PET等,其在临床应用中都各自具有不同的特征和优势。超声在临床应用中,因其安全性好,具有无创、重复性及价格较低等优势,受到临床和患者的认可。
首先,胃窗超声造影是把胃本身作为一个空腔器官,在呼吸运动与自体蠕动时因其内部包含空气、胃液等,对患者胃部病症常规超声检查时难度较大,诊断准确率造成影响,因此,通过口服胃窗造影剂能够促使胃部气体排出,减少超声检查时的伪像影响,促进超声在胃部疾病的检查准确率提升[6]。其次,胃窗超声造影在胃癌检查与诊断中,可以清晰地显示胃壁正常的“三强两弱”5层结构,能够对病变位置、形态以及周围正常胃壁结构等进行清晰地显像,同时结合胃壁层次结构的破坏及浸润深度等情况进行判断。但是由于在超声分辨力的限制以及部分组织结构的声阻抗差异性较小等因素的影响下单纯口服胃窗超声造影检查时很难把浸润性生长的肿瘤组织与炎症的反应性水肿、纤维脂肪组织的反应性增生和肿瘤周围组织的炎性反应等区分开。
双重超声造影是在胃窗超声造影的基础上,进行静脉造影剂注射。静脉超声造影剂又称为全血池造影剂,其具有渗透不到组织间质、造影剂微泡到达脏器组织中的数量及其进出快慢的特点可以直观地反出映该组织的微循环血流灌注状况。临床研究表明,静脉超声造影可快速清晰地显示脏器组织和微小血管的血流灌注,增强图像的对比度以及分辨率,从而有利于明确诊断常规超声难以发现的肿瘤,提高了超声检查的敏感性和特异性[7]。肿瘤浸润性生长的特点之一就是新生血管的形成,其往往伴有动-静瘘,缺如的血管壁平滑肌,无血管收缩-舒张的变化,因此导致血流的阻力降低、血流的速度增快等特点,根据造影图像显示,“正性显影”是指动脉期时瘤体先与周围组织呈现快速增强,“负性显影”是指静脉期时瘤体中的造影剂先于周围组织廓清,双重超声造影就是依据这两个显影区的特点以及肿瘤的大小、深度、范围与其周围组织的解剖关系进行T分期,结果明显优于单纯口服胃窗造影。
双重超声造影可根据造影剂对不同组织灌注差异的特点,把肿瘤与肿瘤旁的周围组织区分开。许多坏死物质依附于部分肿瘤组织表面,单纯口服胃窗超声造影,很难将这些坏死组织区分开,肿瘤整体的观察受到一定影响;而双重超声造影时可以开启造影的CPS软件模式,静脉造影时气泡所产生的非线性信号可被单纯提取、并且还可以过滤掉肿瘤表面坏死物质及其口服造影剂时胃腔内所产生的基波信号干扰,因此并未受到肿瘤表面坏死物质的影响,在癌肿分期上优于单纯口服胃窗造影。
综上所述,双重超声造影检查是在口服胃窗超声造影剂与静脉造影剂联合应用下,能够清晰地显示胃壁各个层次的解剖结构以及血流微循环灌注等情况,可对病变的肿瘤及其周围组织造影灌注进行实时动态监测与观察分析,为胃癌术前提供解剖基础和肿瘤微循环灌注评价,应用于术前进展期胃癌T分期判断准确率较高,临床应用价值更为显著。

