后弹力层剥除联合角膜内皮移植手术技巧在大泡性角膜病变中的应用
程 燕,吴 洁,朱海峰,惠 玲,李 波
0引言
一直以来,角膜移植手术是治疗角膜内皮病变的主要手术方式,然而该手术方式具有诸多缺点,如术中眼内组织完全暴露,易出现爆发性脉络膜出血或眼内容物脱出等严重并发症;同时术后因缝线导致不规则散光也是视力不能有效提高的主要原因,且很难矫正。基于以上,眼科医生及相关专家于2000年提出角膜内皮移植术(endothelial keratoplasty,EK),该手术方式克服了上述缺点,成为更加完美的治疗角膜内皮病变的手术方式。随着技术的不断进步和发展,角膜内皮移植术在近年快速发展,具有多种手术方式,其中角膜后弹力层剥除联合自动角膜刀取材的角膜内皮移植术(descemet’s stripping automated endothelium keratoplasty,DSAEK)[1-2]因其手术技术相对较易掌握,取材容易等优点,目前仍然是国内的主流手术方式。但是,植片脱位及层间积液等并发症亦时有发生[3-5]。本研究中我们对DSAEK术中的手术技巧进行了探索研究,并应用于临床实践,取得了良好的临床效果。现报告如下。
1对象和方法
1.1对象回顾性分析研究。收集2018-12/2019-12在我院眼科入院的因不同原因导致的大泡性角膜病变患者10例10眼,其中男4例4眼,女6例6眼,年龄50~69(平均59.3±11.4)岁,均为单眼发病,病程3mo内。患者临床表现为眼磨、眼疼、畏光流泪及视物模糊;裂隙灯检查示角膜呈水肿状态,角膜上皮下大量水泡,角膜基质增厚,后弹力层皱褶,前房深度正常,眼压正常;眼前节光学相干断层成像仪(anterior segment optical coherence tomography,AS-OCT)提示角膜厚度600~1000μm,均符合大泡性角膜病变临床诊断。其中,3眼为白内障超声乳化术后所致大泡性角膜病变;1眼曾因人工晶状体脱位行玻璃体切除手术,术后角膜内皮失代偿;1眼白内障超声乳化术中后弹力层脱位,后经反复前房注气使后弹力层复位失败所致大泡性角膜病变;2眼因Fuchs角膜内皮营养不良导致大泡性角膜病变;3眼为白内障联合青光眼术后角膜内皮失代偿导致大泡性角膜病变。排除感染性角膜疾病所导致的角膜水肿、合并青光眼、色素膜炎及伴有自身免疫性疾病的患者。本研究遵守《赫尔辛基宣言》,且已通过医院伦理委员会审批。
1.2方法
1.2.1手术方法所有患者及其家属均对手术知情同意,并签署手术知情同意书。手术均由同一位主刀医师完成。术前,所有患者均检查最佳矫正视力(best corrected visual acuity,BCVA)和眼压,采用裂隙灯显微镜观察角膜及前房反应,AS-OCT测量角膜中央厚度(central corneal thickenss,CCT)并明确植片位置,角膜内皮细胞分析仪观察角膜内皮细胞情况。
1.2.1.1植床的制备患眼球后麻醉,刮除水肿的角膜上皮,根据角膜大小用直径为7.5~8.0mm的环钻于角膜表面压痕,用标记笔使压痕清晰可见。在角膜缘8∶00位隧道切口穿行角膜约3mm进入前房,切口方向朝向6∶00位,插入前房灌注管维持前房稳定(图1A、1B)。3∶00、6∶00位角膜缘内常规辅助侧切口。11∶00位辅助侧切口进入前房,并伸入角膜后弹力膜钩沿标记线环形划开角膜后弹力层(图1C、1D),用宽剥离钩将标记范围内的后弹力层从后基质表面完整剥下,此时前房仍维持稳定。分别在角膜12∶00、6∶00、3∶00及9∶00位视轴周边区域角膜穿刺刀垂直穿刺角膜至房水渗出(图1E、1F)。

图1 植床制备的手术过程
1.2.1.2供体角膜后基质内皮植片的制备本组患者所使用角膜供体来源于西安市眼库,均为意外死亡的供体捐献的角巩膜片(Optisal中期保存液保存,3d内使用),供体年龄35~60岁,排除乙型肝炎、梅毒、艾滋病及丙型肝炎等传染病、肿瘤及血液病患者,供体角膜内皮细胞计数均大于2500个/mm2。将供体角巩膜片固定于人工前房上,采用自动角膜刀取材。将人工前房上固定好的角巩膜片去上皮,用300μm深度的角膜刀进行切削,将切削下的角膜基质复位,取下角膜供体片,内皮面向上置于负压切割枕上,负压环钻钻切与植床直径等大的角膜,在植片中央滴少许黏弹剂保护角膜内皮,将内皮植片拖入内皮植入器并折叠备用。
1.2.1.3移植前房灌注开放,在12∶00位角膜缘行隧道穿刺入前房,隧道刀直径约3.2mm,6∶00位穿刺口伸入植入专用镊至主切口,从植入器中将内皮植片植入前房,10-0缝线缝合主切口,自侧切口注入眼用平衡盐溶液加深前房,并使植片展开,侧切口注入消毒空气于前房内,顶压角膜内皮植片。缝合辅助切口,术毕。患者仰卧位4h后观察眼压及植片贴附情况。1wk内避免剧烈运动。
1.2.2随访观察术后1wk内每天检查视力、眼压,观察植片植床愈合情况、角膜植片脱位及角膜移植术后排斥反应等并发症发生情况。以后每周复查1次,每次随访均检查BCVA,采用裂隙灯显微镜观察角膜及前房反应,AS-OCT测量CCT并明确植片位置,角膜内皮细胞分析仪观察角膜内皮细胞计数(endothelial cell density,ECD)。病情稳定者随访周期适当延长,随访至术后6mo。
统计学分析:采用 SPSS 17.0统计软件进行数据分析。计量资料采用均数±标准差描述,手术前后的比较采用配对样本t检验。P<0.05为差异有统计学意义。
2结果
2.1角膜内皮植片贴附及并发症情况所有患者均顺利完成手术,无术中并发症发生。术后角膜植片脱位及角膜移植术后排斥反应等并发症未见发生。术后4h,3例3眼患者眼压升高,裂隙灯检查气泡充满前房,测眼压均达40mmHg以上,判断为瞳孔阻滞性青光眼,立即行前房穿刺放气后眼压降至正常。术后第1d,裂隙灯显微镜下见10例10眼患者角膜内皮植片位置居中,基质层面与植床贴附良好,均未见植片与植床之间存在层间积液。角膜畏光、眼磨等刺激症状自术后1d开始逐渐减轻,术后2wk完全缓解。随访期间,所有患者眼压正常,角膜植片保持透明,均给予醋酸泼尼松龙滴眼液、环孢素滴眼液及玻璃酸钠滴眼液长期点眼,4次/d,2mo后减为3次/d,并逐渐减量。
2.2视力、眼压、角膜厚度及内皮细胞计数情况本组患者术后角膜植片贴附良好,角膜透明(图2)。术后视力均改善,视力提高程度不同患者间有明显差异;术前视力改善最明显的患者视力由术前的0.05提高至0.6,为1例白内障超声乳化联合人工晶状体植入术后角膜内皮失代偿1mo的58岁女性患者;60%的患者术后视力维持在0.2~0.4。术后1mo,本组患者植床基质层水肿明显减轻,AS-OCT显示CCT由术前的874.0±58.64μm 降至596.8±19.11μm(包括内皮植片),差异有统计学意义(t=6.16,P=0.001),且随访期间持续稳定。术前,本组患者经角膜内皮镜和共焦显微镜检查均未见角膜内皮细胞,无法计数,术后随访,所有患者随时间延长角膜内皮计数逐渐减少,见表1。
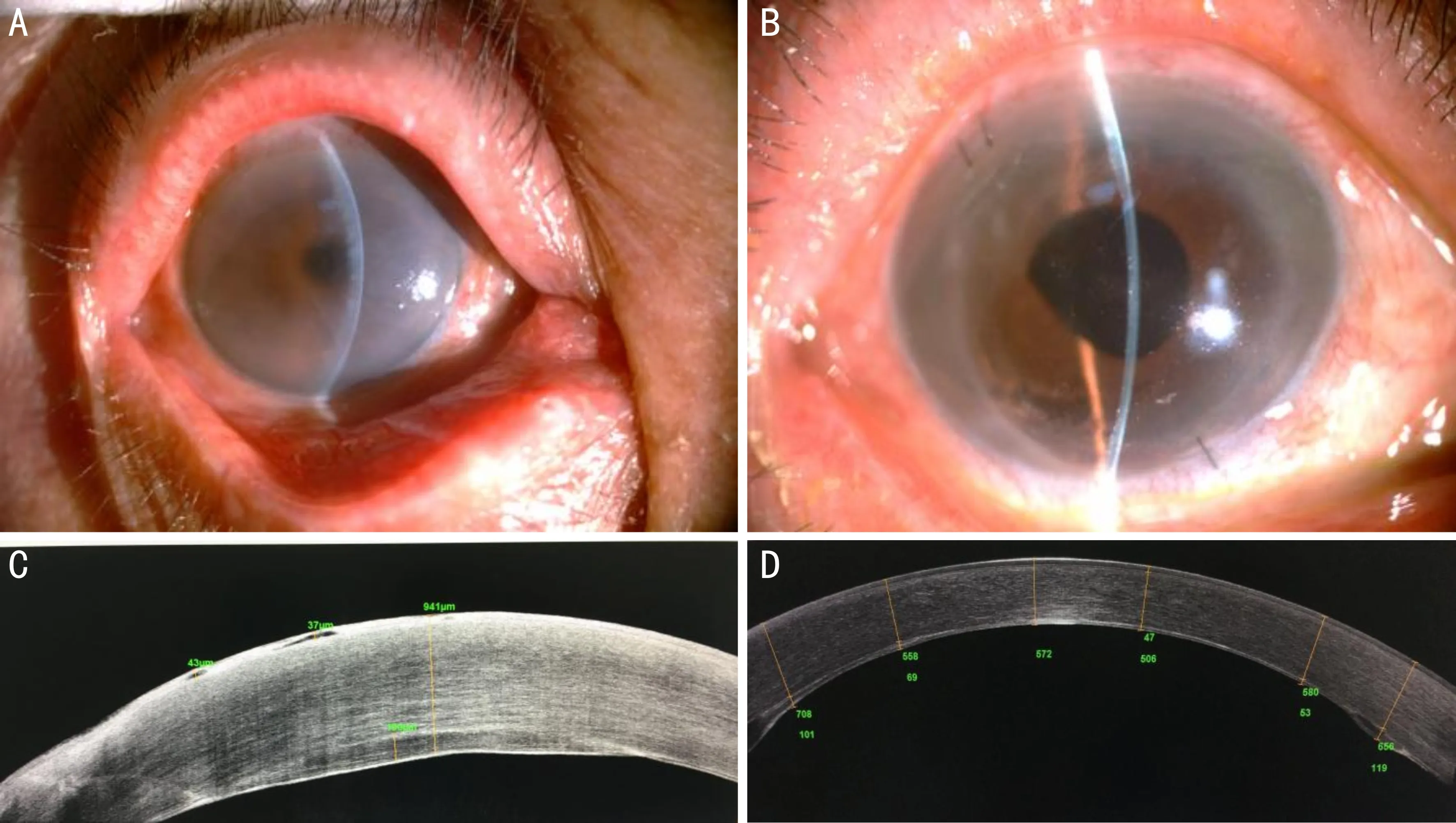
图2 患者,女,69岁,右眼行白内障超声乳化吸除联合人工晶状体植入术后曾行前房注气2次,后弹力层复位失败,反复眼红、眼疼、眼磨2wk,糖尿病史,入院行右眼DSAEK术
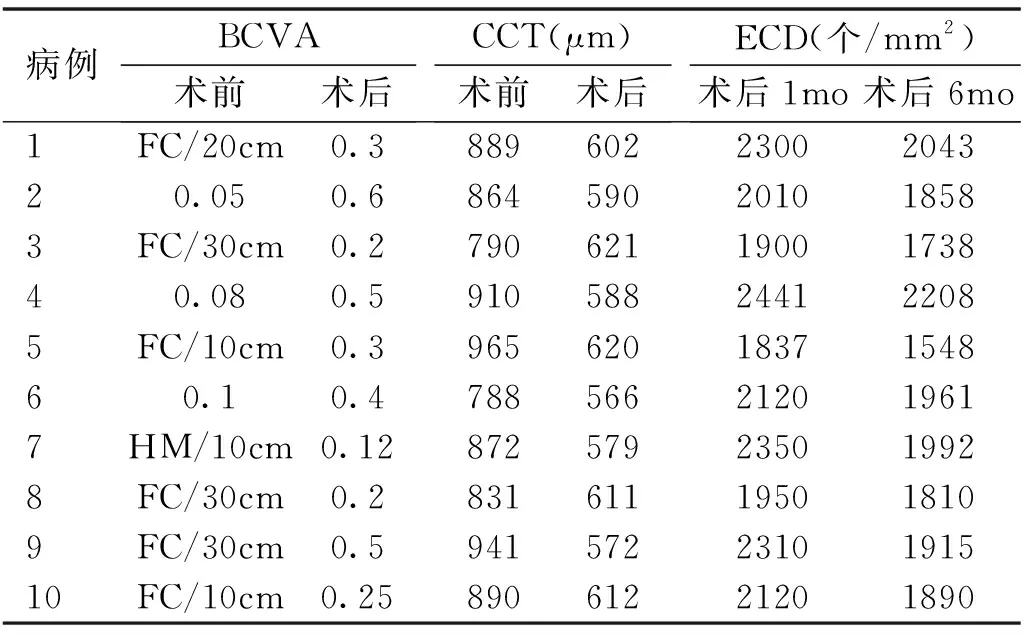
表1 手术前后视力、眼压、角膜厚度及内皮细胞计数
3讨论
众所周知,角膜内皮细胞是不可再生的,角膜内皮细胞损伤后的修复主要依靠临近细胞的移行与扩展。各种原因,如 Fuchs角膜内皮营养不良、内眼手术的开展(白内障超声乳化吸除术、前房型人工晶状体植入术、玻璃体手术等)、外伤等均可导致角膜内皮细胞数量减少或功能受损,失去液体屏障和主动液泵功能,最终导致角膜内皮细胞功能失代偿,不足以维持角膜的透明性[6]。角膜水肿致使视力急剧下降,角膜上皮下大泡与眼睑摩擦导致剧烈眼痛,角膜基质层增厚,后弹力层皱褶等均是大泡性角膜病变典型的临床症状和体征。随着角膜内皮移植技术的不断发展和完善,其无疑是解决角膜内皮病变的最佳手术方式[7-8],其中DSAEK是目前的主流手术方式[9],但术中及术后并发症并不罕见[10]。本研究中,我们在DSAEK常规手术技术的基础上对手术细节及技巧进行了探索,在减少术中及术后并发症方面具有一定意义和作用。
首先,在进行前房灌注管的设置方面,我们采用了斜行隧道穿刺,且穿刺口方向与主切口方向相同而不是相对或垂直。前房灌注管的位置及稳定性影响了角膜内皮移植的整个手术过程。初期需要稳定的前房深度以便于进行病变角膜内皮细胞和后弹力层的剥除;在植入内皮植片的过程中稳定的前房能够保证有足够的操作空间,对于保护角膜内皮细胞的数量至关重要;在内皮植片的后期展开过程中需要前房深度的变化以调整植片的位置和正反面。所以,前房灌注采用较长的隧道切口防止了前房灌注管的脱出,保证了整个手术过程中前房的稳定。另外,本研究中前房灌注的方向与手术主切口远离,即如果主切口在12∶00位,那么前房灌注穿刺口朝向6∶00位。这样,在开放灌注管时植片不会在瞬间受到巨大水流的冲击而从主切口脱出,减少前房灌注时水流对植片的冲击作用,会使角膜内皮细胞减少损失。本研究中所有患者均未出现植片在植入过程中脱出的情况。
其次,我们在进行前房灌注管的设置之后,先行主切口旁的辅助切口,并在此切口进行角膜后弹力层的剥除操作,然后再做主切口,这样可以避免直接行主切口后前房变浅,在进行角膜后弹力层的剥除操作时必须先注入黏弹剂以维持前房稳定,但在植入内皮植片前必须将前房内的黏弹剂吸除干净,否则残留在前房内的少许黏弹剂可能会存在于植片与植床中间,导致术后角膜内皮植片脱位[11]。主切口旁辅助切口的后弹力层剥除操作可有效减少了术中黏弹剂的应用,降低术后内皮植片的脱位率。
此外,在角膜内皮植片植入之前,我们在非光学区角膜周边部位行角膜4个点的垂直穿刺微切口入前房,直到有房水渗出。微穿刺口的目的主要是在植入角膜内皮植片后,前房注气进行内皮植片的顶压,微穿刺口可以有效排出植片植床层间的积液,使得两层能够紧密贴合,同样在一定程度上有效避免了术后植片脱位或贴附欠佳,避免了二次角膜植片复位。
综上所述,角膜内皮移植手术是治疗各种原因角膜内皮疾病所致的大泡性角膜病变的最佳手术方式,但是术中内皮植片的脱出、植片的展开困难及术后角膜内皮植片的脱位、排斥反应等情况亦是时有发生。本研究在进行经典手术操作的同时,在手术的技巧及细节上进行探索改进,可有效减少术中术后并发症的出现,提高手术的安全性和有效性,具有一定的临床意义。

