回春散预防和治疗热性惊厥实验研究*
★ 吴兰生 张志明 罗红婷(.广东健泉大健康产业开发股份有限公司 广东 佛山 5800;.顺德职业技术学院 广东 佛山 58300)
热性惊厥(FC)是小儿时期最常见的惊厥性疾患,约占小儿惊厥的50%,在6岁以下的发病率近5%。因发生惊厥可能会导致神经元的损伤,而神经元的损伤是不可以修复,从而将影响到某些发育障碍。因此预防和治疗热性惊厥的安全药品是现代儿科学的研究热点。回春散源于《敬修堂药说》中的“小儿回春丹”,收录于中医院校本科教材《方剂学》(开窍剂“凉开节”)中[1],其汤头歌为“回春丹中用四香,蔻枳星夏并牛黄;钩蚕陈贝麻全蝎,朱砂草竹共大黄”。同时回春散也被收录于《儿科中医医疗技术及中成药用药指导》中的“上呼吸道感染”治疗用药[2]。其适应症为用于小儿惊风,感冒发热等。临床多有使用,但其作用机制不完全清楚。本实验通过药理学研究,发现其作用机制与大脑组织神经递质含量改变控制有关。
1 受试药物和试剂
回春散,生产单位:国药集团冯了性(佛山)药业有限公司,批号:190001;规格:0.3 g/袋,3袋/盒。地西泮片,生产单位:,批号,规格。Υ-氨基丁酸(GABA)酶联免疫测试盒,生产单位:南京建成生物工程研究所,批号:H16820190507。谷氨酸(Glu)测试盒,生产单位:南京建成生物工程研究所,批号:20190523。
2 试验动物和分组
购入21 d幼龄SD大鼠,生产单位:广东省医学实验动物中心,实验动物生产许可证号为:SCXK(粤)2018-0002,广东省科学技术厅颁发。在动物房正常饲养2 d,温度20.0℃~25.4℃;湿度65.8%~71.0%。以热水浴方法诱导高热惊厥,最终温度确认为46℃,此次筛选的试验大鼠均在5 min内发生惊厥,随机将选出的75只大鼠分成5组:正常组,模型组,地西泮组,回春散低剂量组,回春散高剂量组。
3 主要仪器
水浴槽(自制,将40 cm×40 cm×50 cm分成4个小格,置于恒温水箱中);BS-110S电子天平(北京赛多利斯天平有限公司);TG-16W台式微量高速离心机(长沙湘智离心机仪器有限公司)。
4 剂量设计和实验方法
将选出的75只大鼠,正常组以室温进行水浴[3],模型组和用药组水浴的温度为46℃。正常组和模型组灌胃生理盐水,每日2次,连续2 d。其他3组给药剂量如下:地西泮组:2.632 mg/kg灌胃(相当于儿童0.5 mg/kg临床用量等效量),每日2次,连续2 d;回春散低剂量组:108 mg/kg灌胃(相当于儿童20 mg/kg临床用量等效量),每日2次,连续2 d;回春散高剂量组:354 mg/kg灌胃(相当于儿童60 mg/kg临床用量等效量),每日2次,连续2 d。将分组的大鼠连续灌胃2 d后,将模型组和用药组分别进行46℃热水浴实验,时间为6 min,对于6 min未有惊厥发作视为不发生惊厥。在此过程中观察每组大鼠惊厥潜伏期(指大鼠放入热水中即刻至发生惊厥的时间,单位:秒)、惊厥持续时间(指大鼠由刚开始发生惊厥至惊厥停止的时间,单位:秒)和惊厥级别[4]。惊厥级别依发生的严重程度,具体分为:0级,没有发生惊厥;I级,点头,眨眼等面部抽动行为;II级,有节律性的点头;III级,前肢阵挛,抽搐;IV级,全身强直;V级,全身强直,跌倒。随后将所有大鼠断头处死,迅速取出大脑,称量后置组织冷冻管中用液氮快速冷冻,随后于-80℃低温冰箱中保存待用。
对于保存的大脑组织神经递质含量测定方法如下:准确地称组织质量,按质量(g):体积(mL)=1∶9的比例,加入9倍体积的生理盐水,冰水浴条件下匀浆,2 500转/min,离心10 min,取上清液,按检测试剂盒说明书检测Υ-氨基丁酸(GABA)及谷氨酸(Glu)含量[5]。
5 统计学分析
采用SPSS统计软件进行处理,计量资料用平均值±标准差(±s),两组间比较用t检验,P<0.05时,具有统计学意义。
6 结果
6.1 各组大鼠惊厥程度比较 在常温水中水浴,无惊厥现象的发生。该水浴温度无出现死亡,但无用药组发生惊厥非常明显,用药组与模型组比较:地西泮组P<0.01,回春散低剂量组P<0.01,回春散高剂量组P<0.01,结果见表1。
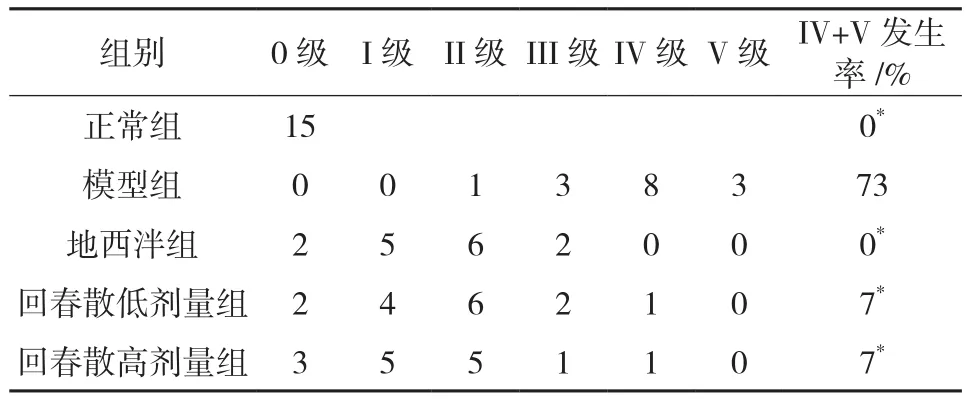
表1 各组大鼠惊厥程度比较(n=15)
6.2 各组大鼠惊厥潜伏期、惊厥持续时间比较 各用药组与模型组比较,惊厥潜伏期、惊厥持续时间均有显著差异:地西泮组P<0.01,回春散低剂量组P<0.01,回春散高剂量组P<0.01。各用药组有差异,但无显示差异,P>0.05,结果见表2。
表2 各组大鼠惊厥潜伏期、惊厥持续时间比较(±s ,n=15)

表2 各组大鼠惊厥潜伏期、惊厥持续时间比较(±s ,n=15)
注:与模型组比较,*P<0.01。
组别 潜伏期 持续时间模型组 240.3±31.2 138.7±22.6地西泮组 290.1±29.5* 99.7±13.2*回春散低剂量组 282.9±27.6* 105.2±16.7*回春散高剂量组 283.1±30.6* 101.3±13.5*
6.3 各组大鼠大脑皮质GABA和Glu检测 各用药组与模型组比较,大鼠大脑皮质组织的GABA和Glu均有显著差异:地西泮组P<0.01,回春散低剂量组P<0.01,回春散高剂量组P<0.01。各用药组有差异,但无显示差异,P>0.05,结果见表3。
表3 各组大鼠大脑皮质GABA和Glu检测结果( ±s,n=15)
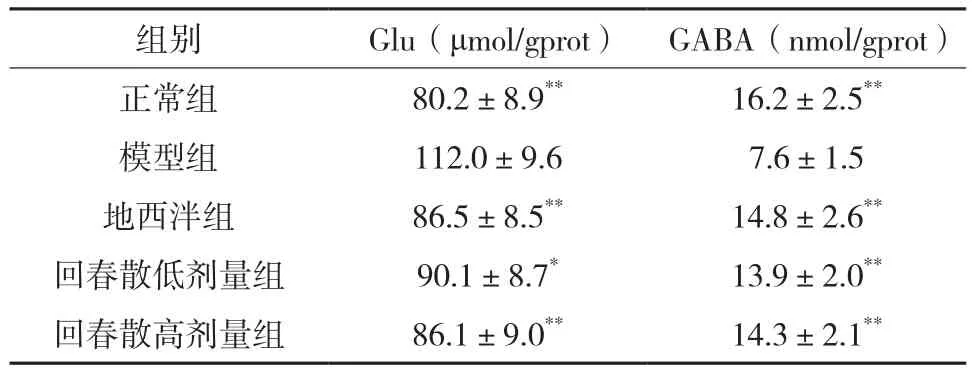
表3 各组大鼠大脑皮质GABA和Glu检测结果( ±s,n=15)
注:与模型组比较,*P<0.05,**P<0.01。
组别 Glu(μmol/gprot) GABA(nmol/gprot)正常组 80.2±8.9** 16.2±2.5**模型组 112.0±9.6 7.6±1.5地西泮组 86.5±8.5** 14.8±2.6**回春散低剂量组 90.1±8.7* 13.9±2.0**回春散高剂量组 86.1±9.0** 14.3±2.1**
7 讨论
有研究表明兴奋性氨基酸递质与抑制性氨基酸递质平衡失调在热性惊厥(FC)发病机制中起到关键性作用,在惊厥发生前期,大脑皮质组织内的抑制性氨基酸递质(GABA)水平降低, 兴奋性氨基酸递质(Glu)水平升高[6]。
回春散为上市多年的产品,在临床上广泛用于小儿惊风,感冒发热等症状,是作为小儿发热脑保护的首选用药。本实验通过热水浴诱发惊厥,观察到临床经典用药地西泮具有明显地降低惊厥的作用,回春散两个剂量组也有明显地降低惊厥的作用,在大鼠惊厥程度、惊厥潜伏期和惊厥持续时间都有明显改善。在用药组中,对于大脑皮质组织内的GABA明显提高,同时降低了Glu水平,该实验结果与已报道的一些实验整体结果一致。在结果中,回春散低剂量组与高剂量组在检验的数据中虽然有些差异,但无显著性的差异,这可能与整个处方有关或其中某个有效物质并没有量效关系,具体作用机制需进一步研究。
通过本实验的整体研究,回春散可以延长热性惊厥大鼠惊厥潜伏期,缩短惊厥持续时间,减轻惊厥严重程度,同时升高GABA水平,降低Glu水平,起到预防和治疗小儿惊风,热性惊厥的作用。

