造血干细胞移植治疗DOCK8基因突变致高IgE综合征2例病例报告
钱晓文 王 苹 王宏胜 江文晋 孙金峤 王晓川 吴冰冰 翟晓文
高IgE综合征(HIES)是一种罕见的原发性免疫缺陷病,临床表现为湿疹样皮肤损害、反复呼吸道感染以及血IgE水平升高[1-3],根据遗传方式可分为常染色体显性遗传和常染色体隐性遗传。由胞质分裂蛋白8(DOCK8)基因突变所致的HIES为常染色体隐性遗传病,远期预后差,常因严重感染或并发恶性肿瘤而死亡。目前,异基因造血干细胞移植是治愈DOCK8基因突变所致HIES的唯一方法[4-5]。复旦大学附属儿科医院(我院)采用异基因造血干细胞移植成功治疗DOCK8基因突变所致HIES患儿2例,现报告如下。
1 病例资料
例1,男,7岁,因“反复皮疹伴反复感染7年,确诊DOCK8基因突变为移植”入我院。患儿生后半月起反复湿疹,伴瘙痒、渗液,3月龄行过敏原检测提示“鸡蛋、牛奶”过敏。6月龄起反复肺炎,多次因肺炎于外院住院治疗。3岁皮疹进行性增多伴腋下、腘窝、腹股沟脓疱疹。6岁发生水痘并脑炎、脊髓炎、EB病毒感染、脓毒症、扁平疣。7岁因肺炎在我院行纤维支气管镜检查,肺泡灌洗液半乳甘露聚糖(GM)试验阳性,宏基因检测卡氏肺囊虫阳性。病程中多次应用抗过敏药、抗生素、糖皮质激素和丙种球蛋白。生后接种乙肝疫苗及卡介苗各1次。后因反复感染未接种其他疫苗。父母体健;姐姐10岁,体健。否认类似疾病家族史。体格检查:体温37.1 ℃,脉搏88·min-1,呼吸20·min-1,体重23 kg,身高122 cm。神志清楚,反应良好;全身皮肤散在红色斑丘疹,部分干燥结痂,耳后、腋下、会阴部较为明显(图1A);颈部可及黄豆大小淋巴结,质韧,活动度好,无触痛;双肺听诊呼吸音粗,未及明显干湿啰音;心率88·min-1,律齐,心前区未及杂音;腹平软,无压痛,肝脾未及明显肿大,肠鸣音5·min-1;四肢肌力、肌张力正常,病理征未引出。移植前实验室检查结果见表1,在我院免疫科住院期间,取得患儿父母知情同意后,留取患儿及父母静脉血于我院分子诊断中心行全外显子测序,结果显示患儿DOCK8基因(NM_203447)exon 2 c.54-5C>G纯合变异,患儿父亲该位点杂合变异,患儿母亲正常,该突变在人类基因突变数据库中未见报道,致病性不明确。经患儿父母同意后,留取患儿姐姐静脉血送检至北京迈基诺医学检验所行该基因位点Sanger测序验证,未发现该位点变异。考虑患儿为DOCK8基因突变所致HIES。
例2,女,9岁,因“反复皮疹伴反复感染8年余,确诊DOCK8基因突变为移植”入院。患儿生后6月起反复皮疹,进行性增多,部分融合成片,伴瘙痒、糜烂、渗液。3岁起反复上呼吸道感染及中耳炎。6岁起反复肺炎。病程中多次应用抗过敏药、抗生素、糖皮质激素和丙种球蛋白。生后按序接种乙肝、卡介苗、百白破疫苗。孤儿,无法获得生物学父母健康状况。体格检查:体温36.6 ℃,脉搏102·min-1,呼吸20·min-1,体重29 kg,身高137 cm。神志清楚,反应良好;全身皮肤散在红色丘疹及色素沉着,融合成片,部分破溃渗液,部分干燥结痂,腹部及会阴部皮肤较为明显(图1C);颈部、颌下及耳后可及淋巴结,右侧颈部最显著,约蚕豆大小,质韧,活动度可,无触痛;双肺听诊呼吸音粗,可及湿性啰音;心率102·min-1,律齐,心前区未及杂音;腹平软,无压痛,肝脾未及明显肿大,肠鸣音3~5·min-1;四肢肌力、肌张力正常,病理征未引出。移植前实验室检查结果见表1。血EB病毒-DNA阳性。外阴皮疹渗液培养:白色念珠菌,高通量测序:屎肠球菌、白色念珠菌、EB病毒、HPV5型、HPV49型、细环病毒16型、小细环病毒18型。过敏原检测:霉菌、户尘螨、鸡蛋白阳性。在我院免疫科住院期间,取得患儿监护人知情同意后,留取患儿静脉血送检至北京迈基诺医学检验所行二代测序(免疫缺陷病相关基因包),DOCK8基因(NM_203447)exon 38 c.4886G>A(p. R1629K)纯合错义突变,不属于多态性位点,人群发生频率极低,人类基因突变数据库中未见报道,临床意义未明。
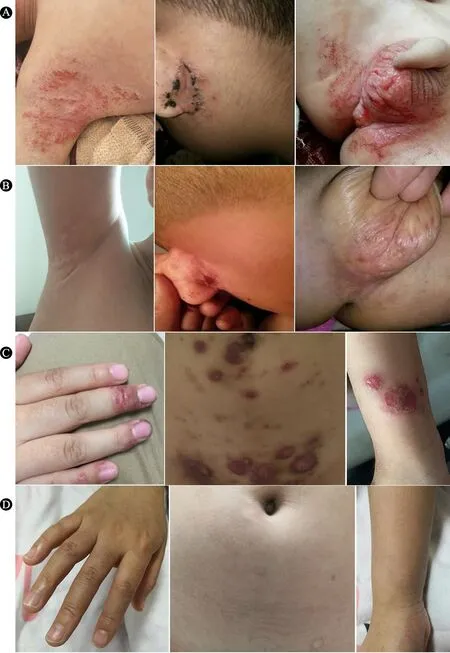
图1 患儿造血干细胞移植后皮肤损害明显改善
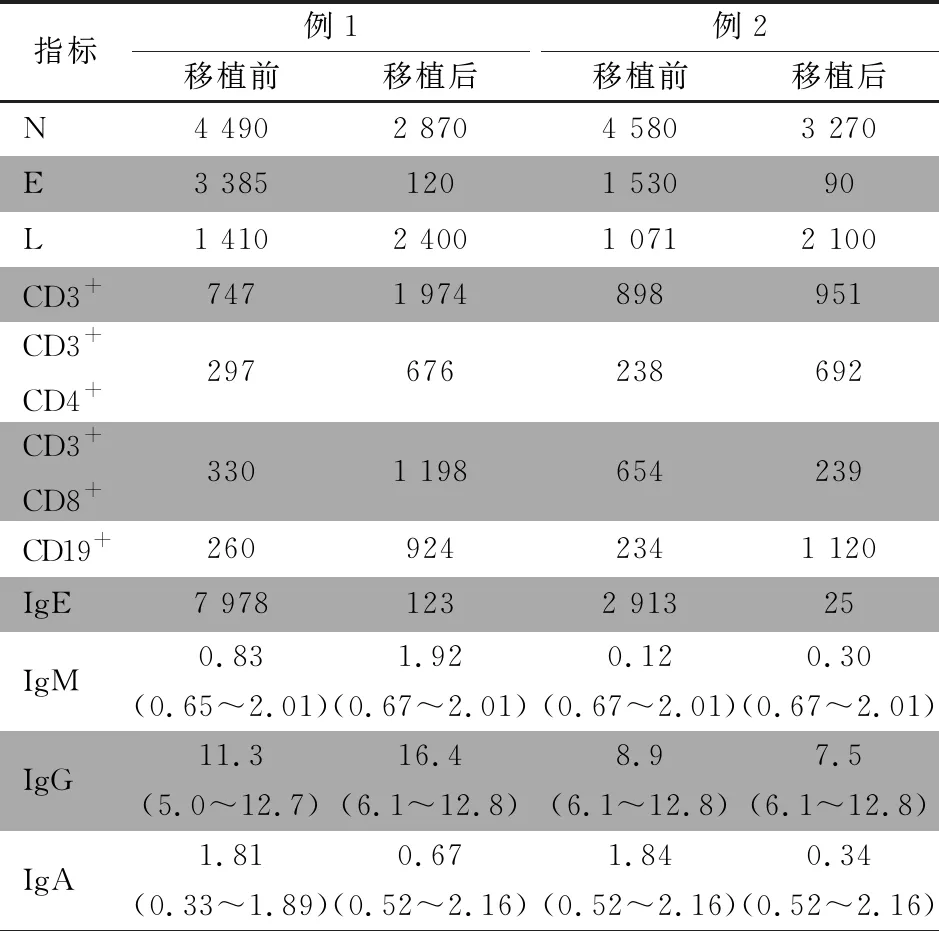
表1 2例患儿造血干细胞移植前后的实验室指标
2例患儿均考虑为DOCK8基因突变所致HIES,有行异基因造血干细胞移植适应证。入院后完善检查,评估感染状态及脏器功能,无移植禁忌。例1与姐姐人类白细胞抗原(HLA)配型为10/10相合,总有核细胞数(TNC)8.18×108·kg-1,CD34+为4.96×106·kg-1;例2配得非亲缘HLA10/10全相合脐血干细胞,脐血TNC为5.68×107·kg-1,CD34+为1.25×105·kg-1。
预处理方案:利妥昔单抗200 mg·m-2+氟达拉滨150~170 mg·m-2+白消安11.4 ~12.0 mg·kg-1,例1+兔抗人胸腺细胞免疫球蛋白5 mg·kg-2,例2+环磷酰胺100 mg·kg-2。均采用他克莫司和霉酸酚酯(MMF)预防排异。
例1移植后10 d出现发热,伴肺部感染加重,予积极抗感染治疗;12 d时中性粒细胞植入(中性粒细胞绝对计数连续3 d >500×109·L-1),伴皮疹增多,考虑皮肤Ⅰ度急性移植物抗宿主反应,予静滴甲泼尼龙后皮疹好转;13 d血小板植入(未输注血小板情况下血小板计数连续7 d >20×109·L-1);14 d嵌合提示为完全供者嵌合;随访嵌合状态稳定;移植后1个月患儿情况稳定出院;移植后100 d患儿脱离IVIG替代支持治疗;表1显示,造血重建后嗜酸性粒细胞明显低于移植前,IgE水平降至正常。截至2020年6月,患儿无病生存18个月,移植前湿疹样皮疹和脓疱疹明显好转(图1B)。
例2移植后5 d出现发热伴皮疹增多,考虑为植入综合征。12 d患儿出现咳嗽并逐渐加重,痰病原学检查提示副流感病毒3型,予抗感染及静脉注射丙种球蛋白(IVIG)支持治疗;24 d中性粒细胞植入;35 d血小板植入;+14 d嵌合提示为完全供者嵌合,后随访嵌合状态稳定;42 d情况稳定,出院。移植后60 d脱离丙种球蛋白替代支持治疗。表1显示,造血重建后嗜酸性粒细胞明显低于移植前,随访IgE水平降至正常水平。随访至2020年6月,患儿无病生存23个月,移植后皮损明显好转(图1D)。
2 讨论
DOCK8基因突变由Engelharts等[6]于2009年首次报道,该基因中大片段缺失频率较高,无大片段缺失的患者中存在明显纯合突变,导致过早终止、移码、剪接位点断裂、单外显子和微缺失,该基因的突变与CD4+和CD8+T细胞活化受损、嗜酸性粒细胞稳态受损和IgE调节失调有关。临床表现包括婴幼儿期起病的顽固湿疹样皮疹,反复发生病毒、细菌或真菌感染[3,7],常伴有过敏性疾病如食物或环境致敏源过敏以及哮喘[8]。此外,近20%的DOCK8基因突变患者发生恶性肿瘤[9]。患者无法获得长期高质量生存,预后较差[2]。本文2例患儿均以顽固性湿疹样皮疹起病,反复发生病毒、细菌感染,伴真菌感染,均存在食物过敏,外周血嗜酸性粒细胞及血清IgE水平明显增高。例1 NM_203447 exon 2 c.54-5C>G Hom exon 15 c.1797G>A(p. P1599P Het),为剪接位点纯合变异,患儿父亲该位点杂合变异,未检测到患儿母亲该位点变异,推测可能为新发突变或存在该基因片段杂合缺失。例2 NM_203447 exon 38 c.4886G>A(p. R1629K),为纯合错义突变,不属于多态性位点,在人群中发生频率极低,致病性分析为未确定。结合2例患儿典型的临床表现,常规抗感染及抗过敏治疗效果欠佳,均诊断DOCK8基因突变所致的HIES。
异基因造血干细胞移植是目前治愈DOCK8基因突变所致HIES的唯一方法。本文例2为孤儿,配得10/10相合非亲缘脐血干细胞,成功移植,为国内首例通过非亲缘脐血干细胞移植治愈DOCK8基因突变所致HIES。关于非亲缘脐血干细胞移植成功治疗原发性免疫缺陷病已有较多报道[10-12],但治疗DOCK8基因突变所致HIES则少见,Uygun等[13]报道1例,未成功植入;Aydin等[14]报道的2例中,1例植入失败,二次移植时死亡。该疾病多为相合同胞[15,16]或相合无关供者[17]或半相合供者[5]骨髓或外周血干细胞移植。Al-Herz等[4]报道了11例DOCK8基因突变所致HIES患儿接受造血干细胞移植治疗,其中7例为相合同胞供者骨髓干细胞移植,4例为(8~10)/10无关供者骨髓或外周血干细胞移植,91%(10/11)的患儿存活且一般情况良好(随访0.6~4.6年)。Shah等[5]报道了7例DOCK8基因突变的儿童和青年患者接受半相合骨髓干细胞移植,所有患者均成功植入,85%(6/7)的患者获得无病生存(随访9.5~31.7个月)。Cuellar-Rodriguez等[18]报道了6例造血干细胞移植治疗DOCK8基因突变所致HIES,为10/10相合亲缘或无关供者骨髓或外周血干细胞移植,所有患儿均获得完全供者嵌合且临床及免疫表型得以纠正,至随访截止,所有患儿存活(14~35个月)。Aydin等[14]多中心回顾性分析中,81例接受造血干细胞移植的患者,中位随访时间26(3~135)个月,总体生存率为84%。
感染是异基因造血干细胞移植过程中的重要并发症,重症感染可导致死亡,DOCK8基因突变所致HIES患者移植前多合并细菌、病毒或真菌感染,故宜采用减低强度的预处理方案。多中心回顾性分析结果显示,预处理强度不影响植入与嵌合,且接受减低强度预处理方案化疗的患者预后更好[14]。在预处理化疗后至血象恢复前,患者既存感染可进一步加重或者出现新发感染。Al-Herz等[4]报道的11例DOCK8基因突变接受移植的患儿中,1例因并发克雷伯菌败血症在移植后58 d死亡。本文2例患儿在移植后10 d左右均出现肺部感染加重表现,与文献报道[18]类似,积极抗感染、雾化对症支持治疗,伴随血象恢复,2例肺部症状逐渐好转。移植时存在感染的HIES患者,采用减低强度预处理方案患者耐受性良好,有利于控制感染、提高移植后生存率。
移植物抗宿主病(GVHD)为异基因造血干细胞移植治疗主要并发症。Al-Herz等[4]报道, 72.7%(8/11)的患儿为完全供者嵌合,无GVHD发生。Cuellar-Rodriguez等[18]报道, 33%(2/6)的患儿发生了Ⅰ~Ⅲ度皮肤急性GVHD(aGVHD)。Shah等[5]的研究结果显示, 57%(4/7)的患儿发生了Ⅰ~Ⅲ度急性皮肤和/或肠道GVHD。Aydin等[14]的多中心数据显示,Ⅲ~Ⅳ度aGVHD发生率为11%,重度慢性GVHD发生率为3%。本文例1接受相合同胞外周血干细胞移植发生了皮肤Ⅰ度aGVHD,例2接受脐血干细胞移植无GVHD发生。脐血干细胞具有检索配型快、免疫原性低等特点,移植后GVHD发生率及严重程度相对较低,故在缺乏相合供者时,可考虑作为移植物来源。
异基因造血干细胞移植治疗DOCK8基因突变所致HIES患儿疗效显著。移植后随着造血恢复及免疫重建,DOCK8基因突变所致HIES患儿的皮肤损害逐渐好转,感染发生频次减少、程度减轻,多数患儿食物过敏现象消失、外周血嗜酸性粒细胞及血清IgE水平较移植前明显下降,可恢复至正常范围[4,12,17]。但是,部分患儿移植成功后仍存在食物过敏,且血清IgE仍高于正常水平,其发生机制目前尚不明确,可能与感染所致的免疫激活与失调相关[4,11,18]。即使移植后发生混合供者嵌合,仍能使DOCK8基因突变所致HIES患儿获得完全的免疫矫正,临床表现为皮肤症状改善、严重感染消失、肺功能改善和IgE水平持续下降[4,19]。本文2例患儿移植后随着造血恢复及免疫重建,皮肤损害明显改善,移植后随访无严重感染发生,外周血嗜酸性粒细胞及血清IgE水平均恢复至正常范围。
总之,DOCK8基因突变所致HIES,因早期反复发生严重感染危及生命,引起脏器损害,并有恶性肿瘤发生倾向,一旦确诊应尽早进入移植程序。同胞相合供者为异基因造血干细胞移植治疗时的首选供者,在缺乏相合供者时,非亲缘脐血干细胞移植也能取得良好疗效。

