基于网络药理学探讨“黄芪-当归-大枣”角药补气养血的分子机制*
周文静,张 萌,周荣荣,赵 乐,李志勇,2,王永辉,李艳彦**
(1. 山西中医药大学基础医学院 晋中 030619;2. 中央民族大学药学院 北京 100081)
角药是基于辨证论治原则与中药药性理论,由三味具有相互促进或相反相成作用的中药联合配伍而成[1]。角药作为中药方剂具体配伍形式,在扩大药物使用范围、协同增效、减毒增效等方面发挥着重要的作用[2]。
黄芪,甘、微温,归脾、肺经,具有补气升阳、益卫固表、托毒敛疮、利水消肿等功效,素有“补气圣药”之称[3]。当归,味甘、辛,性温,归肝、脾经,具有补血活血、调经止痛、润肠通便的功效,为“补血要药”[4]。黄芪与当归配伍构成经典名方当归补血汤,李东垣在《内外伤辨惑论》卷中提出凡属血虚气弱者,均可以当归补血汤加减应用[5]。为增强其补气养血效果,加入平补气血之大枣。大枣,始载于《神农本草经》,列为上品,具有补中益气,养血安神之功,是少有的具有补气养血两者功效的单味中药[6]。黄芪、当归配伍大枣,大枣既可增强黄芪补气之功,又能增加当归养血之效,构成补气养血的角药。同时,黄芪是2018 年国家卫健委新增的药食同源药,当归除药用外,可用于药膳当中或作为天然调味香料使用,大枣是常用的药食同源药材,历史悠久。因此,“黄芪-当归-大枣”角药一方面可作为治疗气血两虚证的常用药物组合,另一方面可作为开发相关功能食品的原料,应用范围广泛。
虽然“黄芪-当归-大枣”角药补气养血的作用明确,但是从分子层面上系统的分析其药效物质基础和作用机制,尚未见相关论述和报道。近年来,兴起的网络药理学方法,其整体性、系统性的研究特点与中药多成分、多靶点和多途径的作用特点相吻合[7],适合探究复方中药的药效物质基础及作用机制,被广泛应用。本研究采用网络药理学方法,从分子层面预测“黄芪-当归-大枣”角药补气养血的物质基础与分子机制,并通过动物实验验证预测的可靠性,以期为进一步临床应用提供理论指导,为药食同源药物研究提供方法思路。
1 材料与方法
1.1 化学成分收集
采用中药系统药理学分析(TCMSP)数据库(http://ibts.hkbu.edu.hk/LSP/tcmsp.php),以口服生物利用度(Oral bioavailability,OB) ≥ 30%、类 药 性(Druglikeness,DL)≥0.18为前提筛选黄芪、当归和大枣的化学成分。
1.2 作用靶点预测
进一步在TCMSP 数据库进行作用靶点预测,使用UniProt 数据库(https://www.uniprot.org/)对靶点蛋白进行名称标准化,统一转换成人源(Homo sapiens)基因靶点名称,剔除重复项。
1.3 蛋白互作PPI网络构建与关键靶点筛选
将以上收集的“中药-成分-靶点”数据库,输入Cytoscape 3.2.1 软件,利用Network Analyzer 插件进行网络拓扑分析,按度值degree 值取其中位数。将筛选的靶点导入STRING 数据库(https://string-db.org),获得靶点蛋白互作PPI 网络,保存为TSV 格式,导入Cytoscape 3.2.1软件,根据degree 值的大小筛选出核心靶点,进行可视化展示,进一步获得关键靶点。
1.4 GO功能及KEGG通路富集分析
使用DAVID 数据库(https://david.ncifcrf.gov/)将筛选的核心靶点进行基因本体论(gene ontology,GO)分析和京都基因与基因组百科全书(KEGG)通路富集分析。设置参数P<0.05,考察“黄芪-当归-大枣”角药作用靶点的生物过程、分子功能和细胞组分及生物学通路,并根据富集程度和P值,将排名前20 位利用Graph Pad Prism 5 绘图。使用Cytoscape 3.2.1 软件构建“中药-成分-靶点-通路”完整网络。通过KEGG(https://www.kegg.jp/)数据库KEGG mapping 获取相关通路图。
1.5 实验验证
1.5.1 造模与给药
选取SPF 级KM 小鼠30 只(购于北京维通利华实验动物技术有限公司,批号:SCXK(京)2016-0011),7周龄左右,体重18±4 g,雌雄各半,分为正常组、模型组和治疗组。除正常组外其余各组在第1 d 与4 d 按照0.2 mg·kg-1皮下注射2%乙酰苯肼(上海易恩化学技术有限公司,批号:R017768),按照0.3 mg·kg-1每天一次腹腔注射1%环磷酰胺(上海易恩化学技术有限公司,批号:R014054),正常组在同时间点仅腹腔注射等体积生理盐水。同时,除正常组每天给予饲料外,其余各组在第1 d 饱食后禁食两天,第4 d 再给饲料,以构建气血两虚小鼠模型[8-10]。第五天开始治疗组灌以“黄芪-当归-大枣”角药,按照当归补血汤黄芪与当归比例为5∶1,并结合前期预实验结果,选取黄芪10 g,当归2 g,大枣8 g 水煎剂,浓度为2.5 g·mL-1,按照0.02 ml·g-1一日一次灌胃,连续六天,正常组与模型组灌以相应剂量的蒸馏水。观察小鼠的一般状态,小鼠末次给药后,禁食,取全血抗凝备用。
1.5.2 小鼠体重、胸腺指数、脾脏指数测定
末次给药后,称取小鼠体重并做好记录,颈椎脱臼处死小鼠后,取整个胸腺和脾脏,用生理盐水冲洗,滤纸沥干,电子天平称重,计算胸腺和脾脏指数。计算公式:胸腺(脾脏)指数=胸腺(脾脏)重量(mg)/小鼠体重(g)。
1.5.3 外周血象检测
采用血液分析仪检测各组小鼠外周血红细胞(Red blood cell,RBC)、血红蛋白(Haemoglobin,HGB)的数量。
1.5.4 Real-time PCR检测PTGS2mRNA表达
前列腺素合成酶2(PTGS2)mRNA 检测,按照Trizol 试剂(北京聚合美生物科技有限公司,批号MF11501)提取总RNA,反转录为cDNA。Real-time PCR 采用Light Cycler®480 II 系统,步骤为:变性95 ℃,15 s;退火56 ℃,30 s;延伸72 ℃,20 s;共扩增44个循环。引物序列为:PTGS2 上游5'-TGAGCAAC⁃TATTCCAAACCAGC-3',下游5'-GCACGTAGTCTTC⁃GATCACTATC-3',扩增片段长度为74 bp;GAPDH 上游5'-AGGTCGGTGTGAACGGATTTG-3',下 游5'-GGGGTCGTTGATGGCAACA-3',扩增片段长度为123 bp。结果处理用ΔΔCT 法:A = CT(目的基因,待测样本)-CT(内标基因,待测样本);B = CT(目的基因,对照样本)-CT(内标基因,对照样本),K=A-B,表达倍数=2-K来计算mRNA的相对表达量。分析得出各个样 品量 的 循环 阈值(Ct),用2-ΔΔCt公式 计算PTGS2mRNA的相对表达量。
1.5.5 ELISA法检测TNF-α的含量
取各组的肝素抗凝血浆严格按照ELISA 试剂盒(北京聚合美生物科技有限公司,批号MF821)操作步骤,测定血浆中肿瘤坏死因子-α(TNF-α)的含量。
1.6 统计学处理
利用统计软件SPSS 21.0统计处理,实验数据以均数±标准差(xˉ±s)表示,组间均数比较采用单因素方差分析,以P<0.05表示差异有统计学意义。
2 结果
2.1 化学成分收集
在TCMSP 数据库中,筛选得到黄芪87 个、当归69个和大枣133 个化学成分,进一步按照OB,DL 参数筛选得黄芪20个,主要为黄芪多糖类、皂苷类、黄酮类及醇类等;当归5 个,主要为挥发油类、多糖类、甾体类等;大枣25个,主要为皂苷类、生物碱类、甾体类、黄酮类等化合物,获得“黄芪-当归-大枣”角药化学成分47个,其中共有成分3个,见表1。
2.2 作用靶点预测
为了揭示“黄芪-当归-大枣”防治气血两虚证的分子机制,预测作用靶点黄芪206 个、当归53 个、大枣204 个,中药两两之间均具有不同数量的共同靶点,说明其之间存在某些相互协同的作用关系(见图1),进一步分析三药共有靶点有43 个,分别为TGFB1、
SLC6A4、SLC6A3、SLC6A2、SCN5A、RXRA、PTGS2、PTGS1、PLAU、PIK3CG、PDE3A、PGR、OPRM1、NCOA2、FOS、KCNH2、JUN、AKT1、HTR2A、GABRA5、GABRA3、GABRA2、GABRA1、EGFR、EGF、CXCL8、ESR1、DRD1、CHRM4、CHRM2、CHRM1、CASP9、CASP8、CASP3、BCL2、BAX、AKR1B1、ADRB2、ADRB1、ADRA1B、ADH1C、IL6 和ERBB2。黄芪、当归、大枣虽然单味药作用广泛,但配伍组合后为补气养血重要组合,由此推测“黄芪-当归-大枣”角药可能通过这些共有靶点发挥补气养血的协同作用。
2.3 蛋白互作PPI网络构建与关键靶点筛选

图1 黄芪、当归、大枣共有靶点韦恩图
根据网络拓扑degree 值由大到小排列,按中位数取221 个“黄芪-当归-大枣”角药作用靶点,输入STRING 数据库构建靶点蛋白互作PPI 网络,选degree值前100位的靶点为核心靶点,并进行可视化展示(见图2),图中越接近红色表明网络中节点越大,即degree值 越 大。 排 名 前10 位 的 包 括:AKT1(RACalphaserine/threonine-proteinkinase,RAC-α丝氨酸/苏氨酸蛋白激酶)、IL6(Interleukin-6,白细胞介素-6)、FOS(Proto-oncogenec-Fos,原 癌 基 因c-Fos)、ESR1(Estrogen receptor1,雌 激 素 受 体 1)、PTGS2(Prostaglandin G/H synthase 2,前列腺素G/H 合成酶2)、EGFR(Epidermal growth factor receptor,表皮生长因子受体)、EGF(Pro-epidermal growth factor,表皮生长因子)、CASP3(Caspase-3,半胱天冬蛋白酶3)、JUN(Jun proto-oncogene/AP-1 transcription factor subunit,
Jun 原癌基因/AP-1 转录因子亚单位)、ERBB2(Erythroblastic leukemia viral oncogene homolog2,红细胞白血病病毒癌基因同源物2)。可以发现这10 个靶点均为三药共有靶点,可能是角药发挥补气养血作用的关键靶点,且网络中节点与节点相互相连,说明靶点之间的关系密切,存在相互协同的作用。
2.4 GO功能及KEGG通路富集分析
对筛选的核心靶点进行GO 功能和KEGG 通路富集分析,发现“黄芪-当归-大枣”角药主要定位在内质网膜、线粒体、胞液;参与免疫应答,神经元凋亡过程负调控、血管收缩正向调节、炎症反应等生物过程;并结合转录因子、血红素、细胞因子、生长因子、过氧化物酶、α-肾上腺素能受体等分子功能发挥补气养血作用,主要涉及癌症(胰腺癌、结直肠癌、前列腺癌、非小细胞肺癌)信号通路,TNF、P53、Foxo、HIF-1 信号通路,钙信号通路以及感染性疾病信号通路等,见图3。

表1 “黄芪-当归-大枣”角药部分化学成分的基本信息

图2 关键靶点网络
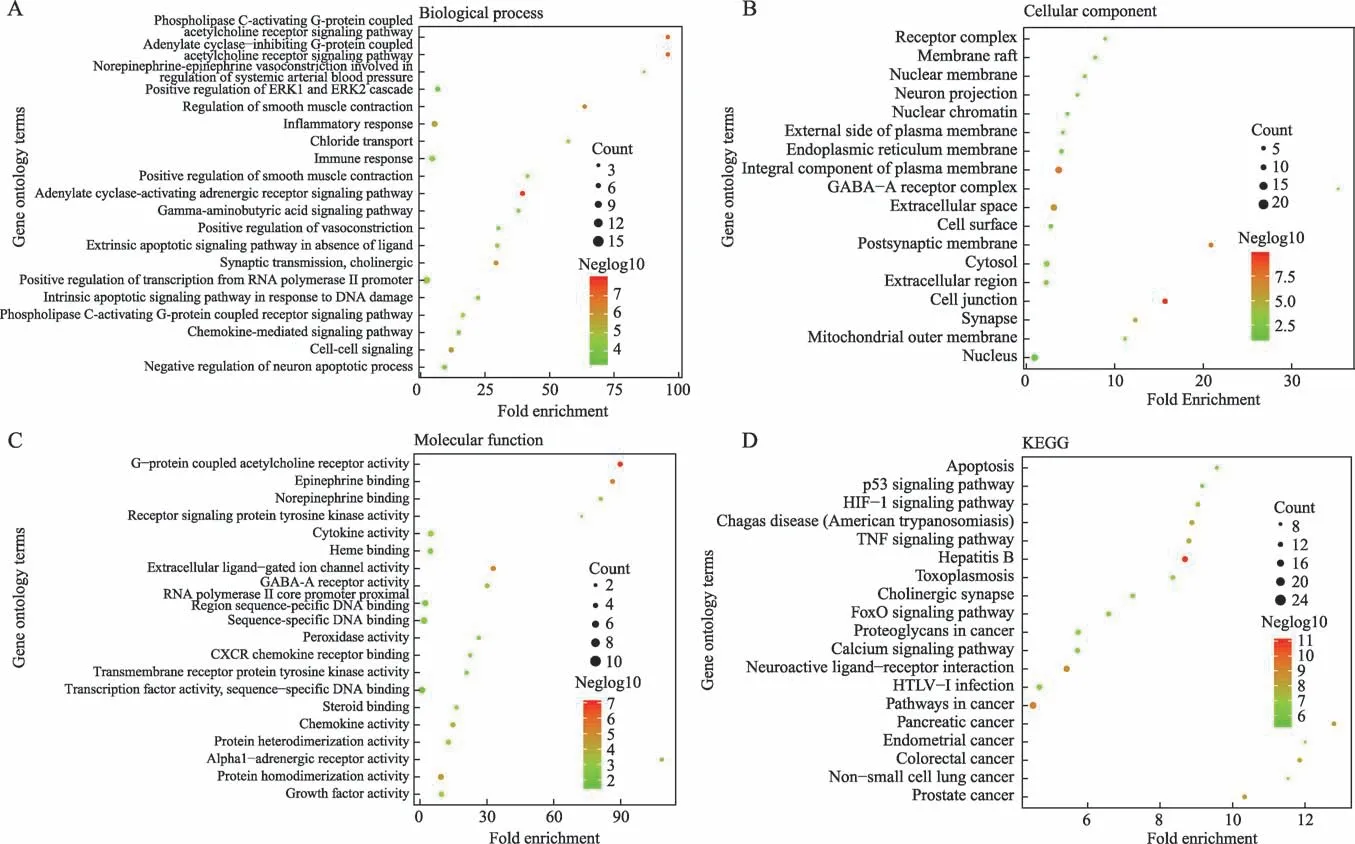
图3 GO功能和KEGG通路富集分析
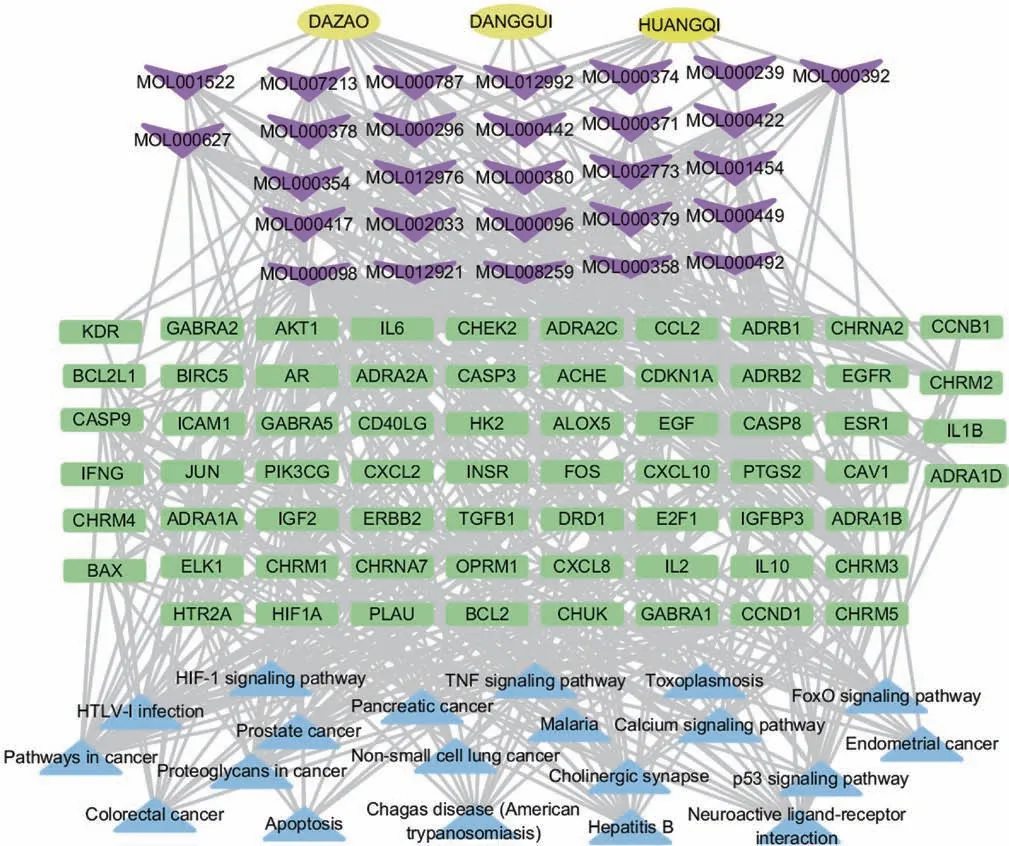
图4 “中药-成分-靶点-通路”网络
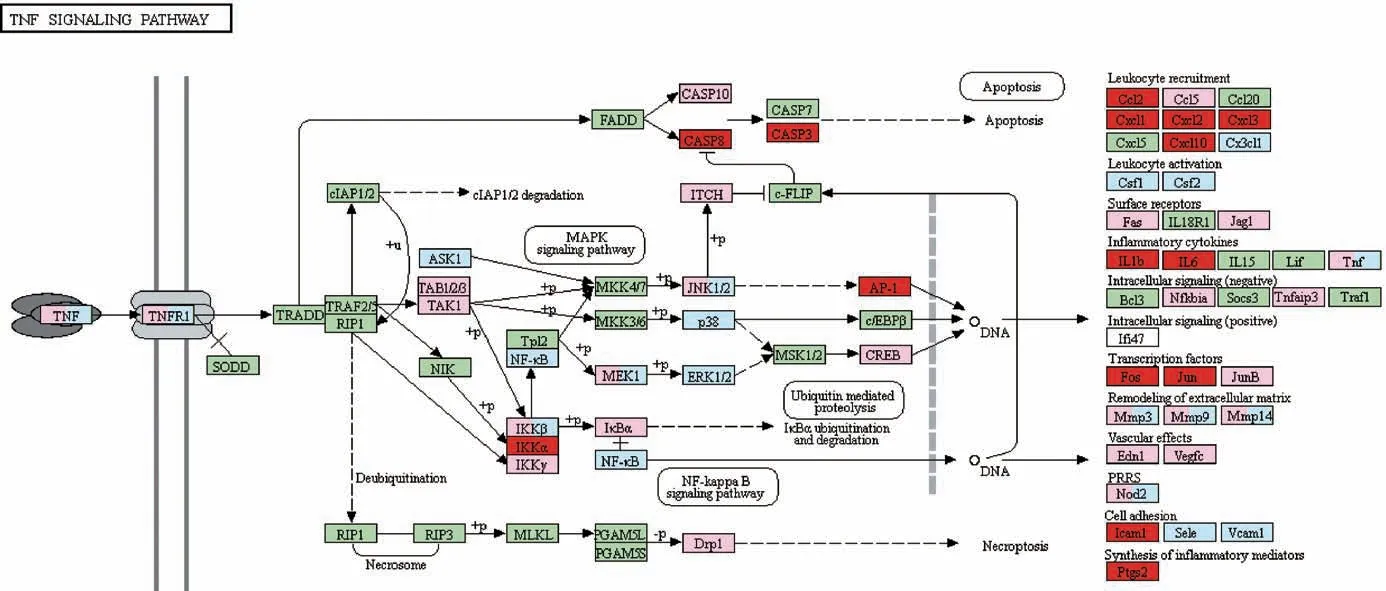
图5 TNF信号通路
为了更好的解释化学成分与相应靶点以及对应信号通路之间复杂的作用关系,将KEGG 通路富集分析前20 位结果绘制“中药-成分-靶点-通路”网络(见图4),可以发现“黄芪-当归-大枣”角药多种药物化学成分对应多种作用靶点,多种靶点又映射于不同通路,体现其多成分、多靶点、多通路和整合调节的复杂网络特点。进一步以TNF 信号通路为例,从KEGG mapping 获取TNF 信号通路图(见图5),红色部分为“黄芪-当归-大枣”角药的作用靶点,得到有15个靶点通过调节其中多个环节发挥作用。
2.5 实验验证
实验期间,正常组小鼠毛色柔顺光亮,活动灵活,爪子、耳朵呈正常淡红色,摄食、饮水量正常。模型组小鼠毛发易脱落,缺少光泽,活动减少、扎堆、倦卧,爪子、耳色颜色偏淡,饮水、摄食量减少。治疗组小鼠精神好转,毛发恢复柔顺,耳色,爪子颜色恢复淡红色,摄食、饮水量逐渐趋于正常。同时,与正常组比较,模型组小鼠的体重、胸腺指数和脾脏指数明显下降,差异具有统计学意义(P<0.01)。与模型组比较,治疗组小鼠的体重、胸腺指数、脾脏指数均显著增加,差异具有统计学意义(P<0.01)。与空白组比较,模型组RBC、HGB 数量显著降低(P<0.01);与模型组比较,治疗组RBC、HGB 数量明显升高(P<0.01)(见表2)。这表明气血两虚证模型小鼠造模成功,且“黄芪-当归-大枣”角药对气血两虚小鼠有一定治疗作用。
表2 各组小鼠胸腺指数、脾脏指数、RBC、HGB检测结果(± s,n = 10)

表2 各组小鼠胸腺指数、脾脏指数、RBC、HGB检测结果(± s,n = 10)
注:与正常组比较*P <0.01;与模型组比较▲P <0.01
HGB/(g·L-1)161.08±6.99 96.22±5.67*137.56±5.86▲组别正常组模型组治疗组体重/g 32.17±2.30 22.31±2.47*29.00±2.01▲胸腺指数/(mg·g-1)2.32±0.23 0.85±0.15*1.92±0.30▲脾脏指数/(mg·g-1)3.84±0.84 2.30±0.05*3.28±0.92▲RBC/(1012·L-1)9.26±0.42 4.20±0.27*8.21±0.16▲
表3 各组PTGS2、TNF-α检测结果(± s,n = 10)

表3 各组PTGS2、TNF-α检测结果(± s,n = 10)
注:与正常组比较*P <0.01;与模型组比较▲P <0.01
TNF-α/(ng·L-1)37.68±4.02 64.58±5.05*40.52±4.89▲组别正常组模型组治疗组PTGS2/(2-ΔΔCT)1.21±0.45 6.03±0.67*2.56±0.76▲
进一步从TNF 信号通路进行实验验证,PTGS2 是“黄芪-当归-大枣”角药的作用于此通路预测的一个关键靶点,且未见气血两虚证中PTGS2 在TNF 通路中表达情况的相关报道,本研究选取PTGS2 进行进一步实验。实验结果显示,与空白组比较,模型组PTGS2mRNA 表达水平与TNF-α含量显著升高(P<0.01);与模型组比较,治疗组PTGS2mRNA 表达水平,TNF-α含量明显降低(P<0.01)(见表3)。表明“黄芪-当归-大枣”角药可能通过调控PTGS2mRNA 表达,降低TNF-α释放,进而抑制TNF 信号通路的激活,发挥对气血两虚小鼠的治疗作用,进一步证实了网络药理学预测的可靠性。
3 讨论
气血两虚证属于中医证候,是指由于素体脾胃虚弱,或饮食不节,或久病大病失养,亦或因产时产后,导致气血两虚,表现为面色萎黄或淡白,头晕目眩,少气懒言,神乏力,或有自汗,心悸失眠,舌质淡嫩,脉细弱等[11]。气血两虚证可见于癌症、手术后、贫血、产后腹痛等多种疾病。“黄芪-当归-大枣”角药作为补气养血的重要组合,既可药用,对于轻度气血两虚者又可食疗,作用广泛。
网络药理学分析得到“黄芪-当归-大枣”角药化合物47 个,共有成分为槲皮素(Quercetin)、丁子香萜(Mairin)和豆甾醇(Stigmasterol),预测得到共有靶点43 个。三药之间存在共同成分、共同靶标,说明合用可起到协同增效的作用,充分体现多成分,多靶点的协同作用特点。
进一步分析,得到“黄芪-当归-大枣”角药补气养血 关 键 靶 点10 个,包 括AKT1、IL6、FOS、ESR1、PTGS2、EGFR、EGF、CASP3、JUN 和ERBB2。AKT1 是一种丝氨酸/苏氨酸蛋白激酶,与肿瘤、心血管、神经系统等疾病发生相关[12]。FOS 与JUN 家族的蛋白以同源或异源二聚体的形式结合形成AP-1,进而调控细胞生长、分裂、增殖等活动,原癌基因蛋白c-fos 和c-Jun在多种恶性肿瘤中呈高表达[13]。ESR1(雌激素受体1)是雌激素及选择性雌激素受体调节生物学效应的主要介导者,参与乳腺癌、子宫内膜癌和骨质疏松症等疾病的病理过程[14]。EGF 是一种多肽类生长因子[15],EGFR 为原癌基因C-erbB 表达产物,与EGF 特异性结合后,可以促进细胞分裂和增殖,形成机体上皮组织增生[16],在许多实体肿瘤中存在EGFR 与EGF 的高表达或异常表达。已有研究报道,气血两虚型胃癌癌前病变存在EGFR 高表达[17],气血两虚型胃癌血清中EGF 明显升高[18]。而ERBB2 为EGF 受体家族成员之一[19],研究发现,C-erBb-2 蛋白的阳性率在胃癌不同中医证型之间存在差异,其中气血两虚型阳性率达63.2%[20]。CASP3 是细胞凋亡的主要执行者。PTGS2为前列腺素内源性过氧化物合酶,参与炎症和有丝分裂形成的前列腺样生物合成[21]。多功能细胞因子IL-6,在免疫炎症反应中发挥重要作用[22]。可以发现,这些靶点主要为一些转录因子、细胞因子、生长因子和过氧化物酶等,在免疫炎症反应、细胞凋亡等方面发挥作用,疾病方面主要富集于癌症。气血两虚证是癌症常见的证型,中医认为“正气存内,邪不可干”,恶性肿瘤的发病有多种因素,总体来说是因虚发病,其中以气虚质发病最高[23],而气虚常伴随血虚,形成气血两虚证。“邪之所凑,其气必虚”,肿瘤放疗或化疗等术后亦会出现气血两虚证[24]。推测“黄芪-当归-大枣”角药一定程度可作为防治癌症的药物组合或食疗方。
KEGG 通路富集分析结果显示,“黄芪-当归-大枣”角药主要介导癌症信号通路,TNF、P53、Foxo、HIF-1 信号通路,钙信号通路等发挥补气养血的作用。选取KEGG 通路排名前20 位构建“中药-成分-靶点-通路”网络图,可以发现“黄芪-当归-大枣”角药作用多靶点映射于不同通路。本研究以TNF 信号通路为例,选取“黄芪-当归-大枣”角药作用于此通路的关键靶点PTGS2 进行实验验证。PTGS2 是前列腺素合成起始步骤的关键酶,其负责催化产生PGE2 等炎症介质,从而扩张血管、提高血管通透性,促进炎症反应。TNF-α是一类具有多种生物效应的细胞因子,其通过和细胞膜上特异性受体结合,实现促进细胞生长,分化,调亡及诱发炎症等生物学效应。TNF-α属于TNF家族,可以激活TNF 信号通路,实现其细胞毒性,炎性反应,免疫调节和细胞凋亡等生物学功能[25]。通过建立气血两虚小鼠模型,治疗组灌胃以“黄芪-当归-大枣”角药水煎剂,结果显示:模型组小鼠PTGS2mRNA表达、TNF-α含量明显升高(P<0.01),治疗组PTGS2mRNA表达、TNF-α含量明显降低(P<0.01),说明“黄芪-当归-大枣”角药可能通过降低PTGS2mRNA 表达,减少TNF-α的释放,进而抑制TNF 信号通路的激活而发挥补气养血的作用。进一步证实了,网络药理学预测得到的“黄芪-当归-大枣”角药补气养血可能的分子机制,确保方法和所得结论的可靠性。
综上所述,本研究运用网络药理学方法探讨“黄芪-当归-大枣”角药补气养血作用的化学成分、作用靶点、生物过程和信号通路,形成“中药-成分-靶点-通路”的完整作用过程,并加以实验验证。体现了“黄芪-当归-大枣”通过多成分、多靶点和多通路发挥治疗作用的特点,为其进一步临床应用提供理论指导,为药食同源药物研究提供方法思路。

