流动注射-化学发光法测定饲料中环丙氨嗪
李献锐,王 娜,王贝贝,籍雪平*,刘学锋
(1.河北医科大学药学院,河北石家庄 050017;2.河北医科大学基础医学院,河北石家庄 050017)
环丙氨嗪(Cyromazine,CYR)又名灭蝇胺,它是一种三嗪类昆虫生长调节剂,可以抑制双翅目及部分鞘翅目昆虫幼虫的生长发育和羽化[1,2],被广泛添加到动物饲料中以控制动物厩舍内蝇蛆的生长发育。然而毒理学研究证明,环丙氨嗪能导致动物的乳房肿瘤,其代谢产物三聚氰胺能够引起膀胱肿瘤[3]。若环丙氨嗪长期被用做饲料添加剂,容易导致动物源性食品中药物残留超标,影响人民身体健康[4]。世界各国均制定了严格的饲料添加浓度和畜产品中的最高残留限量[3,5,6]。有关环丙氨嗪的分析方法有荧光法[2]侧流免疫层析法[3]、高效液相色谱法[4,7]、液相色谱-串联质谱法[8,9]、气相色谱-质谱法[10]、核磁共振法[11]等。
流动注射-化学发光法因其具有仪器简单、易于实现自动化、灵敏度高及干扰小等优点,近年来在药物分析、生化分析等领域的应用日趋活跃[12]。唐晓爽等[13]和丁彦庭等[14]利用流动注射-化学发光法测定了奶粉中的三聚氰胺,而用化学发光法测定环丙氨嗪含量的方法未见报道。本实验研究了环丙氨嗪对K3[Fe(CN)6]-鲁米诺体系化学发光行为的影响。研究发现,环丙氨嗪可使该体系发光信号增强,结合流动注射技术,建立了一种简单、灵敏的测定环丙氨嗪的新方法,并应用于饲料中环丙氨嗪的分析测定。
1 实验部分
1.1 仪器与试剂
IFFS-A型多功能化学发光检测器(西安瑞迈公司);IFFM-E型流动注射化学发光分析仪(西安瑞迈公司);F-7000型荧光分光光度计(日本,日立公司);TU-1901型紫外-可见分光光度计(北京普析通用公司);微型高速离心机(Sigma公司)。
环丙氨嗪标准储备溶液(100.0 mg/L):称取10.00 mg环丙氨嗪标准品(阿拉丁公司),用适量水溶解并定容于100 mL棕色容量瓶中,贮存于4 ℃冰箱中,使用时用水稀释到所需浓度。鲁米诺储备溶液(1.0×10-2mol/L):称取0.1772 g鲁米诺(阿拉丁公司),用0.10 mol/L的NaOH溶液溶解并定容于100 mL棕色容量瓶中,使用时用0.03 mol/L NaOH溶液稀释。K3[Fe(CN)6]储备溶液:2.0×10-3mol/L,使用时用水稀释。所用试剂均为分析纯,水为超纯水(18 MΩ·cm)。
1.2 实验方法
流动注射-化学发光(FI-CL)流程如图1所示。鲁米诺碱性溶液与K3[Fe(CN)6]溶液经过三通管混合后载入流路,待基线稳定后,通过进样阀将环丙氨嗪溶液注入到鲁米诺与K3[Fe(CN)6]的混合液流中,发生化学发光反应。记录化学发光信号,以峰高定量。
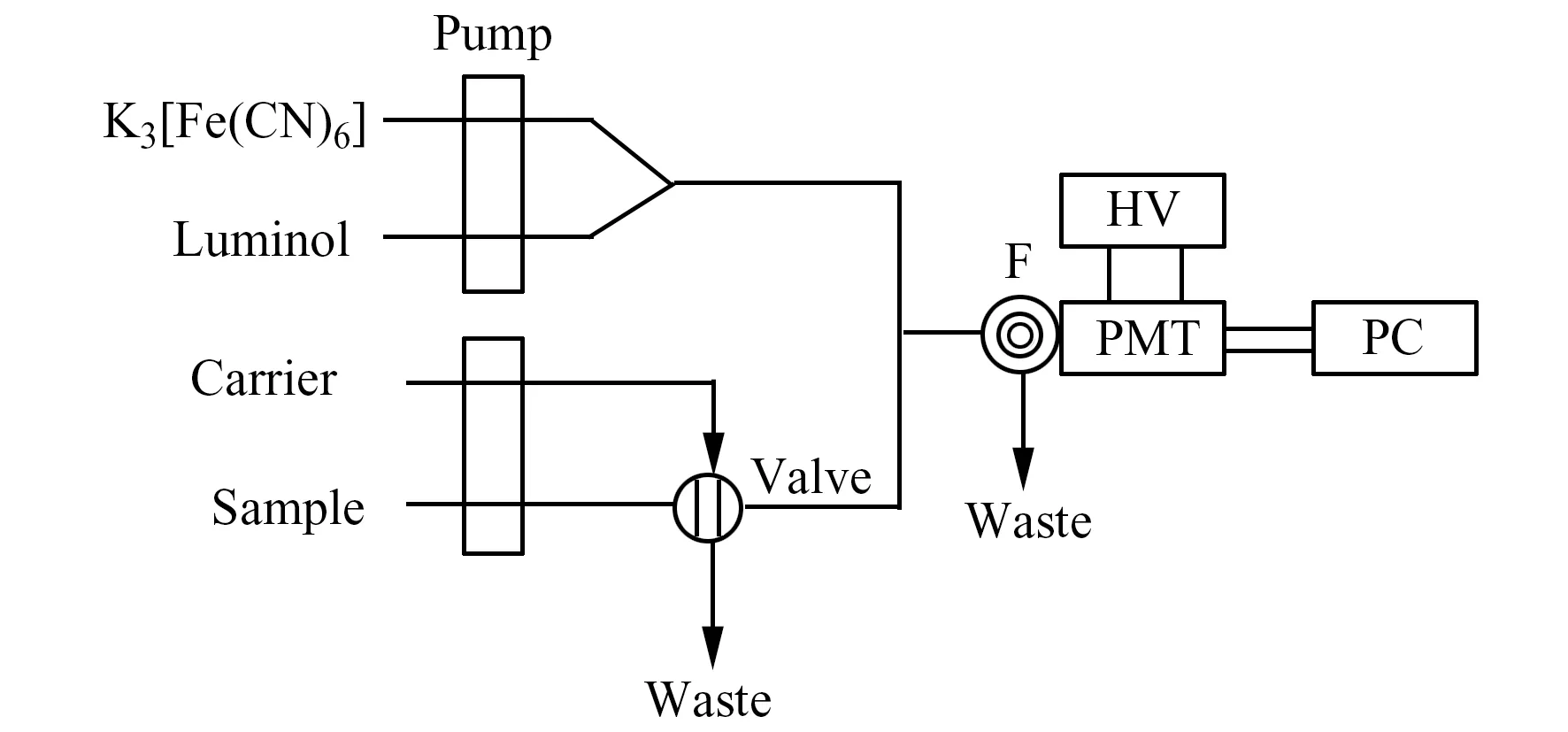
图1 流动注射化学发光分析流程示意图Fig.1 Schematic diagram of FI-CL system
1.3 样品处理
准确称取0.2000 g待测样品于小烧杯中,依次加入5 mL 1%三氯乙酸溶液和2 mL 2%Pb(Ac)2溶液,摇匀。将混合液以4 000 r/min离心5 min,吸取上清液,重复提取2次。将上清液合并,并以5 000 r/min离心5 min 后,取上清液5 mL,氮吹仪吹干后用水溶解,定容至100 mL即得样品溶液。
2 结果与讨论
2.1 化学发光反应的动力学曲线
采用静态注射的方式考察了K3[Fe(CN)6]-鲁米诺-环丙氨嗪发光体系的动力学性质(图2)。由动力学曲线可以发现,从试剂混合到发光信号达到最大值大约需2~3 s的时间,随后化学发光信号逐渐降低回到基线,说明K3[Fe(CN)6]氧化鲁米诺的反应为快发光反应。将50 μL 100.0 mg/L的环丙氨嗪注入5 mL 的K3[Fe(CN)6]-鲁米诺体系中,发光强度由原来的2 900增加到7 500,表明环丙氨嗪对K3[Fe(CN)6]-鲁米诺体系的化学发光具有增敏作用。
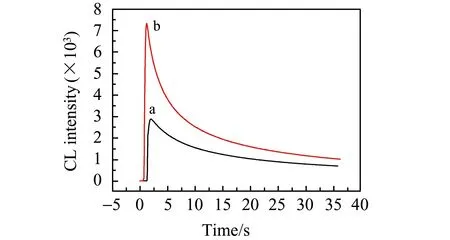
图2 化学发光的动力学曲线Fig.2 Kinetic curve of chemiluminescence reactiona.luminol-K3[Fe(CN)6];b.CYR-luminol-K3[Fe(CN)6].cluminol:1.0×10-5 mol/L,c(K3[Fe(CN)6]):2.0×10-5 mol/L,cCYR:1.0 mg/L.
2.2 流路参数的选择
在其它实验条件确定的情况下,分别考察了光电倍增管的负高压、混合管长度和试剂流速对信噪比的影响。结果表明,在光电倍增管的负高压为-650 V、混合管长度为10 cm、进样体积为100 μL和蠕动泵泵速在30 r/min时具有最佳的信噪比。
2.3 化学发光条件的优化
2.3.1 鲁米诺碱性介质的选择鲁米诺在碱性条件下容易被氧化。实验对比了同一浓度NaOH、Na2CO3、NaHCO3三种碱性介质对K3[Fe(CN)6]-鲁米诺化学发光体系的影响,发现在NaOH溶液中,环丙氨嗪对该发光体系具有最显著的增敏效果。因此选择NaOH作为碱性介质。
考察了不同浓度NaOH(0.005~0.2 mol/L)的影响。结果显示,随着其浓度的增大,发光信号先增强后减弱,但噪声也随之增大,根据最佳信噪比,确定NaOH的最佳浓度为0.03 mol/L。
2.3.2 鲁米诺浓度的选择发光强度的大小依赖于发光试剂的浓度。考察了鲁米诺浓度在1.0×10-8~5.0×10-5mol/L范围内对发光强度的影响。实验发现(图3),鲁米诺浓度从1.0×10-8增大至1.0×10-5mol/L,相对发光强度明显增强,但1.0×10-5mol/L以后相对发光强度增大不太明显。因此优化鲁米诺溶液的浓度为1.0×10-5mol/L。
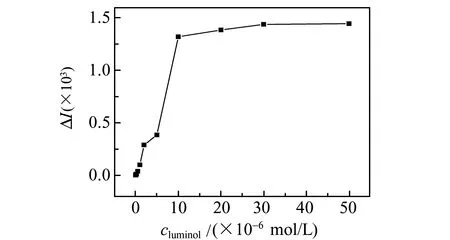
图3 鲁米诺浓度对相对化学发光强度(ΔI)的影响Fig.3 Effect of luminol concentration on ΔI2.0×10-5 mol/L K3[Fe(CN)6] + 0.10 mg/L CYR+ luminol from top to bottom(c luminol /10-6 mol/L):50,30,20,10,5,2,1,0.5,0.2.
2.3.3 K3[Fe(CN)6]浓度的选择考察了5.0×10-6~2.0×10-4mol/L浓度范围内的K3[Fe(CN)6]对光强的影响。结果如图4所示,当K3[Fe(CN)6]浓度为2.0×10-5mol/L时,相对发光强度达到最大值。超过2.0×10-5mol/L发光信号有所降低,因此确定K3[Fe(CN)6]的最佳浓度为2.0×10-5mol/L。
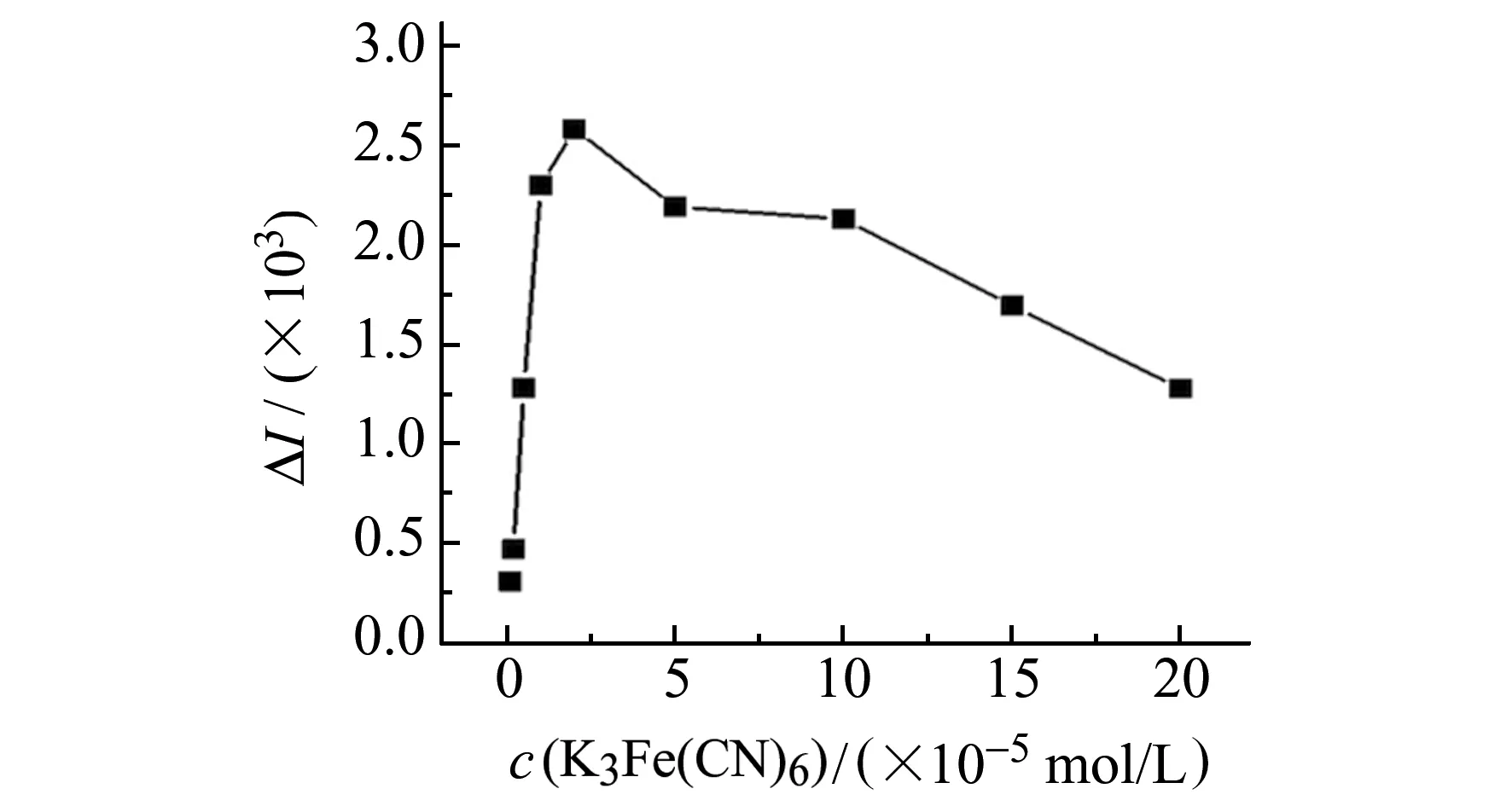
图4 K3[Fe(CN)6]浓度对相对发光信号的影响Fig.4 Effect of K3[Fe(CN)6] concentration on ΔI1.0×10-5 mol/L luminol+0.10 mg/L CYR+K3[Fe(CN)6] from top to bottom(c(K3[Fe(CN)6])/10-5 mol/L):20,15,10,5,2,1,0.5,0.2,0.1.
2.4 线性范围、灵敏度和检出限
在选定的实验条件下,环丙氨嗪在0.05~8.0 mg/L的浓度范围内与体系的发光信号呈良好的线性关系,回归方程为:ΔI=362.8c+10.68,r=0.9991,检出限为3.1×10-2mg/L。在最优条件下对1.50 mg/L的环丙氨嗪连续进行平行测定11次,相对标准偏差(RSD)为2.9%。
2.5 干扰试验
在环丙氨嗪浓度为3.0 mg/L,相对误差±5%的条件下,研究了可能共存的物质对测定的干扰情况。结果表明,1 000倍的K+、Ca2+、Na+、Mg2+、Cl-,100倍的淀粉、糊精不干扰测定。
2.6 样品测定
将3份饲料样品按“1.3”方法处理,在优化实验条件下对样品进行测定,并做加标回收实验,结果见表1。
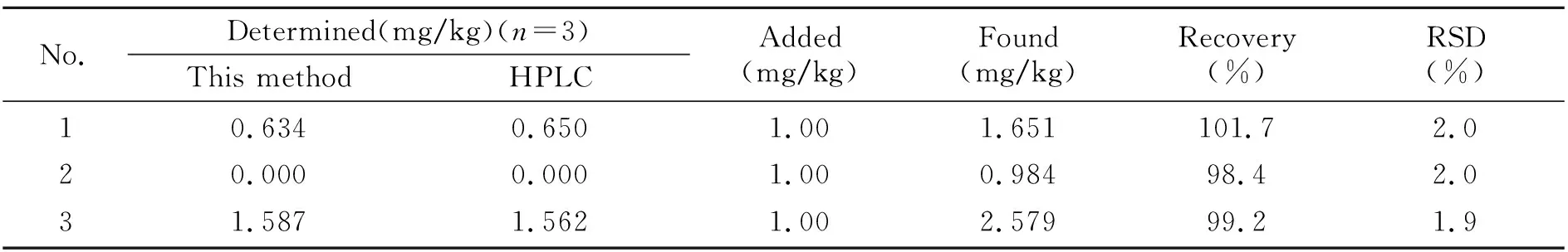
表1 饲料中环丙氨嗪的含量测定及回收率
2.7 反应机理探讨
为了探究可能的反应机理,扫描了体系中不同混合溶液的紫外吸收光谱(图5)和化学发光光谱(图6)。紫外-可见吸收光谱中环丙胺嗪在250 nm之外没有吸收,K3[Fe(CN)6]和鲁米诺混合溶液在加入环丙胺嗪前后体系的特征吸收峰没有变化,只是峰高有所增加。说明反应前后没有新物质生成,环丙胺嗪只起到催化作用。从化学发光图谱可以看到,K3[Fe(CN)6]-鲁米诺和K3[Fe(CN)6]-鲁米诺-CYR体系的最大发光波长都是425 nm,表明两个体系的发光物质相同,都是3-aminophthalate[15]。实验还发现通氮除氧,会降低增敏效果,说明环丙胺嗪的增敏效果和溶解氧有关。
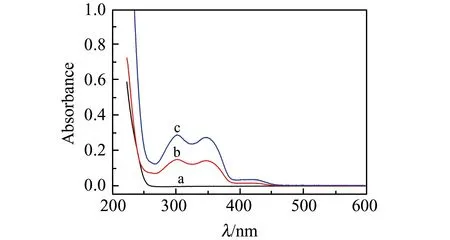
图5 紫外-可见(UV-Vis)吸收光谱图Fig.5 UV-Vis absorption spectrum of CL systema.cyromazine;b.K3[Fe(CN)6]-luminol;c.K3[Fe(CN)6]-luminol-cyromazine.
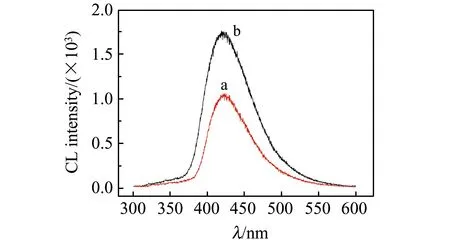
图6 化学发光光谱图Fig.6 Luminescence spectrum a.K3[Fe(CN)6]-luminol;b.K3[Fe(CN)6]-luminol-cyromazine.
基于以上实验结果,环丙胺嗪对K3[Fe(CN)6]-鲁米诺发光体系的增敏机理可推测如下:

3 结论
基于在碱性条件下,环丙氨嗪对鲁米诺-铁氰化钾体系发光反应具有明显的增敏作用,建立了流动注射化学发光测定环丙氨嗪的分析方法,并应用于动物饲料中的测定,取得了令人满意的结果。

