COVID-19疫情期间成人水痘-带状疱疹病毒性肺炎1例并文献复习
付蓉 崇延坤 张茜云 姜海波 彭剑 李一鸣
水痘是一种好发于儿童的良性自限性疾病,成人与儿童的发病率比例约为25∶1,但近年成人水痘发病率有增高趋势[1]。水痘-带状疱疹病毒性肺炎(varicella-zoster virus pneumonia,VZVP)由水痘-带状疱疹病毒(varicella-zoster virus,VZV)感染引起,也是水痘病人病情进展为重症以及死亡的主要原因[2-3]。VZV是人类疱疹病毒α亚型中的一种含包膜的双链DNA病毒,常引起皮肤和呼吸道感染,可通过呼吸道飞沫或接触传播,病人在发病前几天至疱疹结痂期间具有很强的传染力[4]。成人原发性VZVP相对少见,1942年Waring等首次报道了2例成人原发性VZVP,并将其分为一般支气管肺炎和原发性水痘肺炎[5-7]。大多数成人感染VZV后临床症状相对较重,并发VZVP的概率为10%~15%,有免疫抑制的VZVP病人发生严重并发症及死亡的风险更大。本文就1例成人VZVP的临床及影像资料进行分析并结合相关文献,简述VZVP的临床特征、影像表现及鉴别诊断。
1 临床资料
病人男,36岁,COVID-19疫情期间因感乏力,畏寒,自测体温38.4℃,遂至医院发热门诊就诊并接受住院隔离治疗。病人自发病后至就诊前未进行药物治疗,无腹痛、腹泻等胃肠道症状,但近10 d内接触过1例有武汉疫区旅居史者(无COVID-19症状及体征)。本例病人既往体健,无“结核、乙肝、伤寒”等传染病史,无粉尘及放射性物质接触史;无水痘病史,但其家属近期有水痘感染史。病人入院首日及次日有高热,至第3天体温降至正常范围;首日全身未见皮疹,次日躯干见几枚散在绿豆大小红色水泡样皮疹伴瘙痒、皮疹周围见红晕,并出现咳嗽、咳痰;入院第10天水疱开始干瘪、结痂,咳嗽、咳痰等呼吸道症状明显好转。相关实验室检查结果:入院当日、第3、8、12天检查严重急性呼吸综合征冠状病毒2(SARS-CoV-2)核酸检测结果均为阴性,血常规、肝功能及肾功能指标均在正常范围内;入院第3天超敏C反应蛋白为5.1 mg/L,乙肝抗体、丙肝抗体、人类免疫缺陷病毒及梅毒抗体、降钙素原均在正常范围内。
2 CT检查及影像表现
2.1 设备与方法 采用GE Light Speed VCT 64层螺旋CT扫描设备,扫描范围自胸廓入口至横膈下方。扫描参数:管电压 120 kV,管电流220~250 mA,准直器宽度 64×0.625 mm,矩阵 512×512,螺距 0.138,重建层厚及层间距均为1.25 mm。窗宽/窗位分别为:纵隔窗360 HU/60 HU,肺窗1 500 HU/-700 HU。原始数据传至GE Advantage Workstation工作站行薄层重组,重组影像的层厚及层间距均为1.25 mm。
2.2 影像表现 CT平扫影像上可见双肺多发斑片状磨玻璃影(ground-glass opacities,GGO)及不规则小结节影,结节直径为5~10 mm,部分结节周围可见晕征;病灶未见明显分叶及毛刺,部分病灶内可见含气支气管征,未见钙化影。病灶主要沿肺外周部、胸膜下及支气管血管束周围分布。纵隔及双肺门区未见增大淋巴结,双侧胸腔未见积液。经规范的抗病毒治疗3 d后,可见病灶逐渐吸收、消散。1个月后复查CT显示双肺内结节基本吸收消失,仅于双肺上叶各见1枚结节影、右肺中叶3枚结节影,双肺内未见钙化灶(图1)。
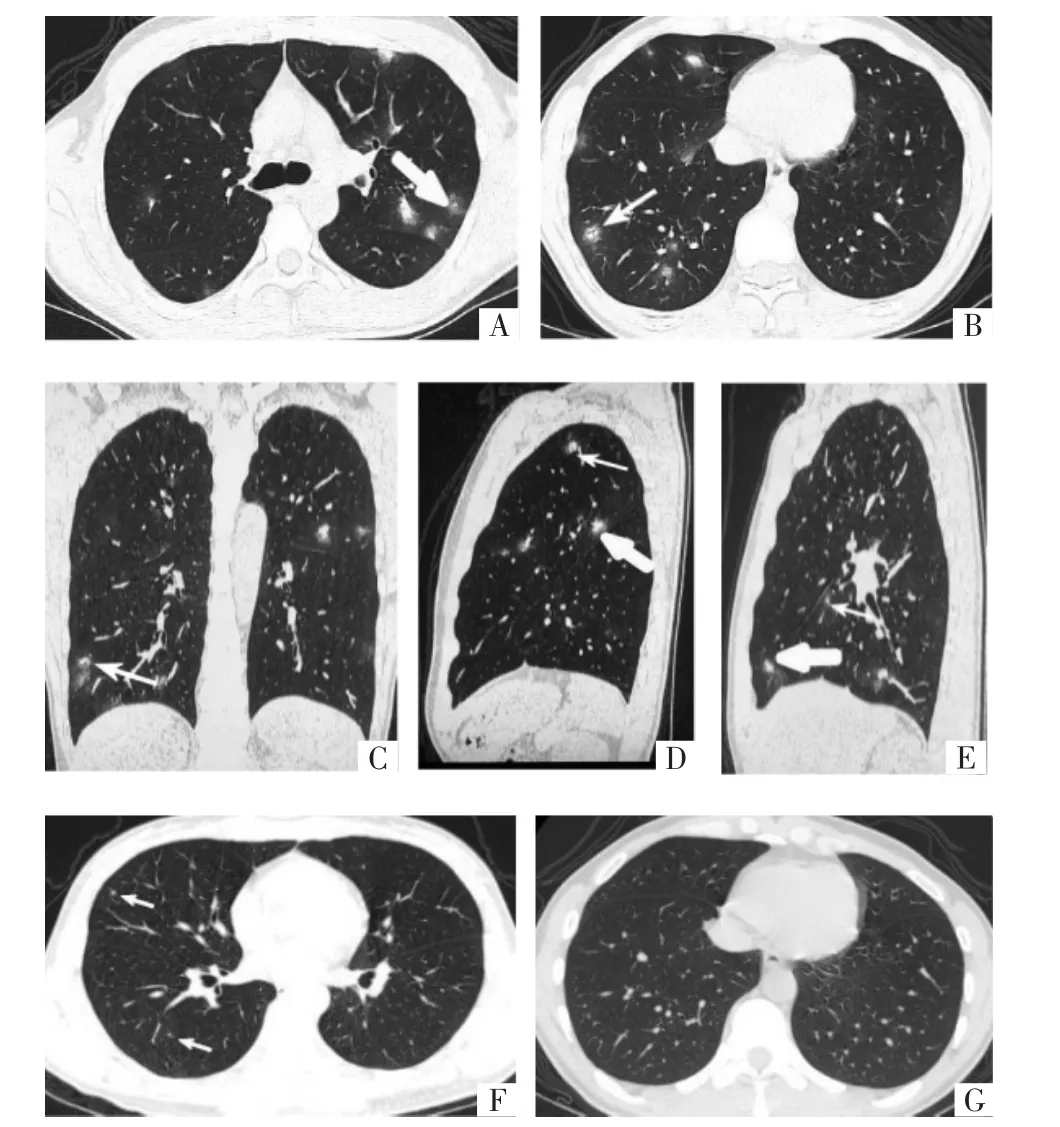
图1 A-E图为病人入院当天的CT平扫影像。A、B图为横断面肺窗薄层影像,示双肺胸膜下及支气管旁多发的不规则形结节影,周围伴晕征(A,粗箭),部分结节内见含气支气管征(B,细箭),结节内均未见钙化,纵隔淋巴结未见增大,未见胸腔积液;C图为冠状面薄层重组影像,示两肺胸膜下及支气管旁见多发不规则形结节影,部分结节内见含气支气管征(细箭);D、E图分别为左、右肺矢状面薄层重组影像,示支气管旁周围伴晕征的结节影(粗箭),部分结节内见含气支气管征(细箭);F图为入院第12天的横断面肺窗薄层CT平扫影像,经抗病毒治疗后双肺结节大部分完全吸收,仅剩余数枚小结节影 (细箭);G图为1个月后横断面肺窗薄层CT平扫影像,示两肺结节基本吸收好转,肺内未见钙化灶。
3 治疗
入院后给予奥司他韦静脉滴注及莫西沙星口服进行抗病毒、抗感染治疗,并给予散寒宣肺、燥湿化痰及益气健脾扶正的中药汤剂进行辅助治疗。皮疹瘙痒时辅以炉甘石洗剂涂抹患处。入院10 d后停止静脉用药。
4 讨论
4.1 临床特点 水痘为良性自限性疾病,可在病后获得终身免疫,但有时病毒以静止状态存留于神经节,多年后感染复发而出现带状疱疹[3]。部分水痘病人在感染VZV后可出现VZVP,其临床表现不尽相同,可以无症状,可以呈轻度病毒肺炎表现,严重者甚至死亡,死亡率为11%~20%[8]。有研究[8-10]显示,大多数VZVP病人通常在皮疹出现后1~7 d内开始出现肺炎症状,包括咳嗽、呼吸困难、咯血、呼吸急促、胸痛、发热,部分病人可以发生急性呼吸窘迫综合征,重症病人可进展为呼吸衰竭。通常VZVP发生在皮疹出现后2~7 d,恢复后可能出现肺部钙化灶,而本例病人先发生肺炎而后出现少量皮疹。Kim等[11]研究发现,部分VZVP病人的口腔及咽部黏膜也可以出现水痘皮疹。本病例是在出现VZVP次日躯干部出现少量水痘皮疹,这与其他VZVP表现不尽相同,可能是由于以下原因:①本例发病正好处于COVID-19疫情期间,在此期间医疗机构对于发热病人首先需要进行胸部CT平扫、血常规及SARS-CoV-2病毒核酸检查,因此本病例在出现发热后立即进行上述检查,而以往大多数水痘病人由于病程中不会出现呼吸系统疾病症状或进行住院治疗,也不会例行胸部CT检查,因此虽然少数病人在皮疹出现之前可能已有肺部感染,但不能及时发现肺部表现;②早期轻症水痘病人尤其是发病12 h内常规不会进行抗病毒治疗,而本病例在发病当日就入院行抗病毒治疗,由于病毒增殖受到抑制,因而没有出现大量水痘皮疹。
4.2 影像表现 既往有文献[1,12]报道VZVP主要的CT表现为多发结节,本病例在首次进行胸部CT平扫检查时也发现双肺多发斑片状GGO及不规则小结节影。Kim等[11]研究显示,免疫功能正常的VZVP病人CT常表现为双肺多发1~10 mm边界清楚或模糊的结节影,病灶周围有GGO晕斑或斑片状GGO,部分结节可以融合;肺门淋巴结病变和胸腔积液少见;肺部小结节一般在水痘皮疹干瘪、结痂后的1周内开始消失,但也有可能存在数周;部分病灶可有钙化,且治愈后钙化病灶持续存在。Ogawa等[13]报道1例较罕见的VZVP病例,该病人的肺部结节中有多个结节直径在5~20 mm之间。本病例双肺结节直径为5~10 mm,部分结节周围可见晕征,部分病灶内可见含气支气管征,病灶主要沿肺外周部、胸膜下及支气管血管束周围分布,与上述文献研究结果基本一致,但本例肺部结节内并未出现钙化灶。通常VZVP肺结节内的钙化灶由纤毛囊、肺泡内蛋白渗出或坏死组织组成,结节内钙化程度不一,本病例可能由于发病早期就开始进行规范治疗,抑制了肺泡内胶原蛋白渗出及炎性细胞浸润,使肺部结节内的组织坏死程度减轻,甚至部分肺组织并未发生坏死,因此多次CT检查中均未发现结节内钙化灶。Frangides等[8]研究发现,免疫功能受损的肺移植病人发生VZVP时可出现纵隔淋巴结肿大和小叶间隔增厚,而本例病人既往免疫功能正常,胸部CT检查未见纵隔及双肺门区的淋巴结增大。
4.3 鉴别诊断 由于该病例于COVID-19疫情期间发病且同为病毒性肺炎,因此须与COVID-19鉴别。一般情况下,VZVP要与单纯疱疹病毒肺炎(herpes-simplex viral pneumonia,HSVP)、 巨细胞病毒肺炎、EB病毒肺炎等病毒性肺炎、血管侵袭性曲霉菌病等进行鉴别诊断。
4.3.1 COVID-19 Han等[14]对 17例 COVID-19病人的临床资料及HRCT表现进行研究发现,该疾病主要引起深部气道和肺泡损伤为特征的炎性反应,故COVID-19病人不出现胸腔积液或者仅出现少量胸腔积液。仝等[15]报道COVID-19的CT影像主要表现为肺野外周和胸膜下区单发或者多发片状(类圆形)的GGO影,肺实变较少,部分病灶可见充气支气管征和铺路石征(GGO影和小叶间隔增厚或小叶间质线的结合),随着部分病变范围扩大及密度增高,病灶边缘模糊并呈楔形或扇形分布,疾病晚期呈“白肺”。COVID-19病人进行核酸检测后结果为阳性,特异性IgM抗体多在发病后3~5 d开始出现阳性,IgG抗体滴度恢复期较急性期增高4倍以上。VZVP在整个病程中也不出现或者可能出现少量胸腔积液,所以不能通过有无胸腔积液鉴别VZVP与COVID-19,需要结合其他影像表现及实验室检查结果进一步分析。本病例主要表现为分布在两肺野外周及支气管周围的不规则结节影并伴晕征,虽然有少数病灶仅表现为GGO影,但是周围伴晕征的不规则结节仍可作为与COVID-19的鉴别点,尤其是本病例无流行病接触史且2019-nCoV核酸及特异性抗体(IgM、IgG)检测均为阴性。
4.3.2 HSVP 主要由单纯疱疹病毒1型引起,多见于免疫功能低下的病人或气道受到创伤者,多表现为坏死性气管支气管炎、坏死性肺炎或间质性肺炎。胸部X线片上可见双侧肺叶、段或亚段分布的实变或GGO,也可见网状影。CT上可见弥漫性GGO、小叶间隔增厚、实变,甚至铺路石征,与VZVP鉴别存在一定困难,但多灶性或亚段GGO局灶实变及铺路石征更多见于HSVP,且其多伴有胸腔积液[3],可作为两者的鉴别点。
4.3.3 巨细胞病毒肺炎 免疫功能下降(移植手术后、长期糖皮质激素治疗)的病人感染巨细胞病毒后可引起肺部感染,通常在使用免疫抑制剂治疗后的数周或数月出现。最常见的影像表现为双肺不对称的弥漫性GGO,其次为边界不清楚的中央小叶结节、铺路石征和结节,而在VZVP中上述结节形态表现很少见,约1/3的巨细胞病毒肺炎病人可见胸水,但未见纵隔淋巴结增大[16-17]。
4.3.4 EB病毒肺炎 临床罕见。Shiranee等[18]曾在1996年报道了1例,其病理特征为沿间质性肺浸润的支气管血管束和小叶间隔,可见单核炎性细胞;影像表现为纵隔淋巴结病变,间质浸润和广泛的GGO较少见,脾肿大较常见[19],故不难与VZVP进行鉴别。
4.3.5 血管侵袭性曲霉菌病 该病是由于曲霉菌菌丝穿过肺中-小动脉血管壁进入血管,菌丝在血管内形成真菌血栓,血栓随着肺血循环阻塞部分肺中-小动脉从而引起肺梗死。最常见的危险因素是长期的中性粒细胞减少、造血干细胞或实体器官移植、遗传或获得性免疫缺陷以及使用类固醇或其他免疫抑制药物。早期CT上常可见结节伴晕征,但其结节直径常>1 cm,这种结节的形成多由曲霉菌菌丝阻塞肺中-小动脉后引起肺组织梗死所致,与VZVP的炎性结节不同。另一典型表现是结节内出现空气新月征,反映了坏死组织的收缩,通常从中性粒细胞减少恢复开始。空气新月征可进一步发展为厚壁空腔,最后形成残余薄壁空腔[20]。该疾病早期CT上出现结节伴晕征与VZVP的表现较为相似,依靠结节形态和结节周围的晕征较难鉴别两者,而血管侵袭性曲霉菌病的结节可出现空气新月征并可进展为厚壁空腔,而VZVP结节内出现的是空气支气管征且经过治疗后结节最终吸收消失,因此可根据这一影像特点对这两种疾病进行鉴别。
4.4 治疗与预后 成人VZVP在明确诊断后应及早采取抗病毒药物治疗,并积极预防并发症的发生,而对于重症VZVP成年病人,必要时可联用机械通气、丙种球蛋白及激素等,以有效控制病情,改善病人预后[4]。
4.5 小结 VZVP相对于免疫功能下降(包括恶性疾病、化疗、免疫系统疾病、获得性免疫缺陷综合征、器官和骨髓移植后进行免疫抑制治疗期间、营养不良等)的病人是一种重要的致死性疾病,这类人群在感染VZV后死亡率可达15%~18%[21-22]。目前,临床上主要依据病人的接触史、临床表现、病毒检测及影像表现等对VZVP进行诊断。由于VZVP比较少见,而且一部分VZVP病人的呼吸道症状并不明显或者不能明确提供与水痘病人接触史,因此不进行相关的影像检查可能难以对本病进行明确诊断。胸部CT检查可以清楚显示病灶的部位、大小,并且可以评估病情严重程度及病情的进展,具有较高的诊断符合率,可为临床诊疗工作提供一定的参考。

