松萝酸的结构修饰与生物活性研究进展
贾 妍,邓雁如,王莉宁
天津中医药大学中药学院,天津 301617
松萝酸(usnic acid)又名地衣酸,是地衣中分布最广泛的重要次级代谢产物之一。1844年,德国科学家克诺普(knop)从地衣中首次分离出来。其化学名为2,6-二乙酰基-7,9-二羟基-8,9b-二甲基-1,3(2H,9bH)-二苯并呋喃二酮,存在左旋(-)、右旋(+)两种构型(结构式见图1),多分布于松萝属Usnea、树花属Ramalina、石蕊属Cladonia、树发属Alectoria、梅衣属Parmelia、茶渍属Lecanora等[1,2]。松萝酸或粗提物多用于护肤品、保健品、抑菌剂等;在欧洲等地区,已经将松萝酸作为膏剂、乳剂用于治疗创伤及化脓性伤口;还作为膳食补充剂在美国销售;松萝酸钠可用于治疗肺结核[3,4];目前,已有一些松萝酸药物作为抗菌剂上市,如意大利的Foot zeta、Micofoot Zeta和Steril Zeta,印度尼西亚的Scabicid等,松萝酸有着广泛的应用前景。由于其结构独特且具有多种生物活性,因此受到化学家及药物学家的广泛关注[5]。
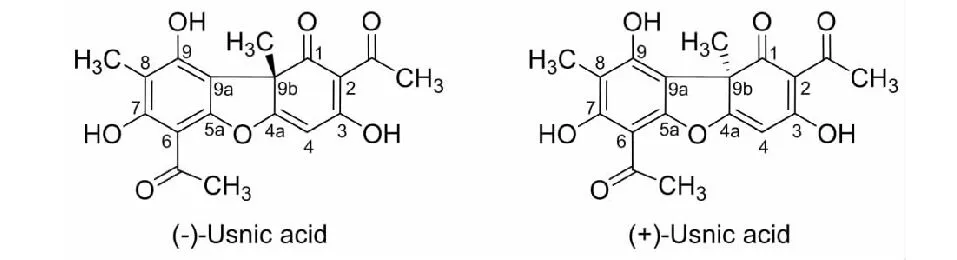
图1 松萝酸的化学结构
研究表明,松萝酸具有广谱生物活性,体外实验已经证明抗菌[6-8]、抗肿瘤[9]、抗病毒、抗结核[3,10]、促进伤口愈合[11]、抗有丝分裂[12]、诱导细胞凋亡和抗增殖[13],还可用作昆虫病原微生物的杀虫增效剂[14]等多种生理活性。然而由于溶解度较差,体内生物利用度低等原因[1,3,15,16],使得松萝酸的应用受到很大限制。为了改善溶解性并提高生物活性,研究者对其进行了结构修饰,发现其衍生物在抗菌、抗病毒、抗肿瘤等方面具有较好的活性。结合本课题组研究方向,现从松萝酸的结构修饰和衍生物的生物活性两方面进行介绍,并总结其构效关系。
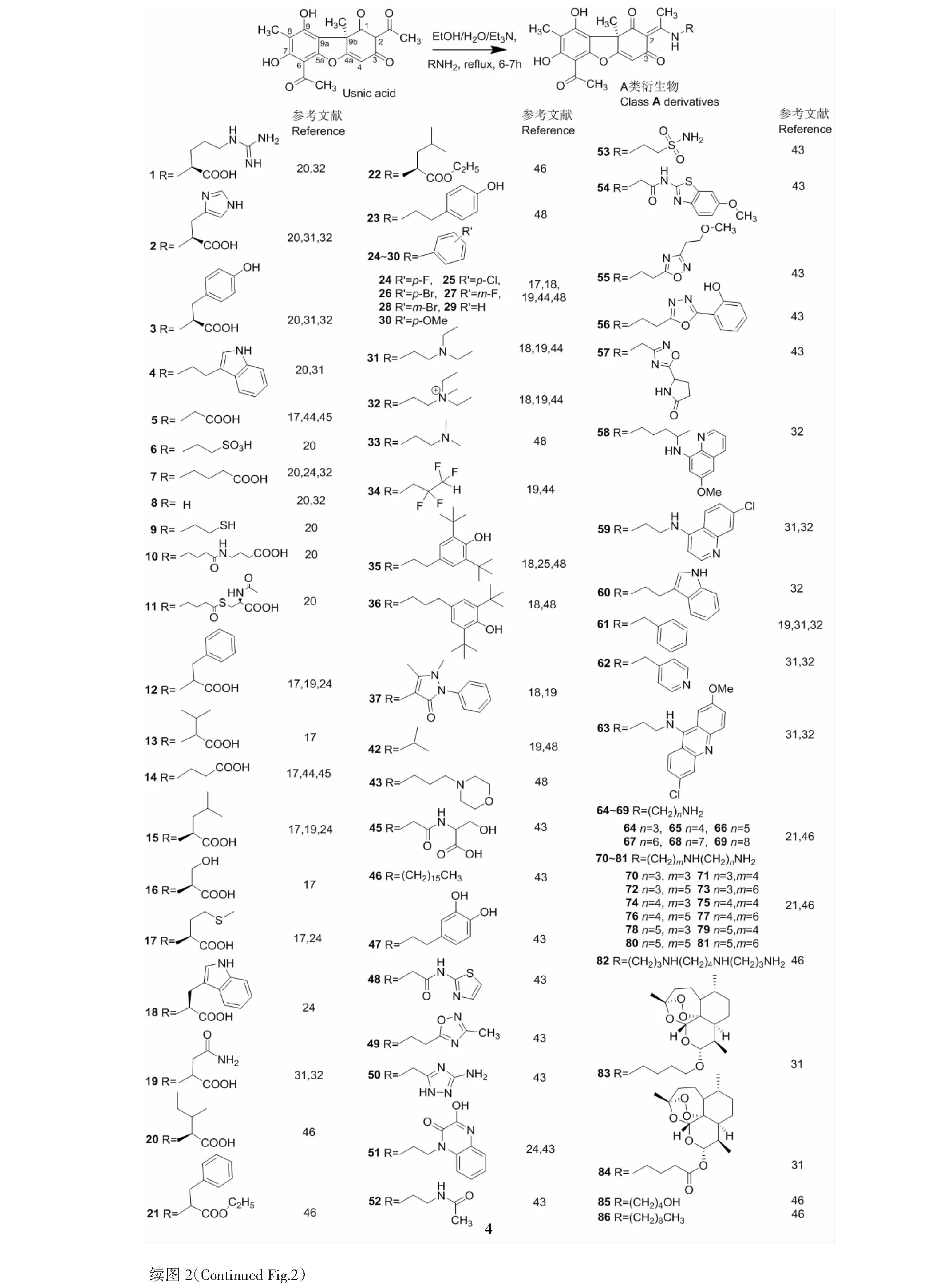
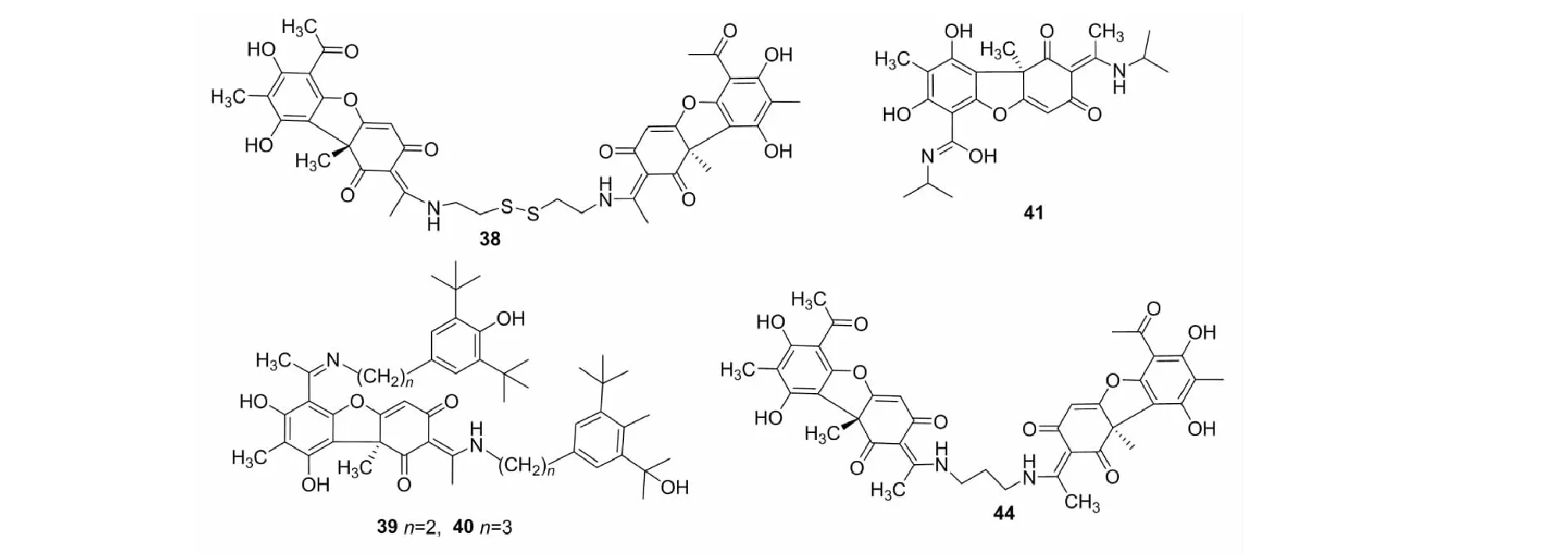
图2 A类衍生物的反应路线与化学结构
1 松萝酸的结构修饰
目前已研究的松萝酸衍生物主要有8类:(1)A类衍生物:松萝酸的烯胺衍生物1~86;(2)B类衍生物:松萝酸6位乙酰基与溴取代反应的衍生物,包括呋喃酮衍生物87~118(B1系列)、硫醚衍生物119~128(B2系列)、噻唑衍生物129~144(B3系列);(3)C类衍生物:松萝酸与芳香醛的Claisen-Schmidt反应衍生物145~194;(4)D类衍生物:松萝酸与苯肼类化合物反应的衍生物,包括腙衍生物195~201(D1系列)、吡唑衍生物202~242(D2系列);(5)E类衍生物:松萝酸的酯化衍生物243~253;(6)F类衍生物:松萝酸的醚化衍生物254~258;(7)G类衍生物:松萝酸的曼尼希衍生物259~263;(8)其他衍生物264~266。具体衍生物反应路线描述如下。
1.1 松萝酸烯胺衍生物(A类衍生物)
在乙醇回流条件下,松萝酸的2位(或6位)乙酰羰基对伯胺、仲胺进行亲核攻击,发生烯胺反应[17,18],生成衍生物1~86(结构见图2),其中39和40[18]、41[19]修饰位点在2和6位,38[20]和44[21]形成二聚体衍生物,其余修饰位点均只在2位。松萝酸与不同胺试剂反应,所得衍生物产率不同,丝氨酸衍生物(16)、蛋氨酸衍生物(17)衍生物产率低于30%,其他10种氨基酸衍生物(1~3、5、12~15、18、20)和苯胺衍生物(24~30)产率均大于60%;46、70~81、85和86为松萝酸的长烷基链烯胺衍生物,其中只含一个氮原子的较长烷基链衍生物(46、85和86)产率为70%左右,含有三个氮原子的较长支链衍生物(70~81)产率为34%~49%,从反应产率来看,支链中杂原子越多,产率越低。
1.2 松萝酸6位乙酰基与溴取代反应的衍生物(B类衍生物)
松萝酸与溴在二恶烷中发生亲电取代反应生成中间体a。a在不同条件下与不同试剂进一步反应生成B1、B2、B3系列衍生物(见图3),具体反应路线如下。
1.2.1 松萝酸呋喃酮衍生物(B1系列衍生物)
中间体a经过两个连续亲核取代反应,形成6,7位环化的呋喃酮衍生物87(产率90%);在碱催化条件下,87呋喃酮环上的活泼亚甲基与适当的醛进一步缩合,得松萝酸呋喃酮衍生物88~91[22,23]、92和93[23]、94和95[22]、96[23]、97和98[23,24]、99[23]、100和101[22]、102和103[23]、104[22]、105[23]、106[22,23]、107[22]、108和109[23]、110[22,23]、111~118[23](B1系列衍生物取代基R如图4所示)。取代基R为烷基链(100和101)产率较低为10%~20%,且链越长,产率越低;取代基R为连有甲基或溴的2-噻吩环(113~116)时,产率可高达90%,其余产率均在50%~70%。
1.2.2 松萝酸硫醚衍生物(B2系列衍生物)
在碱性条件下,中间体a与适当的硫醇回流得硫醚衍生物119~123[24]、124[19,25,26];松萝酸先经过C7位甲基化,再通过与119~123相同的合成方法得衍生物125~128[24](B2系列衍生物结构如图5所示)。119~124修饰位点在6位;125~128在6、7位同时修饰。取代基R2为4-氯苯基的衍生物122产率高达82%,119和120产率较低为16%,其余产率均在50%~60%。

图3 B类衍生物的反应路线
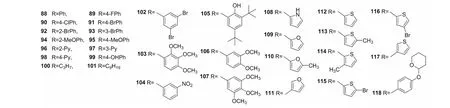
图4 B1系列衍生物取代基

图5 B2系列衍生物的化学结构
1.2.3 松萝酸噻唑衍生物(B3系列衍生物)
a与稍过量的取代硫脲回流得噻唑衍生物129~135[25,27]、136~144[25,28](B3系列衍生物取代基R2如图6所示)。修饰位点均在6位,噻唑衍生物129~131、氨基噻唑衍生物132~135产率为50%~70%,肼基噻唑衍生物136~144产率为70%~90%。
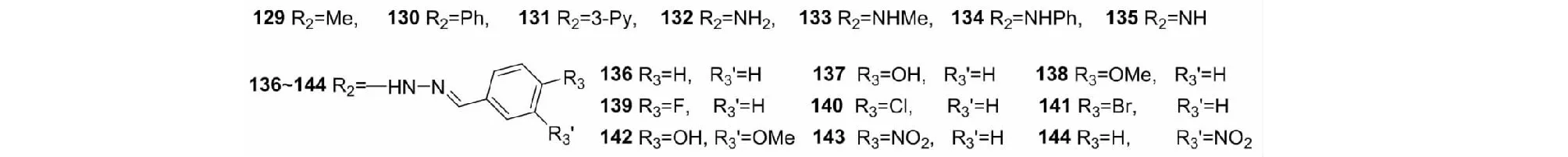
图6 B3系列衍生物取代基
1.3 松萝酸与芳香醛的Claisen-Schmidt缩合反应衍生物(C类衍生物)
在碱催化条件下,松萝酸6位乙酰基与不同芳香醛在甲醇中发生缩合反应,生成苯亚甲基衍生物162~194,和6、7位环化的吡喃酮衍生物145~161[29](C类衍生物反应路线与结构式见图7),产率均在10%~30%。
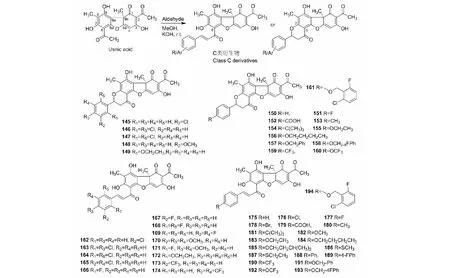
图7 C类衍生物的反应路线与化学结构
1.4 松萝酸与苯肼类化合物反应的衍生物(D类衍生物)
在乙醇回流条件下,松萝酸与苯肼类化合物反应,生成松萝酸的腙与吡唑衍生物,具体反应如下。
1.4.1 松萝酸的腙衍生物(D1系列衍生物)
松萝酸与等摩尔量含硝基、羰基等吸电子基取代的苯肼反应,由于这些吸电子基使肼氮原子的亲核性降低,仅在C2上的乙酰基上与松萝酸反应形成腙195和196[19,30]、197和198[31,32]、199[32]、200[31,32]、201[32](产率80%~90%)(D1系列衍生物反应路线与结构式见图8)。
1.4.2 松萝酸的吡唑衍生物(D2系列衍生物)
松萝酸与等摩尔量取代苯肼反应生成腙,肼氮上的氢与3位羟基进一步缩合,形成2,3位稠合的吡唑衍生物202~207[19,30]、208[30]、209~211[19,30](产率80%~90%);当取代苯肼摩尔量为两倍及以上时,第二分子取代苯肼同时在C6位的乙酰基羰基上加成形成衍生物212~214[19,30]、215[30]、216~218[19,30](产率10%~40%)(反应路线与化学结构见图9)。这个过程相当缓慢,并且在大多数情况下会相互转化,即使将松萝酸加入到大量的取代苯肼中,反应也不会只生成两分子肼的衍生物。但是,松萝酸与过量的甲氧基和乙氧基取代的苯肼在长时间加热条件下,只生成单一的衍生物207与208,且产率分别高达98%和96%。
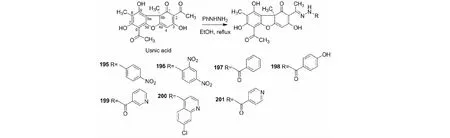
图8 D1系列衍生物反应路线与化学结构

图9 D2系列衍生物反应路线与化学结构
其中松萝酸与苯肼反应生成的产物202(产率96%),1位羰基经NaBH4进一步还原生成219[33,34](产率94%);重氮甲烷对中间体化合物219甲基化,生成9位甲基化的220[35](产率为80%);220与取代的苯甲醛在C6位乙酰基上缩合,生成松萝酸的查尔酮类衍生物221和222[24,35],223[35],224[35,36],225[24],226[24,35],227和228[24],229[24,35],230~232[24],233~235[24,35](反应路线与化学结构见图10)。此类化合物均在1位还原,2、3位稠合形成吡唑环,6位乙酰基缩合,9位甲基化。硝基取代的苯甲醛衍生物235产率为40%,其余衍生物产率均为60%~80%。
224与水合肼在乙醇中回流生成236和237[36],227与叔丁基氢过氧化物在无水甲苯中反应生成238[24]。202氧化生成吡唑氧化产物239[37]。202还可直接与重氮甲烷反应得中间体240[33,35](产率55%),与取代苯甲醛进一步反应生成241[24,35],242[35](产率为20%~30%)。
1.5 松萝酸酯化衍生物(E类衍生物)
松萝酸与支链酰氯混溶于硫酸乙醚中,加入三乙胺和五甲基氨基吡啶做催化剂反应;或在氯仿、吡啶同时存在下反应得7,9-二酯衍生物243和244[19]、245[19,24]、246~248[38],产率为60%~80%。在氯仿中,用吡啶催化,松萝酸与芳酰氯反应得2,3-二酯衍生物249~251[38,39],产率在40%左右,反应过程中还会得到少量的四酯衍生物252[38](产率31%),246与苯甲酰氯反应得四酯衍生物253(产率35%)。松萝酸与支链酰氯反应产物为7,9-二酯衍生物;与芳酰氯的产物,则是2,3-二酯衍生物,同时还有少量四酯(E类衍生物反应路线与结构式见图11)。
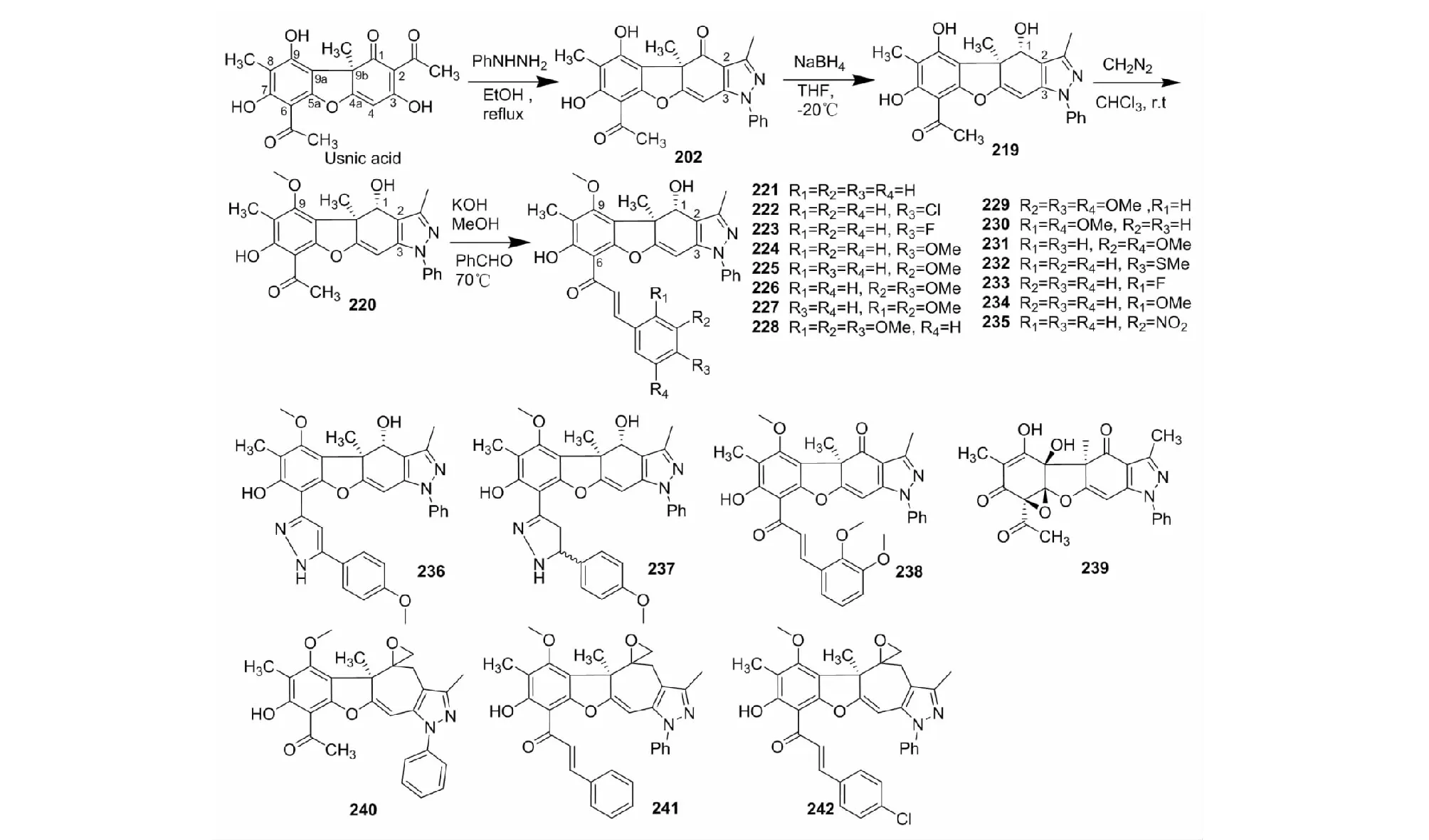
图10 D2系列衍生物的反应路线与化学结构
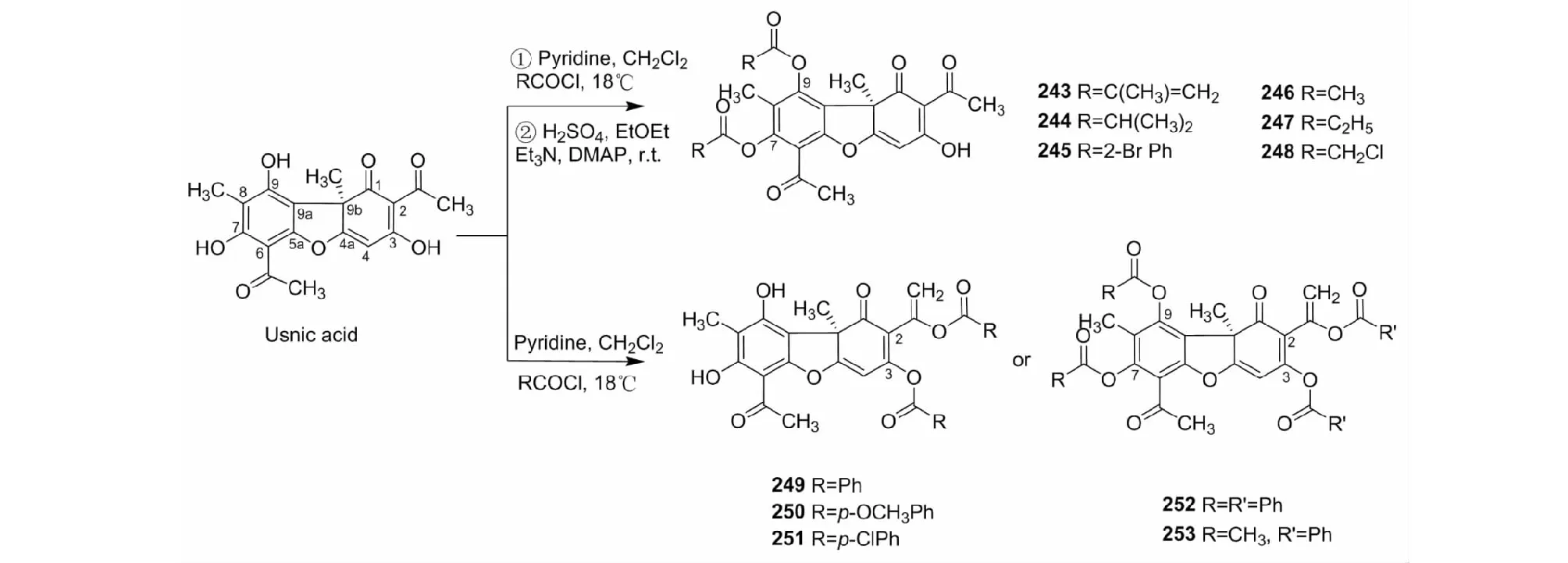
图11 E类衍生物的反应路线与化学结构
1.6 松萝酸醚化衍生物(F类衍生物)
在松萝酸的无水DMF溶液中,加入K2CO3与等摩尔量的多氟芳族化合物反应得7位醚化的松萝酸衍生物254[19]、255[19,40]、256[19]、257[19,24,40]、258[19](F类衍生物反应路线与结构式见图12)。除255和256(产率为34%~55%)外,其余衍生物产率为80%~90%。

图12 F类衍生物的反应路线与化学结构
1.7 松萝酸的曼尼希碱衍生物(G类衍生物)
松萝酸与仲胺、甲醛在甲醇溶液中发生Mannich反应,得到C2位脱乙酰基的曼尼希衍生物259~263[41](G类衍生物反应路线与结构式见图13)产率为60%~70%。
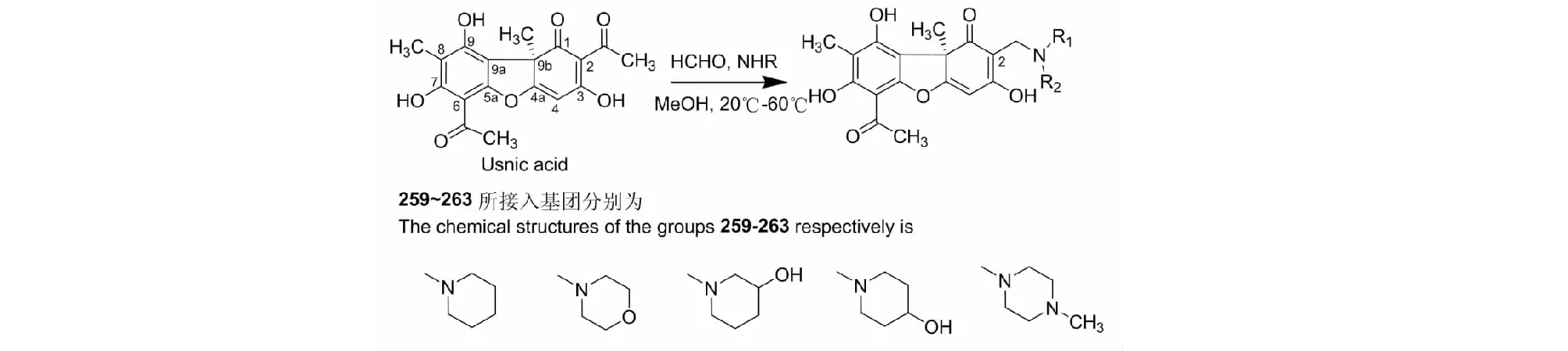
图13 G类衍生物反应路线与结构式
1.8 其他
此外,还有松萝酸的氧化产物264和265[37],266[19],分解产物267[42](结构式见图14)。
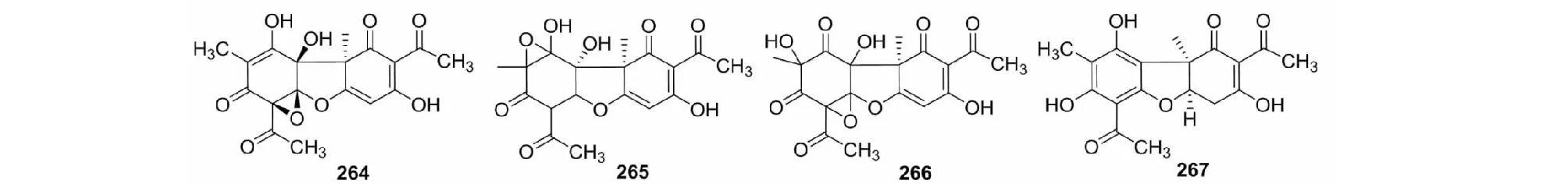
图14 松萝酸其他衍生物的化学结构
研究报道的对松萝酸的修饰主要有上述8类,以右旋为主,大部分衍生物的改造是在松萝酸的2位或6位乙酰基以及羟基上。其中烯胺衍生物、腙类衍生物、曼尼希类衍生物主要发生在2位乙酰基上;B系列衍生物以及Claisen-Schmidt缩合反应主要在6位乙酰基上;醚化和酯化发生在不同的羟基上,形成不同的取代衍生物。这对研究松萝酸衍生物的合成路线、工艺优化及探讨新的修饰路线,具有一定的参考价值。文献也报道了这些化合物的生物活性,下面将介绍这些衍生物的生物活性。
2 松萝酸衍生物的活性研究
研究表明,松萝酸衍生物具有多种生物活性,如抗菌[32,43]、抗病毒[24,44,45]、抗肿瘤[23,25,29,46-48]、抗疟疾[31]、促进伤口愈合[20]等。由于反应类型、修饰位点、接入的取代基不同,其生物活性也不同,目前主要研究了抗菌、抗病毒、抗肿瘤活性,下面将分别进行介绍。
2.1 松萝酸衍生物抗菌活性
松萝酸具有广泛的抗菌活性,有研究发现,松萝酸可以通过抑制RNA和DNA的合成,从而达到抑制革兰氏阳性菌的作用[49];或通过抑制细菌生物膜,发挥抑菌作用等[50,51]。
松萝酸衍生物则对革兰氏阳性菌金黄色葡萄球菌Staphylococcusaureus(S.aureus)、耐甲氧西林金黄色葡萄球菌Methicillin-resistantStaphylococcusaureus(MRSA)、结核分枝杆菌Mycobacteriumtuberculosis(M.tuber)等细菌[6,52]和致病真菌[24,53]具有良好的活性。
抗S.aureus活性方面,A类烯胺衍生物64、70、74和78[21]活性优于松萝酸,45~57活性低于松萝酸[43],由此可知,通过烯胺反应在2位引入多胺链可增强其活性;另外E类酯化衍生物249[39]活性优于松萝酸。
抗MRSA活性方面,A类衍生物45~57中,除53(MIC = 2.22 × 10-2mmol/mL)优于松萝酸(MIC = 4.28 × 10-2mmol/mL)外,其余活性均低于松萝酸[43]。
抗M.tuber活性方面,A类烯胺衍生物3、5、60与松萝酸活性相当(MIC值均为32 μg/mL);A类烯胺衍生物59、61、63与D1系列腙衍生物199~201活性高于松萝酸,其中63与200活性最好(MIC值均为8 μg/mL),表明氯取代喹啉(59、200)与氯取代吖啶(63)基团的引入,可增强活性,然而,通过长链(4个C原子)间隔连接喹啉的衍生物58(MIC = 64 μg/mL),活性显著降低[32]。
A类衍生物45~57对革兰氏阴性菌大肠杆菌Escherichiacoli、阴沟肠杆菌Enterobactercloacae、铜绿假单胞菌Pseudomonasaeruginosa的活性均低于松萝酸;除55(MIC = 0.20 × 10-2mmol/mL)抗蜡状芽孢杆菌Bacilluscereus活性优于松萝酸(MIC = 1.07 × 10-2mmol/mL)外,其余活性均低于松萝酸[43]。此外,衍生物45~57还对曲霉菌、木霉菌、青霉菌等真菌具有非常强的活性(尤其是曲霉菌)MIC为0.35~7.53 × 10-2mmol/mL,其中,46活性最佳(MIC = 0.35~0.70 × 10-2mmol/mL),其次是57和56[43]。
E类衍生物249对P.aeruginosa的活性高于松萝酸,对弗氏志贺氏菌Shigellaflexner和枯草芽孢杆菌Bacillussubtilis活性均低于松萝酸[39]。
综上,部分A类烯胺衍生物对革兰氏阳性菌具有较好的活性,对革兰氏阴性菌活性差;2位引入十六烷基或多个杂原子取代基的烯胺衍生物具有良好的抗真菌活性;引入芳基喹啉的腙衍生物,抗结核分枝杆菌活性增强,这为进一步开发优良的抗菌类药物奠定了良好的基础。
2.2 松萝酸衍生物抗病毒活性
松萝酸具有抗疱疹病毒[54,55]、沙粒病毒[56]、人乳头瘤病毒[57]和多瘤病毒[58]的作用。松萝酸衍生物主要是针对甲型H1N1流感病毒pdm09的研究。所研究的松萝酸衍生物中,大部分活性强于松萝酸(ED50= 51.7 μM),其中A类烯胺衍生物除7(ED50= 35.0 μM)外,5、12、14和15、17、24、27和28、32、34和B1呋喃酮衍生物91、94、97和98活性明显增强(ED50为4.2~11.2 μM);B2硫醚衍生物119~128活性普遍增强:120~122活性最强(ED50最低为2.0 μM),且7位甲醚化的化合物较未甲醚化的化合物活性低,而6位接入含有COOH基团的衍生物128,活性明显降低(ED50= 160.7 μM);D2系列衍生物202、210、221、222、225~232、236、238~240中,219(ED50= 2.4 μM)活性明显优于202(ED50= 69.5 μM)表明1位碳基还原为羟基的重要性,除衍生物238(ED50= 8.7 μM)、239(ED50= 13.4 μM)、241(ED50= 5.5 μM)活性明显增强而240(ED50= 262 μM)显著降低外,其余化合物活性均在25.9~82.7 μM;E类酯化双取代衍生物245(ED50= 7.8 μM),F类醚化衍生物257(ED50= 7.2 μM),氧化衍生物264(ED50= 10.6 μM)活性均增强。此外,本节所涉及衍生物的对映异构体活性研究表明,(-)-松萝酸比(+)-松萝酸抗病毒活性强,经结构修饰后,(+)-松萝酸衍生物(烯胺、吡唑)活性更强[24,44]。
衍生物13、202、238、264对不同流感病毒A/California/7/09(H1N1pdm)、A/Aichi/2/68(H3N2)、A/Vladivostok/2/09(H1N1)、A/PR/8/34(H1N1)的活性无明显差别。其中,13活性明显增加,且不会引起抗性菌株的出现,同时还可降低肝毒性[45],有希望成为抗流感新药的候选化合物。
基于上述研究可知,松萝酸经结构修饰,如引入小支链的氨基酸、硫原子或酯化、氧化产物等能够增强其抗病毒活性,可促进开发具有病毒抑制作用的替代靶标新型抗流感化合物。
2.3 松萝酸衍生物抗肿瘤活性
松萝酸具有抗肿瘤作用,其作用机制与抑制酪氨酰-DNA磷酸二酯酶1(Tyrosyl-DNA phosphodiesterase 1,Tdp1,PBD code:1MU7)有关[23,25,48]。Tdp1是用于停滞的DNA-拓扑异构酶1(Top1)切割复合物和其他3′-末端DNA损伤的修复酶,是抗肿瘤治疗的有希望的靶标[48]。松萝酸衍生物对Tdp1的研究也成为近几年的热点之一。
文献对A类烯胺衍生物23~29、35和36、42和43、B1系列呋喃酮衍生物88~118、B3系列噻唑衍生物129~144对Tdp1抑制活性进行了研究。除33、43外,活性都比松萝酸(IC50>50 μM)强,39个衍生物强于阳性对照药呋喃二脒(IC50= 1.23 μM)。105、115、139、143、138、144抑制酶的浓度在纳摩尔范围内(IC50为25~86 nM),其中,105活性最好(IC50= 25 nM),139次之(IC50= 26 nM)。105和115的对应异构体活性相似,表明松萝酸衍生物中不对称中心的绝对构型不影响化合物对Tdp1的抑制活性。
松萝酸B3系列噻唑衍生物129~135(IC50为0.61~5.9 μM)与肼基噻唑衍生物136~144(IC50为0.026~0.457 μM)相比,后者活性提高1~2个数量级,表明腙片段的重要性[25]。
松萝酸的B1系列呋喃酮衍生物88~118(除105与115在纳摩尔范围内抑制),在0.16~6.73 μM范围显示出较好的活性。与88(IC50= 0.72 μM)相比,溴原子(91~93、102,IC50为0.15~0.53 μM)的加入会增强其活性,且取代位置影响不明显,而F,Cl原子则会降低其抑制活性;甲氧基取代苯基衍生物(94、95、103)活性增强两倍左右[23]。
松萝酸A类衍生物除33、43活性低于松萝酸外,23~29、35和36、42和43活性较好(IC50为0.16~2.0 μM),且对人MCF-7和A-549肿瘤细胞均具有低毒性。35(IC50= 0.19 μM)和36(IC50= 0.16 μM)在高纳摩尔浓度范围内显示出抑制活性,表明叔丁基在抑制Tdp1中的重要作用。引入卤代苯胺基团,活性增强,且位置影响不大,溴取代最有效(衍生物26IC50= 0.26 μM);甲基取代没有明显影响,而芳香取代基比较重要,无环取代的33与吗啉取代43在研究浓度范围不能抑制Tdp1[48]。
松萝酸在人类乳腺癌细胞系中诱导自噬,显示出较高抗增殖活性,可作为一种新型的潜在大分子靶标雷帕霉素(Mammalian target of rapamycin,mTOR,PDB code:4JT5)抑制剂[29],且研究表明,松萝酸C类衍生物145~194对mTOR失调的人类乳腺癌细胞系MCF-7和MDAMB-231表现出类似的的活性:192活性最强,IC50分别为0.28 μM和0.32 μM;对位单取代的苯亚甲基衍生物175~194与其他位置取代或多取代的衍生物相比,活性普遍较好;145~161的活性都低于相应的亚苄基对应物162~194,这表明了亚苄基和二苯并呋喃部分在维持mTOR相互作用和细胞效力方面的重要性;由于疏水性差异,对-溴亚苄基类似物178,氯化物176,氟化物177活性依次减弱;181(异叔丁基取代)比180(甲基取代)活性更强,烷基硫代亚苄基类似物活性强于烷氧基对应物,说明增加苄基取代基的疏水性可以增强抗增殖活性;衍生物182、183、184、185活性依次增强,表明增加烷氧基侧链的长度可以提高抗增殖活性。衍生物192能够显著抑制裸鼠乳腺癌模型中肿瘤的生长,是潜在的先导mTOR抑制剂。
A类衍生物69对小鼠淋巴细胞白血病L1210、中国仓鼠卵巢CHO、鼠Lewis肺癌3LL、人前列腺癌脑转移瘤DU145、人乳腺腺癌MCF7、人类慢性粒细胞性白血病K-562、人类慢性粒细胞性白血病K-562与人胶质母细胞瘤U251的活性(IC50为3~14 μM)均强于松萝酸(IC50为19.5~105.4 μM),65、71、82对上述8种癌细胞也具有较好活性(IC50为4.4~15.3 μM)[46]。与69相比,71的活性较低,表明了长亲脂性烷基链的重要性,疏水链可以促进穿过细胞膜;对小鼠淋巴细胞白血病L1210来说,86与链长相等的69相比,活性显著降低(IC50> 500 μM),表明了烷基链末端存在伯氨基的重要性。证明了松萝酸对癌细胞系的细胞毒活性可以通过与多胺链的缀合来改善,二氨基辛烷链是改善松萝酸细胞毒性的良好载体,可作为抗癌前提药物进一步开发。
总结上述研究发现,无论是呋喃酮衍生物还是烯胺衍生物,取代基中含有3,5-二叔丁基-4-羟基苯基时,活性显著增强;噻唑衍生物、呋喃酮衍生物、烯胺衍生物中溴取代均会增强活性;整体来看,肼基噻唑衍生物对Tdp1活性最好,呋喃酮衍生物次之,烯胺衍生物较差。松萝酸亚苄基衍生物中,亚苄基和二苯并呋喃部分对mTOR有重要作用;增加苄基取代基的疏水性与烷氧基侧链的长度可以增强抗增殖活性。烯胺反应引入长亲脂性末端存在伯氨基的烷基链,抗癌活性明显增强。
2.4 松萝酸衍生物其他活性的研究
此外,还有文献研究表明,松萝酸衍生物63、84和83在抗疟疾方面活性明显增强[31,59]。改变结构以增加水溶性进而改善衍生物的抗寄生虫作用,这为开发新的抗疟疾药物提供了研究思路。化合物9和7具有低细胞毒性和高伤口愈合性能[20],可能与溶解度的增加有关。松萝酸部分衍生物还有PARP1抑制[19]与抗炎[60]等作用。
3 总结与展望
松萝酸是来源于地衣中的一种天然产物,具有抗菌、抗病毒、抗肿瘤等生物活性,研究人员希望将其开发为一种药物。目前,已报道的松萝酸的结构修饰主要有上述8类,大部分衍生物的改造是在松萝酸的2位或6位乙酰基以及羟基上。其中,烯胺衍生物结构最为丰富。在活性方面,抗菌活性研究主要涉及烯胺衍生物;抗病毒活性涉及多类型的衍生物,但是化合物数量较少,可进一步研究多数量的不同衍生物类型,更加准确的总结其抗病毒规律,以发现更有效的抗病毒药物;在抗肿瘤方面,主要研究有呋喃酮衍生物、噻唑衍生物和烯胺衍生物对Tdp1的抑制作用,其中肼基噻唑衍生物活性最好;还有亚苄基衍生物对mTOR失调的人类乳腺癌细胞系作用的研究。现对松萝酸衍生物的主要构效关系总结如图15所示。

图15 松萝酸衍生物的构效关系
这些研究结果为松萝酸的结构修饰积累了一定的经验,在今后的开发中可以摒弃一些活性差的基团或修饰方案,朝着活性好的方面去开发此类化合物。进一步研究其作用机制,以及结合计算机辅助药物设计等手段去更好的开发松萝酸衍生物类药物。

