稀酸预处理玉米芯提取木糖的研究
傅丹宁 唐艳军 李 勉
(1.浙江理工大学材纺学院制浆造纸研究所,浙江杭州,310018;2.浙江华康药业股份有限公司,浙江衢州,324302)
木糖是重要的食品添加剂和甜味剂,因其独特的化学性质和生理功能,可用作糖尿病、肥胖病等疾病患者的良好食疗添加剂;此外,木糖还被广泛应用于肉食加工、肉料香料以及制备食品抗氧剂等领域[1-2]。随着我国经济的发展,人们的生活质量水平已经从温饱型走向营养型和保健型,木糖日益广泛地渗透于人们的生活中,预计在未来几年,食品级木糖的需求量将会持续快速增长。木糖除了本身具有较高的应用价值外,还可用其制取其他高附加值的化学产品,木糖的高值化利用途径如图1所示。如木糖加氢还原可获得木糖醇[3-4],它是一种健康的甜味剂;木糖进一步降解生成的产物糠醛是一种重要的化工原料,其应用也十分广泛[5-6];此外,木糖通过发酵可制得可再生清洁燃料——乙醇[7],它对于缓解当今世界面临的能源、环境问题具有十分重要的现实意义。因此,寻求一种环保高效、便于工业化生产且低污染的木糖制备方法意义重大。
木质纤维是地球上最丰富的生物质资源,其主要由纤维素、半纤维素和木质素构成;对于木质纤维中各组分的利用具有经济、环保和可再生等优点[8]。据报道,我国的玉米年产量位居世界第二,玉米芯则是玉米在加工过程中产生的大量废弃物料之一。研究发现,玉米芯是一种开发利用潜力巨大的生物质资源[9]。玉米芯中的半纤维素含量较高,是聚木糖含量最为丰富的农副产品;玉米芯中一般含有30%~40%的多缩戊糖,多缩戊糖经水解作用可制得木糖。因而,玉米芯被视为提取木糖的优良原料[10]。半纤维素水解制备木糖的过程如图2所示。
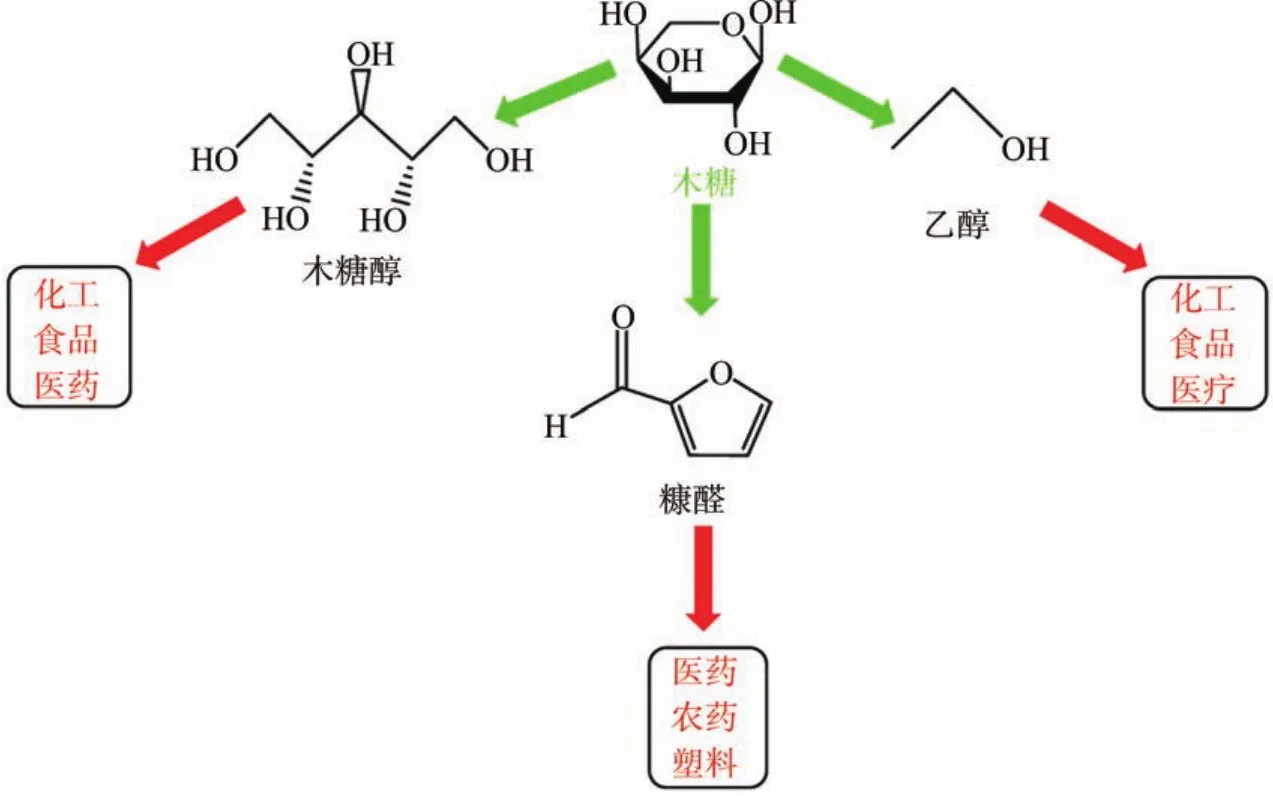
图1 木糖高值化利用途径
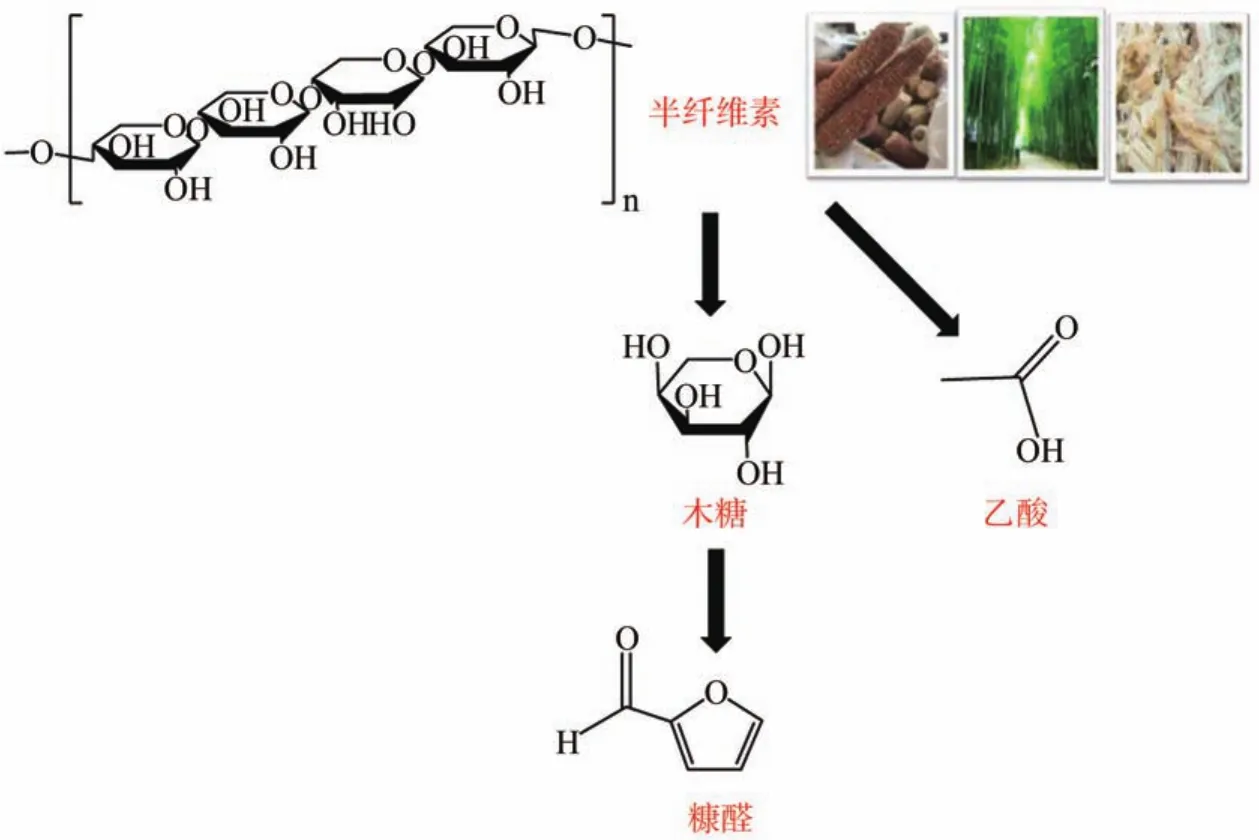
图2 半纤维素水解制备木糖过程
大量的实验研究[11]表明,利用不同的提取方法从玉米芯中提取木糖切实可行,且提取率较高。当前化学法预处理玉米芯制备木糖的途径主要包括酸处理法[12]、碱处理法[13-15]、氧化预处理法[16]、离子液体预处理法[5]以及有机溶剂预处理法[17-18]等,其中酸处理法由于具有水解效果好,稀酸一定程度上不会水解或破坏生物质原料中的纤维素和木质素等优点,因而被广泛应用于工业化木糖的制备。目前对于酸处理法制备木糖的工艺研究重点主要集中在酸水解条件的优化上,如章磊等人[19]以油茶壳为原料,采用正交实验法探究了稀硫酸浓度、水解温度以及水解时间对酸解效率的影响,结果表明,在酸浓度1.0%、催化温度80°C,保温时间2 h的条件下,木糖得率高达98%以上。许国辉等人[20]利用玉米芯为原料,采用酸解法研究确定玉米芯制备木糖的最佳工艺条件,结果显示,在酸解温度为120°C,酸浓度为1.0%,固液比为1∶10,酸水解2 h后,木糖最终得率达到80%左右。
基于前期研究结果[20-23],本实验以玉米芯为原料,通过优化稀硫酸预处理提取木糖的工艺参数,欲在较低成本、低污染的条件下获得更高得率、高浓度的木糖产品,为有效提取和利用木糖提供可靠的实验数据,并为进一步地综合利用玉米芯提供理论参考。
1 实 验
1.1 材料与试剂
超纯水,实验室自制;硫酸,购自浙江三鹰化学试剂有限公司;木糖、葡萄糖、阿拉伯糖、乙酸,购自Sigma-Aldrich上海斯信生物科技有限公司。
1.2 仪器与设备
JA1003N型电子分析天平,上海精密科学仪器有限公司;101A型数显电热鼓风干燥箱,上海一恒科学仪器有限公司;9FZ-35型电动直联多功能粉碎机,泰安市岱岳区泰峰农牧机械厂;304型皇代高速多功能粉碎机,永康市铂欧五金制品有限公司;分子筛(35目、80目),浙江上虞市道墟仪器筛具厂;XW-80A型旋涡混合器Vortex,上海驰唐电子有限公司;SHZ-III型循环水真空泵,上海亚荣生化仪器厂;LDZF-30KB型立式压力蒸汽灭菌器,上海申安医疗器械厂;1260 Infinity II型高效液相色谱仪,美国安捷伦科技公司。
1.3 实验方法
1.3.1 主要实验步骤
采用单因素实验法优化稀硫酸预处理玉米芯提取木糖的工艺参数:固液比(A)、酸浓度(B)、处理温度(C)和处理时间(D)。以2.00 g(绝干质量)35~80目粒径大小的玉米芯为原料,以一定浓度的稀硫酸为催化剂,在立式压力蒸汽灭菌器中保温一定时间,获得玉米芯稀硫酸水解液;自然冷却后进行真空抽滤,分离得到玉米芯酸水解滤液和玉米芯纤维滤渣,分别对玉米芯酸水解液中的单糖、乙酸浓度及玉米芯滤渣中的组分含量进行测定,以分析稀硫酸预处理玉米芯过程中各工艺参数对木糖提取效果的影响。稀硫酸预处理玉米芯的主要工艺流程如图3所示。
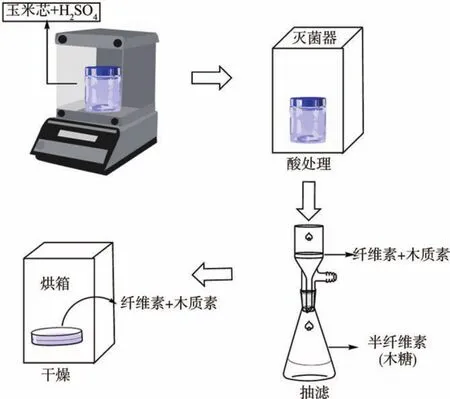
图3 稀硫酸预处理玉米芯工艺流程图
1.3.2 具体实验方法
(1)玉米芯原料组分分析
玉米芯原料中纤维素、半纤维素、木质素等的组分分析参照文献[24]进行。
(2)各样品标准曲线绘制
分别称取0.02、0.2、0.4、0.6、0.8 g的木糖/阿拉伯糖标准样品置于烧杯中加超纯水溶解,转移至洗净并干燥的20 mL容量瓶中,加水定容至刻度,静置待测。
分别称取0.02、0.1、0.2、0.3、0.4 g的葡萄糖标准样品置于烧杯中加超纯水溶解,转移至洗净并干燥的20 mL容量瓶中,加水定容至刻度,静置待测。
分 别 称 取 0.0002、 0.0008、 0.002、 0.004、0.008、0.01、0.02 g的乙酸标准样品置于烧杯中加超纯水溶解,转移至洗净并干燥的20 mL容量瓶中,加水定容至刻度,静置待测。
将上述4种标准样品用0.22 μm微孔滤膜过滤后,依次装入2.5 mL棕色试剂瓶中,利用高效液相色谱仪(HPLC检测参数:HPX-87H型色谱柱,示差检测器,流动相为5 mmol/L稀硫酸溶液,样品进样量为20 μL)进行检测,并将得到的色谱图进行处理,以标准溶液浓度(g/L)为横坐标,峰面积为纵坐标,分别绘制出木糖、葡萄糖、阿拉伯糖和乙酸的标准曲线图。
(3)稀硫酸预处理玉米芯工艺
首先将玉米芯用粉碎机粉碎,然后利用分子筛筛选得到35~80目粒径大小的玉米芯颗粒,于105°C下干燥3 h后取出,放入棕色细口玻璃瓶中密封保存。
用电子天平称取2.00 g(绝干质量)玉米芯置于蓝盖水解瓶中,加入一定质量的超纯水(将固液比控制在一定范围内)和一定浓度的稀硫酸溶液,再将该水解瓶置于旋涡混合器上进行料液的快速均匀混合,然后转移至立式压力蒸汽灭菌器中保温一段时间后取出冷却。最后,将酸水解液进行真空抽滤,收集滤液于具塞三角烧瓶中,并在4°C下冷藏备用;收集滤渣于称量瓶中,在105°C温度下进行干燥,取出冷却后用密封袋保存备用。
(4)水解滤液中成分分析与木糖得率的计算
将玉米芯水解滤液稀释至一定倍数,再利用高效液相色谱仪(HPLC)进行检测分析,将检测结果与各标准曲线对比以获得滤液中各单糖以及副产物的浓度。
木糖得率计算公式如式(1)所示。

式中,Y为玉米芯水解成木糖的得率,%;c为水解滤液中的木糖浓度,g/L;V为水解滤液的体积,L;m为玉米芯原料的绝干质量,g;0.88为理论上半纤维素完全水解成木糖的转化系数。
(5)水解滤渣中组分分析
玉米芯水解滤渣中纤维素、半纤维素、木质素等的组分分析参照文献[24]进行。
1.3.3 稀硫酸预处理单因素实验设计
以固液比(A)、酸浓度(B)、处理温度(C)和处理时间(D)为影响因素,设计单因素实验如表1所示。
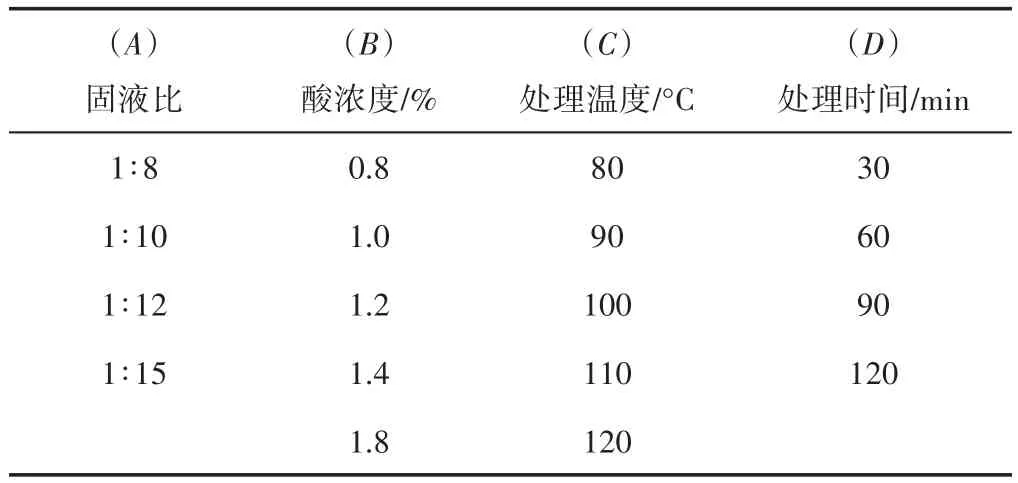
表1 单因素实验设计
1.3.4 稀硫酸预处理正交实验设计
在单因素实验的基础上,以酸浓度(B)、处理温度(C)和处理时间(D)为影响因素,以酸处理后玉米芯滤液中的木糖得率为指标,设计正交实验如表2所示。
2 结果与讨论
2.1 各样品的标准曲线
各标样的高效液相色谱图如图4所示。由图4可知,葡萄糖、木糖、阿拉伯糖和乙酸的保留时间依次约为8.076、8.646、9.399和13.661 min。
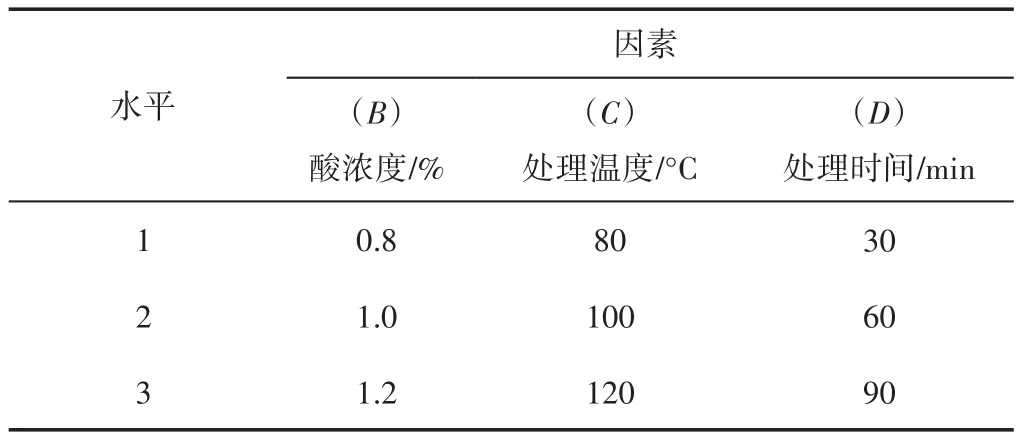
表2 正交实验因素与水平

表3 各样品的标准曲线方程
木糖、葡萄糖、阿拉伯糖、乙酸标准曲线的绘制如图5所示,标准曲线方程汇总见表3。
由图5和表3可知,木糖和阿拉伯糖浓度在0~40 g/L内线性关系良好,葡萄糖浓度在0~20 g/L内线性关系很好,乙酸浓度在0~1 g/L内线性关系很好。
2.2 单因素实验结果
2.2.1 固液比对玉米芯预处理效果的影响
设定酸浓度为1.0%,处理温度120°C,处理时间60 min,探究固液比对稀硫酸预处理玉米芯的影响,结果如图6所示。
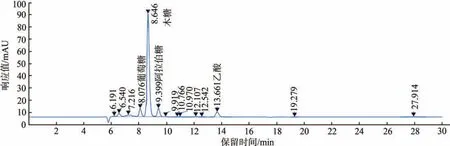
图4 各标样的液相色谱图
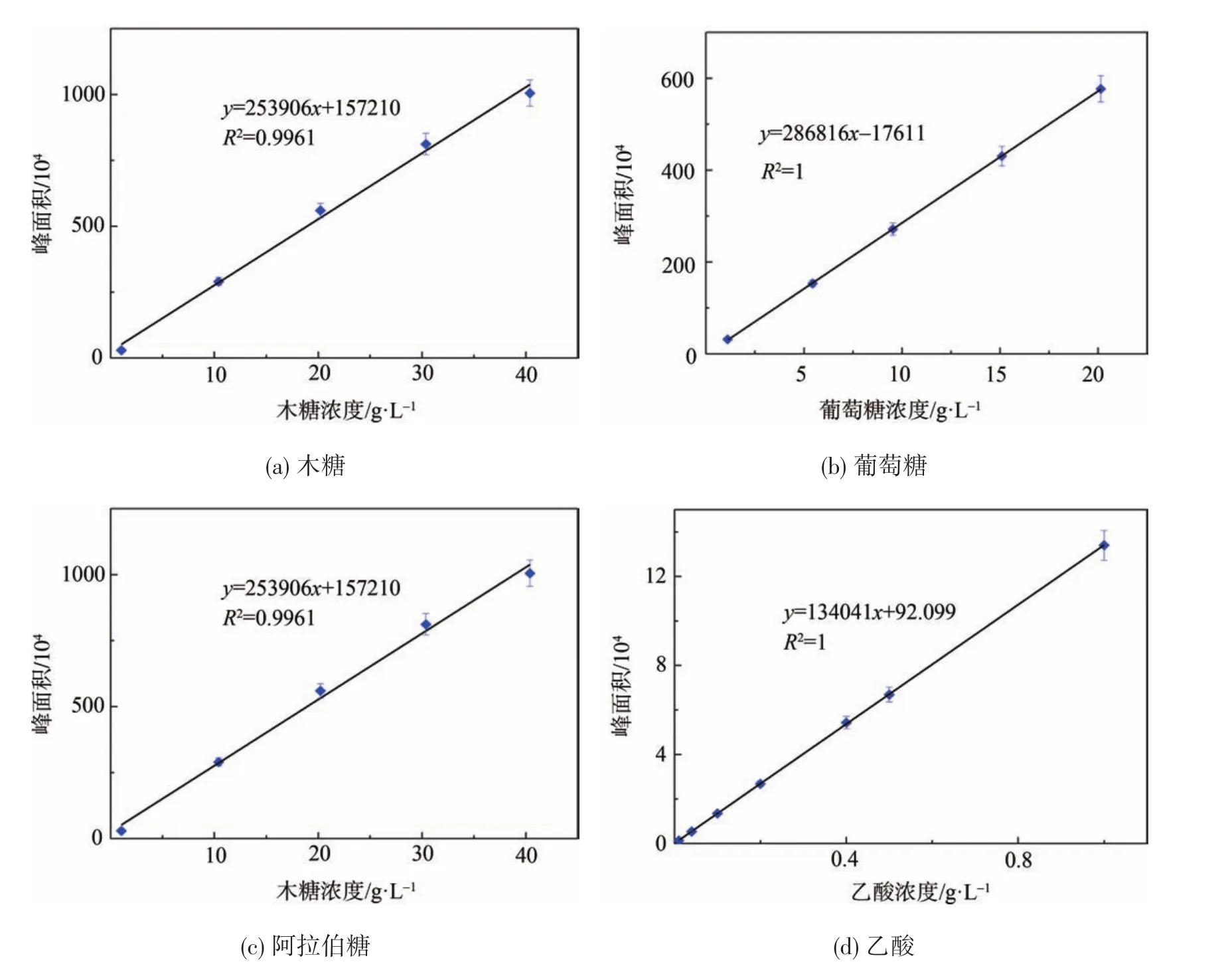
图5 各样品的标准曲线图
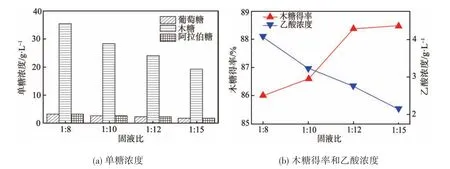
图6 固液比对稀硫酸预处理玉米芯的影响
由图6可知,随着玉米芯水解过程中固液比的逐渐增大,即水解液越来越稀,水解后液体中各单糖的浓度(玉米芯中半纤维素水解得到的单体主要是木糖、葡萄糖和阿拉伯糖等单糖)和酸水解副产物——乙酸(由半纤维素脱乙酰基而得)的浓度越来越低,一定浓度的乙酸可促使半纤维素中糖基之间的糖苷键断裂,从而加速玉米芯的水解[25];然而,玉米芯水解得到的木糖得率却呈现相反的趋势,其随固液比的增大出现上升的现象。过低的固液比可能无法将玉米芯原料中的木糖完全浸提出来,导致木糖得率降低;过高的固液比会造成水资源浪费,且由于产物浓度的降低易加大后续蒸发浓缩等过程的能耗和难度。因此,为制得高浓度、高得率的木糖水解液,同时降低后续酶解过程前脱毒等工艺的难度,可综合选择适宜的固液比为1∶10。且由图6(b)可知,固液比因素实验的选择范围较广,但随着固液比的增加,木糖得率的变化区间仅为2.5%左右,这表明固液比对实验结果影响较小,故在正交实验中不做体现。
由该实验结果可知,水解时间设定为60 min时,木糖得率最高可达88%以上,即半纤维素几乎完全水解;因此,为了同时达到提高实验效率与节约成本的目的,将后续实验过程中的水解时间均设定为60 min。
2.2.2 酸浓度对玉米芯预处理效果的影响
设定酸处理的固液比为1∶10,处理温度120°C,处理时间60 min,探究酸浓度对稀硫酸预处理玉米芯的影响,结果如图7所示。
由图7(a)可知,随着玉米芯水解过程中所添加稀硫酸浓度的逐渐上升,水解液中各单糖的浓度呈现先缓慢上升,随后趋于平缓的趋势。由图7(b)可以发现,当酸浓度约为1.0%时,木糖得率已处于较高值(约为87%)。由于酸浓度越高,其对设备的腐蚀性越大,且酸会进一步催化单糖降解和促进其他非半纤维素物质发生副反应,最终导致水解液中的副产物(主要为乙酸、糠醛、酚类等物质)浓度也升高[26-27],水解后的木糖液颜色加深,这不利于后续木糖的分离纯化,一定程度上降低了木糖最终得率,因此稀硫酸预处理过程的适宜酸浓度可初步定为1.0%。
2.2.3 处理温度对玉米芯预处理效果的影响
设定酸处理的固液比为1∶10,酸浓度1.0%,处理时间60 min,探究处理温度对稀硫酸预处理玉米芯的影响,结果如图8所示。
由图8可知,随着玉米芯水解过程中处理温度的缓慢升高,玉米芯水解液中各单糖浓度以及木糖得率增加得越来越快,且当处理温度由100°C升至120°C时,水解液的木糖得率上升了60个百分点(从27%升至87%),因此可以得出,处理温度是影响酸水解工艺的关键因素,温度控制在水解玉米芯制备木糖的工艺中极其重要。然而,处理温度的上升代表能耗的增加,且由图8(b)可知,副产物乙酸浓度也随处理温度的上升而迅速增加;此外,高温条件也可能会导致部分戊糖转化为糠醛从而降低木糖得率[28-29]。综合各方面因素,最终将酸处理的适宜温度确定为120°C。
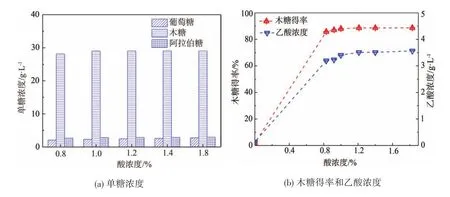
图7 酸浓度对稀硫酸预处理玉米芯的影响
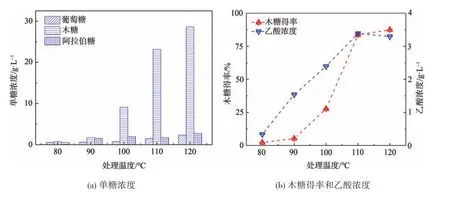
图8 处理温度对稀硫酸预处理玉米芯的影响
2.2.4 处理时间对玉米芯预处理效果的影响
设定酸处理的固液比为1∶10、酸浓度1.0%、处理温度120°C,探究处理时间对稀硫酸预处理玉米芯的影响,结果如图9所示。
由图9可知,酸水解时间在30~60 min时,随着玉米芯水解时间的延长,玉米芯水解滤液中各单糖浓度以及木糖得率都略微增加,这表明水解反应在持续进行;在60~120 min时,随着反应时间的增加,各单糖浓度仍旧呈现上升的趋势,但副产物乙酸的浓度也一直上升,木糖得率开始出现下降的情况。该实验结果表明,反应时间过长会提高生成副产物的可能性,木糖极可能进一步降解成糠醛,因而木糖得率会出现略微下降的趋势。为了得到较高得率的木糖产品,同时降低副反应发生的可能性,可将酸处理的适宜时间确定为60 min。
2.3 玉米芯组分分析
玉米芯稀硫酸处理前后主要组分含量变化情况如表4所示。
对酸解后的玉米芯滤渣进行组分分析,酸解条件为:固液比1∶10,酸浓度1.0%,处理温度120°C,处理时间60 min。与玉米芯相比,酸处理大大降低了玉米芯半纤维素含量,这表明玉米芯中的大部分半纤维素被利用生成木糖。酸处理在一定程度上还降低了木质素和灰分含量,其原因可能是酸解破坏了木质素结构单元之间的醚键和碳-碳键,生成了醛类和羧酸类物质,使木质素含量出现一定程度的降低,纤维素更多地裸露出来,这对于后续玉米芯滤渣的综合利用具有重要意义[30-32]。
2.4 正交实验结果
正交实验结果与极差分析如表5所示。
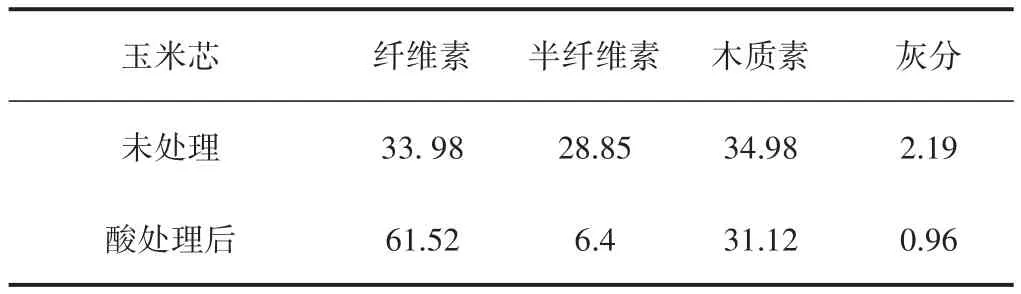
表4 稀硫酸预处理前后玉米芯中组分含量 %
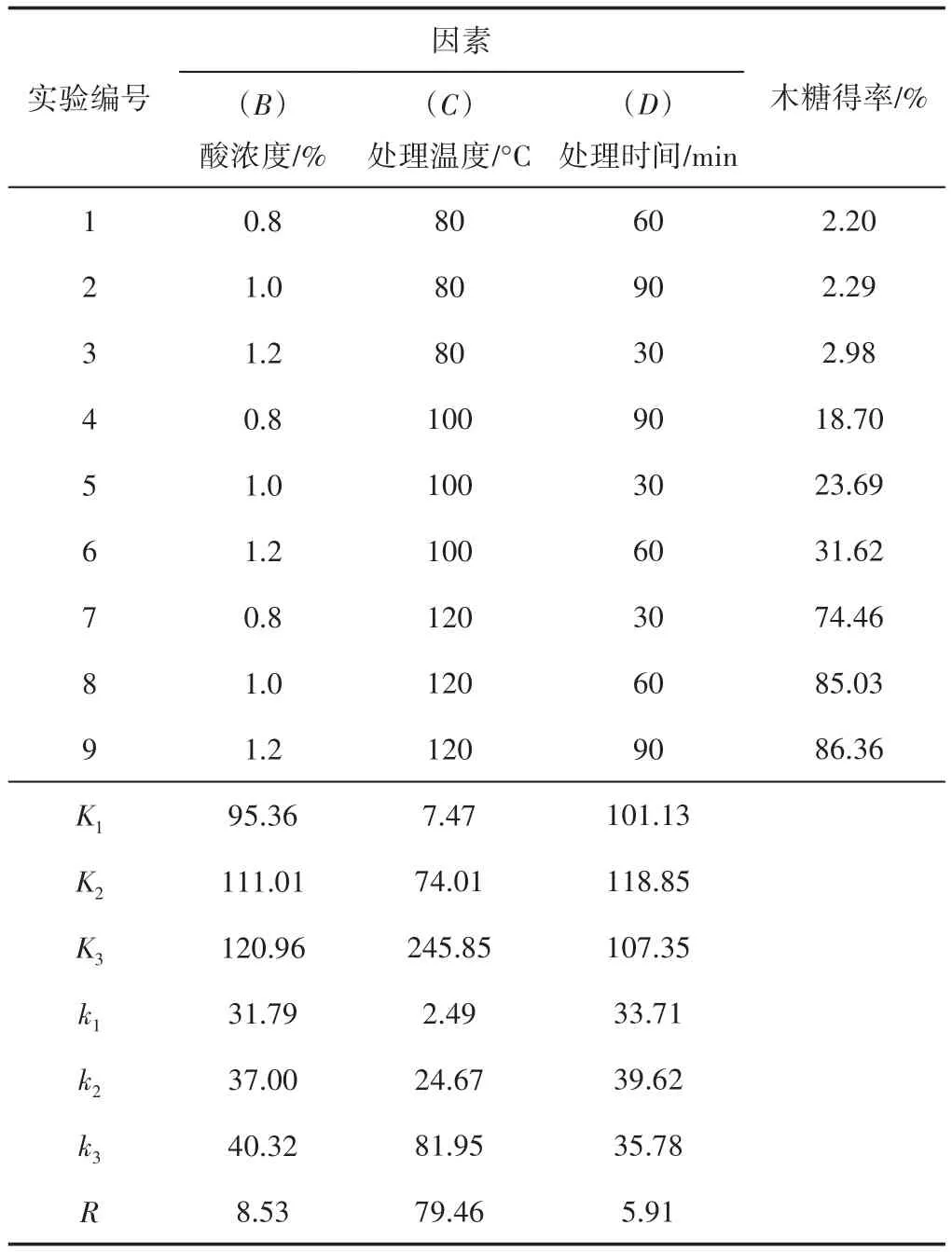
表5 正交实验结果与极差分析
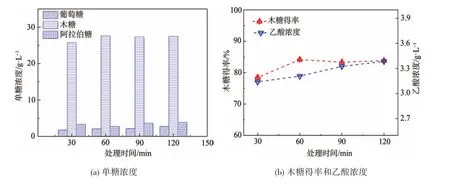
图9 处理时间对稀硫酸预处理玉米芯的影响
在表5中,极差R值的大小表示各因素对稀硫酸预处理玉米芯效果的影响程度,酸浓度极差值为8.53,处理温度极差值为79.46,处理时间极差值为5.91,即影响酸解玉米芯制取木糖得率的主次因素为:处理温度>酸浓度>处理时间。直接比较表5可知,9个实验结果中,以实验9中的木糖得率最高,按因素列来看,其水平组合为B3C3D3,分别是各因素中影响最大的水平,即理论上最佳稀硫酸预处理条件为B3C3D3,具体值为:酸浓度1.2%,处理温度120°C,处理时间90 min。在该最佳预处理条件下进行3组验证实验,得到的木糖得率分别为86.31%、86.36%和86.28%,相对偏差分别为0.01%、0和0.05%,标准差为0.03,即验证结果显示出较高的木糖得率和数据可靠性。
3 结论
通过单因素实验和正交实验,得到稀硫酸预处理玉米芯制备木糖的较优工艺条件为:固液比1∶10、酸浓度1.2%、处理温度120°C和处理时间90 min,此条件下玉米芯制备木糖的得率高达86.36%。稀酸预处理玉米芯制备木糖过程中,处理温度对预处理效果影响最为显著,而处理时间的影响最小,稀酸预处理过程各因素对玉米芯木糖提取率影响程度由大到小的顺序为:处理温度>酸浓度>处理时间。

