大肠杆菌O157:H7能力验证的结果与分析
刘秋婷 苏妙贞 陈丹霞 苏嘉妮 周 露
(广东省食品检验所 广东广州 510435)
1 前言
大肠杆菌O157:H7(简称O157:H7)是有周鞭毛且不产生芽孢的革兰氏阴性杆菌。1982年,O157:H7型肠出血性大肠杆菌食物中毒事件首次在美国发生,随后该菌引起的食物安全问题相继在德国、美国、加拿大、日本、中国等地区出现,受到全球民众的广泛关注[1-3]。人类食用O157:H7污染的食物后,最常见的症状是腹泻,严重者会引起出血性肠炎、血小板减少性紫癜、溶血性贫血等致死率高的食源性疾病[4,5]。 O157:H7在低温、强酸环境下容易存活,主要存在于牛肉、羊肉、猪肉、乳制品等食品中,可通过人与人接触和饮水进行传播。因此,我国将其列为21世纪可能对中国人群公共卫生健康有重大影响的12种病原微生物之一[6,7]。GB 4789.36—2016《食品安全国家标准 食品微生物学检验大肠埃希氏菌O157:H7/NM检验》[8]规定各种食品中不得检出O157:H7。
为了加强食源性致病菌的检测能力,提高实验室对O157:H7的检验鉴定水平,广东省食品检验所实验室在2019年11月参加了英国食品分析实验室质量评估体系(FAPAS)组织的能力验证活动,验证从牛肉中分离鉴定O157:H7的能力,为O157:H7的检测提供参考。
2 材料与方法
2.1 材料
2.1.1 样品
英国 FAPAS组织方提供了2份样品,样品编号为M247d11A和M247d11B。
2.1.2 培养基和试剂
缓冲蛋白胨水(BPW);改良 EC肉汤(mEC+n);改良山梨醇麦康凯琼脂(CT-SMAC);月桂基硫酸盐胰蛋白胨肉汤-MUG(MUG-LST);三糖铁琼脂(TSI);营养琼脂;氧化酶试剂;革兰氏染色液;大肠埃希菌O157:H7生化鉴定盒(广东环凯微生物科技有限公司);大肠杆菌O157免疫磁珠分离检测试剂盒(天津生物芯片技术有限公司);CHRMAGAR O157显色培养基(法国科玛嘉公司);革兰阴性细菌鉴定卡(GN卡);VIDAS UP E.coli O157:H7试剂盒(法国梅里埃生物有限公司);大肠埃希菌断血清 O157;大肠埃希菌诊断血清H7(宁波天润生物药业有限公司)。
2.1.3 标准菌株
大肠埃希菌 O157:H7(NCTC12900);大肠埃希菌(ATCC25922)。
2.2 仪器
磁力架-样品混合器(Dynal)均质器(IUL);生物安全柜(赛默飞世尔公司);生化培养箱(上海一恒科学仪器有限公司);显微镜(卡尔蔡司);暗箱式四用紫外分析仪(上海嘉鹏科技有限公司);VITEK 2compact全自动微生物快速检测分析系统 (法国梅里埃公司);VIDAS 30全自动酶联免疫分析仪(法国梅里埃公司)。
2.3 方法
参照英国FAPAS实验室提供的O157:H7的作业指导书进行前处理和GB 4789.36—2016第二法免疫磁珠捕获法进行O157分离鉴定和生化血清鉴定,并借助VIDAS 30全自动酶联免疫分析系统进行初步快速筛选,同时以VITEK 2 compact全自动微生物快速检测分析系统进行生化鉴定,确保检验结果的准确性。
2.3.1 样品处理
实验开始前先对待测样品进行水化,在生物安全柜开启样品瓶盖,样品M247d11A和M247d11B中各添加20 mL BPW进行水化并轻轻翻转样品瓶几次以充分混匀,将样品在室温下放置28~30 min,即可测试。
2.3.2 增菌
以无菌操作将2份样品分别加入225 mL改良EC肉汤中,用均质器连续拍打1~2 min,在36℃条件下培养24 h。同时取阳性对照菌NCTC12900大肠埃希菌O157:H7和阴性对照菌ATCC25922大肠埃希菌于225 mL改良EC肉汤中,在36℃条件下培养24 h,后续同步进行选择性分离与生化鉴定实验。
2.3.3 免疫磁珠捕获与分离
将1.5 mL灭菌离心管按样品和质控菌株进行编号,在管中加入20 μL免疫磁珠,然后加入1 mL样品增菌液,振荡混匀后将离心管夹在混合器上,以12 r/min转速旋转混合10 min。取下离心管,放在磁力架的孔中,静置3 min,磁珠被吸附在管壁上形成棕色聚集物,轻轻吸走管中上清液。加入1 mL洗脱缓冲液重悬磁珠,将离心管颠倒混合5~8次,再置于磁力架中,静置3 min,吸走多余液体。重复洗涤一次,最后加入50 μL洗脱缓冲液重悬磁珠。各吸取25 μL免疫磁珠悬液至CT-SMAC平板和改良O157显色琼脂平板一侧,然后用无菌涂布棒将免疫磁珠涂布平板的一半,再用接种环划线接种平板的另一半。待琼脂表面水分完全吸收后,翻转平板,在36℃±1℃条件下培养24 h,观察2种平板上的菌落特征。
2.3.4 VIDAS 30全自动酶联免疫分析系统检测
依据VIDAS UP E.coli O157:H7试剂盒说明书,取1 mL增菌后的改良EC肉汤,在100℃水浴中煮沸10 min。冷却至室温后,取0.5 mL增菌液至VIDAS大肠埃希菌O157试剂条的样品孔中,按仪器操作规程进行检测。
2.3.5 生化实验
挑取2.3.3得到的大肠埃希菌O157:H7可疑菌落接种于营养琼脂平板上进行纯化,36℃培养24 h,进行生化鉴定和VITEK 2 Compact鉴定实验。
2.3.6 血清学实验
对符合生化鉴定和VITEK 2 Compact鉴定结果的菌株进行血清学鉴定。采用玻片凝集试验,在洁净玻片上2个不同区域各滴1滴O157血清和H7血清,在另一干净玻片加入1滴生理盐水做对照,用接种环挑取菌落分别与血清和生理盐水研磨混匀,轻轻摇动玻片1min,对照黑背景观察有无凝集现象。1min内呈明显凝集者为阳性,呈均匀浑浊者为阴性。
3 结果与分析
3.1 免疫磁珠捕获与分离结果
样品M247d11A、M247d11B、阳性对照大肠埃希菌O157:H7、阴性对照大肠埃希菌经过免疫磁珠富集和平板划线分离后,结果详见表1。
3.2 VIDAS 30全自动酶联免疫分析系统检测和VITEK鉴定结果
使用VIDAS UP E.coli O157:H7试剂盒检测后,样品M247d11A为O157:H7阳性,样品M247d11B为O157:H7阴性。VITEK检测结果显示,样品M247d11A检出O157:H7,样品M247d11B未检出,两者的鉴定结果一致,详见表2。

表1 免疫磁珠捕获与分离结果
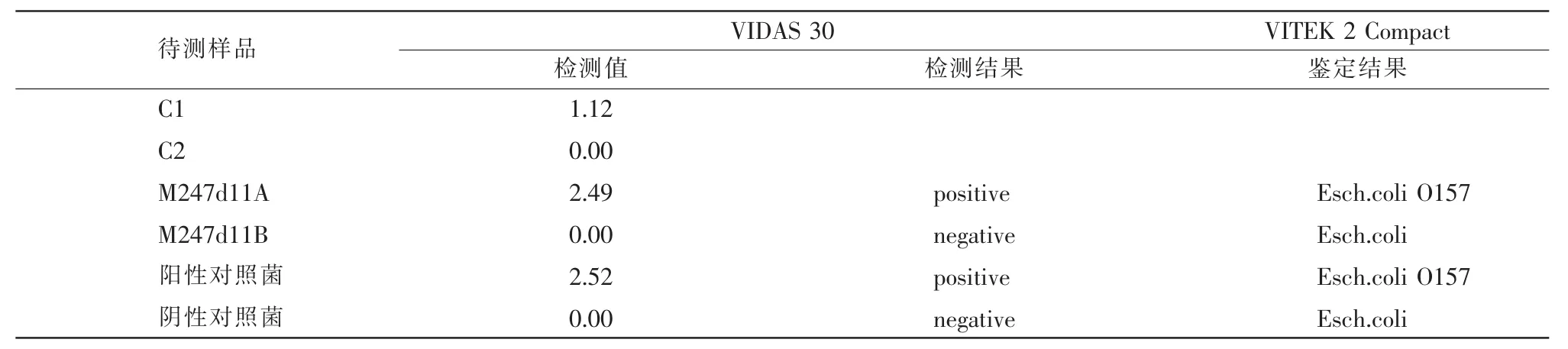
表2 VIDAS 30全自动酶联免疫分析系统检测和VITEK鉴定结果
3.3 生化鉴定结果
按照国家标准GB 4789.36—2016进行鉴定,可以判断M247d11A检出O157:H7,M247d11B未检出O157:H7,详见表 3。

表3 生化鉴定结果
3.4 血清学试验结果
将M247d11A和M247d11B上的可疑菌落进行纯化培养后,按照国家标准GB 4789.36—2016第二法中血清学试验要求用O157和H7诊断血清做玻片凝集试验,详见表4。

表4 血清学试验结果
4 结论
本次能力验证实验先用BPW肉汤进行水化,再加入改良EC肉汤进行前增菌,这样可以激活样品中目标菌的生物学特性[9],避免出现假阴性,对实验结果造成影响。由于O157:H7编码的β-葡萄糖醛酸酶无活性,不能分解4-甲基伞形酮-β-D-葡萄糖醛酸苷产生荧光,样品M247d11A观察到的MUGLST为无荧光现象,结果表现为阴性,这对区分各种大肠杆菌具有重要作用。O157在显色培养基上呈现淡紫色,而其他杆菌呈现无色或被抑制,其抗干扰能力和特异性均比较强,在24 h内即可观察菌落形态,减少产生假阳性菌的机率[10]。而在CT-SMAC平板中,由于O157:H7不发酵或迟缓发酵山梨醇,故在平板上为圆形,无色,中心呈现灰褐色的菌落。日常检验中可以根据O157:H7的这几个主要生物学特征,初步判定可疑菌,再结合后续生化实验,更好地作出判断。
免疫磁珠捕获法是利用磁珠表面的O157特异性抗体来捕获样品中的表面抗原,磁珠在磁场作用下,被吸附沉淀,与样品中的其他物质快速分离,从而达到分离O157:H7的目的[11]。实验增菌后,先利用免疫磁珠进行捕获,再结合选择性分离培养,这样可以减少样品残渣和其他大肠杆菌属等杂菌的干扰,从而达到在成分复杂的食品中富集到目标菌的目的[12]。该方法与常规检验方法相比,能准确、迅速地分离样品中的目标菌,但也存在影响检测结果的因素,如样品存在其他杂菌的污染、磁珠表面抗体的特异性、磁珠捕获时间长短等,而且其价格较高,不能被广泛运用到量大的检测工作中。
在2种快速鉴定方法中,VIDAS 30能快速筛选出待测增菌液中的目标菌,减少检测时间,提高效率,但也会有漏检的情况出现,所以得出阳性结果后还要做进一步的验证实验。VITEK 2 Compact能对分离出的可疑菌落进行比较准确的生化鉴定,但可疑菌落的选择和菌液的纯度对该方法有一定的影响。因此,在检测工作中,可在国标法的基础上将VIDAS 30和VITEK 2 Compact相结合,快速筛查出目标菌,再按传统细菌生化试验和血清学进行下一步验证,使结果更加准确可靠。免疫磁珠分离技术具有强特异性、高敏感性以及快速筛选等特点[13],目前,该方法可与PCR(多聚酶链式反应)技术[14]、胶体金免疫层析技术[15]、红外光谱技术[16]等各种高灵敏检测方法结合,对O157:H7进行分离鉴定,高效完成检测任务,提高食源性致病菌的检出率。
能力验证是利用实验室间的比对,按照预先制定的准则对参加者的能力进行评价,是一种有效的外部质量控制手段[17]。参加O157:H7国际性能力验证,不仅可以验证实验室自身的检验能力,也可以提升实验室在食源性致病菌方面的检测技术水平,对完善实验室管理体系文件起到积极作用。通过验证能够了解技术上的不足及存在的问题,采取正确的改进措施,更好地完成今后的检测工作。

