离子交换色谱法测定调制乳粉和固体饮料中低聚木糖
宋戈,刘长玲,张胜楠
(黑龙江省华测检测技术有限公司,哈尔滨150028)
0 引 言
低聚木糖是一类由2-9 个D-木糖分子分子以β-1, 4 木糖苷键连接而成的功能性低聚糖[1]。低聚木糖作为一种可溶性膳食纤维[2],具有很好的生理特性,可以调节肠道菌群,预防癌症,降低血压、血脂和血糖等生理学功效,是一种提高免疫力、促进身体健康的理想益生元[3]。除被应用于调理肠胃、缓解便秘的保健食品中外,低聚木糖作为一种效价比较高的双歧因子,现已成功地应用到调制乳粉、固体饮料等行业中,能高效准确地测定其中低聚木糖含量十分必要。目前常见的测定方法有通过直接测定木二糖至木七糖组分含量[1,4-6]的方法,但木四糖、木五糖木六糖标准品价格昂贵,木七糖和木八糖等高聚合度低聚木糖标准样品难以获取, 而且测定复杂基质的样品时,木二糖和木三糖会受到杂质干扰无法准确定量。也有经酸水解为木糖来间接测定[7-13]的方法和再进行衍生反应后测定的方法[14],但只适用于含量较高基质简单的保健食品,前处理不适用基质复杂的调制奶粉和固体饮料中低聚木糖的提取与测定。
本研究尝试复杂基质的调制乳粉和固体饮料样品中低聚木糖提取和水解的条件,采用优化的离子色谱分析条件直接测定样品水解前后木糖的含量,二者之差经换算后获得低聚木糖的含量,操作简便,结果可靠,干扰小,可为复杂基质的调制乳粉和固体饮料中低聚木糖含量的测定提供参考。
1 实 验
1.1 仪器与设备
ICS-5000 离子色谱仪配备脉冲安培检测器,thermo 公司;TTL-DCⅡ水浴加热仪,北京同泰联科技发展有限公司;pB-10 酸度计,德国Sartorius 公司;KQ-250DE 超声波振荡器,昆山市超声仪器有限公司;VORTEX3 涡旋混合器,德国 IKA 公司;SQP 天平,德国Sartorius公司。
1.2 材料与试剂
木糖(≥99%),德国 Dr.Ehretorfer 公司;50%氢氧化钠(色谱纯)、乙酸钠(色谱纯),SIGMA 公司;浓硫酸(分析纯)、氢氧化钠(分析纯),西陇公司;WatersOasis HLB 固相萃取柱 3cc/60mg,美国 Waters 公司;所有用水均为电阻率≥18.2 MΩ·cm 的超纯水;以上试剂除标注的外均为分析纯。
1.3 实验方法
1.3.1 标准溶液与淋洗液的配制
木糖标准储备液(500 mg/L):准确称取0.05 g(精确至0.1 mg)的木糖标准物质于50 mL 烧杯中,加入约10 mL 热水,溶解后冷却至室温,用水稀释至25 mL 容量瓶中,摇匀。
木糖标准工作溶液:取适量木糖标准储备液,用水配制成质量浓度为 1.0、5.0、10.0、25.0、50.0、100.0、1 000.0 mg/L的标准曲线工作溶液,现配现用。
淋洗液A 纯水:电阻率≥18.2 MΩ·cm 的超纯水。
淋洗液B 氢氧化钠溶液(200 mmol/L):取10.4 mL 50%氢氧化钠溶液,用水稀释至1 000 mL,通入氮气保护,缓慢摇匀。
淋洗液C乙酸钠(500 mmol/L)混合溶液:称取41 g无水乙酸钠(精确至0.01 g),用约500 mL 水溶解,0.22 μm 滤膜过滤,脱气10 min,加入7.8 mL50%氢氧化钠溶液,并用水稀释至1 000 mL,通入氮气保护,缓慢摇匀。
1.3.2 样品处理
称取调制乳粉或固体饮料约2.5 g 于50 mL 三角瓶中,加入20 mL (50±5 ℃)的水将试样振荡溶解并超声20 min,再用1.0 mol/L NaOH 溶液调节溶液pH 值到4.5,用水定容至50 mL 过滤,此为水解前供试品溶液,滤液依次通过0.22 μm 水相滤膜和活化过的HLB净化柱,弃去前面2 mL,收集后面溶液上机测定水解前木糖含量。准确移取5.0 mL 样品滤液于带螺纹盖的水解玻璃管中,加1.0 mL 4.0 mol/L 硫酸溶液混匀后于沸水浴水解100 min,取出,冷却,用水转移到三角瓶中,再用1.0 mol/L NaOH 溶液调节溶液pH 值到4.5,用水定容至50 mL 过滤,滤液依次通过0.22 μm水相滤膜和活化过的HLB 净化柱,弃去前面2 mL,收集后面溶液上机测定水解后木糖含量。
1.3.3 色谱条件
色谱柱:CarboPac PA10,250×4.6 mm;保护柱:CarboPac PA10,50×4 mm ;检测器参数:Au 电极,Ag-Cl参比模式,标准四电位波形;流速:1.0mL/min。
淋洗条件:0~20 min,20 mmol/LNaOH;20.1~30 min,100mmol/L NaOH 500 mmol/L NaAc ;30.1~40 min,200 mmol/L NaOH ;40.1~50 min,20 mmol/L NaOH 。进样方式:自动进样;进样体积:25 μL;柱温:30 ℃。木糖标准溶液的色谱见图1。
1.3.4 木糖与低聚木糖的换算
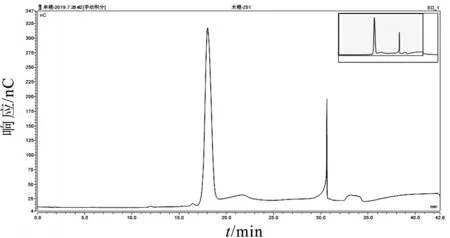
图1 木糖标准溶液色谱
在水解过程中,低聚木糖的β-1, 4-糖苷键会断裂并与水分子结合生成糖苷羟基,使得生成的木糖质量比水解前的低聚木糖质量高。水解后木糖与水解前的低聚木糖质量之比用平均转化系数表示,其数值因低聚木糖的聚合度而异,均值约为1.06(以木二糖计)[1]。因此,测定样品中水解前后木糖含量的差值除以1.06即为样品中低聚木糖的含量。
2 结果与讨论
2.1 水解条件的优化
低聚木糖由2~9 个木糖单元,以β-1, 4-糖苷键连接而成的低聚糖混合物[1],易溶于水。文献报道[7-14]均选取4 mol/L 硫酸在100 ℃的温度条件下水解条件,以尽可能地完全水解低聚木糖。调制乳粉和固体饮料不同于文献报道中的低聚木糖保健品和原料,成分较为复杂,为提高检测的准确性,对含70.0 mg/L 低聚木糖的调制乳粉样品溶液进行不同水解条件的测定。考察了在100 ℃的温度条件下, 加入1 mL 4 mol/L 硫酸溶液,反应时间对测定结果的影响见图2。
另外考察了在100 ℃的温度条件下, 反应时间为100 min,加入4 mol/L 硫酸溶液,加入的硫酸溶液体积对测定结果的影响见图3。最终确定为1.3.2 中的水解条件。
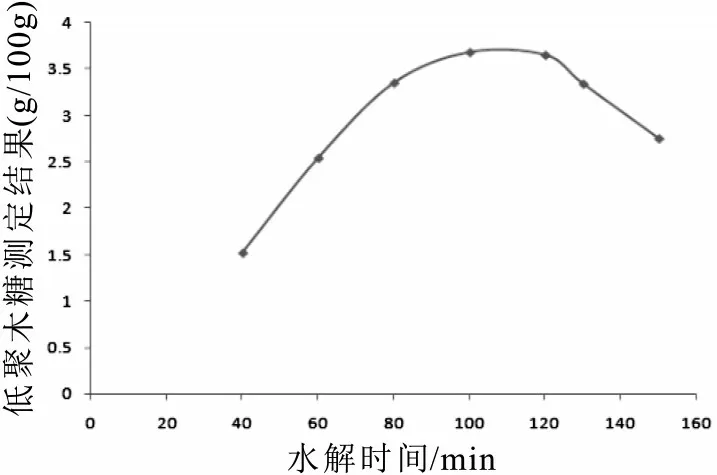
图2 样品水解时间对测定结果的影响
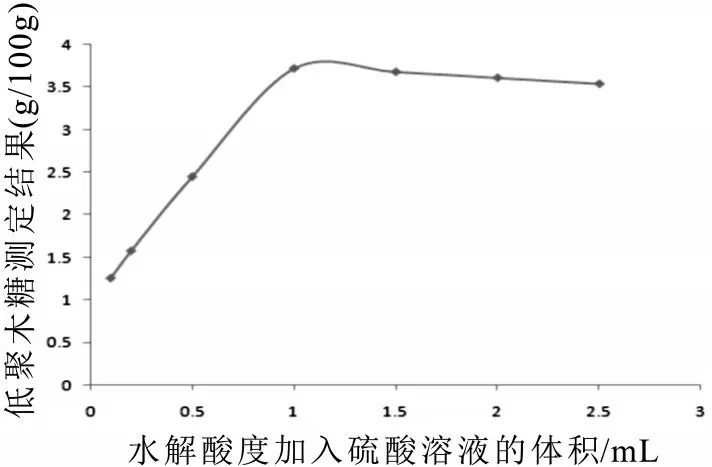
图3 样品水解酸度对测定结果的影响
2.2 色谱条件的确定
NaOH 溶液中所含有的OH-离子可以促进糖中羟基的酸性解离, 从而增强它们在阴离子交换色谱柱上的保留。各种糖在碱性条件下存在电离度的差异,可以通过调节洗脱液的组成及浓度实现分离。NaOH 作为常规洗脱液之一,在糖的分析中扮演着双重角色,既为糖的电离提供碱性环境,同时也是洗脱剂,因此改变NaOH 的浓度对于糖的保留时间有较大的影响。调制乳粉和固体饮料水解后会有大量的半乳糖、葡萄糖和其他单糖生成产生,当淋洗液中NaOH 溶液的浓度过大,测定低聚木糖水解生成的木糖就会受干扰。采用20 mmol/L NaOH 为淋洗液等度洗脱时, 样品中低聚木糖水解生成的木糖与样品中乳糖水解产生的半乳糖、葡萄糖和其他单糖能完全分离,但是对于强保留的杂质洗脱不下来。没能洗脱下来的杂质会对下一个样品的测定产生影响,导致保留时间的不稳定和测定结果的重复性差,必须采用具有更强淋洗能力的醋酸钠溶液进行洗脱[15-16]。NaAc 相对于NaOH 具有更强的洗脱力,采用1.3.3 的色谱条件,样品中低聚木糖测定结果的稳定性和准确性较好。样品水解前与水解后测定色谱见图4和图5。
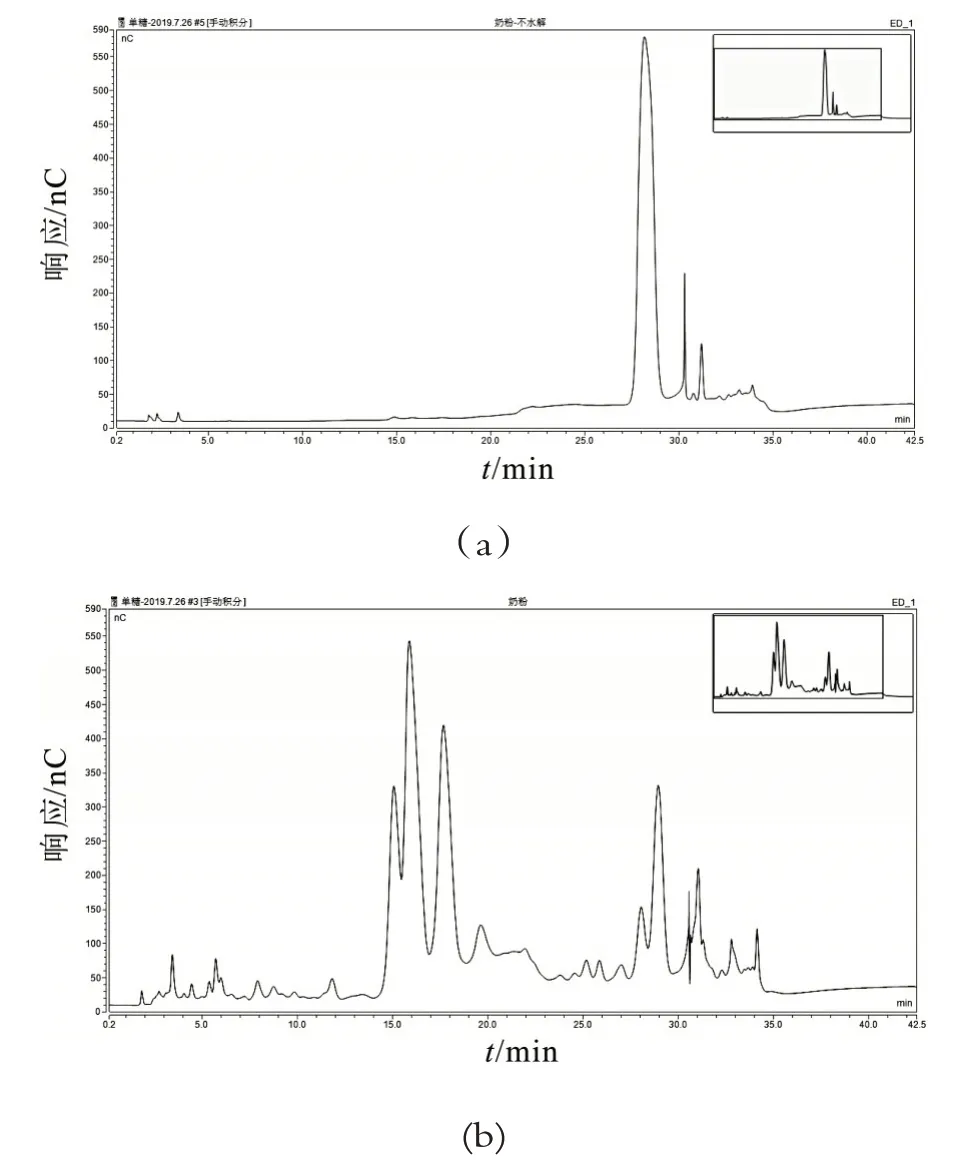
图4 调制乳粉水解前(a)与水解后(b)测定色谱
2.3 标准曲线和检出限
取不同浓度1.0 mg/L、5.0 mg/L、10.0 mg/L、25.0 mg/L、50.0 mg/L、100.0 mg/L、1 000.0 mg/L 的木糖标准工作溶液,注入离子色谱仪,记录目标峰峰面积。以峰面积与标准溶液浓度绘制线性回归曲线,其线性关系为:y=13.717x-1.311,相关系数R2=0.9993,线性范围1.0~1 000 mg/L,并以3 倍信噪比计算出固体样品称取2.5克的检出限为200 mg/kg。
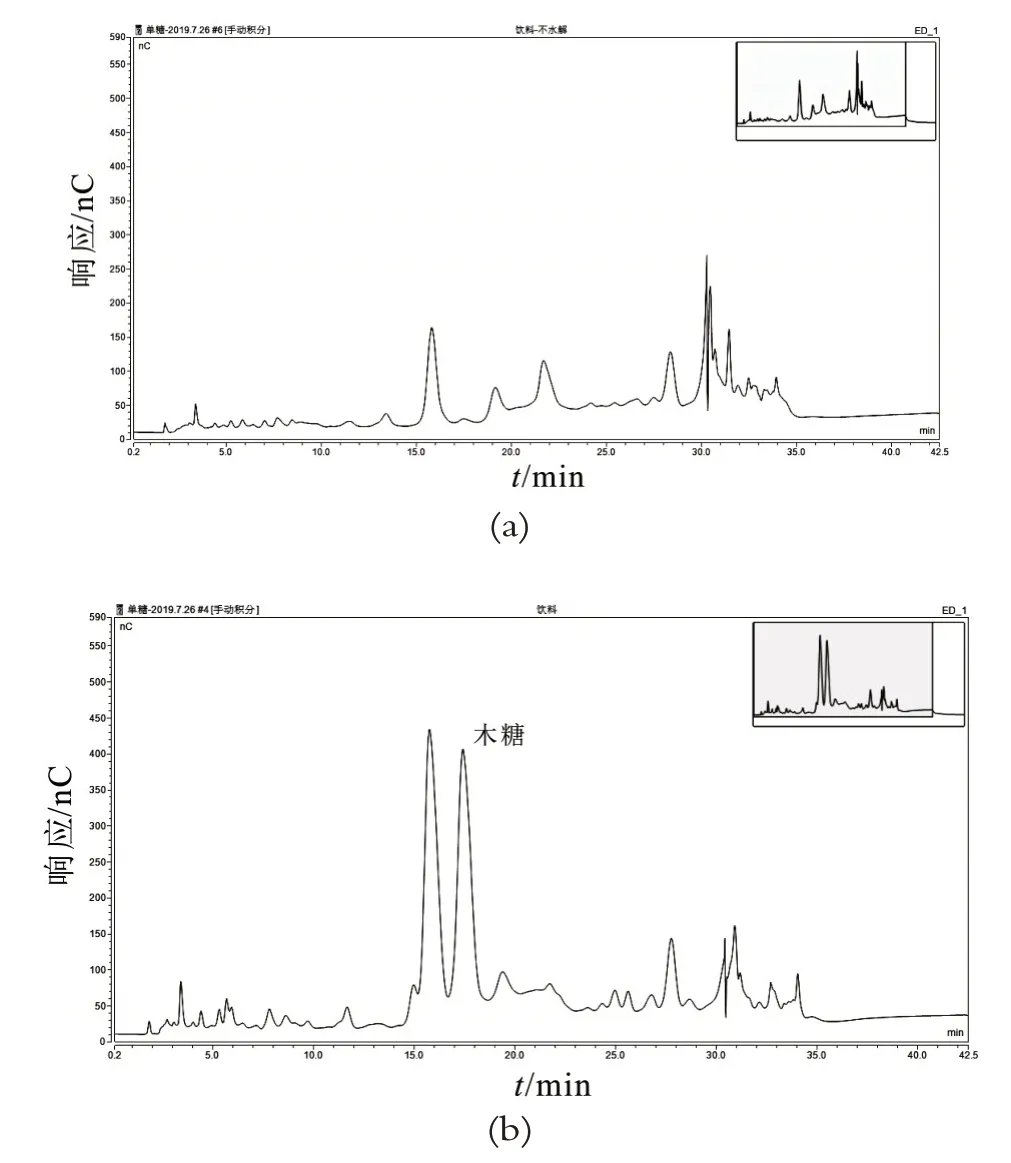
图5 固体饮料水解前(a)与水解后(b)测定色谱
2.4 回收率和精密度
以同一个不含低聚木糖的配方乳粉为实验材料,称取2.5 g样品后,再分别加入1.0 mg和5.0 mg的低聚木糖添加剂原料(纯度大于95%),每个浓度的添加样品进行8 次平行测定,计算回收率与回收率的相对标准偏差(RSD)。回收率在87.2%~102.9%,回收率的RSD 在3.89%~8.36%。同时对含低聚木糖的配方乳粉和固体饮料2 个样品进行测试,每个样品进行8 次平行测定,样品测定值的RSD 在2.39%~6.56%。由此可以看出,测定结果的较为稳定,方法的重复性较好,准确性较好。
2.5 实际样品的测定
按照本方法对市售的配方乳粉和固体饮料样品进行低聚木糖含量的测定,结果见表1。从实际样品的检测结果来看,该方法的灵敏度和准确度可以满足实际测试的需求。
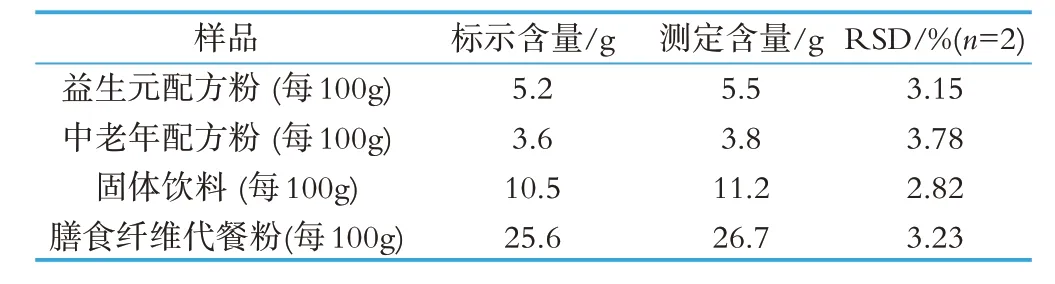
表1 样品中低聚木糖的含量
3 结 论
本文重点探讨了复杂基质的调制乳粉和固体饮料样品中低聚木糖水解的条件,将低聚木糖各组分完全水解为木糖,再结合优化的离子色谱分析条件直接测定样品水解前后木糖的含量,二者之差经换算后获得低聚木糖的含量。该方法具有良好的线性,操作简便,结果可靠,干扰小,同时重复性好,准确度高,适合复杂基质的调制乳粉和固体饮料中低聚木糖含量的生产监测和日常监管检测。

