BRAF抑制剂联合抗EGFR单抗和伊立替康解救治疗BRAF V600E突变的转移性结肠癌一例报告并文献复习
彭黎明 王静 杨林
结直肠癌(colorectal cancer,CRC)是常见的消化道恶性肿瘤之一,全球每年有超过120万新发病例及60多万的死亡病例,总病死率高达45%,约20%CRC患者就诊时已出现远处转移[1]。全身化疗能延长转移性结直肠癌(metastatic colorectal cancer, mCRC)患者的生存,但这些患者的5年生存率仍不到10%[2]。CRC是一组异质性很强的疾病,因分子机制不同,而表现出不同的预后和对同种治疗的不同反应。丝裂原活化蛋白激酶(mitogen-activated protein kinase,MAPK)信号通路是细胞内最重要的信号通路之一,包含一组能被不同的细胞外信号激活的丝氨酸-苏氨酸蛋白激酶,如RAS、RAF、MEK、ERK等。BRAF(v-raf murine sarcoma viral oncogene homolog B1)作为激活下游MAPK信号通路转导的最强基因,约14%的原发性CRC和8%mCRC患者发生BRAF突变[3],其中90%以上为BRAF V600E位点的突变[3-4]。当BRAF V600E突变时,BRAF的第600位氨基酸残基由缬氨酸(valine)变成谷氨酸(glutamic acid),从而使BRAF蛋白激酶一直处于激活状态,导致下游MAPK信号通路的持续激活,引起肿瘤细胞分化、增殖和生长。多个临床研究表明,BRAF V600E突变的mCRC患者常规治疗效果差,疾病进展快、生存期短、预后差[5-6]。近期中国医学科学院肿瘤医院收治1例经二线治疗后疾病进展的BRAF V600E突变的mCRC患者,采用BRAF抑制剂维莫非尼联合西妥昔单抗和伊立替康治疗后肿瘤明显缩小并获得较长的无进展生存期(progression-free survival,PFS)。
一、病史
患者70岁,男性。2016年11月在当地医院体检,腹部超声、CT及肝脏MRI显示:肝内多发结节伴肝门区淋巴结肿大。进一步PET-CT:降结肠局部肠壁增厚,考虑肿瘤性病变。肝内多发占位,考虑多发转移瘤。血清CA19-9:10 000 U/mL,CEA:32.75 ng/mL,CA242:18 992 U/mL(见图1),乙肝五项阴性。结肠镜检查:横结肠脾曲见巨大环形浸润型病变,侵及肠腔全周致肠腔狭窄,镜身无法通过。活检病理:(横结肠脾曲)中-低分化腺癌。免疫组化:Ki67(40%),MLH1(+),PMS2(+),MSH2(+),MSH6(+)。基因检测(直接测序法):NRAS、KRAS野生型。2016年11月29日因脐下阵发性绞痛就诊于中国医学科学院肿瘤医院。2016年12月5日查肠镜:进镜至距肛缘约70 cm结肠全周可见一溃疡性肿物,溃疡底深且覆以大量污物,溃疡周边不规则隆起且表面破溃、出血,肿物处肠腔偏心性狭窄。2016年12月8日于肠镜下行肠道支架植入术,术后患者腹痛缓解。因外院肠镜活检肿瘤组织量少,无法进一步行BRAF等基因检测,患者也拒绝再次肠镜或肝穿刺取活检。既往高血压病史20余年,血压控制在130/80 mmHg(1 mmHg=0.133 kPa)左右;胆囊切除术后21年。家族史:母亲患肝癌去世,妹妹患乳腺癌。
二、治疗过程
2016年12月15日开始全身治疗:XELOX方案+西妥昔单抗(奥沙利铂150 mg静脉滴注,第1天;卡培他滨3 500 mg/天,口服,第1~10天;西妥昔单抗900 mg静脉滴注,第1天,每14天1个周期)共6周期,期间最佳疗效评价为疾病稳定(stable disease,SD)。主要不良反应为Ⅰ度痤疮样皮疹。2017年3月复查CT提示降结肠原发灶无明显变化,肝转移瘤明显增大(见图2)。血清CA19-9:10 000 U/mL,CEA:124.8 ng/mL,CA242:37 049 U/mL,评价为疾病进展(progressive disease,PD),一线治疗PFS为2.5个月。2017年3月29日开始二线治疗:FOLFIRI方案+贝伐珠单抗(伊立替康300 mg静脉滴注,第1天;亚叶酸钙300 mg静脉滴注,第1天;氟尿嘧啶625 mg静脉滴注,之后氟尿嘧啶4 125 mg持续静脉泵入46小时;贝伐珠单抗300 mg静脉滴注,第1天,每14天1个周期)共6周期,期间评价最佳疗效SD(肿瘤略增大),2017年6月CT提示降结肠原发灶无变化,肝转移灶明显增大(血清 CA19-9:10 000 U/mL,CEA:94.97 ng/mL,CA242:35 315 U/mL),疗效评价PD(见图2),二线治疗PFS为2.5个月。主要不良反应为Ⅱ度白细胞下降。
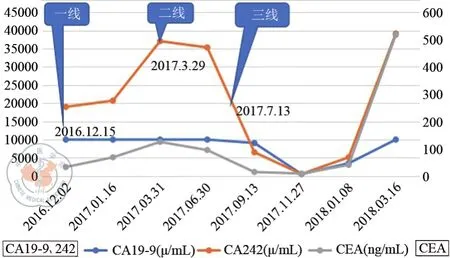
图1 治疗过程中肿瘤标记物变化情况

图2 腹部增强CT。2A:一线基线;2B:二线基线;2C:三线基线;2D:三线最佳疗效;2E:三线进展
与患者沟通后,患者同意再次活检,于2017年6月28日行肝穿刺,病理提示为结肠腺癌肝转移。免疫组化:HER2( +),BRAF V600E(3+),MSH2( +),MSH6(+),MLH1(+),PMS2(+)。NGS结果显示KRAS、NRAS为野生型,BRAF第15号外显子V600E突变。2017年7月13日开始三线治疗:VIC方案(维莫非尼960 mg Bid,口服:伊立替康240 mg静脉滴注,第1天;西妥昔单抗800 mg静脉滴注,第1天,每14天为1个周期)共13个周期(其中三药联合共11个周期,之后维莫非尼+西妥昔单抗两药联合治疗2个周期)。治疗期间降结肠原发灶无明显变化,3周期治疗后,肝转移灶数量减少,体积明显缩小,最佳疗效为部分缓解(partial response,PR),靶病灶较基线缩小85%~90%,PFS为8.5个月。主要不良反应为Ⅱ度白细胞减少、Ⅱ度乏力及Ⅰ度食欲下降。
2018年2月初开始患者逐渐出现乏力、食欲下降,明显消瘦。2018年3月8日复查胸腹CT提示降结肠原发部位肠壁不规则增厚较前加重。肝脏多发转移灶数量较前增多、体积增大。新出现腹盆腔腹膜转移伴大量腹水及双侧胸腔积液,双肺及骨多发转移。患者上述症状逐渐加重,一般状况快速衰退,未再能接受抗肿瘤治疗(见图3)。2018年3月20日死亡。从第1次化疗开始计算的生存时间为15个月。
三、讨论
本例BRAF V600E突变的转移性结肠癌发生于70岁男性的左半结肠,经二线化疗联合西妥昔单抗及贝伐珠单抗治疗,肿瘤均无明显缩小,一、二线化疗的PFS均仅2.5个月。三线使用BRAF抑制剂维莫非尼联合西妥昔单抗及伊立替康,最佳疗效达到PR,PFS达到8.5个月,且耐受性好。
文献报道BRAF突变多见于60岁以上老年、女性、右半结肠癌患者[7-8],组织学表现多为黏液癌[9],微卫星高度不稳定(MSI-H),预后差[10-11],EGFR单抗治疗疗效差[12]。在根治术后的CRC患者中,BRAF突变与差的总生存(overall survival,OS)相关,而与无病生存(disease-free survival,DFS)或无进展生存(PFS)相关性不明显,原因尚不清楚[13]。BRAF V600E突变CRC患者更常发生腹膜转移和远处淋巴结转移,通常疾病进展快,生存期短,预后差[6,9]。BRAF 突变一般不与 RAS 突变同时存在[14],既往研究都是按RAS野生型患者的治疗方案进行治疗[15]。但标准一线治疗即使给予强烈的化疗方案,预后仍较差,中位OS仅9~14个月[16-18]。一线治疗后进展的患者,后续治疗缓解率低于10%,中位PFS仅约2个月,中位OS仅4~6个月[19]。本例患者初诊时即为结肠癌伴同时性不可切除肝转移,病程后期出现广泛腹膜转移。尽管接受了规范的全身治疗,但从开始化疗计算的OS仅15个月,预后明显差于RAS野生型mCRC总体人群[20]。
BRAF抑制剂维莫非尼(vemurafenib)或达拉非尼(dabrafenib)以及encorafenib单药治疗BRAF V600E突变恶性黑色素瘤可使肿瘤明显缩小[9],但长期生存获益有限,部分原因可能是由于其他旁路被激活导致产生快速耐药。维莫非尼单药治疗mCRC几乎无效[21],原因可能是BRAF被抑制后反馈性引起上游EGFR的激活[22],从而持续驱动肿瘤增殖(黑色素瘤EGFR表达量较低,反馈激活耐药机制不易起作用)。这些都提示同时进行多靶点抑制(EGFR、MEK、PI3K)可能会产生协同效应。临床前研究提示维莫非尼联合抗EGFR单抗和/或化疗(伊立替康),在BRAF V600E突变mCRC中的抗肿瘤活性会明显提高[23-24]。Ⅰ/Ⅱ期临床研究也支持多靶点联合治疗[25],客观缓解率(overall response rate,ORR)4%~27%,PFS为3.2~7.7个月[26]。一项Ⅱ期临床研究(SWOG S1406)表明:在至少接受过1个化疗方案治疗后进展的mCRC患者中,无论之前是否曾用伊立替康化疗,采用VIC方案(维莫非尼960 mg bid+西妥昔单抗500 mg/m2+伊立替康180 mg/m2每2周1次)的中位PFS、ORR和疾病控制率(disease control rate,DCR)分别为4.4个月、16%和67%,高于伊立替康联合西妥昔单抗的两药方案(分别为2.0个月、4%和22%)[19]。基于此项研究结果,2018年第一版NCCN指南开始推荐VIC方案用于BRAF V600E突变的mCRC患者的二线及后线治疗。本例患者既往接受了包括伊立替康在内的两个标准两药化疗联合靶向药物(抗VEGF单抗和抗EGFR单抗)治疗,肿瘤缩小均不明显,PFS均仅为2.5个月。在采用VIC方案治疗后,肿瘤明显缩小达到PR(缩小85%~90%),PFS达8.5个月,明显高于文献报告的中位PFS,证实了该联合方案在BRAF V600E突变mCRC中的有效性。也有个案报告将该联合方案用于BRAF突变mCRC的一线治疗并达到临床完全缓解的报道[27]。其他多靶点抑制方案也在临床试验中。正在进行的一项Ⅲ期临床研究BEACON CRC备受瞩目。该研究采用另一个BRAF抑制剂encocrafenib,与MEK抑制剂binimetinib和西妥昔单抗联合,治疗既往1~2个方案治疗后进展的BRAF V600E突变mCRC患者。在初始30例患者中进行的安全性、耐受性和初步疗效的探索性研究(SLI)结果显示,ORR为48%,PFS 8个月,中位OS 15.3个月,1年总生存率为62%。而且三类靶向药物联合治疗的耐受性良好,不良反应与已知的BRAF、MEK和EGFR抑制剂的毒性一致[28]。该三药方案用于BRAF突变mCRC一线治疗的研究ANCHOR-CRC已经启动(Clinical Trials.gov identifier:NCT03693170)。

图3 腹部、盆腔CT。3A、3B、3C为肿瘤终末期
本例个案报告提示,维莫非尼联合西妥昔单抗和伊立替康的VIC方案用于既往化疗失败的BRAF V600E突变mCRC是有效的,安全性好。可考虑将该方案进行一线治疗的探索。通过本例患者的诊治也提示,对于初诊的mCRC患者,除了检测肿瘤组织KRAS、NRAS基因突变以及微卫星状态、HER2表达外,BRAF突变状态也是必须检测的,这对于判断患者预后、制定合理的治疗策略和方案非常重要。

