LiZr2(PO4)3包覆LiNi0.8Co0.15Al0.05O2的制备与改性研究
张秋歌,丁举宣,杜一博
(合肥工业大学化学与化工学院,安徽合肥230009)
随着能源危机的出现以及环保意识的提升,发展新型可再生清洁能源成为当今社会的趋势。对于汽车行业而言,由于传统燃油汽车能耗高、不可再生、尾气污染比较严重,相比之下新能源汽车锂离子动力电池具有污染小、可再生、成本低等优势,所以世界各国争相推出新能源汽车替代传统燃油汽车。近年来,得益于良好的市场环境以及政策的影响,新能源汽车取得了飞速的进展。为了追求更高的能量密度以及使用寿命,市场对新能源动力锂电池提出了更高的标准和要求[1-3]。
与传统橄榄石结构的磷酸铁锂(LiFePO4)、尖晶石结构锰酸锂(LiMn2O4)、层状结构钴酸锂(LiCoO2)相比,α-NaFeO2层状晶体结构的镍钴铝酸锂(LiNixCoyAl1-x-yO2)由于 Ni、Co、Al 三元素明显的协同作用,其综合了 LiNiO2、LiCoO2以及LiAlO2三者的特征,同时兼具高放电比容量、长使用寿命和良好的安全稳定性等优点[5-6],从而引起科研工作者的目光,被认为在当前锂电池中最有希望解决新能源续航里程短、安全性能差的问题。对于高镍系三元体系而言,Ni 为+2 和+3 价共存,Co 主要是+3 价以及少量的+4价,Al为+3价,材料的容量主要来源于镍离子的氧化还原,因此其能量密度和充放电容量与Ni的含量有着密切的关系。随着过渡金属元素中Ni 的比例增加其容量也会相应提升[7-8]。为了追求高能量密度和循环寿命,本研究LiNixCoyAl1-x-yO2中镍含量选取为x=0.8,但是与此同时,Ni 含量过高也会带来诸多问题,加剧Li+/Ni2+阳离子混排效应[9-10],无序排列结构阻碍充放电过程中锂离子的脱嵌。目前市场上电解液成分主要包含LiPF6,它容易分解成HF,进而攻击正极材料[11-12],破坏原有的层状结构;镍含量过高会增加阳离子混排,材料有序程度降低,导致循环性能和安全性能降低。
表面包覆和掺杂被认为是当前解决电池性能衰减快、安全稳定性差等问题的有效手段。包覆改性是在三元前驱体或者产物表面包覆一层合适厚度的金属氧化物、氟化物或者锂盐,包覆层可以有效避免电解液和活性材料的直接接触,将两者隔离开,减少活性材料表面副反应的发生,同时也可以抑制电解液对活性材料的腐蚀。
金属氧化物属于惰性材料,本身不能提供容量,它是通过抑制表面副反应和电解液对活性材料的腐蚀来提高三元材料的循环和热稳定性。相比之下,锂盐类包覆层能够促进锂离子的扩散,同时提高材料的循环稳定性和倍率性能。
LiZr2(PO4)3是一种快离子导体,能够提高充放电过程中锂离子扩散速率,并且包覆层能够将正极材料和电解液隔离开,能够有效减少电解液对正极材料主体的侵蚀,提高正极材料的循环稳定性。为此,我们通过氢氧化物共沉淀法首先合成Ni0.8Co0.15Al0.05(OH)2前驱体,然后通过湿法在其表面包覆一层LiZr2(PO4)3,最后高温烧结得到最终产物。通过电化学表征研究LiZr2(PO4)3包覆后对三元材料电化学性能的影响。
1 实验部分
1.1 前驱体制备
本实验采用氢氧化物共沉淀法制备化学计量比的Ni0.8Co0.15Al0.05(OH)2前驱体。首先以 NiSO4·6H2O、CoSO4·7H2O为原料按照金属摩尔比Ni∶Co=80∶15配制2 mol·L-1的总体积为1 200 mL 混合金属盐溶液A,按照化学计量比称量NaAlO2配制 0.5 mol·L-1的NaAlO2盐溶液B,同时配制10 mol·L-1的氢氧化钠溶液C,氢氧化钠作为沉淀剂,5 mol·L-1的氨水溶液D 作为反应络合剂。蠕动泵采用并流的方式将上述溶液输送到装有底液的持续搅拌的5 L密闭反应釜中,反应全程通入氮气作为保护气氛,搅拌速度为1 000 r·min-1,采用pH计实时监测反应体系pH 值,通过调节氢氧化钠进料速度使反应体系pH 值稳定在11.0±0.05,与此同时采用恒温水浴加热使反应保持在恒温60℃。进料完毕后,经过陈化将沉淀物抽滤,并用水和乙醇反复洗涤数次清除多余杂质,然后放置在120℃烘箱中烘干12 h得到Ni0.8Co0.15Al0.05(OH)2前驱体。
1.2 正极材料的制备
将上述制备的Ni0.8Co0.15Al0.05(OH)2前驱体与Li2CO3按照化学计量比1∶1.05比例称量置于研钵中混合均匀,然后将混合物置于氧气气氛(纯度99.99%)下的管式炉中焙烧,采用两段式方法加热:首先由室温以2℃·min-1的升温速度加热至450℃,在此温度下恒温预烧5 h,然后继续以2℃·min-1的升温速度加热至750℃恒温煅烧15 h,加热结束后经过自然冷却,取出得到LiNi0.8Co0.15Al0.05O2正极材料。
1.3 改性研究
称量1 g 自制的Ni0.8Co0.15Al0.05(OH)2前驱体分散在100 mL 水-乙二醇混合体系中(体积比1∶1)。称取适量的焦磷酸钠、氧氯化锆溶解,然后将其加入分散有前驱体的混合体系中,放置在磁力搅拌器上边搅拌边加热,反应体系温度控制在80℃,加热过程中同时向反应容器中缓慢滴加尿素溶液,反应数小时结束后进行离心、抽滤、干燥,干燥后的样品与碳酸锂混合均匀放置在管式炉中烧结得到包覆改性后的正极材料。
1.4 物相表征测试
合成样品的形貌和微观结构采用日立公司的SU8020 型场发射电子显微镜(FESEM)测试,加速电压为5 kV;样品中各元素的含量以及分布采用能谱仪表征(EDS);采用荷兰帕纳科公司X’PERT PRO MPD 型X 射线衍射仪对粉体物相结构和晶体组成表征,测试条件为:Cu Kα 靶(λ= 0.154 178 nm),操作电压为40 kV,工作电流为80 mA。样品以波长λ= 0.154 178 nm 的X 射线在扫描区间为2θ= 10~80o之间进行扫描,扫描速率为4°min-1;通过热重分析仪分析样品的烧结机制和热稳定性。
1.5 电池组装机电化学性能测试
(1)电极片制备
将高温烧结的正极材料、粘结剂PVDF(聚偏氟乙烯)以及导电剂乙炔黑按照质量比8∶1∶1 称量,溶于NMP(1-甲基-2-吡咯烷酮)溶液中,搅拌均匀得到具有流动性混合浆料,然后用75 mm刮刀均匀涂在平整集流体铝箔上,放置在80℃烘箱中干燥除去多余溶剂和水分,然后经过剪裁、辊压、切片等流程得到直径12 mm的圆形电极片,用分析天平称量电极片质量,然后放入80℃真空烘箱中干燥除去表面接触到的水分备用。
(2)电池组装
将上述干燥后的电极片放入充满氩气气氛的手套箱中,操作前观察手套箱和氧分压应小于0.5 mL/m3方可进行。本实验采用上述制备的12 mm 电极片作为征集正极,金属锂片作为对电极制作CR2032纽扣电池,其中使用1 mol·L-1的LiPF6有机溶液(乙基甲基碳酸酯、碳酸乙烯酯、二甲基碳酸酯三者按照体积比1∶1∶1 配制)作为电解液,隔膜采用Celgaed 2400 多空聚丙烯膜,按照负极壳、锂片、电解液、隔膜、电极片、钢片、弹簧片、正极壳顺序组装电池,最后经过液压封口机封装得到扣式电池。
(3)电化学性能表征
组装好的扣式电池经过数小时的静置,采用深圳新威尔公司生产的充放电测试系统对其进行电化学性能测试,主要包括循环性能和倍率性能测试,测试电化学窗口为2.8~4.3 V,设置电流密度为1C=180 mA·g-1,测试环境为25℃。
2 结果与讨论
2.1 形貌、结构物相表征
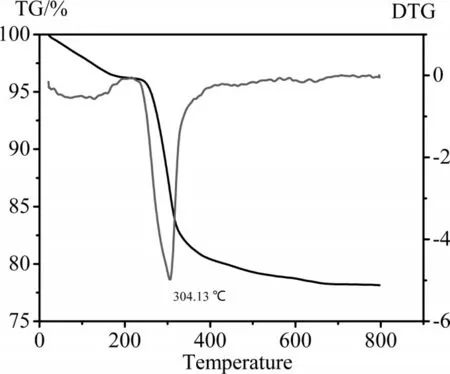
图1 Ni0.8Co0.15Al0.05(OH)2前驱体和Li2CO3混合物料的热重-差热曲线Fig.1 TG/DTG curves of Ni0.8Co0.15Al0.05(OH)2 and Li2CO3
图1 为氢氧化物共沉淀法制备的Ni0.8Co0.15Al0.05(OH)2前驱体和Li2CO3混合物料的TG-DTG 曲线,30℃~800℃温度范围热重曲线大致可以分为三次失重阶段:第一次失重现象出现在室温~200℃温度范围,此阶段为颗粒表面吸附的水分受热挥发导致;第二次失重出现在200℃~400℃,DTG 显示在304.13℃出现一个明显吸热峰,这个阶段主要为Ni0.8Co0.15Al0.05(OH)2前驱体脱水分解成氧化物;第三阶段发生在400℃~600℃,此阶段为碳酸锂的熔融分解以及和过渡金属氧化物重组生成LiTMO2化合物。当煅烧温度超过600℃时,质量只有轻微减少,变化不是很明显,这是因为微量的碳酸锂高温下挥发导致。因此,烧结过程中我们采用两步法进行煅烧:第一步,将前驱体和碳酸锂混合物料以2℃·min-1的升温速度升温至450℃恒温预烧5 h;第二步,继续以2℃·min-1的升温速率升温到750℃恒温焙烧15 h最终得到LiNi0.8Co0.15Al0.05O2正极材料。

图2 LiNi0.8Co0.15Al0.05O2正极材料以及锆改性修饰后样品的XRDFig.2 XRD curves of the original LiNi0.8Co0.15Al0.05O2 and after Zr-modified
图2 为经过高温煅烧后得到的包覆改性样品以及原始LiNi0.8Co0.15Al0.05O2正极材料的XRD 图,样品的衍射峰与LiNiO2的标准卡片(PDF#74-0919)的特征峰基本吻合,这可能是因为镍含量过高的原因,并且无杂峰出现,说明材料具有典型的α-NaFeO2六方层状晶体结构。从XRD 图中一些指标可以判断材料晶体结构的状况,从(003)和(104)衍射峰的比值可以判断材料中阳离子混排程度,两者比值越高,阳离子混排越少,并且普遍认为I(003)/(104)≥1.2 时,表明阳离子混排较少。本实验最初制备的LiNi0.8Co0.15Al0.05O2正极材料的I 值为1.46,包覆改性后I值为1.50,说明样品中Li+/Ni2+阳离子混排较少,并且改性后样品中阳离子混排程度有所减少;同时可以观察到(006)/(102)和(008)/(110)特征峰分裂比较明显,说明层状结构发育比较完善,包覆过程未对层状结构造成破坏。通过对XRD 进行晶格参数计算得到其数值见表1,其中c/a的比值可以代表晶体结晶程度和层状发育程度,一般认为c/a≥4.9 表明结晶程度和发育程度比较良好,包覆前后样品的c/a 值分别为4.930 8 和4.938 4,对应着材料晶体发育良好,也预示着优秀的电化学性能。

Tab.1 Lattice parameters of different LNCM samples

图 3 (a,b)LiNi0.8Co0.15Al0.05O2 正极材料的 FESEM 图;(c,d)LiZr2(PO4)3包覆改性LiNi0.8Co0.15Al0.05O2后正极材料的FESEM图Fig.3 (a, b) FESEM images of LiNi0.8Co0.15Al0.05O2 cathode ma⁃terial; (c, d) FESEM images of LiNi0.8Co0.15Al0.05O2 cathode ma⁃terial coated with LiZr2(PO4)3
图3(a,b)为高温烧结后LiNi0.8Co0.15Al0.05O2正极材料不同分辨率下的FESEM 照片,图3(c,d)为LiZr2(PO4)3包覆改性后的LiNi0.8Co0.15Al0.05O2正极材料的FESEM图。从图中可以看出,正极材料是由一次颗粒紧密堆积组成的二次颗粒,颗粒呈类球形,粒径分布比较均一,平均粒径为6 μm。从图中可以明显看出,与改性前样品相比,改性后样品在光滑表面涂覆一层物质,它能抑制表面副反应的发生。

图4 LiZr2(PO4)3包覆改性LiNi0.8Co0.15Al0.05O2后正极材料的EDS和MappingFig.4 EDS and mapping of LiNi0.8Co0.15Al0.05O2 cathode material coated with LiZr2(PO4)3
图4展示了EDS和Mapping对改性后样品进行元素表面含量和分布表征,从图 4 可以看出,Ni、Co、Al、O 元素分布比较均匀,元素含量测定也与设计材料化学计量比比较一致,说明沉淀过程Ni、Co、Al 过渡金属实现了均匀共沉淀。另外Zr、P 元素均匀分布在颗粒表层,也说明本实验成功地在LiNi0.8Co0.15Al0.05O2三元复合正极材料表面包覆一层磷酸锆锂。
2.2 电化学性能表征
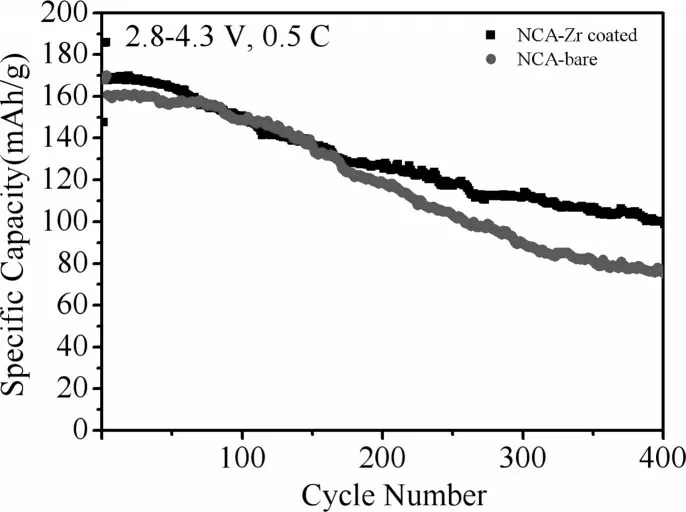
图5 NCA样品在0.5 t C电流密度下的循环性能图Fig.5 Cycling performance of NCA at a current density of 0.5 C
对合成的材料组装电池进行电化学性能测试,测试条件为常温25℃,电化学平台2.8~4.3 V。循环性能测试采用0.2 C 小电流密度下活化三次,然后0.5 C 下循环。图5 展示了NCA 样品在0.5 C电流密度下的循环性能,未改性材料在0.2 C电流密度活化下的首次库伦效率为81.9%,0.5 C 下放电比容量为160.84 mAh·g-1,而包覆后样品的首次库伦效率增加到84.4%,0.5 C下放电比容量也提升到167.78 mAh·g-1,其充放电曲线展示在图6中。循环400 圈后改性前后样品放电容量分别为75.4 mAh·g-1和 98.59 mAh·g-1。经过 400 圈循环后,改性后容量保持率由46.88%提升到58.76%,说明包覆改性后有效抑制电解液的腐蚀,材料的结构稳定性得到提高。
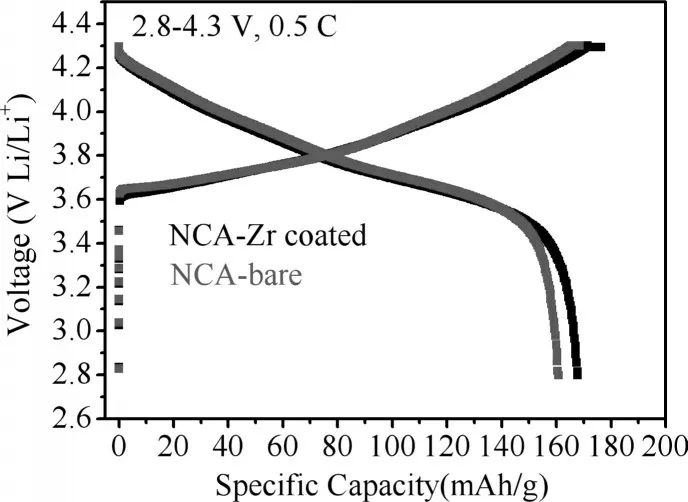
图6 NCA样品在0.5 C电流密度下的充放电曲线图Fig.6 The charge-discharge curves of NCA at a current den⁃sity of 0.5 C
3 结论
本文采用氢氧化物共沉淀方法合成Ni0.8Co0.15Al0.05(OH)2前驱体,然后与碳酸锂混合研磨成功制备出LiNi0.8Co0.15Al0.05O2正极材料。另外通过湿法在表面包覆一层LiZr2(PO4)3,LiZr2(PO4)3包覆是快离子导体,抑制电解液对正极材料腐蚀的同时,能够提高锂离子扩散速率,提高材料循环和结构稳定性。0.5 C 电流密度下经过400 圈循环后,容量保持率由原来的46.88%提升到58.76%,较好地解决了原材料衰减快的问题。

