分散式生活垃圾热处理底渣特性及生态风险评价
黄超民 龙於洋 沈东升

【摘 要】随着垃圾围城问题的日益突出,传统生活垃圾处理方式存在各种弊端,因此分散式生活垃圾热处理方式开始受到关注。由于其处理温度相对较低,可能大部分重金属等有害物质将会残留在底渣中,因此底渣处理处置是分散式生活垃圾热处理能否顺利推广的关键。为了评估分散式生活垃圾热处理产生的底渣是否存在生态风险问题,文章通过分析底渣物理、化学特征及底渣中重金属含量,并考察其斑马鱼生物毒性,进而综合评估其生态风险。结果表明,分散式垃圾热处理产生底渣重金属含量符合《生活垃圾填埋场污染控制标准》(GB16889—2008)入场填埋标准,生物毒性较低,可安全填埋。
【关键词】分散式生活垃圾热处理;底渣;重金属;斑马鱼;生态风险
【中图分类号】X701 【文献标识码】A 【文章编号】1674-0688(2020)03-0108-05
0 前言
近年来,我国城市生活垃圾以每年约4亿t的产生量快速增长[1],随之而来的生活垃圾处理问题也日益窘迫。垃圾最传统的处理方式是填埋,但填埋厂址选择需远离居住区,这造成垃圾运输费用相应增加,垃圾处理成本随之提高[2]。同时,填埋方式造成的二次污染也非常严重,如渗滤液等处理也较为困难[3]。
目前,热处理是全球生活垃圾处理的主流工艺[4]。城市生活垃圾热处理由于具有处理时间短、减量化显著(减重率达70%,减容率达90%)[4]、无害化彻底及可回收垃圾燃烧余热等优点已经成为不少城市解决垃圾问题的主要手段。然而,我国近年来由于邻避效应等问题造成垃圾集中式处理选址困难,同时存在运输成本高等问题,导致垃圾集中式热处理在我国大范围推广受阻,分散式生活垃圾热处理技术的市场需求开始扩大,该技术已经在全国各地进行了试用,在很大程度上解决了生活垃圾围城问题。
但相较于传统热处理方法,分散式生活垃圾热处理仍存在较多问题。由于燃烧温度比传统热处理低,因此重金属等有害物质可能大部分残留在底渣内。如果对燃烧产生的底渣处置不当,会占用大量土地资源,而且其中的有害成分随着雨水进入水体和土壤,存在潜在的生态风险,并可能通过食物链危及人体健康[5]。垃圾热处理后底渣的安全性是直接关系该类技术能否顺利推广的关键问题之一。因此,针对燃烧后产生的底渣有必要进行生态风险评估。
综上所述,本文基于某公司开发的分散式垃圾热处理设备,为了明确组分不同的垃圾汽化后底渣的安全处置及再生资源化利用可能性,分析两类典型的生活垃圾(纸张类与餐厨类)的底渣的物化性质,提出可再生利用方向;研究了燃烧后底渣的斑马鱼生物毒性和重金属含量,从而综合评估其生态风险,判断其是否达到填埋处理标准。
1 材料与方法
1.1 分散式垃圾热处理设备及生活垃圾来源
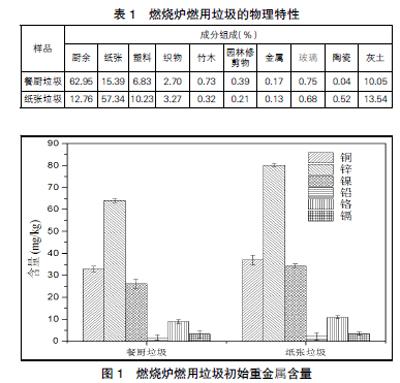
本文选用的是某公司所提供的分散式生活垃圾热处理设备。设备燃烧的生活垃圾取自附近若干村庄日常产生的生活垃圾。通过分拣处理与组分调节,按照质量百分比将生活垃圾调节组分分拣为两类生活垃圾(以餐厨类为主和以纸张类为主)。两类生活垃圾的物理性质见表1,两种生活垃圾的原始重金属含量如图1所示。
1.2 燃烧炉工况
两类生活垃圾分别在分散式垃圾热处理设备燃烧炉中进行燃烧实验,投料方式为机械进料,进料时间间隔约24 h,燃烧处理量约1 m3/d。两次燃烧实验过程中助燃系统的参数基本保持一致,进气量约80 m3/h,炉膛内氧气含量约11.2%。两次燃烧过程中,炉膛温度基本保持一致,整体平均温度控制在300~400 ℃,但局部温度短时间内会高于450 ℃。
1.3 底渣物理化学特征分析
为明确垃圾燃烧后产生的底渣再生资源化利用可能性,需要分析底渣的物理、化学特征。为此,对以上两类垃圾燃烧底渣样本进行如下测试。
(1)烧失量:按四分法取样,准确称取1 g试样,置于已灼烧恒重的瓷坩埚中,将盖斜置于坩埚上,放在高温炉内从低温开始逐渐升高温度,在600~700 ℃灼烧15~20 min,取出坩埚,置于干燥器中冷至室温。称量,如此反复灼烧,直至恒重,实验重复3次。
(2)化学能谱分析(EDS):外送至天合科研协作中心测定。
1.4 重金属测定
采用三酸消解的方法对底渣样品进行消解[6]。称取0.25 g样品至聚四氟乙烯坩埚中,加入浓硝酸5 mL,密封加热1 h,后加入5 mL高氯酸,加盖消解3 h,加2.5 mL氢氟酸消解,直到颜色透明,开盖赶酸。待剩余溶液约1 mL时停止加热,冷却至常温后加入2.5 mL硝酸,定容至50 mL,过膜后待测。重金属浸出液,采用FZ-4翻转型振荡器,根据国标法《固体废物浸出毒性浸出方法——硫酸硝酸法》(HJ/T 299—2007)得到浸出液。重金属含量测定参照Tessier法[7],使用原子吸收光谱仪——火焰法进行测定,测定的元素包括铅(Pb)、镍(Ni)、镉(Cd)、铬(Cr)、铜(Cu)、锌(Zn)。
1.5 重金属平衡分析
本文依托的分散式垃圾热处理设备,由气化室、焦油吸收塔、生物滴滤塔组成。因此,本文研究重金属平衡,计算重金属含量由原始垃圾、底渣、直排煙气、处理后的烟气、处理后的废水、污泥等部分组成,以燃烧纸张垃圾进行燃烧过程重金属平衡计算,原始垃圾取自进炉燃烧垃圾,并用破碎机将其剪切破碎制得样品进行消解处理;底渣取自燃烧垃圾后产生的炉渣并进行消解;污泥取自生物滴滤塔中生物电化学系统和生物填料中产生的污泥;直排烟气和处理后烟气分别于直排烟囱和生物滴滤塔出气口进行取样,处理后的废水取自焦油吸收塔和生物滴滤塔。重金属平衡计算方法如下:
原始垃圾中重金属含量(单位:mg/kg):=
底渣中重金属含量(单位:mg):= ×ma
污泥中重金属含量(单位:mg):= ×mb
烟气中重金属含量(单位:mg):= ×V4
废水中重金属含量(单位:mg):= ×V5
其中, 、 、 、 、 为原始垃圾、底渣、污泥、烟气、废水消解液的浓度(mg/L);V1、V2、V3为消解液的定容体积(L);V4、V5为吸收液的定容体积(L);m1、m2、m3为原始垃圾消解的质量(kg);ma、mb为燃烧后底渣、污泥产生的质量(kg)。
1.6 斑马鱼生物毒性分析
在斑马鱼胚胎暴毒过程,每隔24 h于显微镜下观察,挑出死亡胚胎以免感染其他个体,统计死亡个数及躯体弯曲、心包囊肿、游囊缺陷和躯体痉挛发生率,连续观察6 d(144 hpf)。其中,躯体痉挛主要表现为斑马鱼发生连续性或间断性身体震颤、抽搐行为,不同于正常游动行为[8];判定死亡和其他畸形率按照经济合作与发展组织(OECD)的标准方法(OECD TG236,2006)。本实验中每个试验组投放30条斑马鱼,设置平行组,为保证溶液浓度恒定和溶氧充分,本试验选择半静态实验法,8 h更换一次试验液,试验周期为6 d(144 hpf)。观察144 h内斑马鱼的行为特征、中毒症状,记录死亡数和畸形数。
2 结果
2.1 生活垃圾底渣物化性质
2.1.1 物理特性
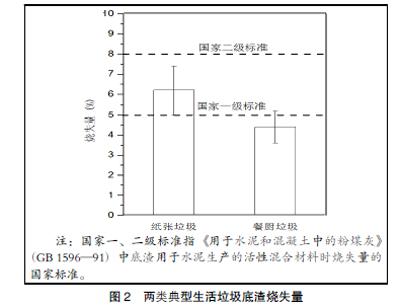
图2为两类垃圾底渣的烧失量,纸张类和餐厨类两类垃圾的底渣烧失量都较低,分别为6.2%和4.4%,而一般情况下混合生活垃圾的烧失量约5%[11]。根据《用于水泥和混凝土中的粉煤灰》(GB 1596—91),水泥生产中通常作为活性混合材料的底渣,其烧失量的国家标准分别为低于5%(一级)和低于8%(二级)。
2.1.2 化学组成
为确定燃烧底渣的化学成分,明确其综合化利用的可能方向,对其进行EDS能谱分析。纸张类和餐厨类底渣的EDS能谱结果见表2。纸张垃圾底渣的主要元素(质量分数>5%)有C、O、Al、Si、Ti,此外有少量的Na、Cl、K、Ca等。该类垃圾底渣中C含量较高,达到51.19%;而餐厨类底渣中O含量较高,达到22.94%,这可能与不同类生活垃圾本身元素组成有关。由图3可知,两类垃圾气化底渣的元素组成形态有Al2O3、SiO2、MgO等。
2.2 生活垃圾底渣重金属分析
2.2.1 重金属质量平衡分析
为明确燃烧过程中重金属的迁移状况,需要进行生活垃圾重金属平衡研究,主要考虑生活垃圾燃烧底渣中重金属含量、燃烧产生废水中的重金属含量、烟气中重金属含量及废气处理生物吸附的重金属含量。以纸张垃圾燃烧后产生的底渣为研究对象(如图4所示),结果表明,该设备燃烧过程中重金属输入量与输出量基本守恒。6种元素在底渣中的富集程度为Pb,Ni>Cr,Cd>Cu,Zn。镍、铅主要残留在底渣中(约50%),铜、锌主要富集在后续处理设备产生的废水和烟气中(约80%)。
2.2.2 底渣重金属含量
纸张类垃圾底渣浸出液中Cd、Cr、Ni、Cu、Zn、Pb 6种重金属的浓度分别为0.006、0.051、0.106、0.078、0.367、
0.002 mg/L(如图5所示),而餐厨类垃圾浸出液中各种重金属含量比纸张类垃圾中同类重金属含量都低。根据《生活垃圾填埋场污染控制标准》(GB 16889—2008)对燃烧底渣的入场要求可知(浸出液中Cd、Cr、Ni、Cu、Zn、Pb标准限值分别为0.15、4.5、0.5、40、100、0.25mg/L),该设备燃烧产生的不同类垃圾的底渣皆符合填埋标准。
2.3 生活垃圾底渣生物毒性
水体中重金属、持久性有机物、氨氮等有毒物质会影响斑马鱼的存活,通过LC50(半数致死浓度)来衡量其毒性大小。如图6所示,将各试验组144 h的斑马鱼死亡条数换算成死亡率,可以看出,不同垃圾底渣浸出液的生物毒性不同,但总体来说,两种未稀释倍数的底渣浸出液对斑马鱼的致死率均控制在20%以下,对斑马鱼胚胎造成的畸形率均未超过50%,且两类底渣的死亡率和畸形率均有显著性差异(P<0.05)。虽然暴露期内斑马鱼存在死亡个体,但死亡的斑马鱼并未出现腮部、腹部微红等急性中毒现象,且致死率均超过50%,无法计算半致死浓度[20],因此受试浸出液无急性毒性效应。
3 讨论
垃圾底渣烧失量越低,表明燃烧效率越高[9]。同时,烧失量也会影响底渣的综合利用,对于水泥、烧砖等行业来说,底渣中的未燃碳是有害成分[10]。因此,底渣烧失量越低,表明底渣综合利用的可能性越高。根据实验结果,相比较而言,餐厨类垃圾的燃烧底渣(烧失量为4.4%)作为水泥原料的资源化利用可能性更高。纸张类垃圾仅符合二级标准,这可能是因为纸张类垃圾主要由纤维状有机物质和结合水组成[12],该分散式热处理设备由于其局部温度远低于集中式焚烧炉,纤维状有机物质和结合水未能全部矿化,形成的底渣在600 ℃环境下进一步矿化,導致纸张类垃圾底渣烧失量偏高。因此,控制降低燃烧垃圾中纸张类垃圾的比重是降低烧失量最直接有效的措施,同时适当提高炉内燃烧温度,亦可降低烧失量[13]。
垃圾热处理所产生炉渣的处置目前主要有两个途径,即安全填埋或综合化利用。其中,炉渣的可资源化利用的方向如制备陶瓷砖或制作混凝土,伍浩然[14]报道了将炉渣制备陶瓷砖,其性能指标可达到国家标准;Pyo[15]报道了炉渣作混凝土原料,研究发现湿渣固化技术可提高混凝土试件质量,提高抗压强度。根据实验结果,两类垃圾底渣的元素组成含量虽差异较大,但组分类似,均含有一定量的水泥原料成分,如Al2O3、SiO2、MgO等。采用合适的工艺手段,垃圾底渣可以用作水泥混合材、水泥原料,丰富其综合利用的可能性[16,17]。
生活垃圾在燃烧处理过程中重金属会发生不同程度的迁移,由固态向气态迁移,从而使其分布在底渣和烟气中。Cahill[18]和Davison[19]等人对重金属的迁移进行研究,指出影响重金属在燃烧过程中迁变特性的最大因素是重金属蒸发压力和沸点。针对该设备燃烧垃圾过程重金属平衡分析,结果表明,镍、铅主要残留在底渣中(约50%),这是由于其沸点高于2 000 ℃,属于难挥发性重金属。镍、铅大量保留在底渣中,对于后续底渣填埋处理,可能造成镍、铅等重金属成分随着雨水进入水体和土壤,对水体和土壤及植被和生物等造成危害,并通过食物链危及人体健康。因此,针对该热处理设备底渣的重金属毒性分析时,镍、铅是重点检测对象。铜、锌主要富集在后续处理设备产生的废水和烟气中(约80%),这是由于其沸点相对较低,属于挥发性重金属。因此,针对该设备后续废水和烟气达标排放考察时,重金属类铜、锌是重点检测对象。在燃烧过程中,大部分以气态形式进入后续处理设备中。结果表明,造成重金属在燃烧过程中迁移的最大因素是炉膛温度和压力,与Cahill[18]和Davison[19]等研究结果一致。
針对两类垃圾测定其重金属含量,结果表明,该设备燃烧不同类垃圾产生的底渣皆符合填埋标准。此外,通过分析垃圾底渣本身的重金属含量发现,纸张类垃圾底渣中会存在较多的铜、锌元素(Cu、Zn含量分别为7.32、7.81 mg/kg),铜、锌的沸点相对较低,主要富集在后续处理设备产生的废水和烟气中,为了确保后续的烟气及废水达到国家排放标准,可适当减少纸张类垃圾进炉处理量。
虽然上述两类垃圾底渣中重金属含量较低,填埋不存在重金属污染风险,但是底渣仍旧存在其他有机物的残留可能性。因此,将底渣填埋时,需选用一种综合性的判断标准。本文进行生物毒性测试,综合评价其生态风险性。以斑马鱼为受试鱼类,考察两类垃圾底渣溶出水质的生物毒性,评估底渣填埋处置对环境的生态风险。试验结果表明,两种底渣浸出液无明显急性毒性效应,不会对斑马鱼的存活造成影响。虽然水体中的污染物质会破坏斑马鱼胚胎的组织结构,影响胚胎的正常孵化,造成心功能异常、心包囊水肿、躯体弯曲等多种畸形[21],但是两种底渣浸出液对斑马鱼胚胎造成的畸形率均未超过50%,对孵化率的影响不大,仍有较高的孵化率[22],因此两种底渣浸出液发育毒性效应较低,不会对斑马鱼造成明显危害。致死率和畸形率的结果表明,这两种底渣的生物毒性都较小。综合重金属含量和斑马鱼生物毒性,结果表明,产生的底渣生态毒性风险较低,可填埋处置或综合利用。
参 考 文 献
[1]Shi D Z,Wu W X,Lu S Y,et al.Effect of MSW source-classified collection on the emission of PCDDs/Fs and heavy metals from incineration in China[J].Journal of Hazardous Materials,2008,153
(1):685-694.
[2]Komilis D P,Ham R K,Stegmann R.The effect of municipal solid waste pretreatment on landfill behavior:a literature review[J].Waste Management
& Research,2010,17(1):10-19.
[3]Mor S,Ravindra K,Dahiya R P,et al.Leachate characterization and assessment of groundwater pollution near municipal solid waste landfill site[J].Environmental Monitoring & Assessment,2006,118
(1-3):435-456.
[4]Kosson D S,Sloot H A V D,Eighmy T T.An approach for estimation of contaminant release during utilization and disposal of municipal waste combustion residues[J].Journal of Hazardous Materials,1996,47(1-3):43-75.
[5]Adama M,Esena R,Fosumensah B,et al.Heavy metal contamination of soils around a hospital waste incinerator bottom ash dumps site[J].Journal of Environmental & Public Health,2016,2016(3):292-296.
[6]Kalbitz K ,Solinger S ,Park J H ,et al.Controls on the dynamics of dissolved organic matter in soils:
a review[J].Soil Science,2000,165(4):277-304.
[7]Tessier A,Campbell P G C,Bisson M.Sequential extraction procedure for the speciation of particulate trace metals[J].Analytical chemistry,1979,51(7):844-851.
[8]DeMicco A,Cooper K R,Richardson J R,et al.Developmental neurotoxicity of pyrethroid insecticides in zebrafish embryos[J].Toxicological Scien-
ces,2009,113(1):177-186.
[9]Rocca S,Van Z A,Costa G,et al.Mechanisms contributing to the thermal analysis of waste incin-
eration bottom ash and quantification of different carbon species[J].Waste Management,2013,33(2):373-381.
[10]Zhou X,Li J,Zhou S,et al.Process and case analysis of brick making by bottom ash in waste incineration[J].Environmental Sanitation Engineering,2016,24(2):25-27.
[11]Lin K L.Feasibility study of using brick made from
municipal solid waste incinerator fly ash slag[J].Journal of Hazardous Materials,2006,137(3):1810-1816.
[12]Sivasundaram M,Drew R A L,Caley W F.Mineralogical aspects of devitrified pulp and paper fly ash[J].Canadian Metallurgical Quarterly,2003,42
(1):113-120.
[13]Jalal M,Pouladkhan A,Harandi O F,et al.Com-
parative study on effects of Class F fly ash,nano silica and silica fume on properties of high performance self compacting concrete[J].Construction and Building Materials,2015,94:90-104.
[14]Haoran W,Qianni L,LiuYan,et al.Preparation of
ceramic tile with incineration bottom ash of MSW[J].Ceramics,2017(2):23-28.
[15]Pyo S,Kim H K.Fresh and hardened properties of ultra-high performance concrete incorporating coal bottom ash and slag powder[J].Construction & Building Materials,2017,131:459-466.
[16]Liu D,Zhu Y.Experimental study on performance of municipal solid waste incineration bottom ash treated subgrade soils[R].2018.
[17]Izquierdo M,Vazquez E,Querol X,et al.Use of bottom ash from municipal solid waste incineration as a road material[C].International ash utilization symposium,4th,Lexington,KY,United States,2001:31-38.
[18]Cahill C A,Newland L W.Comparative efficienc-
ies of trace metal extraction from municipal incinerator ashes[J].International Journal of Environm-
ental Analytical Chemistry,1982,11(3-4):227-239.
[19]Davison R L,Natusch D F S,Wallace J R,et al.Trace elements in fly ash.Dependence of concentration on particle size[J].Environmental Sc-
ience & Technology,1974,8(13):1107-1113.
[20]Weber,Cornelius I.Methods for measuring the acute toxicity of effluents and receiving waters to freshwater and marine organisms[M].Cincinnati,Ohio:Environmental Monitoring Systems Laboratory,Office of Research and Development,US Environmental Protection Agency,1991.
[21]Renée Katrin Bechmann,Larsen B K,Taban I C,et al.Chronic exposure of adults and embryos of Pandalus borealis to oil causes PAH accumulation,initiation of biomarker responses and an increase in larval mortality[J].Marine Pollution Bulletin,2010,
60(11):2087-2098.
[22]Incardona J P ,Collier T K ,Scholz N L.Defects in cardiac function precede morphological abnormalities in fish embryos exposed to polycyclic aro-
matic hydrocarbons[J].Toxicology and Applied Ph-
armacology,2004,196(2):191-205.

