FadD9重组蛋白在活动性肺结核诊断中的价值
张君丽, 林 晨, 王玉臣, 刘 军, 袁 俐, 潘稚芬, 张 鹭
(1.复旦大学生命科学学院遗传工程国家重点实验室,上海 200438;2.新疆石河子大学医学院,新疆 石河子 832002;3. 嘉兴学院附属第一医院 嘉兴市第一医院结核科,浙江 嘉兴 314000)
结核病是由结核分枝杆菌(Mycobacterium tuberculosis,MTB)引起的传染性疾病,是单病因致死率较高的疾病之一。世界卫生组织2018年的报告显示,全球有近1/4的人口(约23亿人)被MTB感染过,每年新增结核病患者约960万例,约有150万死于结核病[1]。我国是全球22个结核病高危国家和地区之一,MTB的感染人数已超5亿,结核病发病数约为450万例[1]。MTB进入宿主后根据机体的免疫水平会呈现3种不同的结果:(1)被免疫系统清除;(2)未被彻底清除而发展成潜伏性结核感染(latent tuberculosis infection,LTBI);(3)形成活动性结核(active tuberculosis,ATB)。约有90%的MTB感染会发展成为LTBI[2]。LTBI是一种未出现临床症状的持续性感染状态,表现为结核菌素皮肤试验阳性,但痰培养阴性且无影像学检查征象[3]。随着广泛耐药结核(extensive drug-resistant tuberculosis,XDR-TB)患者及结核病合并人类免疫缺陷病毒(human immunodeficiency virus,HIV)感染患者的增多,结核病防控形势尤为严峻,主要的原因包括缺乏快速、准确的诊断技术,缺乏有效的抗结核疫苗和过长的结核病药物疗程(9~12个月)。现有的用于诊断MTB感染及区分ATB和LTBI的方法,如酶联免疫吸附试验(enzymelinked immunosorbent assay,ELISA)、酶联免疫斑点试验(enzyme-linked immunospot assay,ELISPOT)和γ-干扰素释放试验(interferongamma release assay,IGRA)等都或多或少存在一些缺陷,敏感性与特异性难以兼顾[4]。筛选、优化哪些抗原或多肽用于MTB感染的诊断是研究者首先需要面对的难题,也是突破这一瓶颈的关键。目前,早期分泌靶抗原6(early secretory antigenic target-6,ESAT-6)和培养滤液蛋白10(culture filtrate protein-10,CFP-10)是现有诊断方法的核心抗原,但在不同高危人群中进行活动性结核病筛查时,这2个抗原的检测结果有时会不一致[5],其原因尚待进一步研究。因此,筛选更多可用于临床鉴别诊断的MTB候选抗原是提高结核病诊断能力的重要环节。fadD9(Rv2590)是MTB的一个脂质代谢相关基因,作为脂肪酸-CoA连接酶参与细菌脂质降解,具体功能还有待进一步探索。本研究团队前期通过生物信息学表位预测,发现fadD9是一个很有潜力的诊断候选靶基因。为此,本研究拟探讨通过基因表达和蛋白纯化得到的FadD9重组蛋白在诊断MTB感染中的潜在价值。
1 材料和方法
1.1 研究对象
1.1.1 用于FadD9特异性抗体水平检测的人群 选取2017年3月—2018年12月新疆石河子大学附属医院确诊的活动性肺结核患者145例(活动性肺结核组),其中男65例、女80例,年龄(55.56±15.76)岁。选取同期与结核病患者有1年以上密切接触史者38名(MTB密切接触组),其中男17名、女21名,年龄(60.42±9.74)岁。选取同期新疆石河子大学附属医院体检健康者101名(正常对照组),其中男51名、女50名,年龄(41.50±19.52)岁,均无结核病史及临床结核病状,且不曾与结核病患者接触过。所有研究对象均无HIV感染,均有卡介苗接种史。以上人群的所有样本均委托新疆石河子大学医学院项目合作组收集、鉴定。生物医学研究伦理学审查经新疆石河子大学医学院附属医院伦理委员会审批通过。
1.1.2 用于基于FadD9重组蛋白的IGRA检测的人群 选取嘉兴市第一医院2018年8—10月确诊的肺结核患者58例,其中男40例、女18例,年龄(53±40)岁,均为痰涂片阳性或X线检查具有结核影像学表现,且有相应的临床症状。以同期嘉兴市第一医院就诊的未感染MTB的其他患者34例作为对照(非肺结核组),其中男16例、女18例,年龄(51±35)岁,均无结核病史及临床结核症状,且不曾与结核病患者有密切接触史。所有研究对象均无HIV感染,均有卡介苗接种史。以上人群的所有样本均委托嘉兴市第一医院收集。生物医学研究伦理学审查经嘉兴市第一医院医学伦理委员会审批通过。
1.2 方法
1.2.1 FadD9重组蛋白的制备和鉴定 在美国国立生物技术信息中心网站(https://www.ncbi.nlm.nih.gov/)上获取fadD9基因序列(基因 ID:888574)。以MTBH37Rv基因组为模板,用fadD9基因的上、下游引物(上游引物为5'-GT GGGATCCATGTCGATCAACGATCAGCGACT GAC-3',下游引物为5'-TATAAGCTTTCACAG CAGCCCGAGCAGTCGCAG-3')进行聚合酶链反应(polymerase chain reaction,PCR)。PCR产物经酶切后连接至pET28a载体中,将构建好并经测序验证正确的重组表达质粒转入大肠埃希菌BL21(DE3)中,涂布在含50 μg/mL卡那霉素的LB固体培养基上,37 ℃培养过夜,随机挑取单个菌落接种至5 mL含50 μg/mL卡那霉素的LB液体培养基中,进一步扩大培养至1 L。待菌液浊度达到0.6[600 nm处的吸光度(A)值]时加入1 mL异丙基-β-D-硫代半乳糖苷(isopropylbeta-D-thiogalactoside,IPTG)(终浓度为1 mmol/L)继续诱导培养3~4 h,12 000×g离心1 min,收集菌体并用超声裂解,4 ℃ 12 000×g离心10 min,收集上清液。FadD9重组蛋白的N末端带有pET28a载体上的6个组氨酸标签,可与镍离子螯合,因此将Ni-NTA His·Bind Resin介质(美国Novagen公司)与收集的上清液混合后加入到空色谱柱中,按照介质说明书中的步骤进行纯化,获得FadD9重组蛋白。纯化好的蛋白采用10%十二烷基硫酸钠-聚丙烯酰胺凝胶电泳(sodium dodecyl sulfate-polyacrylamide gel electrophoresis,SDS-PAGE)鉴定纯度。
1.2.2 FadD9抗原免疫原性分析 选取C57BL/6小鼠8只,每组4只,进行皮下免疫注射,其中FadD9免疫组注射50 μL FadD9蛋白与等体积弗氏佐剂(美国Sigma公司)的混合物,阳性对照组注射50μL Ag85a蛋白(阳性参照抗原)与等体积弗氏佐剂的混合物,阴性对照组注射等量的磷酸盐缓冲液(phosphate-buffered saline,PBS)。小鼠分别在第1、3、5周进行免疫注射,第1次免疫注射使用弗氏完全佐剂,第2、3次使用弗氏不完全佐剂。首次免疫8周后分离小鼠脾脏淋巴细胞和小鼠血清,用ELISA分别检测脾细胞γ-干扰素(interferon-gamma,IFN-γ)、肿瘤坏死因子-α(tumor necrosis factor-alpha,TNF-α)和白细胞介素-2(interleukin 2,IL-2)释放水平及FadD9重组蛋白的特异性IgG抗体水平。
1.2.3 血清中FadD9重组蛋白与特异性抗体的反应性 以FadD9重组蛋白和Ag85A蛋白为抗原包被96孔板,以活动性肺结核组、MTB密切接触组和正常对照组的血清样本分别作为一抗,按1∶100稀释,二抗为过氧化物酶标记的山羊抗人IgG(美国CMCTAG公司),用前1∶3 000稀释。检测各组FadD9重组蛋白和Ag85A蛋白抗原抗体特异性反应水平。
1.2.4 FadD9重组蛋白T细胞表位预测分析 使用NetMHCcons 1.1 Server和NetMHCⅡ2.3 Server在线网站,对选定的等位基因逐一进行分析,记录预测得到的FadD9重组蛋白T细胞表位,分析FadD9重组蛋白与主要组织相容性复合物(major histocompatibility complex,MHC)-Ⅰ和MHC-Ⅱ的结合能力[6-7]。
1.2.5 FadD9重组蛋白诊断结核病的价值 将FadD9重组蛋白和Ag85A蛋白作为抗原与肺结核组和非肺结核组的全血样本37 ℃共孵育20~24 h后,离心分离血浆并进行IGRA,试剂盒(ELISA)购自北京万泰生物药业股份有限公司。将检测结果与试剂盒中的标准管进行比对,检测FadD9重组蛋白和Ag85A蛋白在临床血浆样本中激起的细胞免疫水平。
1.3 统计学方法
采用GraphPad prism 8.0.2软件进行统计分析。呈正态分布的数据以±s表示,2个组之间比较采用t检验,多组间比较采用方差分析。采用受试者工作特征(receiver operating characteristic,ROC)曲线评估FadD9重组蛋白诊断肺结核的价值。以P<0.05为差异有统计学意义。
2 结果
2.1 FadD9重组蛋白的制备和鉴定结果
FadD9重组蛋白均以可溶形式表达。纯化后的FadD9重组蛋白经10%SDS-PAGE鉴定,蛋白纯度>95%。见图1。
2.2 FadD9重组蛋白的免疫原性评估结果
检测抗原免疫后小鼠血清中的IgG(H+L)效价可评估抗原激起的体液免疫水平。FadD9重组蛋白的A值变化与阳性参照抗原Ag85A蛋白基本一致,均高于阴性对照组。FadD9重组蛋白的血清抗体滴度达1∶12 800,与阳性参照抗原Ag85A蛋白接近。见图2。
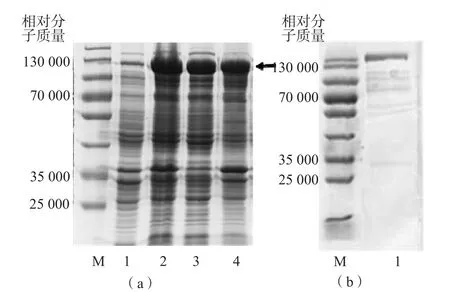
图1 FadD9重组蛋白的制备和鉴定结果
采用ELISA分别检测小鼠脾细胞的IFN-γ、TNF-α和IL-2水平。FadD9免疫组IFN-γ、TNF-α和IL-2水平分别为390.12、226.52、125.84 pg/mL ,三者比例为3.1∶1.8∶1.0。阳性对照组分别为333.97、190.84、159.0 pg/mL,三者比例为2.1∶1.2∶1.0。说明FadD9重组蛋白具有良好的免疫原性。
2.3 活动性肺结核组、MTB密切接触组与正常对照组FadD9重组蛋白和Ag85A蛋白的特异性抗体水平比较
活动性肺结核组抗FadD9抗体水平高于MTB密切接触组和正常对照组(P<0.000 1),MTB密切接触组与正常对照组之间差异无统计学意义(P>0.05)。抗Ag85A抗体水平3组之间差异均无统计学意义(P>0.05)。见图3。
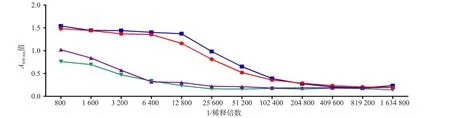
图2 FadD9免疫小鼠血清抗体水平
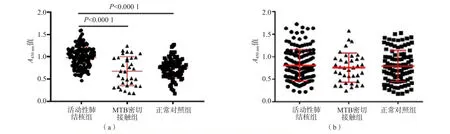
图3 活动性肺结核组、MTB密切接触组及正常对照组FadD9重组蛋白和Ag85A蛋白特异性抗体水平的比较
2.4 FadD9蛋白T细胞表位预测结果
FadD9天然蛋白与不同人群的人白细胞抗原(human leukocyte antigen,HLA)-DR、HLA-A和HLA-B受体具有结合位点。使用NetMHCⅠ和NetMHCⅡ数据库对FadD9重组蛋白T细胞表位进行初步分析。FadD9在2个数据库中的19个亚型中至少具有4个以上强结合位点以及33个以上弱结合位点。见图4。
2.5 FadD9重组蛋白诊断肺结核的效能
将FadD9重组蛋白和Ag85A蛋白作为抗原与肺结核组和非肺结核组的全血样本37 ℃共孵育20~24 h,然后进行IGRA,将检测结果与试剂盒中的标准管进行比对。ROC曲线分析结果显示,FadD9重组蛋白诊断肺结核的曲线下面积(area under curve,AUC)为0.682,最佳临界值为0.343,敏感性为96.8%,特异性为37.5%。见表2、图5。
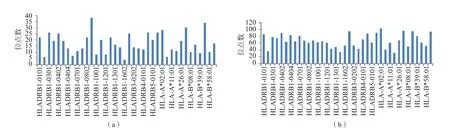
图4 FadD9重组蛋白T细胞表位预测结果
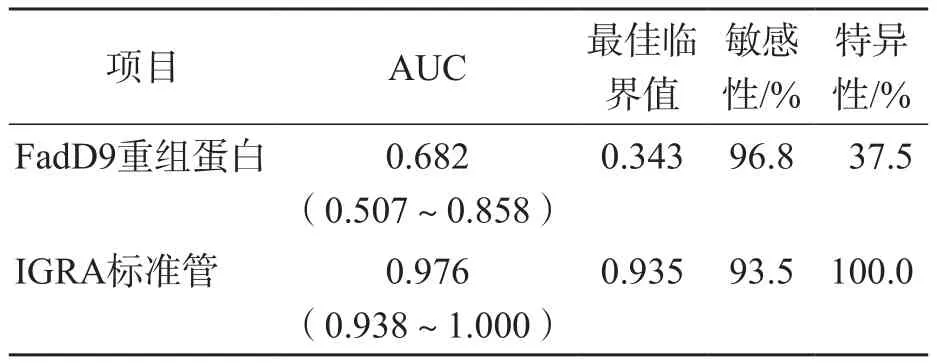
表2 FadD9重组蛋白和IGRA标准管诊断肺结核的ROC曲线参数
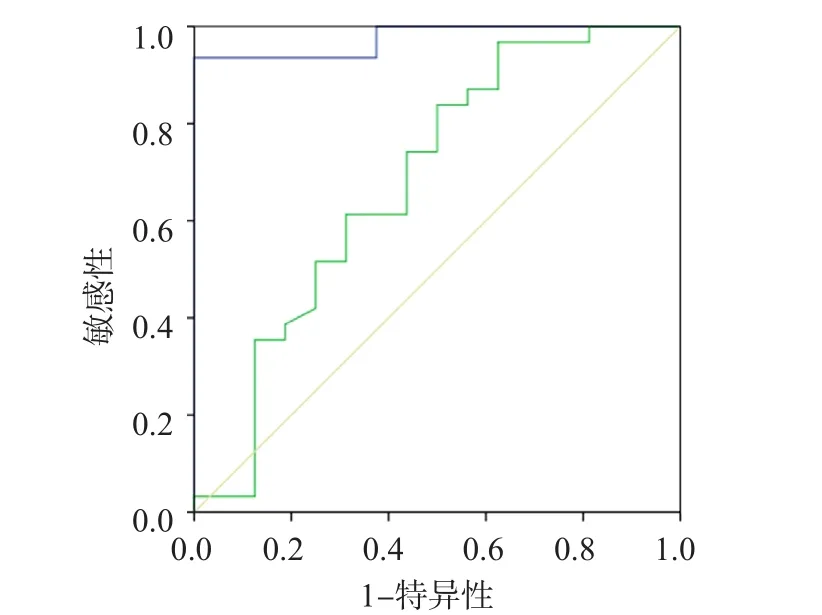
图5 FadD9重组蛋白与IGRA标准管诊断肺结核的ROC曲线
3 讨论
FadD9(Rv2590)是MTB的脂质代谢相关基因,可能与脂质降解有关,但更多的生理功能仍有待进一步研究。NORTH等[8]的研究结果显示,在小鼠模型中,FadD9抗原能够诱导辅助性T细胞1(T helper cell 1,Th1)型细胞因子,尤其是IFN-γ,而IFN-γ被认为是控制MTB感染最重要的细胞因子,也是IGRA的效应因子,足量的IFN-γ分泌是IGRA诊断成功的前提。同样由Th1分泌的TNF-α可将免疫细胞招募至感染部位,控制MTB在体内的散播,同时在肉芽肿的形成过程中也发挥着重要作用[9]。IL-2可促进细胞毒性T淋巴细胞的增殖[10]。这些细胞因子水平的升高提示FadD9蛋白在病原体-宿主相互作用的过程中发挥重要的细胞免疫调节作用,具有用于诊断试剂和疫苗开发的潜力。本研究结果显示,FadD9重组蛋白激发的小鼠血清特异性抗体的水平与阳性参照抗原Ag85A蛋白接近,提示FadD9重组蛋白可同时在MTB感染者体内激起较高水平的体液和细胞免疫反应。另外,活动性肺结核组抗FadD9抗体水平高于MTB密切接触组和正常对照组(P<0.000 1),MTB密切接触组与正常对照组之间差异无统计学意义(P>0.05),提示FadD9重组蛋白可用于活动性结核患者的相关血清学诊断试验。
抗原激发细胞免疫的水平取决于其一级结构中细胞表位的数量。本研究选择HLA-DRB、HLA-A和HLA-B亚群作为分析对象,HLA-DRB属于MHC-Ⅱ型受体,可以识别超过90%的已知MTB抗原表位(约500个),刺激更多CD4+T细胞活化,释放大量细胞因子,发挥抗结核的中心反应。HLA-A和HLA-B属于MHC-Ⅰ型受体,可活化CD8+T细胞发挥细胞毒效应,在抗结核免疫中起重要作用[11-12]。本研究结果显示,FadD9蛋白具有大量的T细胞表位,在人群中具有广泛的一致性。结合FadD9蛋白能够在小鼠中诱导出较强的Th1型细胞免疫反应,提示FadD9蛋白或许能在结核病患者中激发出具有诊断意义的细胞免疫反应。ROC曲线分析结果显示,FadD9重组蛋白诊断结核病的AUC为0.682,表明FadD9重组蛋白具有用于以细胞免疫反应为基础的IGRA的潜力。虽然与IGRA试剂盒中的标准管相比,FadD9重组蛋白的敏感性较低,特异性也有待提高,但考虑到IGRA试剂盒使用的抗原为2种以上的抗原组合,因此FadD9重组蛋白及部分表位肽或可作为新型抗原组合的候选成分。
目前,结核病的诊断金标准依然是病原学检查,但大量痰培养阴性结核病、潜伏感染人群的存在以及MTB生长缓慢等特点,限制了病原学诊断的即时性和准确性。而免疫学检测方法具有快速、灵敏和特异性高的优势。目前,用于MTB感染诊断的免疫学方法较多,如ELISA、ELISPOT、IGRA等。ELISA是采用血清学方法诊断结核病,针对的是体液免疫。ELISPOT和IGRA针对的是细胞免疫,这2种方法的原理都是基于MTB感染后机体内存在具有抗原特异性的记忆T细胞,用特定抗原刺激记忆T细胞,使其迅速活化增殖,ELISPOT检测的是合成IFN-γ的细胞数量,IGRA则检测IFN-γ的分泌量。ELISPOT和IGRA使用的核心抗原均为ESAT-6和CFP-10,对ATB的诊断有较好的表现,但无法很好地鉴别LTBI。因此只适用于MTB感染的辅助诊断,无法区分新近感染和既往感染,其结果仍存在假阳性、对于LTBI敏感性低等缺点,尚无法替代痰涂片、培养或影像学等其他较为经典的诊断方法[13-14]。实现结核病的早期、快速、特异性诊断还有很长的一段路要走,改进或开发新型、高效的检测试剂意义重大,其核心是病原菌关键抗原(簇)的发现和验证。本研究结果显示,与阳性参照抗原Ag85A蛋白比较,FadD9重组蛋白表现出了良好的免疫原性,并能引起较高的体液免疫和细胞免疫反应水平,具有用于开发成诊断试剂的潜力。后续将根据抗原T细胞表位预测结果,合成不同的抗原表位,进一步研究不同抗原表位用于结核病诊断的潜力;同时将FadD9重组蛋白/多肽与市售其他核心抗原混合使用,提高现有诊断抗原的敏感性和特异性,为诊断抗原的补充、检测方法的优化提供拓展性思路与方法[15-16]。
总之,寻找新型的MTB生物标志物,提高诊断和鉴别诊断结核病的能力,对于结核病的早期诊断、疗效监测及制定相关的防疫措施至关重要。

