FAM198B通过激活PI3K-AKT信号通路促进胃癌细胞的恶性增殖及转移
王秀芝,王国强,路以荣,金立慧,夏营营,周传义
1.聊城市第四人民医院内科,山东 聊城 252000; 2.莘县第二人民医院神经内二科
胃癌在人类与癌症有关的死亡中居第三位,按发病部位,可分为胃底贲门癌、胃体癌、胃窦癌等[1-4],国际“世界癌症研究基金”最近报道称,胃癌是第五种常见癌症,在发展中国家更为常见,2012年诊断出75.2万新病例。在中国大陆,胃癌被认为是最常见的恶性肿瘤,在2010年被列为第三大死亡原因。其中男性的发病率是女性的两倍[5]。已发现生物标志物可用于诊断胃癌和其他癌性疾病,并且还可以定量用于预测胃癌状态,这为胃癌预后研究提供了有效的诊断工具和各种新颖的治疗方案。其中,生物标志物领域具有在早期发现癌症、改善癌症监测和进展、辅助预后以及为癌症患者正确选择治疗方案提供最佳指导的巨大潜力。例如:在胃癌中,CAMKK2可激活AMPK并在胃癌组织中高表达。通过使用siRNA沉默CAMKK2,可减少胃癌细胞的增殖、克隆形成和侵袭[6],HER-2在胃癌中呈现高表达的特征,临床前研究已证明抗HER-2治疗具有显著的抗肿瘤功效。由于许多临床试验正在研究不同的设置和不同的设计,因此抗HER-2治疗在胃癌患者中的治疗效果令人期待[7]。P28/PSMD10与胃癌预后相关,并可调节人26S蛋白酶体的肿瘤发生。在胃癌组织中,P28表达显著升高,且胃癌组织P28高表达的患者总体生存率较低表达者低[8]。在本研究中,我们确定了在胃癌发生、发展中有重要作用的FAM198B,并研究了其在胃癌中的功能以及分子机制。
1 材料与方法
1.1 细胞培养人胃癌细胞BGC-823购自美国ATCC细胞库,培养在含质量浓度为100 g/L胎牛血清的RPMI-1640培养基中,并加入100 μg/ml链霉素和100 IU/ml青霉素。细胞培养瓶置于含体积分数为5%的CO2和95%湿度的37 ℃培养箱中。
1.2 临床数据筛选在临床数据库GEPIA(Gene Expression Profiling Interactive Analysis)[9]中,通过tumor/normal>2找到在胃癌中高表达的蛋白,并通过GEPIA数据库找到与胃癌临床预后密切相关的蛋白,将两部分蛋白进行重合性分析,从而筛选到目的蛋白。
1.3 实时荧光定量PCR实验(qRT-PCR)使用primer3(http://frodo.wi.mit.edu/primer3/)设计特异性qPCR引物;cDNA用灭菌纯水稀释适当的浓度,一般稀释20倍,按照qPCR mix 5 μl,primer 1 μl,cDNA 4 μl的配方加入到96孔PCR板中;贴膜,以2 500 r/min离心1 min,将样品放入qPCR仪器中进行实验,反应完成后,拷贝数据,进行分析。
1.4 转染以6孔板转染siRNA(购自广州锐博公司)为例:将1 μl siRNA与250 μl Opti-MEM(购自BI代理公司)混匀,1 μl lipo2000与250 μl Opti-MEM混匀,室温放置5 min,然后将两部分合并,混匀,静置15 min,之后逐滴、均匀加入6孔板中的1个孔中。
1.5 细胞增殖实验取消化长满的细胞,重悬于1 ml新鲜培养基中,采用96孔板,每孔铺设20 μl。在体积分数为5% CO2,37 ℃条件下孵育。细胞贴壁后即可转染siRNA,48 h后开始测量吸光度。配制MTS(购自Abcam代理公司)反应液,按照MTS∶培养液=1∶20的比例配制反应液。每孔加入100 μl MTS反应溶液,37 ℃继续培养。每隔半小时检测一次吸光度。将培养皿置摇床上低速振荡10 s以充分溶解结晶物。实验重复3次,在490 nm处测量各孔的吸光值。将每天的吸光值转换成代表每日细胞生长的参数,并绘制细胞增殖曲线。
1.6 划痕迁移实验10 cm盘的1/4铺整个6孔板,待细胞贴壁后分别转染siRNA,待细胞长到90%用枪头在盘中央划痕,并用PBS洗1遍,拍摄0 h图片作为对照,之后24 h再次进行拍摄观察。
1.7 基因功能分析在临床数据库cBioPortal[10-11]中找到与FAM198B共表达的基因,将这些基因在metascape[12]中进行信号通路分析,从而为解析目的蛋白在癌症进程中发挥的功能提供参考。
1.8 蛋白质免疫印迹实验收细胞进行蛋白定量并制样,准备电泳、电转装置,电泳液以及电转液,装样品加入在凝胶中,100 V进行电泳,待蓝色条带跑出即进行电转,100 V电转2 h,将蛋白膜放在牛奶中封闭1 h,4 ℃孵育一抗过夜,洗膜4次,每次5 min,室温孵育二抗1 h,洗膜4次,每次5 min,暗房显影。
2 结果
2.1 筛选胃癌中具有临床意义的靶基因为了筛选在胃癌中具有重要作用的靶基因,首先我们通过GEPIA数据库[9]找到在胃癌中相比临近正常组织高表达的基因(tumor/normal>2),共3 745个,同时找到在胃癌中具有显著临床预后相关性的基因(P<0.05),共500个,将这两部分基因进行重合性分析,找到在胃癌中显著高表达且具有明显临床预后相关性的基因,共46个(见图1A),将这46个基因进行热图分析,筛选到在胃癌中高表达且具有显著临床预后相关性的目的基因FAM198B(见图1B)。
2.2 FAM198B在胃癌中的表达特征确定了目的基因FAM198B,探究FAM198B在胃癌中的特征,发现FAM198B在胃癌中相比临近正常组织显著高表达(见图2A),且具有明显的高表达预后差的临床预后相关性(见图2B),随着肿瘤恶性程度的升高,FAM198B的表达逐步升高(见图2C),随后在30组临床样品中进行了FAM198B的表达验证,发现FAM198B在胃癌中相比邻近组织显著高表达(见图2D)。
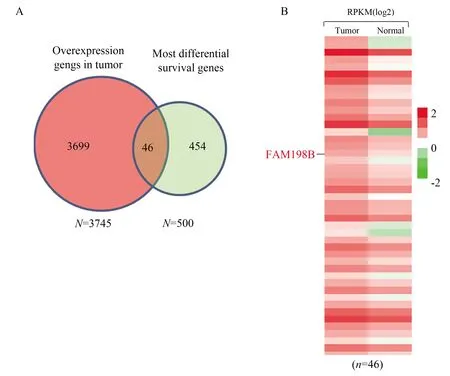
图1 筛选胃癌中具有临床意义的靶基因 A:找出GEPIA数据库中胃癌高表达的基因和具有显著胃癌临床预后相关性的基因并进行重合性分析;B:热图分析胃癌中高表达且具有显著临床预后的基因
Fig 1 Screening of clinically meaningful target genes in gastric cancer A: identify genes that were highly expressed in gastric cancer in the GEPIA database, found genes that had a significant correlation with clinical prognosis of gastric cancer, and analyzed the coincidence of these two genes; B: heat map analysis of genes that were highly expressed in gastric cancer and had a significantly clinical prognosis
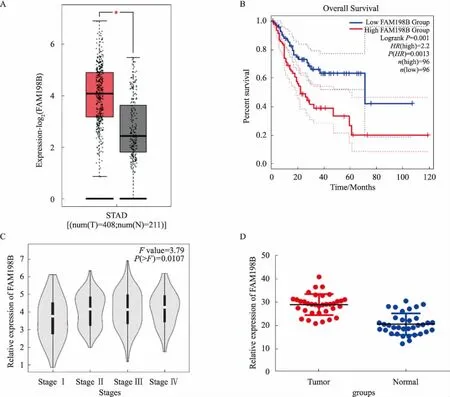
图 2 FAM198B在胃癌中的表达特征 A:FAM198B在胃癌及邻近组织中的表达情况;B:FAM198B与胃癌的临床预后相关性;C:FAM198B在胃癌各种恶性程度下的表达情况;D:qPCR数据显示FAM198B在胃癌临床样品中的表达情况
Fig 2 Expression characteristics of FAM198B in gastric cancer A: expression of FAM198B in gastric cancer and adjacent tissues; B: correlation of FAM198B and clinical prognosis of gastric cancer; C: expression of FAM198B in various malignant degrees of gastric cancer;D: qPCR data showed that FAM198B expression in clinical samples of gastric cancer
2.3 FAM198B促进胃癌细胞的增殖和迁移上述特征说明了FAM198B在胃癌发生、发展中有重要作用,为了进一步验证FAM198B在胃癌中的作用,我们进行了经典的分子生物学实验验证,发现在siRNA介导敲低FAM198B表达的胃癌细胞中,细胞增殖速率较对照组显著减慢(见图3A),划痕迁移速率也显著减慢(见图3B),由此进一步验证了FAM198B在胃癌发生、发展中的重要性。
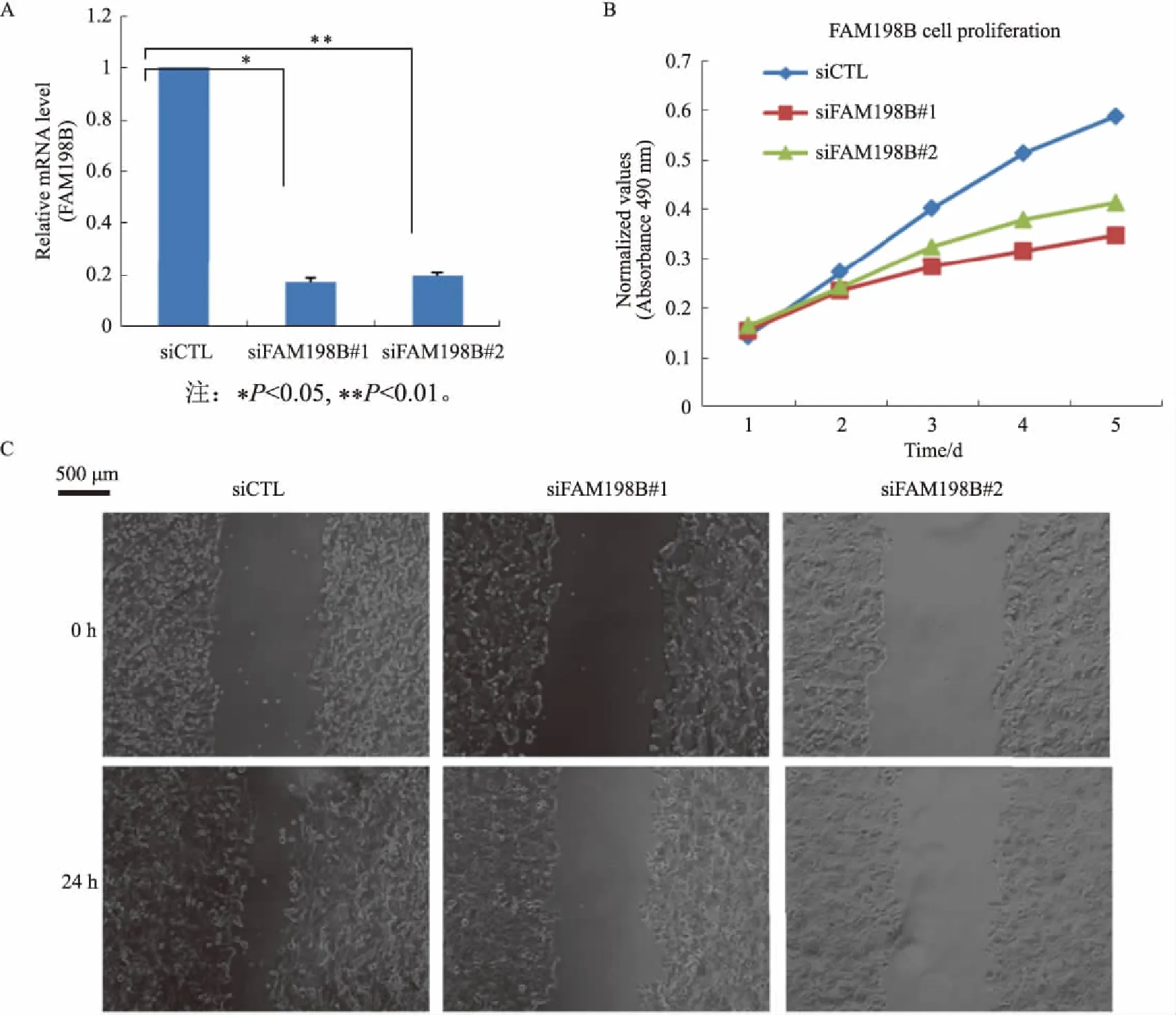
图3 FAM198B促进胃癌细胞的增殖和迁移 A:siRNA介导敲低FAM198B的表达效率;B:siRNA介导敲低FAM198B的细胞增殖速率;C:siRNA介导敲低FAM198B的划痕迁移速率
Fig 3 FAM198B promoted the proliferation and migration of gastric cancer cells A: siRNA-mediated knockdown of FAM198B expression efficiency; B: siRNA-mediated knockdown of FAM198B cell proliferation rate; C: siRNA-mediated knockdown of FAM198B scratch migration rate
2.4 FAM198B通过PI3K-AKT信号通路促进胃癌细胞增殖和迁移上述实验证明了FAM198B在胃癌中的重要性,进一步对其发挥功能的分子机制进行初步探讨,首先通过分析与FAM198B共表达的基因参与的信号通路,HallMark分析发现FAM198B与凋亡、紫外照射、IL6等致癌相关通路相关(见图4A),提示FAM198B的重要性,KEGG分析发现可能通过PI3K-AKT信号通路发挥功能(见图4B),接着利用蛋白免疫印迹实验进行验证,发现在敲低FAM198B表达的细胞中,PI3K-AKT信号通路中的关键靶基因PI3K、AKT本底表达不变,磷酸化水平均显著降低(见图4C~4D),证明FAM198B促进胃癌细胞增殖和迁移可能是通过PI3K-AKT信号通路发挥功能。
3 讨论
具有序列相似性198的人类家族成员B(FAM198B)是功能未知的新基因,预计是位于高尔基体上的膜结合糖蛋白[12-13]。FAM198B可能在调节小鼠和非洲爪蟾的胚胎发育中起作用[14-15]。所有已知的真核蛋白质中几乎有一半是N-糖基化的,这是普遍存在的翻译后修饰[16],据报道,糖基化的改变与肿瘤增殖、侵袭、转移、血管生成、受体活化和细胞内或细胞-基质相互作用有关[17-19]。而我们首次在胃癌中研究了FAM198B本身的功能,并初步证明其参与PI3K-AKT信号通路,为进一步研究FAM198B在细胞内的功能提供参考。
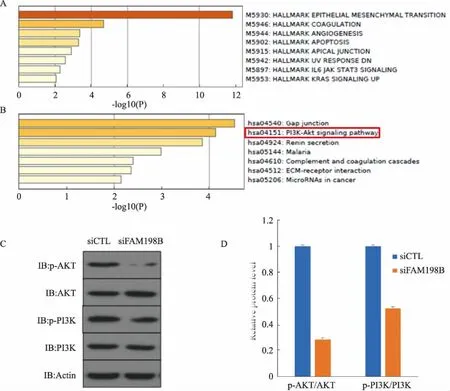
图4 FAM198B通过PI3K-AKT信号通路促进胃癌细胞增殖和迁移 A:与FAM198B共表达基因参与的HallMark信号通路; B:与FAM198B共表达基因参与的KEGG信号通路;C:敲低FAM198B表达对AKT和PI3K表达的影响;D:对C图的定量分析
Fig 4 FAM198B promoted the proliferation and migration of gastric cancer cells through the PI3K-AKT signaling pathway A: HallMark signaling pathway with FAM198B co-expression genes; B: KEGG signaling pathway with FAM198B co-expression genes; C: effect of knockdown FAM198B on AKT and PI3K expression; D: quantitative analysis of the figure C
在本文中,我们首先通过GEPIA数据库[9]找到在胃癌中较邻近组织高表达的基因,同时找到在胃癌中具有显著临床预后相关性的基因,将这两部分基因进行重合性分析,找到既在胃癌中高表达且具有显著临床预后的基因,最后根据高表达预后差原则确定FAM198B在胃癌中必然存在重要功能;接着研究了FAM198B在胃癌中的表达特征,FAM198B在胃癌中高表达,具有显著高表达预后差特征,且随着癌症恶性程度的加深,FAM198B的表达逐步升高,说明FAM198B在胃癌中的重要性,同时在30组临床胃癌样品中也发现FAM198B在胃癌中显著高表达;确定了FAM198B在胃癌中存在重要功能,随即进行细胞增殖和迁移实验进行验证,发现FAM198B可促进胃癌细胞增殖和迁移;我们进一步探讨了FAM198B在胃癌中发挥功能的分子机制,通过共表达基因发现FAM198B可能参与PI3K-AKT信号通路,我们在敲低FAM198B的细胞中进行了验证,发现敲低FAM198B可降低PI3K-AKT信号通路中关键靶基因的磷酸化水平。综上所述,我们认为FAM198B可能通过激活PI3K-AKT信号通路从而促进胃癌细胞增殖和迁移。
本文从筛选胃癌中高表达且具有显著临床预后相关性的基因、功能验证以及分子机制等方面对促进胃癌发生、发展的进程进行了研究,但这其中的研究还不全面,功能验证除了细胞增殖和迁移实验,还可利用细胞周期、克隆形成等表型实验进行进一步的验证,分子机制也只是初步的探讨,需要更多的全转录组结合高通量测序实验以及后续的qRT-PCR、相互作用蛋白及质谱的进一步验证,使研究结论更具有说服力。

